[2026] Thi thử TN sở GDĐT Cà Mau (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 106
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2D | 3B | 4C | 5B | 6B | 7B | 8D | 9C |
| 10C | 11B | 12D | 13C | 14C | 15A | 16A | 17D | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | Đ | Đ |
| (b) | Đ | Đ | S | Đ |
| (c) | Đ | S | Đ | S |
| (d) | S | Đ | S | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 8,52 | 12 | 2000 | 1 | 24 | 38,7 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Trong bảng tuần hoàn các nguyên tố hoá học, các nguyên tố halogen thuộc nhóm
A. VIIIA. B. IA. C. IIA. D. VIIA.
(Xem giải) Câu 2. Các tính chất vật lí chung của kim loại (dẻo, dẫn điện, dẫn nhiệt, ánh kim) gây ra chủ yếu bởi nhân tố nào sau đây?
A. Các ion dương kim loại ở các nút mạng tinh thể.
B. Các nguyên tử kim loại đứng khít nhau.
C. Liên kết cộng hóa trị giữa các nguyên tử.
D. Sự hiện diện của các electron tự do trong mạng tinh thể.
(Xem giải) Câu 3. Cho các phát biểu sau:
(1) Glucose và fructose đều có phản ứng tráng bạc.
(2) Trong môi trường kiềm, fructose chuyển hóa thành glucose.
(3) Tất cả các carbohydrate đều tham gia phản ứng thủy phân.
(4) Ở điều kiện thường, tinh bột là chất rắn, dạng bột vô định hình, màu trắng.
Số phát biểu đúng là
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 4. Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một nhóm học sinh xác định độ tinh khiết (a%) của muối Mohr bằng cách tiến hành các thí nghiệm sau: Cân 3,443 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,01M. Thực hiện chuẩn độ 3 lần. Kết quả như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích dung dịch KMnO4 (mL) | 16 | 16,1 | 16 |
Giá trị của a là (không làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)
A. 92,78. B. 95,59. C. 91,27. D. 90,02.
(Xem giải) Câu 5. Tiến hành các thí nghiệm sau:
(1) Cho Mg vào lượng dư dung dịch FeCl3.
(2) Cho Ba vào lượng dư dung dịch CuSO4.
(3) Cho Zn vào dung dịch CuSO4.
(4) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
Có bao nhiêu thí nghiệm tạo thành kim loại?
A. 3. B. 2. C. 4. D. 1.
(Xem giải) Câu 6. Thực hiện phản ứng hoá học: Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g). Sau 40 giây, nồng độ của dung dịch HCl giảm từ 0,8M còn 0,6M. Tốc độ trung bình của phản ứng trên theo nồng độ HCl trong 40 giây là
A. 1,5.10-2 (M.s-1). B. 2,5.10-3 (M.s-1). C. 5,0.10-3 (M.s-1). D. -5,0.10-3 (M.s-1).
(Xem giải) Câu 7. Cho polymer có cấu tạo như sau:
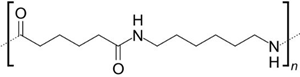
Polymer trên được dùng để sản xuất loại vật liệu polymer nào sau đây?
A. Chất dẻo. B. Tơ. C. Keo dán. D. Cao su.
(Xem giải) Câu 8. Carbohydrate được tổng hợp bởi thực vật và chiếm khoảng 90% khối lượng sợi bông là
A. saccharose. B. maltose. C. tinh bột. D. cellulose.
(Xem giải) Câu 9. Ethylene là một hydrocarbon không no, có thể tham gia phản ứng với nhiều chất. Phản ứng hóa học của ethylene với dung dịch Br2 được cho bởi phương trình:
CH2=CH2 + Br2 → CH2Br-CH2Br.
Cơ chế của phản ứng trên xảy ra như sau:
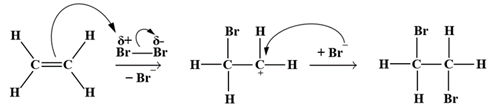
Cho các phát biểu sau:
(1) Phản ứng xảy ra theo cơ chế cộng electrophile (AE).
(2) Giai đoạn đầu tiên là quá trình phản ứng của Br+ với C=C tạo carbocation trung gian.
(3) Giai đoạn thứ 2 là quá trình kết hợp của carbocation với Br- tạo thành sản phẩm.
(4) Br+ là tác nhân electrophile và Br- là tác nhân nucleophile.
Số phát biểu đúng là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 10. Xác định giá trị pH của một dung dịch bằng máy đo pH, thu được giá trị pH = 3,0. Phát biểu nào sau đây là đúng?
A. Nồng độ ion OH- trong dung dịch là 10^-3,0 M.
B. Nồng độ ion H+ trong dung dịch là 3,0 M.
C. Nồng độ ion H+ trong dung dịch là 10^-3,0 M.
D. Nồng độ ion OH- trong dung dịch là 3,0 M.
(Xem giải) Câu 11. Hợp chất hữu cơ X có công thức đơn giản nhất là CH2O. Công thức phân tử có thể có của X là
A. C3H6O. B. C3H6O3. C. C4H8O. D. C2H4O.
(Xem giải) Câu 12. Trong phòng thí nghiệm, dung dịch chất nào sau đây phù hợp để kiểm tra sự có mặt của ion NH4+(aq)?
A. Na2SO4. B. HCl. C. NaCl. D. NaOH.
(Xem giải) Câu 13. Trong cây thuốc lá tự nhiên và khói thuốc lá chứa một amine rất độc, đó là nicotine với công thức cấu tạo như sau:

Nicotine làm tăng huyết áp và nhịp tim, có khả năng gây xơ vữa động mạch vành và suy giảm trí nhớ. Công thức phân tử của nicotine là
A. C10H8N2. B. C10H10N2. C. C10H14N2. D. C10H12N2.
(Xem giải) Câu 14. Ethyl acetate được sử dụng để tách caffeine khỏi cà phê, ethyl acetate có công thức cấu tạo thu gọn là
A. C2H5COOC2H5. B. CH2=CHCOOCH3. C. CH3COOC2H5. D. C2H5COOCH3.
(Xem giải) Câu 15. Ammonia (NH3) là nguyên liệu sản xuất nitric acid và nhiều loại phân bón. Số oxi hóa của nitrogen trong ammonia là
A. -3. B. 0. C. 3. D. +3.
(Xem giải) Câu 16. Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Pb; Fe và Zn; Fe và Sn; Fe và Ni. Khi nhúng các cặp kim loại trên vào dung dịch acid, số cặp kim loại trong đó Fe bị phá hủy trước là
A. 3. B. 1. C. 4. D. 2.
(Xem giải) Câu 17. Phản ứng nào sau đây không điều chế được kim loại đồng (copper)?
A. Điện phân dung dịch CuSO4 điện cực trơ. B. Cho H2 tác dụng với CuO nung nóng.
C. Cho Fe tác dụng với dung dịch CuSO4. D. Cho Na tác dụng với dung dịch CuSO4.
(Xem giải) Câu 18. Xét phức chất [CoCl2(NH3)4]+
(1) Nguyên tử trung tâm trong phức chất là Co2+.
(2) Các phối tử có trong phức chất là Cl- và NH3.
(3) Số lượng phối tử trong phức chất là 6.
(4) Điện tích của phức chất là +3.
Số phát biểu đúng là
A. 1. B. 2. C. 4. D. 3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Sodium hydrogencarbonate hay còn gọi là baking soda được sử dụng để trị chứng dư acid ở dạ dày và làm tăng độ xốp của bánh.
(a) Công thức hóa học của sodium hydrogencarbonate là NaHCO3.
(b) Khi làm bánh người ta thường cho bột nở (baking soda) vì khi nung nóng bột NaHCO3 sẽ bị nhiệt phân tạo ra khí CO2 thoát ra từ trong bánh, giúp bánh phồng lên và tơi xốp hơn khi không có bột nở.
(c) Giả sử có V lít dung dịch HCl 0,02 M (nồng độ acid trong dạ dày) được trung hòa hoàn toàn sau khi uống 0,336 gam NaHCO3 thì giá trị của V là 0,2.
(d) Sodium hydrogencarbonate được dùng để trung hòa hydrochloric acid để làm giảm độ pH trong dịch vị dạ dày.
(Xem giải) Câu 20. Isoamyl acetate có mùi thơm đặc trưng của chuối chín nên còn được gọi là dầu chuối. Khi đun nóng hỗn hợp gồm 9,00 gam acetic acid và 10,56 gam isoamyl alcohol với xúc tác là H2SO4 đặc, thu được 9,75 gam dầu chuối (xem như chỉ chứa isoamyl acetate). Hiệu suất của phản ứng điều chế dầu chuối trên là h%.
(a) Phản ứng điều chế isoamyl acetate ở trên có đặc điểm là phản ứng một chiều.
(b) Isoamyl alcohol có công thức cấu tạo thu gọn là (CH3)2CHCH2CH2OH.
(c) Phản ứng điều chế isoamyl acetate ở trên còn có tên gọi là phản ứng xà phòng hoá.
(d) Giá trị của h là 62,5. (Làm tròn kết quả đến hàng phần mười).
(Xem giải) Câu 21. Acquy chì được sử dụng phổ biến trong đời sống, đặc biệt ở các phương tiện giao thông và hệ thống điện cơ bản. Acquy chì gồm một điện cực Pb và một điện cực PbO2 nhúng trong dung dịch H2SO4 nồng độ khoảng 40%. Phản ứng xảy ra trong acquy chì khi phóng điện và khi nạp điện như sau:
Pb(s) + PbO2(s) + 2H+(aq) + 2HSO4-(aq) → 2PbSO4(s) + 2H2O
Trong đó quá trình thuận là quá trình phóng điện (1), quá trình nghịch là quá trình nạp điện (2).
Biết điện lượng được tính theo công thức: q = I.t = n.F. Trong đó t là thời gian (s), I là cường độ dòng điện (A), n là số mol electron trao đổi ở mỗi điện cực, F = 96485 C/mol. (Kết quả chỉ được làm tròn ở bước tính cuối cùng và làm tròn đến hàng phần trăm).
(a) Khi acquy phóng điện, ở anode xảy ra quá trình oxi hóa Pb.
(b) Trong quá trình phóng điện, khối lượng của anode giảm còn khối lượng của cathode tăng.
(c) Khi nạp điện cho acquy chì bằng dòng điện một chiều có cường độ 2,0 A trong 1 giờ với hiệu suất 100%, khối lượng Pb được tái tạo ở cực âm là 7,72 gam.
(d) Khi acquy đang cung cấp điện cho xe máy, nồng độ dung dịch sulfuric acid sẽ tăng dần do nước bị tiêu thụ.
(Xem giải) Câu 22. Cho sơ đồ chuyển hóa sau: (X, Y, Z, T đều là các chất hữu cơ)
![]()
(a) Phản ứng (1) là phản ứng thế trên vòng benzene, X là C6H5NO2.
(b) Từ 100 lít benzene (D = 0,879 g/mL) ban đầu có thể thu được 84 kg chất Z, hiệu suất cả quá trình là 80%. (không làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị)
(c) Z có lực base mạnh hơn methylamine, dung dịch làm quỳ tím hóa xanh.
(d) Trong phản ứng (2) C6H5NO2 bị khử thành Y là C6H5NH2.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Trong công nghiệp, nhôm (aluminium) được sản xuất bằng phương pháp điện phân nóng chảy Al2O3 với điện cực than chì và có mặt cryolite. Nguyên liệu của quá trình điện phân là quặng bauxite có chứa 80% Al2O3.2H2O về khối lượng, tạp chất còn lại không chứa nhôm. Trong quá trình sản xuất, khi điện phân hết x tấn quặng bauxite nói trên thì tiêu tốn y tấn than chì ở anode (do bị oxi hóa bởi khí O2). Tỉ lệ của x/y là bao nhiêu? Biết rằng, chỉ có 90% Al2O3 bị điện phân và hỗn hợp khí thoát ra chỉ có CO và CO2 với tỉ lệ thể tích là 2 : 3. (Chỉ được làm tròn ở phép tính cuối cùng và kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 24. Cisplatin là tên thương mại của phức chất có công thức hoá học là [Pt(NH3)2Cl2]. Trong phức chất, hai phối tử Cl- nằm ở vị trí liền kề nhau xung quanh nguyên tử trung tâm, tạo thành cấu hình cis. Trong phòng thí nghiệm, cisplatin được điều chế theo sơ đồ gồm hai giai đoạn:
![]()
Cho các phát biểu sau:
(1) Phức chất cisplatin có dạng hình học vuông phẳng.
(2) Ở giai đoạn (1) và (2) đều xảy ra phản ứng thế 1 phối tử Cl- bằng 1 phối tử NH3.
(3) Điện tích của ba phức chất trong sơ đồ lần lượt là -2, -1 và 0.
(4) Trong sơ đồ trên, có thể thay phức chất [PtCl4]2- bằng phức chất [PtCl6]2-.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần. (Ví dụ: 123, 124, 14,…)
(Xem giải) Câu 25. Một ruột phích có diện tích bề mặt là 0,35 m². Để tráng được a ruột phích như trên với độ dày lớp bạc (Ag) là 0,1 μm thì cần dùng 8160 gam dung dịch glucose 10% tác dụng với lượng dư dung dịch AgNO3 trong NH3. Biết hiệu suất phản ứng tráng bạc là 75% và khối lượng riêng của bạc là 10,49 g/cm³. Tính giá trị của a? (Kết quả chỉ được làm tròn ở bước tính cuối cùng và làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Cho các polymer sau: polyethylene, poly(vinyl chloride), polypropylene, polystyrene, nylon-6,6. Có bao nhiêu polymer được tổng hợp bằng phản ứng trùng ngưng?
(Xem giải) Câu 27. Dựa vào phương trình nhiệt hoá học của các phản ứng sau:
(1) CS2(l) + 3O2(g) → CO2(g) + 2SO2(g) ![]() = -1110,21 kJ
= -1110,21 kJ
(2) CO2(g) → CO(g) + O2(g) ![]() = +283,00 kJ
= +283,00 kJ
(3) 2Na(s) + 2H2O(l) → 2NaOH(aq) + H2(g) ![]() = -367,50 kJ
= -367,50 kJ
(4) ZnSO4(s) → ZnO(s) + SO3(g) ![]() = +235,21 kJ
= +235,21 kJ
Liệt kê những phản ứng thu nhiệt theo số thứ tự tăng dần. (Ví dụ: 123, 124, 14,…)
(Xem giải) Câu 28. Phần trăm khối lượng carbon trong ethylene glycol là a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).

Bình luận