[2026] Thi thử TN trường Đông Sơn 1 – Thanh Hóa (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 105
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2C | 3C | 4C | 5A | 6C | 7A | 8C | 9B |
| 10D | 11C | 12C | 13D | 14C | 15D | 16B | 17A | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | S | S | Đ | Đ |
| (b) | S | S | Đ | S |
| (c) | Đ | Đ | Đ | S |
| (d) | S | Đ | S | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 5668 | 3 | 135 | 135 | 0,84 | 1,08 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Polymer nào được tạo thành từ monomer có phân tử khối là 28 amu?
A. Polystyrene (PS). B. Poly(vinyl chloride) (PVC).
C. Polypropylene (PP). D. Polyethylene (PE).
(Xem giải) Câu 2: Ô nhiễm môi trường do chất thải nhựa và túi nylon (PE, PVC…) hay còn gọi là “ô nhiễm trắng” gây ảnh hưởng nghiêm trọng đến môi trường. Giải pháp xử lý rác thải nhựa nào sau đây không hợp lý?
A. Phân loại rác thải nhựa từ đầu nguồn để tái chế.
B. Tái sử dụng đồ nhựa, chai nhựa làm đồ dùng.
C. Tiêu hủy các chất thải nhựa và túi nylon bằng phương pháp đốt hoặc chôn lấp.
D. Thay thế túi nylon bằng túi giấy, túi vải tái sử dụng nhiều lần.
(Xem giải) Câu 3: Saccharin (C7H5O3NS) được biết đến là một loại đường hóa học, công dụng chính của saccharin là chất làm ngọt không chứa calo. Để so sánh độ ngọt của các chất tạo ngọt với một số loại đường, người ta chọn độ ngọt của saccharose làm đơn vị.
| Chất ngọt | Glucose | Fructose | Saccharose | Saccharin |
| Độ ngọt | 0,75 | 1,75 | 1,00 | 350 |
Để pha chế một loại nước giải khát, người ta dùng 30 g saccharose cho 1 lít nước. Nếu dùng 15 gam saccharin thì sẽ pha được khoảng bao nhiêu lít nước có độ ngọt tương đối với loại nước giải khát đã nêu?
A. 200. B. 35. C. 175. D. 150.
(Xem giải) Câu 4: Cho dipeptide X có công thức cấu tạo: H2NCH2CO-NHCH(CH3)COOH. Phát biểu nào sau đây về X là sai?
A. Thủy phân hoàn toàn 1 mol X thu được 1 mol glycine và 1 mol alanine.
B. Phân tử X có hai đầu: đầu N chứa nhóm -NH2 và đầu C chứa nhóm -COOH.
C. Dung dịch X hòa tan được Cu(OH)2 tạo thành hợp chất màu tím đặc trưng.
D. Trong phân tử X có chứa một liên kết peptide.
(Xem giải) Câu 5: Đun nước lâu ngày hóa xuất hiện một lớp cặn bám dưới đáy ấm đun nước. Chất cặn bám vào đáy ấm đun nước có công thức hóa học là
A. CaCO3. B. Ca(HCO3)2. C. NaCl. D. Na2CO3.
(Xem giải) Câu 6: Để tái chế nhôm, người ta sử dụng phế liệu kim loại như các lon, hộp đựng nước giải khát hay thực phẩm. Phế liệu còn lẫn các tạp chất là các chất vô cơ và hữu cơ (có trong nhãn, mác in hoặc sơn trên vỏ lon, hộp). Phế liệu được cắt, băm nhỏ rồi cho vào lò nung đến khi chảy lỏng. Phần xỉ lỏng, nổi lên trên được vớt ra khỏi lò. Phần còn lại trong lò là nhôm tái chế ở trạng thái nóng chảy. Chọn phát biểu sai:
A. Việc tái chế nhôm giúp giảm tác động tiêu cực của việc khai thác mỏ quặng, do tiết kiệm tài nguyên thiên nhiên.
B. Việc cắt, băm nhỏ phế liệu giúp giảm thể tích, tránh hao phí năng lượng khi nung.
C. Các loại thau, chậu, xô… làm bằng nhôm là vật đựng tốt nhất dùng để bảo quản vôi (Ca(OH)2).
D. Quá trình tái chế nhôm thủ công cho lợi nhuận cao nhưng gây ô nhiễm môi trường trầm trọng nếu không có biện pháp xử lý các chất thải.
(Xem giải) Câu 7: Thành phần của dịch vị dạ dày gồm 95% là nước, enzyme và hydrochloric acid. Sự có mặt của hydrochloric acid làm cho pH của dịch vị trong khoảng từ 2 – 3. Để làm giảm bớt lượng acid dư trong dạ dày người ta thường uống thuốc muối “Nabica” từng lượng nhỏ và cách quãng. Cho các nhận định sau:
1) Công thức hóa học của muối Nabica là NaHCO3.
2) Khi uống từng lượng nhỏ và cách quãng “Nabica” thì pH của dịch vị dạ dày sẽ tăng từ từ và không sinh quá nhiều khí CO2.
3) Uống nhiều NaHCO3 liên tục sẽ giúp chữa khỏi hẳn bệnh dư acid dạ dày.
4) Phản ứng giữa Nabica và hydrochloric acid trong dạ dày là phản ứng oxi hóa – khử, sinh ra khí carbon dioxide.
Những phát biểu sai là
A. 1, 2. B. 2, 3. C. 1, 4. D. 3, 4.
(Xem giải) Câu 8: Cho các đặc điểm sau của các kim loại chuyển tiếp dãy thứ nhất:
(1) Có nhiều trạng thái oxi hóa khác nhau.
(2) Có khả năng hình thành các ion phức có màu đặc trưng.
(3) Đều là những kim loại có tính khử mạnh hơn so với các kim loại nhóm IA.
(4) Có khả năng đóng vai trò là chất xúc tác trong nhiều phản ứng hóa học.
Số đặc điểm đúng với tính chất chung của các kim loại chuyển tiếp dãy thứ nhất là:
A. 4. B. 1. C. 3. D. 2.
(Xem giải) Câu 9: Cho các phát biểu sau:
a) Để dập tắt đám cháy các kim loại kiềm như Na hay K, có thể dùng cát khô hoặc bình chữa cháy chứa khí CO2 vì chúng làm cách ly kim loại với oxygen.
b) Trong công nghiệp, kim loại magnesium (Mg) được điều chế bằng phương pháp điện phân nóng chảy muối chloride hoặc dùng carbon khử magnesium oxide ở nhiệt độ cao.
c) Trong tự nhiên, các kim loại chuyển tiếp dãy thứ nhất như Fe, Cu, Cr hầu hết tồn tại dưới dạng đơn chất do tính khử yếu.
d) Cấu hình electron của nguyên tử iron (Fe, Z = 26) ở trạng thái cơ bản là [Ar]3d64s2.
e) Đồng chất cesium (Cs) được dùng làm tế bào quang điện; hợp kim Li – Al siêu nhẹ được dùng trong công nghiệp hàng không vũ trụ.
Số phát biểu đúng là
A. 4. B. 2. C. 5. D. 3.
(Xem giải) Câu 10: Kim loại tungsten (W) được sử dụng trong các bóng đèn sợi đốt (bóng dây tóc). Ứng dụng này được dựa trên cơ sở tính chất vật lý nào của tungsten
A. Khối lượng riêng. B. Tính dẫn nhiệt.
C. Độ cứng. D. Nhiệt độ nóng chảy.
(Xem giải) Câu 11: Saccharose và maltose sẽ tạo sản phẩm giống nhau khi tham gia phản ứng nào dưới đây?
A. Tác dụng với Cu(OH)2. B. Thủy phân.
C. Đốt cháy hoàn toàn. D. Tác dụng với dung dịch AgNO3 trong NH3.
(Xem giải) Câu 12: Polymer nào sau đây thuộc loại polymer thiên nhiên?
A. Nylon-6,6. B. Polyethylene. C. Cellulose. D. Poly (vinyl chloride).
(Xem giải) Câu 13: Cho các phản ứng sau:
(1) X + 2X3+ → 3X2+
(2) Y + 2X3+ → 2X2+ + Y2+
(3) X + Y2+ → X2+ + Y.
Cặp oxi hóa – khử nào dưới đây có giá trị thế điện cực chuẩn âm nhất?
A. X3+/X2+. B. X3+/X. C. Y2+/Y. D. X2+/X.
(Xem giải) Câu 14: Cặp oxi hóa – khử thường chứa hai chất (hoặc ion) của cùng một nguyên tố hóa học nhưng có số oxi hóa khác nhau; dạng oxi hóa chứa nguyên tử của nguyên tố với số oxi hóa …(1)… và dạng khử chứa nguyên tử của nguyên tố đó với số oxi hóa …(2)… Thông tin phù hợp điền vào (1) và (2) lần lượt là.
A. thấp hơn và cao hơn. B. dương và âm.
C. cao hơn và thấp hơn. D. âm và dương.
(Xem giải) Câu 15: Hiện nay, tầng ozone đang bị suy giảm nghiêm trọng do sự phát thải các hợp chất chlorofluorocarbon (CFC) từ các thiết bị làm lạnh. Nguyên tố hóa học chính trong hợp chất này gây ra sự phân hủy các phân tử ozone (O3) là
A. Carbon. B. Hydrogen. C. Fluorine. D. Chlorine.
(Xem giải) Câu 16: Cho cân bằng hóa học: PCl5(g) ⇋ PCl3(g) + Cl2(g) ![]() > 0. Yếu tố không ảnh hưởng đến cân bằng hóa học này là
> 0. Yếu tố không ảnh hưởng đến cân bằng hóa học này là
A. Áp suất. B. Chất xúc tác. C. Nồng độ. D. nhiệt độ.
(Xem giải) Câu 17: Hai monosaccharide liên kết với nhau bởi liên kết nào sau đây?
A. Liên kết glycoside. B. Liên kết peptide.
C. Liên kết hydrogen. D. Liên kết van der Waals.
(Xem giải) Câu 18: Tính chất vật lý nào sau đây không đặc trưng cho ester?
A. dễ bay hơi. B. ít tan trong nước.
C. nặng hơn nước. D. có mùi thơm.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Khi thủy phân hoàn toàn 500 mg một protein, chỉ thu được các amino acid với khối lượng như sau:
| Công thức cấu tạo | Kí hiệu | Khối lượng (mg) |
| CH3CH(NH2)COOH | Ala | 178 |
| HOOCCH2CH2CH(NH2)COOH | Glu | 88 |
| (CH3)2CH-CH(NH2)-COOH | Val | 94 |
| H2N-[CH2]4-CH(NH2)-COOH | Lys | 88 |
| HOOC-CH2CH(NH2)COOH | Asp | 67 |
| HOC6H4CH2CH(NH2)COOH | Tyr | 73 |
a) Nếu thủy phân 500 gam protein trên (lấy phân tử khối là 50 000 amu) trong dung dịch HCl (dư) đến phản ứng hoàn toàn, thì thu được tổng khối lượng các muối chloride là 789,5 gam (kết quả làm tròn đến hàng phần mười).
b) Nếu phân tử khối của protein này là 50 000 thì số mắt xích trong 1 phân tử protein ở trên là 200 Ala; 60 Glu; 50 Asp; 80 Val và 40 Tyr (kết quả làm tròn đến hàng đơn vị).
c) Trong các amino acid ở trên, lysine (Lys) là một trong những amino acid đóng vai trò quan trọng cho quá trình xây dựng và tạo ra các mạch máu mới trong cơ thể; ở pH = 6, lysine tồn tại dạng cation.
d) Có thể dựa vào tính chất điện di để tách riêng từng amino acid trong bảng kết quả trên.
(Xem giải) Câu 20: Sự ăn mòn kim loại là bài toán kinh tế và kỹ thuật nan giải trong nhiều lĩnh vực. Các phát biểu sau về hiện tượng này đúng hay sai?
a) Trong quá trình thép bị ăn mòn điện hóa tại môi trường không khí ẩm, tinh thể iron (Fe) đóng vai trò là cathode và là nơi xảy ra quá trình khử oxygen.
b) Khi nối một sợi dây copper (đồng) vào một cột thép chôn dưới lòng đất ẩm, tốc độ ăn mòn của cột thép sẽ giảm xuống do đồng dẫn điện tốt, giúp giải phóng nhanh dòng electron phát sinh từ iron vào môi trường.
c) Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường, dẫn đến việc kim loại bị oxy hóa thành các ion dương.
d) Để bảo vệ các tháp chưng cất dầu mỏ bằng thép, người ta gắn vào mặt trong của tháp các khối hợp kim magnesium (Mg). Khi đó, Mg đóng vai trò là anode hi sinh, sẽ bị ăn mòn trước để bảo vệ thiết bị.
(Xem giải) Câu 21: Để xác định nồng độ acetic acid có trong một mẫu giấm ăn, một nhóm học sinh tiến hành thí nghiệm sau:
• Bước 1: Pha loãng 10,00 mL giấm ăn bằng nước cất trong bình định mức 100,00 mL dung dịch X. Dùng pipet lấy 10,00 mL dung dịch X cho vào bình tam giác rồi thêm vài giọt chất chỉ thị phenolphthalein.
• Bước 2: Tráng sạch buret bằng nước cất, sau đó tráng lại bằng một ít dung dịch NaOH 0,02M. Lắp dụng cụ như hình bên. Cho dung dịch NaOH 0,02M vào cốc thủy tinh, sau đó rót vào buret (đã khóa) và chỉnh về vạch 0.
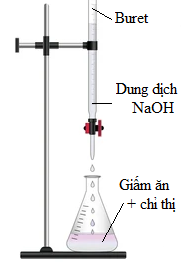
• Bước 3: Vặn khóa buret để dung dịch NaOH trong buret chảy từ từ từng giọt vào bình tam giác đồng thời lắc đều bình. Quan sát đến khi dung dịch trong bình tam giác chuyển từ không màu sang màu hồng bền trong khoảng 20 giây thì dừng lại.
• Bước 4: Ghi lại thể tích dung dịch NaOH đã dùng. Lặp lại thí nghiệm 3 lần.
a) Nếu không tráng buret bằng dung dịch NaOH 0,02 M sau khi rửa bằng nước cất, kết quả nồng độ acetic acid tính được sẽ cao hơn thực tế.
b) Thể tích dung dịch NaOH 0,02 M trong 3 lần thí nghiệm được ghi lại như sau:
| Thí nghiệm | Lần 1 | Lần 2 | Lần 3 |
| Vdd NaOH (mL) | 37,5 | 37,4 | 37,6 |
Nồng độ mol của acetic acid có trong mẫu giấm ăn ban đầu dựa trên các số liệu thực nghiệm là 0,75 M.
c) Trình tự các bước tiến hành thí nghiệm như trên là hoàn toàn hợp lý và đảm bảo tính chính xác về mặt kỹ thuật chuẩn độ.
d) Trong lần thí nghiệm thứ 2, tại thời điểm dung dịch trong bình tam giác đổi màu, thể tích đọc được trên buret là 37,4 mL và có một giọt dung dịch còn treo ở đầu dưới của buret. Một học sinh cho rằng cần lấy giọt dung dịch này vào bình tam giác. Một học sinh khác lại cho rằng nên bỏ giọt dung dịch này. Tại điểm kết thúc chuẩn độ, nếu còn một giọt dung dịch NaOH treo ở đầu buret mà không cho vào bình tam giác thì kết quả tính toán nồng độ acid sẽ bị thấp hơn thực tế.
(Xem giải) Câu 22: Trong quy trình phân tích và thu hồi hóa chất từ nước thải, người ta tách hỗn hợp gồm phenol (C6H5OH) và aniline (C6H5NH2) hòa tan trong dung môi diethyl ether (D ≈ 0,71 g/mL) bằng phương pháp chiết. Quy trình thực hiện như sau:
(1) Lắc hỗn hợp với dung dịch HCl loãng dư;
(2) Tách lớp nước, kiềm hóa để thu hồi aniline;
(3) Chiết lớp hữu cơ còn lại bằng dung dịch NaOH loãng để thu hồi phenol.
a) Khi thực hiện phản ứng với dung dịch Br2 trong môi trường acid mạnh (pH < 1), tốc độ phản ứng thế vào nhân thơm của aniline bị giảm mạnh do nhóm -NH2 bị proton hóa.
b) Một mẫu nước thải có tổng nồng độ phenol và aniline là 0,01 M. Khi cho 100 mL mẫu này tác dụng với Br2 dư, nếu thu được 0,33 gam kết tủa trắng thì có thể khẳng định nồng độ của hai chất trong mẫu là bằng nhau.
c) Về mặt sinh thái, do phenol và aniline đều có khả năng tan một phần trong nước, nên khi xả thải ra sông hồ, chúng sẽ nhanh chóng được pha loãng đến nồng độ vô hại mà không gây độc cho hệ sinh thái thủy sinh.
d) Ở bước (1), sau khi lắc với dung dịch HCl (D ≈ 1,0 g/mL) và để yên, lớp hữu cơ chứa phenol sẽ nổi lên trên, còn lớp nước chứa muối phenylammonium chloride sẽ nằm ở phía dưới.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Trong công nghiệp, giấm ăn được sản xuất bằng phương pháp lên men theo sơ đồ sau:
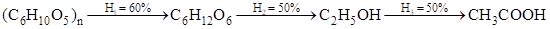
Từ 16,2 tấn sắn chứa 80% tinh bột (còn lại là tạp chất trơ) sản xuất được V (m³) dung dịch giấm ăn có nồng độ acid là 3,2%, khối lượng riêng là 1,0025 gam/cm³. Toàn bộ lượng giấm này được đóng vào các chai 330 ml, sau đó xếp vào các thùng (mỗi thùng 24 chai). Số lượng thùng giấm (làm tròn đến phần nguyên) tối đa thu được là bao nhiêu.
(Xem giải) Câu 24: Cho các phát biểu sau về đơn chất và hợp chất của kim loại nhóm IA, IIA.
1) Trong công nghiệp, baking soda và soda được sản xuất bằng phương pháp Solvay.
2) Trong cùng chu kì, kim loại nhóm IIA có bán kính nguyên tử nhỏ hơn kim loại nhóm IA và khối lượng riêng lớn hơn.
3) Độ bền nhiệt và độ tan trong nước đối với muối carbonate của kim loại nhóm IIA có xu hướng tăng dần từ muối của Mg2+ đến muối của Ba2+.
4) Chỉ dùng quỳ tím làm thuốc thử, có thể phân biệt được 3 dung dịch không màu đựng riêng biệt gồm: Na2CO3, K2SO4 và Ba(NO3)2.
5) Để làm mềm nước cứng tạm thời có thể dùng dung dịch như: xà phòng, giấm (acetic acid), nước vôi trong, sodium carbonate.
Số phát biểu đúng là?
(Xem giải) Câu 25: Có những phản ứng hóa học không cần lò nung hay dòng điện, nhưng chỉ bằng năng lượng hóa học đã có thể tạo ra kim loại nóng chảy ở nhiệt độ lên tới vài nghìn °C; phản ứng nhiệt nhôm là một ví dụ tiêu biểu. Kim loại Fe tạo ra ở trạng thái nóng chảy, dùng để hàn đường ray xe lửa. Phản ứng hóa học xảy ra như sau: 2Al + Fe2O3 → 2Fe + Al2O3.
Cho biết ![]() (Al2O3) = -1675,7 kJ/mol;
(Al2O3) = -1675,7 kJ/mol; ![]() (Fe2O3) = -824,2 kJ/mol. Một mối hàn cần nhiệt lượng thực tế là 426 kJ để làm nóng chảy iron và lấp đầy khe hở. Giả thiết hiệu suất sử dụng nhiệt của quá trình hàn chỉ đạt 80% (20% nhiệt tỏa ra bị thất thoát). Khối lượng hỗn hợp tecmit (Al và Fe2O3 trộn đúng tỉ lệ phản ứng) tối thiểu cần dùng để thực hiện mối hàn trên là bao nhiêu gam? (Làm tròn kết quả đến hàng đơn vị).
(Fe2O3) = -824,2 kJ/mol. Một mối hàn cần nhiệt lượng thực tế là 426 kJ để làm nóng chảy iron và lấp đầy khe hở. Giả thiết hiệu suất sử dụng nhiệt của quá trình hàn chỉ đạt 80% (20% nhiệt tỏa ra bị thất thoát). Khối lượng hỗn hợp tecmit (Al và Fe2O3 trộn đúng tỉ lệ phản ứng) tối thiểu cần dùng để thực hiện mối hàn trên là bao nhiêu gam? (Làm tròn kết quả đến hàng đơn vị).
(Xem giải) Câu 26: Xà phòng, chất giặt rửa được sử dụng rộng rãi trong đời sống: rửa tay, giặt quần áo, rửa chén bát, lau sàn,… Sơ đồ dưới đây mô tả cơ chế giặt rửa của xà phòng và các chất giặt rửa:

Cho các nhận định sau:
(1) Các chất CH3[CH2]10CH2C6H4SO3Na và CH3[CH2]10CH2OSO3Na là chất giặt rửa tổng hợp.
(2) Cấu tạo chung của xà phòng và chất giặt rửa gồm một phần ưa nước nối với một phần kị nước; trong đó phần ưa nước là các gốc hydrocarbon mạch dài tan nhiều trong nước.
(3) Khi xà phòng tan vào nước phần kị nước trong xà phòng thâm nhập vào vết bẩn, phân chia vết bẩn thành những hạt rất nhỏ; phần ưa nước quay ra ngoài, mang theo các vết bẩn phân tán vào nước và bị rửa trôi.
(4) Chất giặt rửa tổng hợp bị giảm hoặc mất tác dụng giặt rửa khi dùng với nước cứng vì tạo kết tủa với cation Ca2+, Mg2+.
(5) Từ dầu mỏ, có thể sản xuất được xà phòng và chất giặt rửa tổng hợp.
Các nhận định đúng gồm những định đề nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 123; 234;.)…
(Xem giải) Câu 27: Xăng E10 là một loại xăng sinh học, được tạo thành khi trộn 10 thể tích C2H5OH (D = 0,8 g/mL) với 90 thể tích xăng truyền thống. Giả sử xăng truyền thống chỉ chứa hai alkane C8H18 và C9H20 (tỉ lệ mol tương ứng 3 : 4, D = 0,7 g/mL). Biết nhiệt lượng tỏa ra khi đốt cháy 1 mol các chất trong xăng E10 như sau:
| Thành phần xăng E10 | C2H5OH | C8H18 | C9H20 |
| Nhiệt tỏa ra kJ/mol | 1365,0 | 5928,7 | 6119,8 |
Trung bình, một chiếc xe máy di chuyển được 1 km thì cần một nhiệt lượng để chuyển thành công cơ học có độ lớn 750 kJ. Nếu chiếc xe máy di chuyển từ “trường THPT Đông Sơn 1” đến “trường THPT chuyên Lam Sơn” với quãng đường được là 15 km thì hết bao nhiêu lít xăng E10 (làm tròn đến hàng phần trăm)? Biết hiệu suất sử dụng nhiên liệu của động cơ xe máy là 40%.
(Xem giải) Câu 28: Để bảo vệ một công trình thép bằng phương pháp hi sinh, kỹ sư cần lựa chọn giữa magnesium (Mg) và zinc (Zn). Biết rằng để cung cấp cùng một điện lượng bảo vệ, khối lượng kim loại tiêu hao thực tế tuân theo công thức: m = Q.M/(n.F.H)
(Q là điện lượng sinh ra, F là hằng số Faraday, H là hiệu suất dòng, n là số electron trao đổi, M khối lượng mol nguyên tử). Trong đó, hiệu suất dòng (H) được xác định dựa trên độ thuần khiết và khả năng chống tự ăn mòn của của kim loại trong môi trường đất: H = (Qlt – Qhp)/Qlt
(Qlt là điện lượng lý thuyết, Qhp là điện lượng tổn hao do phản ứng phụ với môi trường).
Các kỹ sư dùng so sánh hai phương án:
Magnesium (Mg): Do tính hoạt động hóa học mạnh, điện lượng tổn hao do phản ứng phụ chiếm 45% điện lượng lý thuyết. Giá thành: 4,8 USD/kg.
Zinc (Zn): Do tính ổn định cao, điện lượng tổn hao chỉ chiếm 8% điện lượng lý thuyết. Giá thành: 3,2 USD/kg.
Tính tỉ số giữa tổng chi phí khi dùng Zn so với dùng Mg để cung cấp cùng một điện lượng bảo vệ Q (kết quả làm tròn đến hai chữ số thập phân).

Bình luận