[2026] Thi thử TN sở GDĐT Thái Nguyên (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 107
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2B | 3A | 4D | 5B | 6A | 7D | 8A | 9A |
| 10C | 11B | 12A | 13C | 14D | 15C | 16A | 17A | 18D |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | Đ | S |
| (b) | S | S | Đ | Đ |
| (c) | S | Đ | S | S |
| (d) | Đ | Đ | S | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 3 | 38,1 | 2 | 4 | 45,8 | 9,8 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho hỗn hợp các alkane có mạch carbon không phân nhánh: pentane (sôi ở 36°C), heptane (sôi ở 98°C), octane (sôi ở 126°C) và nonane (sôi ở 151°C). Có thể tách riêng các chất đó bằng phương pháp tách và tinh chế nào sau đây?
A. Chưng cất. B. Sắc kí. C. Chiết. D. Kết tinh.
(Xem giải) Câu 2. Trong quá trình điện phân NaCl nóng chảy với các điện cực trơ, ở cathode xảy ra quá trình
A. oxi hóa ion Cl-. B. khử ion Na+. C. khử ion Cl-. D. oxi hóa ion Na+.
(Xem giải) Câu 3. Chất nào sau đây thuộc loại monosaccharide?
A. Fructose. B. Saccharose. C. Tinh bột. D. Cellulose.
(Xem giải) Câu 4. Tên gọi của polymer có công thức (-CH2-CH2-)n là
A. poly(vinyl chloride). B. polystyrene.
C. poly(methyl methacrylate). D. polyethylene.
(Xem giải) Câu 5. Dopamin là một hóa chất quan trọng có trong não, ảnh hưởng đến tâm trạng cũng như cảm giác của bạn về sự hưng phấn, vui vẻ. Vì vậy, dopamine còn được gọi là hormone hạnh phúc. Dopamin có công thức cấu tạo như sau:
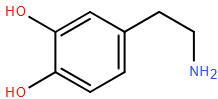
Công thức phân tử của dopamine là
A. C9H14O2N. B. C8H11O2N. C. C9H13O2N. D. C8H9O2N.
(Xem giải) Câu 6. Xà phòng, chất giặt rửa được dùng để loại bỏ các vết bẩn bám trên quần áo, bề mặt các vật dụng. Cho công thức của muối sau:

Phát biểu nào sau đây đúng?
A. Khi thay thế ion Na+ trong muối trên bằng ion K+ thì muối thu được vẫn được dùng làm xà phòng.
B. Có thể điều chế muối trên từ phản ứng giữa (C17H33COO)3C3H5 với dung dịch NaOH vừa đủ.
C. Phần 1 là phần phân cực (ưa nước) và phần 2 là phần không phân cực (kị nước).
D. Muối trên có trong thành phần chính của xà phòng và có tên là sodium palmitate.
(Xem giải) Câu 7. Ở trạng thái cơ bản, cấu hình electron của ion Na+ là 1s2 2s2 2p6. Số hạt mang điện trong nguyên tử Na là
A. 18. B. 11. C. 9. D. 22.
(Xem giải) Câu 8. Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
A. Nhúng thanh Zn vào dung dịch H2SO4 loãng.
B. Nhúng thanh sắt (làm bằng thép) vào dung dịch H2SO4 loãng.
C. Để đinh sắt (làm bằng thép) trong không khí ẩm.
D. Nhúng thanh Zn vào dung dịch hỗn hợp gồm H2SO4 và CuSO4.
(Xem giải) Câu 9. Trong phức chất [Co(OH2)6]2+, 2 phối tử H2O có thể bị thế bởi 2 phối tử OH-. Phát biểu nào sau đây không đúng?
A. Phức chất tạo thành có điện tích là +2.
B. Phức chất tạo thành có 4 phối tử nước và 2 phối tử OH-.
C. Phức chất tạo thành là [Co(OH)2(OH2)4].
D. Phức chất tạo thành có nguyên tử trung tâm là Co2+.
(Xem giải) Câu 10. Cho phương trình nhiệt hóa học: Fe2O3(s) + 2Al(s) → Al2O3(s) + 2Fe(s); ![]() = -851,5kJ. Nhiệt tạo thành chuẩn của Fe2O3(s) là -824,2 kJ/mol. Nhiệt tạo thành chuẩn của Al2O3(s) là bao nhiêu?
= -851,5kJ. Nhiệt tạo thành chuẩn của Fe2O3(s) là -824,2 kJ/mol. Nhiệt tạo thành chuẩn của Al2O3(s) là bao nhiêu?
A. -1524,8 kJ/mol. B. +1524,8 kJ/mol. C. -1675,7 kJ/mol. D. +1675,7 kJ/mol.
(Xem giải) Câu 11. Chất nào sau đây làm giấy quỳ tím ẩm chuyển thành màu xanh?
A. C2H5OH. B. CH3NH2. C. C6H5NH2. D. NaCl.
(Xem giải) Câu 12. Cho các phát biểu sau về quá trình cháy của các hợp chất hữu cơ:
(a) Khí CO là sản phẩm của quá trình cháy không hoàn toàn của các hợp chất hữu cơ.
(b) Trong đám cháy không hoàn toàn, carbon chưa cháy hết dạng hạt có thể tạo ra khói đen.
(c) HCl có thể sinh ra từ các đám cháy có chứa nhựa PVC.
(d) Cách tốt nhất để xử lý rác thải nhựa, túi nylon là đốt cháy hoàn toàn.
Các phát biểu đúng là
A. (a), (b), (c). B. (b), (d). C. (a), (c), (d). D. (a), (c).
(Xem giải) Câu 13. Hệ cân bằng sau được thực hiện trong bình kín: N2(g) + O2(g) ⇋ 2NO(g); ![]() > 0. Cân bằng trên chuyển dịch theo chiều thuận khi
> 0. Cân bằng trên chuyển dịch theo chiều thuận khi
A. giảm áp suất của hệ. B. thêm chất xúc tác vào hệ.
C. tăng nhiệt độ của hệ. D. thêm khí NO vào hệ.
(Xem giải) Câu 14. Ester X được tạo bởi ethyl alcohol và acetic acid. Công thức của X là
A. HCOOC2H5. B. CH3COOCH3. C. HCOOCH3. D. CH3COOC2H5.
(Xem giải) Câu 15. Cho dãy các kim loại: Na, Cu, Al, Cr. Kim loại mềm nhất trong dãy là
A. Cr. B. Cu. C. Na. D. Al.
(Xem giải) Câu 16. Cho các cặp oxi hóa – khử và thế điện cực chuẩn tương ứng
| Cặp oxi hóa – khử | Cr2+/Cr | Cr3+/Cr2+ | Zn2+/Zn | Ni2+/Ni |
| Thế điện cực chuẩn (V) | -0,91 | -0,41 | -0,76 | -0,26 |
Phản ứng nào sau đây đúng?
A. Zn + 2Cr3+ → Zn2+ + 2Cr2+. B. Ni + 2Cr3+ → Ni2+ + 2Cr2+.
C. Zn + Cr2+ → Zn2+ + Cr. D. 3Zn + 2Cr3+ → 3Zn2+ + 2Cr.
(Xem giải) Câu 17. Sodium carbonate là hóa chất quan trọng trong công nghiệp thủy tinh, bột giặt, phẩm nhuộm, giấy, sợi. Công thức của sodium carbonate là
A. Na2CO3. B. NaHCO3. C. CaCO3. D. MgCO3.
(Xem giải) Câu 18. Số nhóm carboxyl (-COOH) trong phân tử alanine là
A. 2. B. 4. C. 3. D. 1.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Oxide của nitrogen là hợp chất trung gian trong công nghiệp sản xuất nitric acid. Cho sơ đồ năng lượng của quá trình tạo thành NO2(g) và N2O4(g) từ các đơn chất:

a) Năng lượng liên kết trong phân tử N2 và O2 lần lượt là 945 kJ/mol và 494 kJ/mol.
b) Phản ứng dimer hoá NO2(g) thành N2O4(g) là phản ứng thu nhiệt, N2O4(g) bền vững hơn NO2(g).
c) Nhiệt tạo thành chuẩn của NO2(g) là 66 kJ/mol.
d) Nhiệt tạo thành chuẩn của N2O4(g) là 11 kJ/mol.
(Xem giải) Câu 20. Trong công nghiệp hiện nay, để hạn chế chất thải ra môi trường và làm tăng hiệu suất của quá trình sản xuất PVC từ ethylene, người ta thực hiện quy trình sản xuất khép kín ứng với các phản ứng (1), (2), (3), (4) theo sơ đồ sau:

a) Để sản xuất 1,0 tấn PVC theo sơ đồ trên với hiệu suất của phản ứng (1), (2), (4) lần lượt là 90%, 85%, 95% thì cần 618,44 kg ethylene (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần trăm).
b) PVC thuộc loại polymer nhiệt rắn, bị phân hủy khi đun nóng.
c) Phản ứng (1) thuộc loại phản ứng cộng, phản ứng (2) thuộc loại phản ứng tách, phản ứng (4) thuộc loại phản ứng trùng hợp.
d) Phản ứng (3) giúp tăng hiệu quả sản xuất và hạn chế gây ô nhiễm môi trường.
(Xem giải) Câu 21. Một nhóm học sinh thực hiện hai thí nghiệm như hình sau đây để khảo sát hiện tượng điện phân và ăn mòn kim loại:

a) Thí nghiệm 1 có sự chuyển hoá điện năng thành hoá năng, thí nghiệm 2 thì ngược lại.
b) Kim loại X, khí Y và khí Z lần lượt là đồng, chlorine và hydrogen.
c) Ở cả hai thí nghiệm, anode là cực dương, cathode là cực âm.
d) Ở thí nghiệm 2 thanh kẽm chỉ xảy ra quá trình ăn mòn điện hoá.
(Xem giải) Câu 22. Ethyl acetate là một ester được sử dụng là dung môi để tách, chiết chất hữu cơ. Hợp chất này được điều chế từ acetic acid, ethanol theo phản ứng và mô hình thí nghiệm sau: CH3COOH + C2H5OH ⇋ CH3COOC2H5 + H2O (∗)
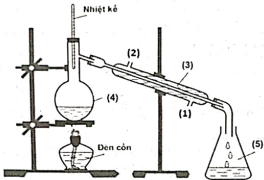
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65 – 70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C. Cho biết nhiệt độ sôi của các hợp chất như sau:
| Hợp chất | C2H5OH | CH3COOH | H2O | CH3COOC2H5 | H2SO4 |
| Nhiệt độ sôi (°C) | 78,3 | 118 | 100 | 77 | 337 |
a) Khi thực hiện đun nóng 6,0 gam acetic acid với 6,0 gam ethanol có H2SO4 đặc làm xúc tác. Khối lượng ester tạo thành với hiệu suất phản ứng 60% là 6,9 gam.
b) Chất lỏng trong bình hứng (5) có ethyl acetate. Vai trò của ống sinh hàn (3) để ngưng tụ hơi, nước vào ở (1) và nước ra ở (2).
c) Ban đầu bình cầu (4) chứa acetic acid, ethanol và sulfuric acid đặc. Nếu nhiệt độ phản ứng ở bình cầu (4) càng cao thì hiệu suất phản ứng điều chế ethyl acetate càng cao.
d) Trong phản ứng (∗) phân tử H2O tạo nên từ -OH trong nhóm –COOH của acetic acid và H trong nhóm –OH của ethanol.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho các chất sau: methane, ethane, ethene, ethyne, propene. Trong số các chất này có bao nhiêu chất có khả năng làm mất màu dung dịch nước bromine?
(Xem giải) Câu 24. Một viên thực phẩm chức năng có khối lượng 250 mg chứa nguyên tố sắt ở dạng muối Fe(II) cùng một số chất khác (giả sử không có tính khử). Kết quả kiểm nghiệm thấy lượng Fe(II) trong viên này phản ứng vừa đủ với 8,5 mL dung dịch KMnO4 0,04M trong môi trường acid H2SO4 loãng, dư. Phần trăm khối lượng của nguyên tố sắt trong viên thực phẩm chức năng trên là x%, giá trị của x là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 25. Kí hiệu “pI” là viết tắt của điểm đẳng điện (isoelectric point) của một chất, thường dùng cho amino acid hoặc protein. pI là giá trị pH mà tại đó phân tử ở dạng lưỡng cực có tổng điện tích bằng 0. Cho biết giá trị pI của một số chất trong bảng dưới đây:
| Amino acid | Glycine | Alanine | Valine | Lysine | Glutamic acid |
| pI ≈ | 6 | 6 | 6 | 9,7 | 3,2 |
Cho lần lượt dung dịch chứa các chất trên vào dung dịch đệm có pH = 6,0 rồi đặt trong điện trường. Có bao nhiêu amino acid di chuyển về phía các điện cực?
(Xem giải) Câu 26. Có bao nhiêu đồng phân cấu tạo có cùng công thức C5H11OH bị oxi hóa không hoàn toàn bởi CuO thu được aldehyde?
(Xem giải) Câu 27. Urea là loại phân đạm có hàm lượng dinh dưỡng cao nhất và được sử dụng phổ biến nhất trên thế giới do có khả năng phát huy tác dụng trên nhiều loại đất khác nhau (kể cả đất nhiễm phèn) và đối với nhiều loại cây trồng khác nhau. Trong quá trình bảo quản, urea dễ bị hút ẩm và chuyển hóa một phần thành (NH4)2CO3. Một loại phân ure chứa 95% (NH2)2CO, còn lại là (NH4)2CO3. Biết độ dinh dưỡng của phân đạm tính bằng phần trăm khối lượng của N tương ứng có trong phân, độ dinh dưỡng của loại phân này là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 28. Trong thực tế, nước Javel được sử dụng rộng rãi để khử trùng nước sinh hoạt, tẩy trắng và vệ sinh bể bơi. Để sản xuất được 100 kg dung dịch nước Javel người ta tiến hành các bước sau:
• Bước 1: Hòa tan m kg NaCl vào nước để tạo thành dung dịch NaCl loãng có nồng độ (15-20%).
• Bước 2: Tiến hành điện phân dung dịch NaCl ở trên với điện cực trơ và không có màng ngăn điện cực.
Giả sử dung dịch nước Javel thu được có nồng độ phần trăm của NaClO là 10%, hiệu suất của cả quá trình đạt 80%. Giá trị của m là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười)

Bình luận