[2026] Thi thử TN sở GDĐT Hưng Yên (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 122
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3D | 4C | 5D | 6D | 7C | 8B | 9A |
| 10A | 11A | 12D | 13D | 14B | 15D | 16A | 17C | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | Đ | Đ |
| (b) | Đ | S | Đ | Đ |
| (c) | Đ | Đ | Đ | S |
| (d) | Đ | Đ | S | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 19,0 | 6 | 3 | 2,42 | 244 | 3 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Ethyl acetate là một ester được sử dụng phổ biến làm dung môi pha sơn, mực in và nước tẩy sơn móng tay nhờ khả năng bay hơi nhanh và hòa tan tốt nhiều chất hữu cơ. Công thức của ethyl acetate là
A. HCOOC2H5. B. C2H5COOCH3. C. CH3COOC2H5. D. CH3COOCH3.
(Xem giải) Câu 2. Trong phân tử chất sau K3[Fe(CN)6], sắt (iron) được gọi là
A. chất khử. B. Phức chất. C. nguyên tử trung tâm. D. phối tử.
(Xem giải) Câu 3. Phản ứng hoá học xảy ra trong pin điện hoá Sn-Cu: Sn + Cu2+ → Sn2+ + Cu. Trong quá trình hoạt động của pin điện hoá, nhận định nào sau đây là đúng?
A. Khối lượng của điện cực Sn tăng. B. Nồng độ Cu2+ trong dung dịch tăng.
C. Khối lượng của điện cực Cu giảm. D. Nồng độ Sn2+ trong dung dịch tăng.
(Xem giải) Câu 4. Bạc được sử dụng trong một số thiết bị điện, linh kiện điện tử chất lượng cao. Nguyên nhân chủ yếu của các ứng dụng trên là
A. bạc có giá rẻ. B. bạc rất nhẹ. C. bạc dẫn điện rất tốt. D. bạc không bị oxi hóa.
(Xem giải) Câu 5. Pin Galvani được coi là nguồn điện hoá học đầu tiên mà con người phát minh ra. Phát biểu nào sau đây sai?
A. Biết thế điện cực chuẩn của cặp oxi hoá – khử Zn2+/Zn là -0,76V và Cu2+/Cu là +0,340V. Sức điện động của pin Galvani Zn-Cu có giá trị bằng 1,10 V.
B. Electron chuyển từ thanh Zn qua dây dẫn đến thanh Cu. Cầu muối đóng vai trò khép kín mạch và trung hoà điện tích của dung dịch ở hai điện cực.
C. Khi pin hoạt động, khối lượng thanh Zn giảm dần.
D. Điện cực âm xảy ra quá trình khử Zn, điện cực dương xảy ra quá trình oxi hóa ion Cu2+.
(Xem giải) Câu 6. Hiện tượng phú dưỡng là một biểu hiện của môi trường ao, hồ bị ô nhiễm do dư thừa các chất dinh dưỡng. Sự dư thừa dinh dưỡng chủ yếu do hàm lượng các ion nào sau đây vượt quá mức cho phép?
A. Sodium, potassium. B. Calcium, magnesium.
C. Chloride, sulfate. D. Nitrate, phosphate.
(Xem giải) Câu 7. Amphetamine (còn được gọi là hồng phiến) là một dạng chất ma tuý có cấu tạo như sau:
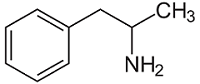
Chọn phát biểu đúng?
A. Đốt cháy hoàn toàn 0,1 mol amphetamine thu được 0,1 mol N2.
B. Công thức phân tử của amphetamine C9H12N.
C. Amphetamine là amine bậc 1.
D. 1 mol amphetamine tác dụng tối đa với 2 mol HCl.
(Xem giải) Câu 8. Cho phản ứng: CH4(g) + 3Cl2(g) → CHCl3(g) + 3HCl(g). Biết năng lượng liên kết của một số liên kết như sau:
| Liên kết | C-H | Cl-Cl | H-Cl | C-Cl |
| Eb (kJ/mol) | 414 | 243 | 431 | 339 |
Biến thiên enthalpy phản ứng là
A. -113 kJ. B. -339 kJ. C. -226 kJ. D. -452 kJ.
(Xem giải) Câu 9. Chất nào sau đây khi phản ứng với HCl chỉ cho 1 sản phẩm duy nhất?
A. CH3-CH=CH-CH3. B. CH2=C(CH3)-CH2-CH3.
C. CH2=C(CH3)2. D. CH2=CH-CH2-CH3.
(Xem giải) Câu 10. Cho các quá trình tạo phức chất bát diện sau: [Fe(OH2)6]3+(aq) + SCN−(aq) → [Fe(OH2)x(SCN)]2+(aq) + H2O(l). Giá trị của x là
A. 5. B. 2. C. 4. D. 3
(Xem giải) Câu 11. Cho hình vẽ mô tả thí nghiệm điều chế kim loại bằng cách dùng khí H2 để khử oxide kim loại:

Thí nghiệm trên dùng phương pháp gì để điều chế kim loại?
A. Nhiệt luyện. B. Điện phân dung dịch.
C. Điện phân nóng chảy. D. Thủy luyện.
(Xem giải) Câu 12. Trong thực tế, đã xảy ra nhiều vụ ngộ độc do người dân sử dụng nhầm cồn công nghiệp chứa methanol thay cho rượu uống (C2H5OH), đặc biệt là các loại rượu không rõ nguồn gốc. Hậu quả xảy ra rất nghiêm trọng như mù mắt, tổn thương não và thậm chí tử vong. Trong phạm vi thí nghiệm hóa học phổ thông, phương pháp phân biệt được cồn công nghiệp và rượu uống một cách an toàn và chính xác là:
A. ngửi trực tiếp để phân biệt mùi. B. quan sát màu sắc bằng mắt thường.
C. nếm thử để nhận biết vị. D. dùng phản ứng iodoform (I2/NaOH) để kiểm tra.
(Xem giải) Câu 13. Trong các cách sau, cách nào giúp bảo vệ kim loại bằng phương pháp điện hóa?
A. Dùng chất chống gỉ hóa học.
B. Phủ sơn cách ly.
C. Đánh bóng bề mặt kim loại.
D. Nối kim loại cần bảo vệ với kim loại hoạt động mạnh hơn.
(Xem giải) Câu 14. Chất nào sau đây có nhiệt độ sôi cao nhất
A. CH3Cl B. CH3COOH C. C2H5OH D. C2H2
(Xem giải) Câu 15. Khi tắm bằng nước giếng, một người nhận thấy da bị khô và tóc trở nên xơ cứng. Kết quả kiểm tra cho thấy nước chứa nhiều ion Ca2+, Mg2+ dạng muối sulfate và chloride (nước cứng vĩnh cửu). Biện pháp đơn giản và hiệu quả nhất để cải thiện tình trạng này là
A. thêm xà phòng nhiều hơn khi tắm. B. giảm lượng nước sử dụng.
C. dùng nước đã đun sôi để nguội để tắm. D. thêm một lượng nhỏ Na2CO3 vào nước.
(Xem giải) Câu 16. Xét cân bằng: C(s) + H2O(g) ⇋ CO(g) + H2(g). Biểu thức hằng số cân bằng của hệ là
A. Kc = [CO][H2]/[H2O]. B. Kc = [CO][H2]/[C][H2O]
C. Kc = [CO][H2]. D. Kc = ([CO] + [H2])/([C] + [H2O])
(Xem giải) Câu 17. Glucose tác dụng với Cu(OH)2 cho dung dịch màu xanh lam chứng tỏ phân tử glucose có
A. 5 nhóm -OH. B. 6 nguyên tử C.
C. nhiều nhóm hydroxyl liền kề. D. nhóm chức -CHO.
(Xem giải) Câu 18. Năm 1897, khi nghiên cứu hiện tượng phóng điện trong chân không, nhà bác học J. J. Thomson nhận thấy sự xuất hiện của một loại tia bị lệch về bản dương của điện trường nên tia này có thể được cấu tạo từ các tiểu phân mang điện âm. Từ đó, J. J. Thomson đã phát hiện ra tia âm cực có bản chất là dòng … chuyển động với tốc độ cao. Từ điền vào “…” là:
A. điện. B. hạt proton. C. hạt electron. D. hạt neutron.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. PBS – Poly(butylene succinate), có tên thương mại Bionolle, là một polymer phân huỷ sinh học (bioplastic) có tính dẻo và bền nhiệt tương tự polyethylene (PE). Nhờ cấu trúc mạch chính chứa các nhóm ester, PBS có khả năng phân rã trong môi trường tự nhiên. Với đặc tính này, PBS được ứng dụng rộng rãi trong sản xuất bao bì và túi nylon thân thiện với môi trường, trở thành giải pháp tiềm năng thay thế các loại nhựa truyền thống khó phân huỷ. PBS được tổng hợp từ hai monomer sau:
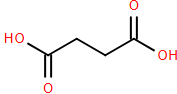
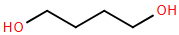
a) Phản ứng tổng hợp PBS thuộc loại phản ứng trùng ngưng.
b) PBS tạo bởi acid có tên thay thế là butane-1,4-dioic acid.
c) Khối lượng của một mắt xích PBS là 172 amu.
d) PBS có khả năng bị thuỷ phân trong môi trường acid.
(Xem giải) Câu 20. Một dung dịch mẫu A chứa hỗn hợp hai muối Fe2+ và Fe3+ được phân tích bằng phương pháp chuẩn độ oxi hóa – khử với dung dịch thuốc tím (KMnO4) trong môi trường acid. Quy trình được thực hiện qua 2 giai đoạn:
Giai đoạn 1: Chuẩn độ trực tiếp
• Lấy 4,0 mL mẫu A, pha loãng bằng nước cất sau đó thêm 2 mL dung dịch H2SO4 0,5 M rồi chuẩn độ bằng dung dịch KMnO4, xác định được lượng Fe2+ ban đầu là 2,54 mmol.
Giai đoạn 2: Chuẩn độ sau khi khử
• Lấy 20,0 mL mẫu A, thêm vào 10 mL dung dịch H2SO4 0,5 M sau đó cho hỗn hợp đi qua cột khử chứa Zn hạt để chuyển toàn bộ Fe3+ về dạng Fe2+. Rửa sạch hóa chất trên cột khử bằng nước cất sau đó pha loãng để được 50 mL dung dịch B. Lấy 10 mL dung dịch B và tiến hành chuẩn độ bằng dung dịch KMnO4, xác định được tổng lượng sắt (bao gồm cả Fe2+ và Fe3+) là 3,58 mmol.
a) Nồng độ (mol/L) của Fe3+ có trong mẫu A là 0,26 M.
b) Ion Zn2+ hình thành từ cột khử ở giai đoạn 2 ảnh hưởng đến kết quả của phép chuẩn độ dung dịch B bằng dung dịch KMnO4 nên cần loại bỏ trước khi chuẩn độ.
c) Dung dịch sau khi đi qua cột khử có lượng dư acid nên không tạo được Fe kim loại.
d) Trong quá trình chuẩn độ không cần dùng chất chỉ thị vì KMnO4 đóng vai trò chỉ thị trực tiếp cho phản ứng.
(Xem giải) Câu 21. Công đoạn chính của công nghiệp chlorine – kiềm là điện phân dung dịch sodium chloride bão hòa trong bể điện phân có màng ngăn xốp. Phương trình hóa học của phản ứng điện phân dung dịch có màng ngăn như sau: 2NaCl(aq) + 2H2O(l) → 2NaOH(aq) + H2(g) + Cl2(g)
a) Khí H2 thoát ra được dùng làm nguyên liệu sản xuất HCl, NH3, nhiên liệu sạch,…
b) Sản phẩm cơ bản của công nghiệp chlorine – kiềm là sodium hydroxide, chlorine và hydrogen.
c) Khí thoát ra ở cathode là H2, khí thoát ra ở anode là Cl2.
d) Nếu điện phân không màng ngăn thu được nước Javel. Một loại nước Javel (có D = 1,15 g/mL) được bán trên thị trường với chai dung tích 1,0 L gồm các chất NaClO, NaCl và NaOH có nồng độ lần lượt là 10%; 8% và 0,8%. Để sản xuất 800 chai nước Javel ở trên cần 784 kg dung dịch NaCl 19,5%. (chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
(Xem giải) Câu 22. Để nghiên cứu sự thủy phân của methyl acetate, một nhóm học sinh pha 500 mL dung dịch hỗn hợp gồm methyl acetate (có nồng độ là 0,4M) và nước với xúc tác H2SO4. Hỗn hợp được chia vào các ống nghiệm kín (mỗi ống lấy 5 mL), đặt trong bể điều nhiệt.
Tại thời điểm t = 0, một ống được lấy ra chuẩn độ ngay để xác định lượng NaOH cần dùng để trung hòa riêng xúc tác H2SO4 (kí hiệu là V₀). Tại các thời điểm t tiếp theo, lấy các ống còn lại ra và chuẩn độ bằng NaOH 0,1 M (kí hiệu là Vt). Kết quả thu được như sau:
| t (phút) | 10 | 20 | 40 | 60 | 100 | 150 | 200 | |
| V(NaOH) (mL) | 2,00 | 6,20 | 9,70 | 13,80 | 15,00 | 15,34 | 15,34 | 15,34 |
Để giải thích dữ liệu này, ba mô hình được đề xuất:
• Mô hình I: Phản ứng xảy ra một chiều và hoàn toàn.
• Mô hình II: Phản ứng thuận nghịch, tiến tới trạng thái cân bằng hóa học.
• Mô hình III: Phản ứng một chiều nhưng dừng lại sớm do xúc tác H+ bị mất hoạt tính.
a) Mô hình III không phù hợp vì xúc tác H+ ở trong dung dịch không bị biến tính và cũng không bị mất đi sau phản ứng.
b) Theo Mô hình I, nếu phản ứng xảy ra hoàn toàn, thể tích dung dịch NaOH 0,1 M cần dùng tại thời điểm phản ứng kết thúc phải là 22,00 mL. Do đó mô hình I là không phù hợp.
c) Tại thời điểm 100 phút, phản ứng đã đạt trạng thái cân bằng; lúc này nồng độ methyl acetate còn lại trong ống nghiệm là 0,153 M.
d) Thể tích V₀ = 2,00 mL là lượng NaOH cần dùng để trung hòa H2SO4 sử dụng làm chất xúc tác.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Pin nhiên liệu sử dụng ethanol được quan tâm vì ethanol là nguồn nhiên liệu sinh học dồi dào. Phản ứng tổng quát xảy ra trong pin ethanol – oxygen là: C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l). Một pin ethanol – oxygen được dùng để thắp sáng liên tục 6 bóng đèn LED, mỗi bóng có công suất 5 W (5 J/s) và 2 bóng LED, mỗi bóng có công suất 3 W. Sau một thời gian hoạt động t (giờ), pin tiêu thụ hết 184 gam ethanol. Biết rằng: 50% nhiệt lượng do phản ứng trên sinh ra ở điều kiện chuẩn được chuyển hóa thành điện năng; 10% điện năng bị hao phí trên đường truyền trước khi đến các bóng đèn.
• Nhiệt tạo thành chuẩn của các chất như sau:
| Chất | C2H5OH(l) | O2(g) | CO2(g) | H2O(l) |
| -277,6 | 0,0 | -393,5 | -285,8 |
Tính giá trị của t. (Chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 24. Thủy phân không hoàn toàn một heptapeptide X mạch hở, không phân nhánh, thu được các tripeptide sau: Ala-Ser-Gly; Ser-Gly-Leu; Gly-Leu-Tyr; Leu-Tyr-Val; Tyr-Val-Asp. Biết mỗi đoạn peptide trên xuất hiện đúng một lần trong X. Nếu đánh số amino acid đầu N là 1, hỏi valine (Val) ở vị trí số mấy trong X?
(Xem giải) Câu 25. Cho các chất sau: HCHO; CH3CHO; C2H5OH; CH3COOH; HOCH2CHO; CH3COCH3. Có bao nhiêu chất trong dãy phản ứng với thuốc thử Tollens tạo bạc kim loại?
(Xem giải) Câu 26. Trong một nhà máy tái chế kim loại, người ta xử lí 18,40 tấn phế liệu đồng thau (hợp kim Cu–Zn). Phân tích cho thấy zinc (Zn) chiếm 12,50% khối lượng phế liệu ban đầu. Sau quá trình tinh luyện, thu được 16,55 tấn hợp kim. Biết rằng trong quá trình này, một phần zinc bị tách ra dưới dạng oxide trong xỉ, một phần dưới dạng bay hơi, phần còn lại nằm trong hợp kim. Tổng khối lượng Zn (tính theo nguyên tố) được tách ra khỏi hợp kim là 1,60 tấn trong xỉ và 0,30 tấn trong khí thải. Phần trăm khối lượng Zn còn lại trong hợp kim sau tinh luyện là a%. Tính a. (Chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)
(Xem giải) Câu 27. Các hợp chất của copper (II) được sử dụng rộng rãi trong nông nghiệp như thuốc trừ sâu, diệt nấm. Một ví dụ điển hình là copper(II) sulfate pentahydrate (CuSO4.5H2O), còn gọi là đá xanh. Trong phòng thí nghiệm, một học sinh tiến hành điều chế tinh thể CuSO4.5H2O từ copper(II) oxide theo các bước sau:
• Hòa tan hoàn toàn 1,5 mol CuO bằng một lượng vừa đủ dung dịch H2SO4 20%, đun nóng để phản ứng xảy ra hoàn toàn, thu được dung dịch X.
• Trong quá trình đun nóng, có 40 gam nước bị bay hơi khỏi dung dịch; ngoài nước bay hơi, không có chất nào khác bị thất thoát.
• Làm lạnh dung dịch X đến 10°C, khi đó tinh thể CuSO4 ⋅ 5H2O tách ra và dung dịch còn lại là dung dịch bão hòa ở 10°C.
Biết rằng ở 10°C, cứ 100 gam nước hòa tan tối đa 17,2 gam CuSO4. Tính khối lượng (g) tinh thể CuSO4.5H2O thu được. (Không làm tròn ở các bước trung gian; kết quả cuối cùng làm tròn đến hàng đơn vị)
(Xem giải) Câu 28. Cho các chất sau: C6H6; C6H5CH3; C6H5OH; C6H12; CH3CH2OH. Có bao nhiêu chất trong dãy có thể tham gia phản ứng thế bromine (xúc tác FeBr3) vào vòng benzene?

Bình luận