[2026] Thi thử TN cụm chuyên môn số 10 Đắk Lắk
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 121
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2A | 3D | 4D | 5A | 6C | 7D | 8B | 9D |
| 10C | 11C | 12D | 13B | 14C | 15A | 16B | 17D | 18A |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | Đ | S |
| (b) | S | Đ | S | S |
| (c) | S | S | Đ | Đ |
| (d) | Đ | S | S | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 214 | 70,6 | 42,7 | 2314 | 6 | 21,5 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Tyrosine là một trong những loại amino acid cần thiết và có thể bổ sung cho cơ thể thông qua các thực phẩm ăn uống hàng ngày. Tyrosine làm tăng mức độ chất dẫn truyền thần kinh dopamine, adrenaline và norepinephrine giúp điều chỉnh tâm trạng, cải thiện trí nhớ, giúp tỉnh táo đầu óc và tăng khả năng tập trung. Với mỗi môi trường có giá trị pH bằng 0,10; 5,65; 9,59 và 12,90, coi tyrosine chỉ tồn tại ở dạng cho dưới đây:
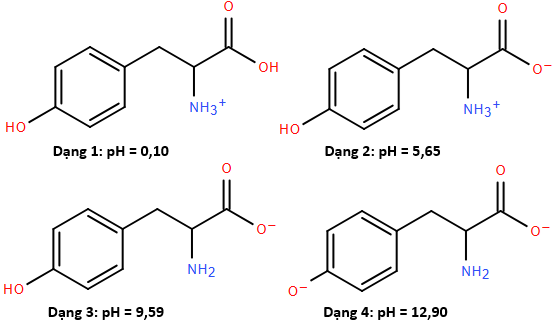
Trong quá trình điện di, ion sẽ chuyển về phía điện cực trái dấu với ion. Giá trị pH bằng bao nhiêu thì tyrosine hầu như không di chuyển trong điện trường?
A. 12,90. B. 0,10. C. 5,65. D. 9,59.
(Xem giải) Câu 2. Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO3 tồn tại cân bằng sau: NaCl + NH3 + CO2 + H2O ⇌ NaHCO3 + NH4Cl. Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
A. NaHCO3. B. NH4HCO3. C. NH4Cl. D. NaCl.
(Xem giải) Câu 3. Reforming heptane theo phản ứng sau
![]()
Hệ số cân bằng trước H2 của phương trình trên là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 4. Nước muối sinh lí là dung dịch của chất X với nồng độ 0,9%, được dùng trong việc ngăn ngừa nguy cơ mất muối do đổ quá nhiều mồ hôi, sau phẫu thuật, mất muối do tiêu chảy hay các nguyên nhân khác. X là muối nào sau đây?
A. Na2SO4. B. NaNO3. C. NaClO. D. NaCl.
(Xem giải) Câu 5. Phức chất cisplatin được dùng làm thuốc chữa bệnh ung thư có công thức phân tử là [PtCl2(NH3)2]. Số loại phối tử trong phức chất là
A. 2. B. 5. C. 3. D. 4.
(Xem giải) Câu 6. Để điều chế kim loại barium (Ba) từ hợp chất BaCl2, phương pháp nào sau đây là phù hợp nhất?
A. Nhiệt luyện. B. Thủy luyện. C. Điện phân nóng chảy. D. Điện phân dung dịch.
(Xem giải) Câu 7. Cellulose là polysaccharide có nhiều trong gỗ, bông, đay, gai,… tập trung ở thành tế bào thực vật. Phát biểu nào sau đây không đúng về cellulose?
A. Thuỷ phân hoàn toàn trong môi trường acid thu được glucose.
B. Là thành phần chính của bông nõn.
C. Được dùng làm vật liệu xây dựng, sản xuất đồ gỗ, vải sợi, giấy.
D. Tan được trong nước và các dung môi thông thường.
(Xem giải) Câu 8. Cách nào sau đây không làm mềm được nước có tính cứng vĩnh cửu?
A. Dùng Na2CO3. B. Đun nóng. C. Dùng nhựa cationite. D. Dùng Na3PO4.
(Xem giải) Câu 9. Phổ khối lượng (MS) là phương pháp để xác định phân tử khối của các hợp chất hữu cơ. Trên phổ khối lượng của ester X xác định được peak ion phân tử [X+] có giá trị m/z lớn nhất bằng 88. Chất X là
A. methyl acetate. B. methyl formate. C. vinyl acetate. D. ethyl acetate.
(Xem giải) Sử dụng dữ kiện cho dưới đây để trả lời các câu 10 – 11
Thiết lập pin Galvani gồm thanh Cu nhúng vào cốc đựng dung dịch CuSO4 1M và thanh Zn nhúng vào cốc đựng dung dịch ZnSO4 1M, ở 25°C. Nối hai thanh bằng dây dẫn, lắp một vôn kế để đo hiệu điện thế. Đóng kín mạch bằng cầu muối dung dịch KNO3 bão hoà. Sơ đồ của pin Zn-Cu được mô tả như hình bên.

Câu 10. Vai trò của cầu muối KNO3 là
A. chuyển ion SO42- từ dung dịch anode sang dung dịch cathode.
B. chuyển các ion Cu2+ từ dung dịch cathode sang dung dịch anode.
C. trung hòa điện tích ở hai dung dịch khi pin hoạt động
D. chuyển electron từ cathode sang anode.
Câu 11. Cho các kết luận sau:
(a) Nếu thế điện cực chuẩn của cặp Cu2+/Cu là 0,34V thì thế điện cực chuẩn của cặp Zn2+/Zn là 0,762V.
(b) Sức điện động của pin duy trì ổn định trong suốt thời gian pin hoạt động.
(c) Khi pin hoạt động, khối lượng dung dịch của hai điện cực không thay đổi.
(d) Trong quá trình pin hoạt động, khối lượng thanh Zn giảm và khối lượng thanh Cu tăng.
Số kết luận đúng là
A. 2. B. 3. C. 1. D. 4.
(Xem giải) Câu 12. Một loại hợp kim của iron trong đó có nguyên tố C chiếm ít hơn 2,0% và một lượng rất ít các nguyên tố Cr, Mn, Si,… Hợp kim đó là
A. gang trắng. B. gang xám. C. duralumin. D. thép.
(Xem giải) Câu 13. Acid béo omega-3 và omega-6 là các acid béo không no với liên kết đôi đầu tiên ở vị trí số 3 và 6 khi đánh số từ nhóm methyl. Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ thể, giúp phòng ngừa nhiều loại bệnh. Chất nào sau đây thuộc loại acid béo omega-3?
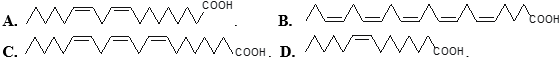
(Xem giải) Câu 14. Sulfur được dùng để sản xuất sulfuric acid, phân bón, thuốc trừ sâu, lưu hoá cao su, diêm, dược phẩm và là nguyên tố cần thiết cho cơ thể sinh vật. Nguyên tử của nguyên tố sulfur có 16 electron. Ở trạng thái cơ bản, sulfur có số orbital chứa electron là
A. 8. B. 10. C. 9. D. 6.
(Xem giải) Câu 15. Khi phân cắt dị li liên kết C-X, tiểu phân trung gian mang điện tích dương trên nguyên tử carbon được gọi là carbocation. Độ bền của carbocation phụ thuộc vào cấu trúc của chúng. Carbocation chứa nguyên tử carbon mang điện tích dương liên kết với càng nhiều nhóm alkyl thì càng bền. Carbocation nào sau đây bền nhất?
A. (CH3)3C+. B. H3C+. C. (CH3)2HC+. D. CH3H2C+.
(Xem giải) Câu 16. Cho cân bằng hoá học sau xảy ra trong bình kín:
2SO2(g) + O2(g) ⇌ 2SO3(g) ![]() = −197,8 kJ.
= −197,8 kJ.
Khi tác động một trong các yếu tố sau thì yếu tố nào sẽ làm cho cân bằng chuyển dịch theo chiều thuận?
A. Tăng nhiệt độ. B. Tăng áp suất.
C. Thêm chất xúc tác. D. Tăng thể tích bình.
(Xem giải) Câu 17. Bậc của amine được tính bằng số gốc hydrocarbon liên kết trực tiếp với nguyên tử N. Amine nào sau đây là amine bậc ba?
A. CH3NH2. B. C2H5NH2. C. (CH3)2NH. D. (CH3)3N.
(Xem giải) Câu 18. Insulin là hoocmon của cơ thể có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide (X). Khi thủy phân không hoàn toàn X thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu; Val-Glu-Ala; His-Leu-Val; Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là số 1 thì amino acid ở vị trí số 3 và số 7 lần lượt là
A. His và Ala. B. Ser và Glu. C. Val và His. D. Gly và Leu.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Nhựa là một loại vật liệu có nhiều ứng dụng trong đời sống. Dưới đáy chai hoặc các vật dụng bằng nhựa thường có kí hiệu các con số. Số 3 là loại đang được sử dụng để sản xuất đồ nhựa như ống dẫn nước, vải che mưa… Ở nhiệt độ cao, nhựa số 3 bị phân hủy, có mùi hôi và gây ngộ độc. Số 2 là loại nhựa mềm, nóng chảy trên 110°C, có tính khá trơ với môi trường acid, kiềm, dầu mỡ, được dùng phổ biến làm màng mỏng, bình chứa…

a) Nhựa số 2 được đánh giá an toàn cho sức khỏe, có thể sản xuất đồ dùng đựng thực phẩm.
b) Nhựa số 3 điều chế từ phản ứng trùng ngưng vinyl chloride và nhựa số 2 điều chế từ phản ứng trùng ngưng 6-aminohexanoic acid.
c) Trong 1,875 gam nhựa số 3 có khoảng 1,806.10E20 mắt xích.
d) Khi chịu tác dụng của nhiệt độ hoặc áp lực bên ngoài, hai loại nhựa trên bị biến dạng và vẫn giữ nguyên sự biến dạng đó khi thôi tác dụng.
(Xem giải) Câu 20. Một kỹ sư hóa học làm việc tại một nhà máy luyện kim đang kiểm tra chất lượng của một lô quặng sắt trước khi đưa vào lò cao. Anh ta lấy 10 gam mẫu chứa Fe3O4, Fe2O3 và các tạp chất trơ. Hòa tan mẫu vào luợng dư dung dịch H2SO4 10% thu được dung dịch A. Pha loãng dung dịch A đến thể tích 50 mL.
• Thí nghiệm 1: Cho 10 mL dung dịch A tác dụng với dung dịch NaOH dư thu được 2,59 gam kết tủa.
• Thí nghiệm 2: Lấy 10 mL dung dịch A đem đi chuẩn độ bằng dung dịch chuẩn KMnO4 0,1 M .Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích dung dịch KMnO4 (mL) | 10,0 | 10,1 | 10,0 |
a) Có thể thay dung dịch H2SO4 bằng dung dịch acid mạnh như HCl, HNO3 nhưng phải đảm bảo lượng H+ dư sau phản ứng.
b) Thời điểm kết thúc chuẩn độ ở thí nghiệm 2 là dung dịch trong bình tam giác xuất hiện màu hồng nhạt, bền trong trong khoảng 20s.
c) Quan sát màu sắc kết tủa trong thí nghiệm 1 thấy màu trắng hơi xanh.
d) Phần trăm khối lượng Fe2O3 trong mẫu ban đầu là 56%. (kết quả làm tròn đến hàng đơn vị)
(Xem giải) Câu 21. Aspirin (hay acetylsalicylic acid) là một dẫn xuất của salicylic acid được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp. Một nhóm học sinh thực hiện tổng hợp Aspirin trong phòng thí nghiệm theo các bước:
• Bước 1: Cho 55,0 gam salicylic acid khan và 80,0 mL acetic anhydride (d = 1,08 g/mL) vào bình cầu 250 mL; thêm 4,0 ml sulfuric acid đặc vào và lắc kĩ. Sau đó, khuấy khối phản ứng ở 50 – 60°C trong khoảng 45 phút cho đến khi tan hết phần chất rắn.
• Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10°C. Cho hỗn hợp vào cốc lớn, thêm từ từ 750 ml nước cất và khuấy kỹ, aspirin sẽ kết tủa. Lọc lấy sản phẩm bằng phễu lọc Buchner.
• Bước 3: Hòa tan aspirin thô trong 100 ml ethanol 90°, đun nóng để tan hoàn toàn, sau đó đổ dung dịch này từ từ vào 450 ml nước nóng khoảng 50°C, đun nóng nhẹ cho chất rắn tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin kết tinh dưới dạng tinh thể, lọc và hút hết nước, sấy khô ở 50°C.
• Bước 4: Cân sản phẩm thu được 52,4 gam aspirin.
Biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau
HOC6H4COOH + (CH3CO)2O → CH3COOC6H4COOH + CH3COOH
salicylic acid acetic anhydride aspirin
a) Hiệu suất của quá trình tổng hợp aspirin ở thí nghiệm trên đạt 73%. (kết quả làm tròn đến hàng đơn vị)
b) Aspirin có khả năng tham gia phản ứng với dung dịch NaOH dư theo tỉ lệ mol 1 : 2.
c) Phương pháp tách và tinh chế aspirin ở trên là phương pháp kết tinh.
d) Aspirin tan trong nước nhiều hơn salicylic acid.
(Xem giải) Câu 22. Sau một thời gian sử dụng các lan can bằng thép bắt đầu xuất hiện lớp gỉ nâu đỏ. Quan sát kĩ cho thấy trên bề mặt kim loại luôn có một lớp nước mỏng do hơi ẩm ngưng tụ, trong đó đã hòa tan O2 và CO2. Lớp nước này tạo môi trường điện li, làm phát sinh nhiều pin điện hóa rất nhỏ trên bề mặt lan can, khiến sắt bị oxi hóa dần và hình thành gỉ. Hình ảnh bên cạnh mô tả về sự ăn mòn của gang, thép trong không khí ẩm.
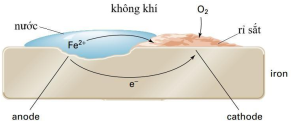
a) Quá trình ăn mòn tạo nên vô số pin điện hóa rất nhỏ mà anode là carbon và cathode là sắt.
b) Các đồ vật bằng gang, thép để trong không khí khô, quá trình ăn mòn xảy ra tương tự khi để trong không khí ẩm.
c) Tại cathode xảy ra quá trình khử: O2(g) + 2H2O(l) + 4e → 4OH-(aq).
d) Lớp gỉ sắt có thành phần chính là Fe2O3.nH2O.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Bisphenol A được dùng nhiều trong công nghiệp điều chế nhựa epoxy và được điều chế theo sơ đồ sau:

Hydrocarbon M có công thức đơn giản nhất là C3H4. Sự hiện diện bất thường của X trong nước tiểu người là một dấu hiệu của bệnh tiểu đường và được phát hiện qua việc xét nghiệm chỉ số KET (viết tắt của KETONE). Tổng phân tử khối của M và Y là bao nhiêu?
(Xem giải) Câu 24. Giá trị phần trăm khối lượng của C trong phân tử sodium stearate là bao nhiêu? (làm tròn đến phần mười).
(Xem giải) Câu 25. Formaldehyde là một hoá chất quan trọng, có thể điều chế bằng phương pháp dehydrogen hoá methanol (trong điều kiện nhiệt độ khoảng 700°C, sử dụng chất xúc tác thích hợp).
CH3OH(g) ⟶ HCHO(g) + H2(g) ![]() = 84,2 kJ (1)
= 84,2 kJ (1)
Nhiệt để duy trì phản ứng (1) được lấy từ phản ứng giữa H2 với O2 của không khí theo phản ứng:
H2(g) + ½O2 (g) ⟶ H2O(g) ![]() = -241,8 kJ (2)
= -241,8 kJ (2)
Tính % thể tích methanol trong hỗn hợp gồm methanol và không khí đưa vào để phản ứng (1) tự duy trì ở 700°C. Biết rằng oxygen chiếm 20% thể tích không khí và phản ứng hết; lượng nhiệt mà nitrogen đã hấp thụ chiếm 35% lượng của phản ứng (2). (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 26. Thực hiện các thí nghiệm về tính chất của một số hợp chất hữu cơ, được đánh số thứ tự như sau:
(1) Cho vài giọt dung dịch aniline loãng vào ống nghiệm chứa nước bromine.
(2) Thêm vài giọt dung dịch HNO3 đặc vào ống nghiệm chứa 2 mL dung dịch lòng trắng trứng.
(3) Nhỏ vài giọt iodine vào ống nghiệm chứa 2 mL dung dịch hồ tinh bột 1%.
(4) Cho 2 mL dung dịch glucose 2% vào ống nghiệm chứa dung dịch AgNO3 trong NH3, đun nhẹ.
Hãy gán số thứ tự của các thí nghiệm trên lần lượt theo các hiện tượng của phản ứng: a) chất rắn màu vàng; b) màu xanh tím; c) kết tủa trắng; d) lớp kim loại sáng bóng bám lên thành ống nghiệm. (Sắp xếp theo trình tự thành dãy bốn số, ví dụ 1234, 4321…).
(Xem giải) Câu 27. Số liên kết cho – nhận mà nguyên tử trung tâm Fe3+ tạo được với phối tử aqua trong phức chất [Fe(OH2)6]3+ là bao nhiêu?
(Xem giải) Câu 28. Một trong những phương pháp thông dụng để bảo vệ kim loại khỏi sự ăn mòn đó là phủ lên kim loại cần bảo vệ một lớp kim loại khác, đó là phương pháp mạ kim loại. Người ta muốn mạ một lớp kim loại nickel có bề dày 200 μm lên bề mặt một thanh kim loại hình trụ có bán kính 20 mm và chiều cao 0,5m bằng phương pháp điện phân. Bình điện phân được thiết kế cho thí nghiệm này chứa 5,4025 kg NiSO4.7H2O và 7,2 lít nước với cathode là thanh kim loại cần mạ và anode là điện cực graphite. Cường độ dòng điện dùng để điện phân là 2,2 A. Cho biết khối lượng riêng của Ni là 8,9 g/cm³, khối lượng riêng của nước là 1,0 g/cm³, π = 3,14. Giả sử quá trình điện phân lượng nước bay hơi không đáng kể. Xác định nồng độ % của dung dịch NiSO4 trong bình điện phân tại thời điểm kết thúc điện phân? (Làm tròn kết quả đến hàng phần mười)

Bình luận