[2026] Thi thử TN sở GDĐT Lào Cai (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 070
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2D | 3A | 4C | 5B | 6D | 7C | 8C | 9B |
| 10D | 11B | 12C | 13B | 14C | 15A | 16C | 17D | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | S | S | Đ | 24 | 84 | 22,6 |
| (b) | S | Đ | S | S | 26 | 27 | 28 |
| (c) | Đ | S | Đ | S | 4 | 177 | 1,46 |
| (d) | S | Đ | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Chất nào sau đây chứa liên kết cộng hoá trị trong phân tử?
A. KF. B. MgO. C. NaCl. D. HCl.
(Xem giải) Câu 2. Phản ứng chlorine hóa methane khi chiếu sáng xảy ra theo cơ chế gốc gồm ba giai đoạn: khơi mào, phát triển mạch và tắt mạch. Trong đó, giai đoạn phát triển mạch diễn ra như sau:
Cl• + CH4 → HCl + •CH3
•CH3 + Cl2 → CH3Cl + Cl•
Nhận định nào sau đây không đúng về giai đoạn này?
A. Có sự hình thành liên kết H-Cl.
B. Có sự hình thành liên kết C-Cl.
C. Có sự phân cắt liên kết C-H.
D. Có sự hình thành liên kết π.
(Xem giải) Câu 3. Thí nghiệm nào dưới đây không tạo ra kim loại?
A. Cho Ba vào dung dịch CuSO4 dư.
B. Đốt cháy HgS trong khí O2.
C. Thổi khí CO dư qua Fe2O3 đun nóng.
D. Điện phân dung dịch ZnSO4 (điện cực trơ).
(Xem giải) Câu 4. Ngâm bột củ nghệ với ethanol nóng, sau đó lọc bỏ bã, lấy dung dịch đem cô để làm bay hơi bớt dung môi. Phần dung dịch còn lại sau khi cô được làm lạnh, để yên một thời gian rồi lọc lấy kết tủa curcumin màu vàng. Từ mô tả ở trên, hãy cho biết, người ta đã sử dụng các kĩ thuật tinh chế nào để lấy được curcumin từ củ nghệ?
A. Chiết và chưng cất. B. Kết tinh và sắc kí.
C. Chiết và kết tinh. D. Chưng cất và sắc kí.
(Xem giải) Câu 5. Đường huyết cần được duy trì ở mức ổn định để đảm bảo cơ thể hoạt động bình thường. Khi nồng độ đường huyết tăng cao kéo dài có thể dẫn đến bệnh tiểu đường. Ngược lại, khi đường huyết giảm thấp có thể gây hoa mắt, chóng mặt, tim đập nhanh. Glucose quyết định nồng độ đường huyết trong cơ thể. Phân tử khối của glucose là
A. 108. B. 180. C. 162. D. 342.
(Xem giải) Câu 6. Ethyl propionate là ester có mùi thơm của dứa. Công thức của ethyl propionate là
A. CH3COOCH3. B. HCOOC2H5. C. C2H5COOCH3. D. C2H5COOC2H5.
(Xem giải) Câu 7. Saccharin (đường hóa học) có công thức cấu tạo như hình bên:
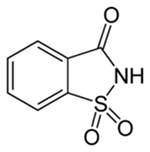
Vị ngọt của nó giống như đường trong mía, củ cải,… nếu saccharose có độ ngọt 1,45 thì sacharin có độ ngọt lên tới 435. Vì thế chỉ cần một lượng nhỏ, nó đã làm cho thực phẩm như bánh kẹo, đồ uống, kể cả trong dược phẩm, kem đánh răng… có vị ngọt đáng kể. Phát biểu đúng là
A. Saccharin là một loại saccharide.
B. Saccharin có tính chất giống saccharose, chỉ khác nhau về độ ngọt.
C. Công thức phân tử của saccharin là C7H5O3NS.
D. Có thể thay thế saccharin cho saccharose vì nó có lợi về kinh tế hơn rất nhiều và có giá trị dinh dưỡng cao.
(Xem giải) Câu 8. Ở các giá trị pH khác nhau, amino acid sẽ tồn tại ở các dạng khác nhau và có khả năng dịch chuyển về các hướng khác nhau dưới tác dụng của điện trường. Cho các dạng tồn tại của một amino acid X ở các giá trị pH khác nhau dưới đây:
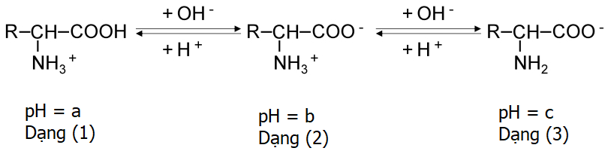
Cho các nhận định sau:
(1) Dạng (1) là dạng cation, dạng (2) là dạng ion lưỡng cực, dạng (3) là dạng anion;
(2) Thứ tự giá trị pH là a < b < c;
(3) Ở pH = a, nếu đặt vào một điện trường, amino acid X sẽ dịch chuyển về phía cực dương (anode);
(4) Trong dung dịch, cả ba dạng (1), (2) và (3) đều có tính chất lưỡng tính.
Các nhận định đúng là
A. (1), (3), (4). B. (1), (2), (4). C. (1), (2). D. (2), (3).
(Xem giải) Câu 9. Cho các phát biểu sau về carbohydrate:
(a) Fructose và saccharose đều là chất rắn có vị ngọt, dễ tan trong nước.
(b) Nhỏ vài giọt dung dịch iodine trong KI vào dung dịch hồ tinh bột: màu xanh xuất hiện; đun nóng, màu xanh biến mất; để nguội, màu xanh xuất hiện trở lại.
(c) Khi đun nóng fructose với AgNO3/NH3 dư thu được Ag.
(d) Khi thủy phân hoàn toàn hỗn hợp gồm cellulose và saccharose trong môi trường acid, chỉ thu được một loại monosaccharide duy nhất.
(e) Phân tử cellulose được cấu tạo bởi nhiều gốc α-glucose.
Số phát biểu đúng là
A. 4. B. 3. C. 5. D. 2.
(Xem giải) Câu 10. Cho biết độ dẫn điện và khối lượng riêng của các kim loại như sau:
| Kim loại | Ag | Cu | Au | Al |
| Độ dẫn điện σ (S/m) | 6,30.107 | 5,98.107 | 4,52.107 | 3,55.107 |
| Khối lượng riêng (g/cm³) | 10,49 | 8,95 | 19,32 | 2,70 |
Dây điện cao thế là loại dây dẫn chuyên dùng để truyền tải điện năng ở điện áp cao, từ nhà máy điện đến trạm biến áp hoặc khu dân cư. Dây điện cao thế thường được làm bằng kim loại nào sau đây?
A. Đồng. B. Vàng. C. Bạc. D. Nhôm.
(Xem giải) Câu 11. Khi điện phân dung dịch CuSO4 bằng dòng điện một chiều (với điện cực anode bằng Cu) thì ở anode xảy ra quá trình
A. oxi hóa H2O thành H+ và O2. B. oxi hóa Cu thành Cu2+.
C. khử Cu2+ thành Cu. D. khử H2O thành H2 và OH-.
(Xem giải) Câu 12. Chanh là thực vật chi Citrus, quả chứa khoảng 5% citric acid (X) tạo nên vị chua và độ pH từ 2 – 3. Dịch quả, múi và vỏ chanh được ứng dụng rộng rãi trong ẩm thực cũng như kỹ nghệ thực phẩm. Dựa vào công thức cấu tạo của (X) ở hình bên, hãy chọn phát biểu đúng về (X)
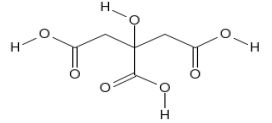
A. Công thức phân tử của (X) là C6H6O7.
B. (X) thuộc loại hợp chất đa chức.
C. 1 mol (X) tác dụng với Na tạo ra 2 mol H2.
D. (X) tác dụng với NaOH theo tỉ lệ mol 1 : 4.
(Xem giải) Câu 13. Cho cân bằng hóa học: N2(g) + 3H2(g) ⇋ 2NH3(g), ![]() = -92 kJ và các yếu tố tác động sau: (a) Thêm H2 vào hệ, (b) Giảm áp suất của hệ, (c) Tăng nhiệt độ, (d) Thêm chất xúc tác. Số yếu tố làm cân bằng trên chuyển dịch theo chiều thuận là
= -92 kJ và các yếu tố tác động sau: (a) Thêm H2 vào hệ, (b) Giảm áp suất của hệ, (c) Tăng nhiệt độ, (d) Thêm chất xúc tác. Số yếu tố làm cân bằng trên chuyển dịch theo chiều thuận là
A. 4. B. 1. C. 3. D. 2.
(Xem giải) Câu 14. Nhỏ dung dịch X vào ống nghiệm chứa Cu(OH)2, lắc đều thấy xuất hiện dung dịch màu tím. X có thể là
A. Gly-Ala. B. methylamine. C. lòng trắng trứng. D. glutamic acid.
(Xem giải) Câu 15. Cho cấu tạo của một đoạn mạch trong polymer như hình sau:
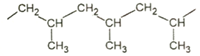
Tên monomer tương ứng tạo polymer là
A. propene. B. buta-1,3-diene. C. ethylene. D. vinyl chloride.
(Xem giải) Câu 16. Cho suất điện động chuẩn của các pin điện hoá: E°X-Y = 0,78V; E°X-Z = 1,24V; E°T-Y = 0,47V (X, Y, Z, T là bốn kim loại). Khẳng định nào sau đây là sai?
A. Trong pin điện hoá Y-Z thì Y là anode.
B. Suất điện động chuẩn của pin điện hoá X-T là 0,31V.
C. Tính khử giảm dần từ trái qua phải theo dãy: X, T, Z, Y.
D. Trong các pin điện hoá: X-Y, X-T và X-Z thì X đều bị oxi hoá.
(Xem giải) Câu 17. Omega-3 là một trong những loại chất béo rất thiết yếu cho cơ thể. Con người không thể tự tổng hợp và tạo ra omega-3 được, do vậy để cung cấp loại acid béo này cho cơ thể là ăn các loại thực phẩm giàu omega-3. Trong các thực phẩm dưới đây, thực phẩm nào chứa hàm lượng omega-3 cao nhất so với các thực phẩm còn lại?
A. Thịt bò. B. Thịt lợn. C. Trứng gà. D. Cá trích, cá hồi.
(Xem giải) Câu 18. Chất giặt rửa tổng hợp chủ yếu được sản xuất từ
A. quả bồ kết, bồ hòn. B. dầu mỏ.
C. dầu thực vật. D. mỡ động vật.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Bã mía (phế phẩm từ ngành đường) là nguồn nguyên liệu dồi dào chứa khoảng 45% cellulose, bã mía được tận dụng để sản xuất cồn thực phẩm và nguyên liệu cho ngành dệt may.
a) Một cơ sở sản xuất sử dụng 5 tấn bã mía (chứa 45% cellulose) làm nguyên liệu. Biết hiệu suất toàn bộ quá trình chuyển hóa cellulose thành ethanol là 60%. Nếu pha chế lượng ethanol này thành cồn 70° (loại cồn sát khuẩn phổ biến), thì thể tích dung dịch cồn 70° thu được là 1369,05 lít. (Biết khối lượng riêng của ethanol là 0,8 g/mL. Kết quả cuối cùng làm tròn đến hàng phần trăm).
b) Cellulose là một polymer thiên nhiên có cấu trúc mạch phân nhánh, đóng vai trò tạo nên bộ khung xương cho thực vật.
c) Trong công nghiệp, người ta dùng phản ứng giữa cellulose và nitric acid (có mặt H2SO4 đặc) để sản xuất cellulose trinitrate làm thuốc súng không khói.
d) Thủy phân hoàn toàn cellulose trong môi trường acid thu được monosaccharide duy nhất là fructose.
(Xem giải) Câu 20. Trong thực tế, sự ăn mòn kim loại gây ra tổn thất to lớn về tài nguyên và chi phí sửa chữa, thay thế các chi tiết bị ăn mòn của máy móc, thiết bị. Một trong số các phương pháp bảo vệ chống ăn mòn kim loại được sử dụng rộng rãi là phương pháp bảo vệ cathode. Trong phương pháp này, người ta sẽ nối hoặc cho kim loại cần được bảo vệ tiếp xúc với kim loại hoạt động hóa học mạnh hơn (kim loại hy sinh)
a) Kim loại hy sinh luôn có thế điện cực chuẩn cao hơn kim loại cần được bảo vệ.
b) Nếu thanh kẽm không tiếp xúc hoặc không nối với thanh sắt thì nó không bảo vệ được thanh sắt khỏi bị ăn mòn.
c) Sắt bị gỉ nhanh hơn khi tiếp xúc với kẽm nhưng bị gỉ chậm hơn khi tiếp xúc với đồng.
d) Trong một thí nghiệm nghiên cứu sự ảnh hưởng của các yếu tố đến khả năng sử dụng kẽm để bảo vệ chống ăn mòn thép. Một khối kẽm có khối lượng 25,0 gam được gắn lên một thiết bị bằng thép đặt trong nước biển. Sau một thời gian, cân lại thì thấy khối lượng của kẽm là 28,0 gam. Giả thiết trong quá trình làm việc, toàn bộ Zn chỉ bị oxi hóa thành Zn(OH)2 và hydroxide này bám hết lên khối kẽm. Phần trăm khối lượng kẽm đã bị oxi hóa là 22,94%. (Kết quả cuối cùng làm tròn đến hàng phần trăm)
(Xem giải) Câu 21. Thuốc DEP (chứa hoạt chất diethyl phthalate) dùng để điều trị ghẻ ngứa hoặc xua đuổi côn trùng, được tổng hợp từ hydrocarbon thơm có công thức phân tử C8H10 theo sơ đồ sau đây:
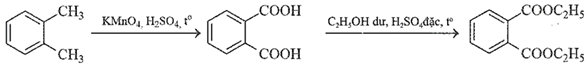
a) Trong phân tử diethyl phthalate có tổng cộng 3 liên kết π.
b) Cho 1 mol diethyl phthalate tác dụng hết 2 mol NaOH thu được 1 mol alcohol và 2 mol muối.
c) Diethyl phthalate thuộc loại ester đa chức (diester).
d) Để sản xuất được 5 triệu hộp DEP (quy cách 10 gam/hộp, hoạt chất DEP chiếm 88,8% khối lượng) với hiệu suất cả quá trình là 80%, cần lượng tối thiểu 26,5 tấn o-dimethylbenzene.
(Xem giải) Câu 22. Để tiến hành mạ một tấm huy chương hình trụ, đáy tròn với bán kính 2,5 cm; chiều cao hình trụ 0,3 cm; với lớp mạ bằng copper dày 0,1 cm như hình bên.
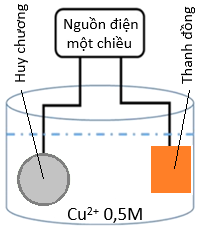
Người ta có thể tiến hành điện phân dung dịch X (CuSO4) nồng độ 0,5M, dư với cường độ dòng điện không đổi 2A, khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t giây. Biết khối lượng riêng của copper là 8,95 g/cm³ và hiệu suất điện phân là 100%, giả thiết lớp mạ huy chương dày như nhau, toàn bộ lượng copper tạo ra đều bám hết vào tấm huy chương. Cho hằng số Faraday F = 96500, π = 3,14.
a) Thanh copper là cực dương, huy chương được mạ sẽ đóng vai trò cực âm.
b) Khi kết thúc điện phân bên điện cực anode thoát ra 8,193 lít (đkc).
c) Chiều dòng electron di chuyển từ huân chương được mạ qua dây dẫn đến thanh copper.
d) Thời gian điện phân 64800 giây.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Amine là loại hợp chất hữu cơ quan trọng được dùng để sản xuất dược phẩm, phẩm nhuộm,… Ngoài ra, các amine còn được ứng dụng để tổng hợp các phức chất. Cho các phát biểu sau:
(1) Trong phân tử aniline, vòng benzene và hai nguyên tử hydrogen phân bố xung quanh nguyên tử nitrogen theo hình chóp tam giác đều.
(2) Khi cho methylamine phản ứng với NaNO2 trong dung dịch HCl ở nhiệt độ thường thấy có khí không màu thoát ra.
(3) Dimethylamine và trimethylamine có cùng bậc amine.
(4) Cho vài giọt nước bromine vào dung dịch aniline thì thấy xuất hiện kết tủa màu trắng.
Các phát biểu đúng gồm những phát biểu nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 123; 234;…).
(Xem giải) Câu 24. Một mẫu nước thải của nhà máy sản xuất có pH = 3. Để thải ra ngoài môi trường thì cần phải tăng pH lên từ 5,8 đến 8,6 (theo đúng qui định), nhà máy phải dùng vôi sống thêm vào nước thải. Để nâng pH của 3 m³ nước thải từ 3 lên 7 cần dùng m gam vôi sống. Tính giá trị m. (Bỏ qua sự thủy phân của các muối. Kết quả cuối cùng làm tròn đến hàng đơn vị).
(Xem giải) Câu 25. Ăcquy chì là nguồn điện hóa học phổ biến, cấu tạo của ăcquy chì gồm cực âm bằng Pb và cực dương bằng Pb có phủ PbO2, cùng nhúng trong dung dịch điện li H2SO4 nồng độ khoảng 30%. Quá trình phóng điện xảy ra theo các phản ứng:
Tại cực (–): Pb(s) + HSO4- (aq) → PbSO4(s) + H+(aq) + 2e
Tại cực (+): PbO2(s) + HSO4- (aq) + 3H+(aq) + 2e → PbSO4(s) + 2H2O(l)
Khi sạc điện cho ăcquy chì, phản ứng điện hóa xảy ra theo chiều ngược lại với phản ứng khi ăcquy chì phóng điện. Để sạc điện cho ăcquy chì, người ta sử dụng dòng điện một chiều có cường độ dòng điện 2,0 A trong 1,0 giờ. Tính khối lượng PbSO4 (theo gam) đã phản ứng trong quá trình này. Giả thiết hiệu suất sạc điện là 100%. (Biết điện lượng được tính theo công thức: q = I.t = ne.F; F = 96500 C/mol. Kết quả cuối cùng làm tròn đến hàng phần mười).
(Xem giải) Câu 26. Cho vào bình cầu: 15 mL isoamyl alchohol, 15 mL acetic acid tuyệt đối và 10 mL dung dịch H2SO4 đặc. Lắp dụng cụ như hình vẽ, tiến hành thực hiện thí nghiệm; chất lỏng thu được ở bình tam giác cho vào phễu chiết cùng dung dịch NaCl bão hòa.
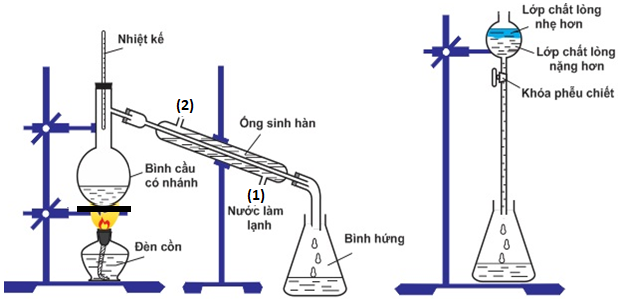
Cho các phát biểu:
(a) Trong phễu chiết lớp chất lỏng nặng hơn có thành phần chính là isoamyl acetate.
(b) Nhiệt kế dùng để kiểm soát nhiệt độ.
(c) Phễu chiết dùng tách các chất lỏng không tan vào nhau ra khỏi nhau.
(d) Isoamyl acetate tinh khiết có thể được sử dụng làm hương liệu phụ gia cho thực phẩm.
(e) Để hiệu suất phản ứng cao hơn nên dùng dung dịch acetic acid 5%.
(f) Nước trong ống sinh hàn được lắp cho chảy vào (1) và ra (2).
Số các phát biểu đúng là bao nhiêu?
(Xem giải) Câu 27. Salicin là một thuốc chống viêm được sản xuất từ vỏ cây liễu. Về mặt hóa học, salicin có quan hệ gần gũi với aspirin và cũng có tác dụng tương tự trên cơ thể người. Salicin được chuyển hóa thành salicylic acid qua 2 phản ứng bên:
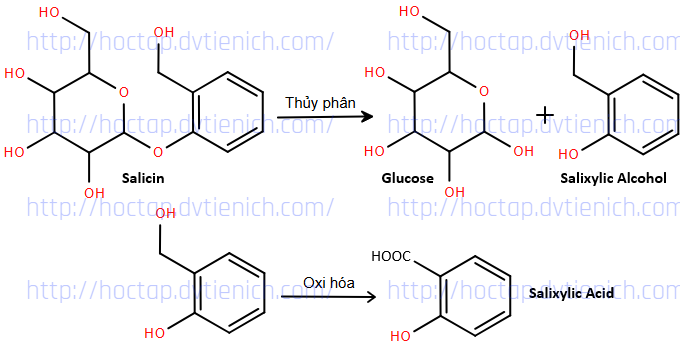
Giả sử hiệu suất chuyển hóa của mỗi giai đoạn là 70%. Từ 1,0 tấn salicin (chứa 25% tạp chất trơ) người ta điều chế được m kg salicylic acid theo quy trình trên. Tính giá trị của m. (Kết quả cuối cùng làm tròn đến hàng đơn vị).
(Xem giải) Câu 28. Biodiesel là nhiên liệu sinh học được sản xuất từ dầu thực vật hoặc mỡ động vật. Đây là giải pháp thay thế cho nhiên liệu diesel (sản xuất từ dầu mỏ) đang dần cạn kiệt trong tương lại. Trong một quy trình sản xuất, người ta cho 10,0 kg triglyceride X (khối lượng mol là 830 g/mol) phản ứng với methanol có mặt xúc tác là potassium hydroxide. Sau phản ứng thu được biodiesel là hỗn hợp methyl ester của các acid béo.
Tính thể tích methanol (D = 0,79 g/mL) cần dùng trong quá trình trên là bao nhiêu lít? Giả thiết hiệu suất phản ứng là 80%. (Kết quả cuối cùng làm tròn đến hàng phầm trăm).


Bình luận