[2026] Thi thử TN trường Như Thanh – Thanh Hóa (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 085
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2D | 3D | 4C | 5B | 6D | 7C | 8B | 9C |
| 10C | 11A | 12C | 13C | 14C | 15C | 16D | 17A | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | S | Đ |
| (b) | Đ | Đ | S | S |
| (c) | S | Đ | Đ | S |
| (d) | Đ | Đ | S | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 0,8 | 3 | 2 | 12 | 19,5 | 5 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Qua nghiên cứu thực nghiệm cho thấy cao su thiên nhiên là polymer của monomer nào sau đây?
A. Buta-1,2-diene. B. Buta-1,3-diene. C. 2-methylbuta-1,3-diene. D. Buta-1,4-diene.
(Xem giải) Câu 2: Sự phát triển của công nghệ tạo ra nhiều phương pháp tổng hợp polymer nhằm phục vụ đời sống, bên cạnh việc khai thác các polymer sẵn có từ thiên nhiên. Phát biểu nào sau đây về các phương pháp điều chế polymer là đúng?
A. Tơ olon (hay polyacrylonitrile) được khai thác từ thiên nhiên.
B. Cellulose là polymer trùng ngưng giữa các phân tử glucose.
C. Poly(vinyl alcohol) được tổng hợp từ alcohol tương ứng.
D. Polystyrene được tổng hợp từ styrene bằng phản ứng trùng hợp.
(Xem giải) Câu 3: NaHCO3 được sử dụng làm phụ gia thực phẩm với tên gọi baking soda, có kí hiệu là E500(ii) dùng làm chất điều chỉnh độ chua trong sốt cà chua, nước ép hoa quả,… Khi đó, NaHCO3 sẽ tác dụng với H+ để làm giảm nồng độ H+. Vai trò của NaHCO3 trong phản ứng là
A. Acid. B. Chất oxi hóa. C. Chất khử. D. Base.
(Xem giải) Câu 4: Phản ứng đốt cháy methane có trong khí thiên nhiên tỏa ra một nhiệt lượng lớn. Cho nhiệt tạo thành chuẩn của các chất:
| Chất | CH4(g) | O2(g) | CO2(g) | H2O(g) |
| -74,9 | 0,0 | -393,5 | -241,8 |
Nhiệt lượng tỏa ra khi đốt cháy 1 kg methane tương đương điện năng của k số điện (1 số điện = 3600 kJ). Giá trị của k là bao nhiêu (làm tròn kết quả đến phần nguyên)?
A. 12. B. 13. C. 14. D. 15.
(Xem giải) Câu 5: Chất nào sau đây thuộc loại disaccharide?
A. Glucose. B. Saccharose. C. Cellulose. D. Fructose.
(Xem giải) Câu 6: Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36°C), heptane (sôi ở 98°C), octane (sôi ở 126°C) và nonane (sôi ở 151°C). Có thể tách riêng các chất đó bằng cách nào sau đây?
A. Chiết. B. Kết tinh. C. Bay hơi. D. Chưng cất.
(Xem giải) Câu 7: Chất ứng với công thức nào sau đây không có tác dụng giặt rửa?
A. CH3[CH2]16COOK. B. CH3[CH2]10CH2C6H4SO3Na.
C. (CH3[CH2]14COO)3C3H5. D. CH3[CH2]10CH2OSO3Na.
(Xem giải) Câu 8: Khi đun nóng protein trong dung dịch acid hoặc kiềm hoặc dưới tác dụng của các enzyme, protein bị thủy phân thành …(1)…, cuối cùng thành …(2)… Điền thông tin vào chỗ trống (1), (2) phù hợp là:
A. (1) phân tử protein nhỏ hơn; (2) amino acid.
B. (1) chuỗi polypeptide; (2) hỗn hợp các α-amino acid.
C. (1) chuỗi polypeptide; (2) amino acid.
D. (1) amino acid; (2) chuỗi polypeptide.
(Xem giải) Câu 9: Trong dung dịch, giá trị pH mà tại đó amino acid tồn tại chủ yếu ở dạng ion lưỡng cực có tổng điện tích bằng 0 được gọi là pHI. Cho giá trị pHI như sau: Glu (pHI = 3,08), Gly (pHI = 5,97), Arg (pHI = 10,76). Tiến hành phương pháp điện di dung dịch gồm ba amino acid trên tại giá trị pH = 5,97 thu được kết quả như hình dưới:

Các kí hiệu A, B, C tương ứng với các amino acid là
A. Arg, Gly, Glu. B. Glu, Gly, Arg. C. Gly, Glu, Arg. D. Glu, Gly, Arg.
(Xem giải) Câu 10: Thủy ngân (Hg) có thể chuyển thành dạng hơi khuếch tán trong không khí, khi đó sẽ làm tăng nguy cơ mắc các bệnh về hô hấp và một số bệnh khác. Khi nhiệt kế thủy ngân bị vỡ, có thể sử dụng hóa chất nào sau đây để loại bỏ thủy ngân?
A. Dung dịch HCl. B. Dung dịch NaOH.
C. Bột lưu huỳnh. D. Bột than gỗ (chứa carbon).
(Xem giải) Câu 11: Cho biết giá trị thế điện cực chuẩn của các cặp oxi hóa – khử sau:
| Cặp oxi hóa – khử | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Ni2+/Ni | 2H+/H2 |
| Thế điện cực chuẩn (V) | 0,340 | -0,763 | -0,440 | -0,257 | 0,000 |
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 12: Tên thay thế của amine CH3CH(CH3)NH2 là
A. Methylethylamine. B. Ethylmethylamine.
C. Propan-2-amine. D. Propan-1-amine.
(Xem giải) Câu 13: Trong cây mía, củ cải, quả thốt nốt có chứa loại đường nào sau đây?
A. Fructose. B. Glucose. C. Saccharose. D. Maltose.
(Xem giải) Câu 14: Các polymer đa dạng về nguồn gốc, thành phần, tính chất,… do đó có nhiều ứng dụng: tinh bột làm lương thực, protein làm thực phẩm, poly(methyl methacrylate) làm thủy tinh hữu cơ,… và rất nhiều vật liệu polymer khác có ứng dụng quan trọng. Cho các phát biểu sau:
(a) Theo nguồn gốc, các polymer được chia thành 4 loại: polymer tự nhiên, polymer tổng hợp, polymer nhân tạo và polymer bán tổng hợp.
(b) Một số polymer tham gia phản ứng giữ nguyên mạch polymer.
(c) Phản ứng thủy phân tinh bột, cellulose, polypeptide thuộc loại phản ứng cắt mạch polymer.
(d) Quá trình lưu hóa cao su xảy ra phản ứng tăng mạch polymer.
Số phát biểu không đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 15: Có 4 ống nghiệm đựng Cu(OH)2 trong môi trường kiềm. Nhỏ từ từ vào từng ống nghiệm và khuấy đều dung dịch đựng các chất riêng rẽ sau: albumin, ethylamine, aniline, alanine. Có bao nhiêu ống nghiệm chứa chất hòa tan được Cu(OH)2?
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 16: Cho các hợp chất có công thức cấu tạo dưới đây:
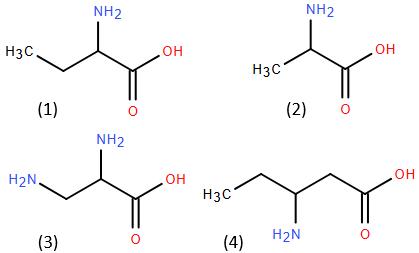
Những hợp chất nào trong số các chất trên thuộc loại α-amino acid?
A. Chất (1) và chất (3).
B. Chất (2), chất (3) và chất (4).
C. Chất (1) và chất (2).
D. Chất (1), chất (2) và chất (3).
(Xem giải) Câu 17: Để đề phòng nguy cơ gây cháy, nổ cần kiểm soát chặt chẽ các nguồn lửa, chất cháy, chất oxi hóa. Cho các biện pháp sau:
(a) Không bật lửa ở nơi cấm lửa, không đốt lửa trong rừng, không đốt rác bừa bãi; đổ nước vào khu vực lửa trại ngay khi kết thúc.
(b) Tập trung khi nấu nướng để tránh thiết bị quá nóng gây cháy hoặc quên tắt thiết bị gây chập điện.
(c) Không tàng trữ, chế tạo trái phép thuốc nổ, thuốc pháo.
(d) Sắp xếp hàng hóa, vật dụng dễ cháy cách xa nguồn lửa, nguồn nhiệt.
Các biện pháp nhằm loại trừ khả năng phát sinh ra nguồn lửa có khả năng gây hỏa hoạn là
A. (a) và (b). B. (a) và (d). C. (b) và (c). D. (c) và (d).
(Xem giải) Câu 18: Đồ thị sau đây biểu diễn sự thay đổi về lượng glucose trong máu của một người sử dụng đồ uống có đường sau 8 giờ nhịn ăn:
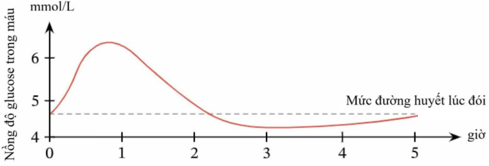
Khi sử dụng đồ uống có đường, nồng độ glucose trong máu tăng cao nhất sau khi
A. Sử dụng khoảng 20 phút. B. Sử dụng khoảng 2 giờ.
C. Sử dụng khoảng 50 phút. D. Sử dụng khoảng 3 giờ.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Trong phòng thí nghiệm, ethyl acetate được điều chế từ acetic acid và ethanol, xúc tác H2SO4 đặc, theo mô hình thí nghiệm sau:
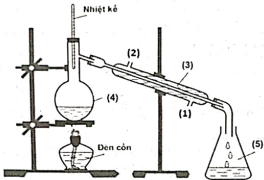
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65 –70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C. Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, ethanol và ethyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O-H (alcohol) | O-H (carboxylic acid) | C=O (ester, carboxylic acid) |
| Số sóng (cm-1) | 3650-3200 | 3300-2500 | 1780-1650 |
a) Chất lỏng trong bình hứng (5) có ethyl acetate.
b) Vai trò của ống sinh hàn (3) để ngưng tụ hơi; nước vào từ (1), nước ra ở (2).
c) Nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
d) Dựa vào phổ hồng ngoại, phân biệt được acetic acid, ethanol và ethyl acetate.
(Xem giải) Câu 20: Khi con người sử dụng thức ăn chứa tinh bột, enzyme α-amylase có trong nước bọt thúc đẩy quá trình thuỷ phân tinh bột thành các phân tử nhỏ hơn gồm dextrin và maltose. Quá trình này tiếp tục ở ruột non, nơi phần lớn tinh bột bị thuỷ phân thành glucose. Glucose được hấp thụ vào máu và di chuyển đến các tế bào trong khắp cơ thể. Glucose có thể được sử dụng cho nhu cầu năng lượng hoặc có thể được chuyển đổi thành glycogen lưu trữ trong gan và cơ.
(a) Khi ăn cơm, nếu nhai kĩ sẽ thấy vị ngọt vì tinh bột bị thuỷ phân thành glucose.
(b) Tinh bột bị thủy phân bởi enzyme α-amylase hoặc môi trường acid.
(c) Glucose chủ yếu đóng vai trò cung cấp năng lượng cho tế bào.
(d) Glycogen lưu trữ trong gan và cơ, khi cần thiết có thể chuyển hoá thành glucose để cung cấp năng lượng cho cơ thể.
(Xem giải) Câu 21: Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Cho khoảng 1 gam tinh bột vào ống nghiệm chứa 5 mL nước ấm (khoảng 50°C), khuấy nhẹ (ống 1).
• Bước 2: Thêm 1 mL dung dịch HCl 1M vào ống 1, khuấy đều, đun cách thủy trong 10 phút, để nguội.
• Bước 3: Thêm từ từ NaHCO3 vào ống 1 đến khi ngừng sủi bọt khí.
• Bước 4: Cho 0,5 mL dung dịch CuSO4 5% vào 1 ống nghiệm (ống 2) có chứa 2 mL dung dịch NaOH 10%, lắc nhẹ, cho tiếp 2 mL dung dịch ở ống 1 (thu được sau bước 3) vào ống 2. Đun cách thủy ở nhiệt độ 80°C trong 5 phút.
a) Sau bước 1, thu được dung dịch đồng nhất.
b) Ở bước 3, NaHCO3 có vai trò chính làm tăng tốc độ phản ứng thủy phân ở bước 2.
c) Trong bước 2, xảy ra phản ứng thủy phân tinh bột tạo thành glucose.
d) Sau bước 4, thu được dung dịch màu xanh lam.
(Xem giải) Câu 22: Phân tích nguyên tố hợp chất hữu cơ E cho kết quả phần trăm khối lượng carbon, hydrogen và oxygen lần lượt là 54,55%; 9,09% và 36,36%. Dựa vào phương pháp phân tích khối phổ (MS) xác định được phân tử khối của E là 88. Thuỷ phân hoàn toàn E trong dung dịch NaOH, thu được muối của carboxylic acid X và chất Y. Chất Y có nhiệt độ sôi (64,7°C) nhỏ hơn nhiệt độ sôi của ethanol (78,3°C) (nhiệt độ sôi đều đo ở áp suất 1 atm).
a) Công thức phân tử của E là C4H8O2.
b) Nhiệt độ sôi của E, X và Y được xếp theo thứ tự sau: Y < X < E.
c) Trong công nghiệp, chất Y được phối trộn với xăng RON 92 để tạo ra xăng sinh học.
d) Dung dịch muối tạo bởi giữa carboxylic acid X và NaOH có môi trường base.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Biết: E°Ni-Ag = 1,06V, E°Ni2+/Ni = -0,26V, thế điện cực chuẩn của cặp oxi hoá – khử Ag+/Ag là bao nhiêu volt (V)?
(Xem giải) Câu 24: Docosahexaenoic acid (DHA) thuộc loại acid béo omega-n, là thành phần quan trọng của não người, vỏ não, da và võng mạc. Docosahexaenoic acid có công thức cấu tạo như sau:

Giá trị của n là bao nhiêu?
(Xem giải) Câu 25: Một số amine no, đơn chức, mạch hở, trong phân tử có phần trăm khối lượng nitrogen bằng 23,73%. Có bao nhiêu chất là đồng phân tác dụng được với dung dịch nitrous acid (HNO2) ở nhiệt độ thích hợp sinh ra alcohol và khí nitrogen?
(Xem giải) Câu 26: Bia, rượu, giấm ăn đều có thể được sản xuất từ nguyên liệu ban đầu là tinh bột trong ngũ cốc theo sơ đồ phản ứng sau:
Tinh bột (1) → maltose (2) → glucose (3) → ethanol (4) → acetic acid.
Phản ứng nào trong chuỗi phản ứng trên thuộc loại phản ứng thuỷ phân? (Liệt kê đáp án theo số thứ tự phản ứng tăng dần).
(Xem giải) Câu 27: Đèn cồn là dụng cụ quen thuộc với học sinh trong giờ thực hành. Xét một đèn cồn có tốc độ tiêu thụ nhiên liệu trung bình 1,0 mL cồn 92°C trong 1 phút. Cho biết enthalpy tạo thành chuẩn của các chất:
| Chất | C2H5OH(l) | O2(g) | CO2(g) | H2O(g) |
| -277,6 | 0,0 | -393,5 | -241,8 |
Khối lượng riêng của ethanol là 0,789 g/mL. Năng lượng của quá trình đốt ethanol giải phóng ra trong 1 phút là bao nhiêu kJ? (Làm tròn kết quả đến hàng phần mười).
(Xem giải) Câu 28: Trong quá trình bảo quản, một phần Fe2+ trong muối FeSO4.7H2O bị oxygen oxi hoá thành Fe3+ (hỗn hợp X). Lấy một lượng thích hợp X đem hoà vào 10,0 mL dung dịch H2SO4 1,00M thu được dung dịch Y. Chia Y thành hai phần bằng nhau:
– Phần 1: Thêm nước vào thu được 100 mL dung dịch Y1. Lượng Fe2+ trong 10,0 mL dung dịch Y1 phản ứng vừa đủ với 3,8 mL dung dịch KMnO4 0,01M.
– Phần 2: Khử hoàn toàn ion Fe3+ thành ion Fe2+, thêm tiếp 5 mL dung dịch H2SO4 1M. Sau đó thêm nước vào đến khi thu được 100,0 mL dung dịch Y2. Lượng Fe2+ trong 10,00 mL Y2 phản ứng vừa đủ với 4,0mL dung dịch KMnO4 0,01M.
Phần trăm khối lượng iron(II) đã bị oxygen trong không khí oxi hoá thành iron(III) là a%. Giá trị của a là bao nhiêu? (kết quả làm tròn đến hàng đơn vị)


https://docs.google.com/document/d/1h6TkcFkjKHzAk7Lu01r4uuaaFLjwqcaW/edit?usp=sharing&ouid=115590581291029337315&rtpof=true&sd=true