[2026] Thi thử TN trường Quang Trung Hà Đông – Hà Nội
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 116
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2A | 3C | 4B | 5B | 6C | 7D | 8B | 9D |
| 10B | 11C | 12A | 13C | 14C | 15B | 16C | 17C | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | Đ | S |
| (b) | Đ | Đ | S | S |
| (c) | S | S | S | Đ |
| (d) | Đ | S | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 145 | 5 | 5 | 250 | 4 | 4,5 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Lysine là một amino acid thiết yếu đóng vai trò quan trọng trong sản xuất collagen, hấp thu calcium và tăng cường miễn dịch cho cơ thể. Lysine có công thức cấu tạo là:
A. H2N[CH2]4CH(NH2)COOH. B. (CH3)2CHCH(NH2)COOH.
C. H2N[CH2]3CH(NH2)COOH. D. HOOC-[CH2]2CH(NH2)COOH.
(Xem giải) Câu 2. Glutathione là tripeptide (Glu-Cys-Gly) được gan sản xuất tự nhiên, được coi như kho dự trữ các chất chống oxy hóa. Biết cysteine là α-amino acid có 1 nhóm –NH2 và 1 nhóm –COOH. Số nguyên tử oxygen có trong Glu-Cys-Gly là:
A. 6. B. 5. C. 3. D. 4.
(Xem giải) Câu 3. Cho phản ứng hoá học sau: 3Fe(s) + 4H2O(g) ⇋ Fe3O4(s) + 4H2(g). Biểu thức hằng số cân bằng của phản ứng trên là
A. Kc = 4[H2] / 4[H2O]. B. Kc = 4[H2][Fe3O4] / 4[H2O].3[Fe].
C. Kc = [H2]⁴ / [H2O]⁴. D. Kc = [H2]⁴[Fe3O4] / [H2O]⁴[Fe]³.
(Xem giải) Câu 4. Ở trạng thái cơ bản, cấu hình electron của kim loại chromium (Z = 24) là
A. [Ar]3d5 4s2. B. [Ar]3d5 4s1. C. [Ar]3d4 4s2. D. [Ar]3d6 4s2
(Xem giải) Câu 5. Oxi hóa không hoàn toàn butan-2-ol bằng CuO, đun nóng thu được hợp chất hữu cơ là:
A. (CH3)2CH-O-CH3. B. CH3CH2COCH3.
C. CH2=C(CH3)CH2OH. D. CH3CH2CH2CHO.
(Xem giải) Câu 6. Điện phân dung dịch NiSO4 với anode là kim loại nickel, cathode là chiếc chìa khóa bằng thép. Ở anode xảy ra quá trình nào dưới đây?
A. 2H2O → O2 + 4H+ + 4e. B. Ni2+ + 2e → Ni.
C. Ni → Ni2+ + 2e. D. 2H2O + 2e → H2 + 2OH-.
(Xem giải) Câu 7. Kim loại nào sau đây không phản ứng với nước?
A. Ca. B. Ba. C. K. D. Be.
(Xem giải) Câu 8. Lauric acid là một acid béo bão hòa (thường chiết xuất từ dầu dừa, dầu hạt cọ), là thành phần phổ biến trong mỹ phẩm nhờ khả năng kháng khuẩn cao, làm sạch sâu và dưỡng ẩm. Công thức của lauric acid là:
A. C17H35COOH. B. C11H23COOH. C. CH3COOH. D. CH2=CHCOOH.
(Xem giải) Sử dụng thông tin giá trị thế điện cực chuẩn dưới đây để trả lời câu 9 – 10
| Cặp oxi hóa-khử | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Fe3+/Fe2+ | Ag+/Ag |
| E°(V) | -0,763 | -0,440 | +0,340 | +0,771 | +0,799 |
Câu 9. Một pin Galvani được thiết lập ở điều kiện chuẩn, biết phản ứng oxi – hóa khử xảy ra trong pin là: Cu + 2Ag+ → Cu2+ + 2Ag. Giá trị sức điện động chuẩn của pin là:
A. 1,562. B. 1,258. C. 1,139. D. 0,459.
Câu 10. Khi lần lượt cho đến dư các kim loại: Zn, Fe, Cu, Ag vào dung dịch dung dịch FeCl3, có bao nhiêu trường hợp thu được kim loại Fe sau phản ứng?
A. 4. B. 1. C. 3. D. 2.
(Xem giải) Câu 11. Ester nào dưới đây thủy phân trong môi trường kiềm không thu được alcohol?
A. Allyl acetate. B. Benzyl formate. C. Vinyl acetate. D. Ethyl formate.
(Xem giải) Câu 12. Chất nào dưới đây là đồng phân của saccharose?
A. Maltose. B. Galactose. C. Fructose. D. Glucose.
(Xem giải) Câu 13. Phức chất cisplatin được ứng dụng trong y học để tiêu diệt các tế bào ung thư. Cisplatin có công thức là [Pt(NH3)2Cl2]. Số oxi hóa của platinum trong phức chất trên là
A. +4. В. 0. C. +2. D. -2.
(Xem giải) Câu 14. Trong thực tiễn, sodium carbonate (Na2CO3) được ứng dụng để xử lý nước nhiễm phèn (chứa nhiều ion Fe3+). Phản ứng ion rút gọn nào dưới đây giải thích khả năng xử lý nước nhiễm phèn của Na2CO3?
A. Na+ + OH- → NaOH. B. 2Fe3+ + 3CO32- → Fe2(CO3)3↓
C. 2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3↓ + 3CO2↑. D. Fe3+ + 3OH- → Fe(OH)3↓
(Xem giải) Câu 15. Ethanolamine là hóa chất được sử dụng rộng rãi làm chất nhũ hóa, chất làm kiềm hóa và trong các ngành công nghiệp xử lý khí. Cho biết công thức của ethanolamine là H2N-CH2-CH2-OH. Phát biểu nào về ethanolamine không chính xác?
A. Công thức phân tử của ethanolamine là C2H7NO.
B. Ethanolamine là hợp chất no, đa chức.
C. Ethanolamine chứa nhóm chức amine bậc I.
D. Ethanolamine chứa nhóm chức alcohol bậc I.
(Xem giải) Câu 16. Sodium cocoyl isethionate (SCI) là một chất hoạt động bề mặt dịu nhẹ, nó tạo ra bọt mịn, ổn định mà không làm khô da. Cho biết công thức của SCI như dưới đây:

Thứ tự vị trí được khoanh tròn nào là đầu ưa nước của chất hoạt động bề mặt trên?
A. (2). B. (1). C. (4). D. (3).
(Xem giải) Câu 17. Chất nào dưới đây làm mất màu dung dịch nước Br2?
A. acetic acid. B. ethanol. C. formaldehyde. D. acetone.
(Xem giải) Câu 18. Polymer nào dưới đây được tổng hợp bằng phản ứng trùng ngưng?
A. Poly (vinyl chloride). B. Nylon-6,6. C. Polyethylene. D. Cao su buna.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Poly (acrylonitrile styrene acrylate) hay nhựa ASA là loại nhựa được phát triển từ nhựa ABS (acrylonitrile butadiene styrene). Nó tạo ra nhằm khắc phục nhược điểm của ABS, thay thế buta-1,3-diene bằng acrylate để tăng khả năng chống tia UV và thời tiết, nhưng vẫn giữ được độ bền và độ cứng. Một số ngành có nhu cầu cao về ASA như công nghệ ô tô, thiết bị điện tử, dụng cụ ngoài trời,… Nhựa ASA được tổng hợp bằng phản ứng đồng trùng hợp acrylonitrile (CH2=CH-CN), styrene (C6H5CH=CH2) và butyl acrylate (CH2=CHCOOC4H9). Cho đoạn mạch của nhựa ASA có công thức sau:

Trong đó: m, n, p là số lượng mắt xích của các monomer tương ứng và tỷ lệ này được nhà sản xuất điều chỉnh linh hoạt tùy thuộc vào yêu cầu tính chất cơ lý của ứng dụng thực tế.
a) Nhựa ASA bền với thời tiết và ánh nắng mặt trời tốt hơn nhựa ABS là do trong cấu trúc mạch chính của ASA không còn các liên kết đôi C=C dễ bị oxi hóa như polybutadiene trong ABS.
b) Acrylonitrile được sử dụng trong phản ứng đồng trùng hợp với buta-1,3-diene để sản xuất cao su Buna-N.
c) Nhựa ASA thuộc loại nhựa nhiệt rắn.
d) Một mẫu nhựa ASA thương mại có tỷ lệ khối lượng acrylonitrile là 21,2%, styrene là 53,2%, còn lại là butyl acrylate. Tỉ lệ số mắt xích m : n : p trong mẫu nhựa này là 2 : 2,56 : 1 (chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 20. Một chiếc chìa khóa cần được phủ một lớp bạc mỏng bằng phương pháp mạ điện. (Cho hằng số Faraday F = 96500 C/mol)
a) Anode cần được nối với thanh bạc tinh khiết, tại đây xảy ra quá trình Ag → Ag+ + 1e
b) Nếu điện phân trong 18 phút với cường độ dòng điện là 1,04 A thì khối lượng bạc phủ lên bề mặt chiếc chìa khóa là 1,257 gam (chỉ làm tròn kết quả cuối cùng đến hàng phần nghìn).
c) Một chiếc chìa khóa đặt làm riêng có diện tích bề mặt 12,92 cm² cần được phủ một lớp bạc dày 0,203 mm. Biết khối lượng của bạc là 10,48 g/cm³. Nếu sử dụng dòng điện cường độ 0,981 A thì cần điện phân trong 32 bằng phút (chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
d) Chìa khóa được nối với cathode, dung dịch trong bình điện phân có thể thay AgNO3 bằng muối AgCl.
(Xem giải) Câu 21. Rơm khô là một phế phẩm nông nghiệp chứa nhiều cellulose, có thể dùng làm nguyên liệu sản xuất ethanol sinh học. Từ 1,8 tấn rơm khô (trong đó 40,0% là khối lượng cellulose, phần còn lại là tạp chất trơ không tham gia phản ứng), người ta thủy phân thành glucose, sau đó toàn bộ lượng glucose được lên men thành ethanol. Biết hiệu suất cả quá trình sản xuất từ cellulose đến ethanol là 70%. Cho biết khối lượng riêng của ethanol là 0,8 g/mL, khối lượng riêng của nước là 1g/mL.
a) Dùng toàn bộ lượng ethanol ở trên pha được thành 3578 (L) xăng E10 (biết xăng E10 chứa 10% thể tích ethanol) (chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
b) Cellulose là polymer có cấu tạo như hình dưới đây:
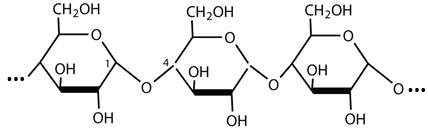
c) Lấy toàn bộ lượng ethanol thu được ở trên pha loãng thành C2H5OH 10° . Lấy 500 mL C2H5OH 10° này đem lên men giấm theo phản ứng sau: C2H5OH + O2 (men giấm) → CH3COOH + H2O. Biết hiệu suất chuyển hóa ethanol thành acetic acid là 65%. Giả sử trong quá trình lên men giấm, không có sự bay hơi, không có các chuyển hóa khác. Nồng độ phần trăm của CH3COOH trong dung dịch thu được là 4,65% (chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
d) Trong mỗi đơn vị glucose cấu thành phân tử cellulose có ba nhóm hydroxy (–OH).
(Xem giải) Câu 22. Calcium trong máu hoặc nước tiểu có thể được xác định bằng phương pháp chuẩn độ permanganate như sau:
• Bước 1: Dùng dung dịch (NH4)2C2O4 kết tủa ion Ca2+ dưới dạng calcium oxalate (CaC2O4) ở môi trường trung tính theo phản ứng: Ca2+ + C2O42- → CaC2O4↓ (1)
• Bước 2: Hòa tan kết tủa trong dung dịch H2SO4 loãng rồi dùng dung dịch KMnO4 để chuẩn độ lượng oxalic acid được giải phóng theo phản ứng:
5H2C2O4 + 2MnO4- + 6H+ → 2Mn2+ + 10CO2 + 8H2O (2)
a) Ở bước 2, có thể thay dung dịch H2SO4 bằng dung dịch HCl đặc.
b) Trong phép chuẩn độ trên, ion Ca2+ đóng vai trò là chất khử, MnO4- đóng vai trò là chất oxi hóa.
c) Calcium oxalate kết tủa từ 1 mL máu một người tác dụng vừa đủ với 2 mL dung dịch KMnO4 5.10^-4 M. Nồng độ ion calcium trong máu người đó bằng 10 mg Ca2+/100 mL máu.
d) Để nhận biết điểm tương đương ở bước 2, không cần sử dụng thêm chất chỉ thị.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho các phản ứng sau:
(1) [Co(OH2)6]2(aq) + 6NH3(aq) → [Co(NH3)6]2+(aq) + 6H2O(l)
(2) 2[Co(NH3)6]2+(aq) + H2O2(aq) → 2[Co(NH3)6]3+(aq) + 2OH-(aq)
(3) Au(s) + NO3-(aq) + 4H+(aq) + 4Cl-(aq) → [AuCl4]-(aq) + NO(g) + 2H2O(l)
(4) [Ag(NH3)2]+(aq) + 2CN-(aq) → [Ag(CN)2]-(aq) + 2NH3(aq).
(5) [Fe(OH2)6]3+(aq) + 2Cl-(aq) → [Fe(OH2)4Cl2]+(aq) + 2H2O(l)
Hãy liệt kê các phản ứng thuộc loại phản ứng thế phối tử của phức chất theo thứ tự từ bé đến lớn. (Ví dụ: 124, 134, 1245…)
(Xem giải) Câu 24. Cho các kim loại sau: K, Mg, Zn, Fe, Ni, Cu, Ag. Có bao nhiêu kim loại có thể được điều chế bằng phương pháp điện phân dung dịch (với điện cực trơ)?
(Xem giải) Câu 25. Cho kí hiệu hóa học của các kim loại sau: Na, V, Al, Mg, Cr, Mn, Fe, Cu. Có bao nhiêu kim loại là kim loại chuyển tiếp?
(Xem giải) Câu 26. Nhựa cationite được sử dụng để làm mềm nước cứng. Khi nước cứng chảy qua cột chứa nhựa trao đổi ion, ion Ca2+ và Mg2+ trong nước sẽ bị hấp phụ và ở lại trên cột, đồng thời các ion H+ hoặc Na+ được giải phóng từ cột vào nước theo phản ứng tổng quát sau: 2RH + Ca2+ → R2Ca + 2H+. Cho 1 L mẫu nước chảy qua cột nhựa trao đổi cation, trong đó H+ được trao đổi với Ca2+. Nước ra khỏi cột cần 50 mL dung dịch NaOH 0,1 M để trung hòa hoàn toàn. Theo TCVN 5502: 2003, độ cứng của nước được xác định bằng tổng hàm lượng Ca2+ và Mg2+ quy đổi về khối lượng (mg) CaCO3 có trong 1 lít nước. Xác định độ cứng của mẫu nước trên (chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
(Xem giải) Câu 27. Để bảo vệ vật bằng thép khỏi bị ăn mòn, trong thực tế người ta sử dụng một số cách sau:
(1) Sơn kín bề mặt cánh cửa bằng thép.
(2) Tráng kẽm lên tấm thép khi làm tôn.
(3) Tráng thiếc lên vỏ hộp thực phẩm bằng thép.
(4) Gắn một số miếng kẽm lên vỏ tàu làm bằng thép.
(5) Bôi dầu mỡ lên ốc vít trên đường ray.
Trong số các cách trên, có bao nhiêu cách sử dụng phương pháp bảo vệ bề mặt?
(Xem giải) Câu 28. Một nhà máy sản xuất urea sử dụng quy trình Haber-Bosch để sản xuất ammonia: N2(g) + 3H2(g) ⇋ 2NH3(g) (1)
Giai đoạn sản xuất khí hydrogen để cung cấp cho phản ứng (1) được thực hiện bằng phản ứng của khí methane và hơi nước theo phương trình hóa học sau:
CH4(g) + H2O(g) → CO(g) + 3H2(g) (2)
Phản ứng (2) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy khí methane theo phương trình hóa học sau:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) (3)
Cho giá trị enthalpy tạo thành chuẩn của các chất được cho trong bảng sau:
| Chất | CH4(g) | CO2(g) | CO(g) | H2O(g) |
| -74,9 | -393,5 | -110,5 | -241,8 |
Biết hiệu suất tổng hợp ammonia theo quy trình Haber-Bosch đạt 98%; hiệu suất chuyển hóa của methane ở phản ứng (2) là 95%. Biết 80% lượng nhiệt tỏa ra từ phản ứng (3) được cung cấp cho phản ứng (2). Xét các phản ứng xảy ra ở điều kiện chuẩn. Tính khối lượng khí methane (theo tấn) cần thiết để sản xuất 6,8 tấn NH3 trong quy trình trên (chỉ làm tròn kết quả cuối cùng đến hàng phần mười).

Bình luận