[2026] Thi thử TN cụm trường phía bắc Lào Cai
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 117
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2A | 3B | 4B | 5D | 6D | 7A | 8C | 9B |
| 10A | 11C | 12D | 13A | 14A | 15C | 16C | 17D | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | S | S |
| (b) | S | S | S | Đ |
| (c) | Đ | Đ | S | S |
| (d) | S | Đ | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 391 | 23 | 0,02 | 23,3 | 5 | 123 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Xà phòng có thể được điều chế từ nguồn nguyên liệu nào sau đây?
A. Dầu thực vật và củ cải đường. B. Dầu thực vật, mỡ động vật và dầu mỏ.
C. Glycerol và dầu mỡ. D. Nước bồ hòn, bồ kết.
(Xem giải) Câu 2: Phản ứng cộng hydrogen bromide vào propylene diễn ra theo cơ chế như sau:
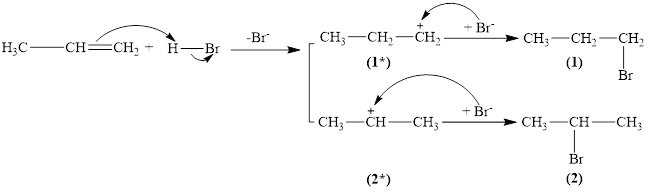
Các tiểu phân trung gian (1∗) và (2∗) là các carbocation. Độ bền tương đối của các carbocation tăng khi bậc của nguyên tử carbon mang điện tích dương tăng. Cho các phát biểu sau:
(1) Liên kết π trong propylene bị phá vỡ trong giai đoạn đầu tiên của phản ứng.
(2) Cơ chế của phản ứng trên diễn ra qua hai giai đoạn.
(3) Sản phẩm chính của phản ứng trên là sản phẩm (2) có tên gọi 2-bromopropane.
(4) Carbocation (1∗) có độ bền cao hơn carbocation (2∗).
Phát biểu đúng là
A. (1), (2), (3). B. (2), (3), (4). C. (1), (2), (4). D. (1), (2), (3), (4).
(Xem giải) Câu 3: Cho các cặp oxi hóa – khử của các kim loại và thế điện cực chuẩn tương ứng:
| Cặp oxi hóa – khử | Cu2+/Cu | Ag+/Ag | Fe2+/Fe | Ni2+/Ni |
| Thế điện cực chuẩn, V | +0,340 | +0,799 | -0,44 | -0,257 |
Trong số các ion kim loại trên, ion có tính oxi hóa mạnh nhất là
A. Fe2+. B. Ag+. C. Cu2+. D. Ni2+.
(Xem giải) Câu 4: Loại carbohydrate mạch phân nhánh, có nhiều trong các loại ngũ cốc là
A. amylose. B. amylopectin. C. cellulose. D. saccharose.
(Xem giải) Câu 5: Ở nơi tồn đọng rác thải, nên dùng chất nào sau đây để sát trùng, diệt khuẩn tạm thời?
A. Đá vôi. B. Than đá. C. Cát vàng. D. Vôi bột.
(Xem giải) Câu 6: Trùng hợp chất nào sau đây tạo thành polymer dùng để sản xuất tơ nitron?
A. H2N[CH2]5COOH. B. H2N[CH2]6NH2. C. CH2=CHCH3. D. CH2=CHCN.
(Xem giải) Câu 7: Phức chất nào sau đây của Cu2+ có màu vàng?
A. [CuCl4]2−. B. [Cu(NH3)4(H2O)2]. C. [Cu(H2O)6]2+. D. [Cu(OH)2(H2O)4].
(Xem giải) Câu 8: Giữa các nguyên tử He có thể có loại liên kết nào?
A. Liên kết cộng hóa trị. B. Liên kết hydrogen.
C. Tương tác van der Waals. D. Không có bất kì liên kết nào.
(Xem giải) Câu 9: Sữa chua được lên men từ các loại sữa (sữa bò, sữa dê, sữa bột,…). Vị chua trong sữa chua tạo bởi acid nào sau đây?
A. Acetic acid. B. Lactic acid. C. Formic acid. D. Benzoic acid.
(Xem giải) Câu 10: Thành phần cơ bản của enzyme là
A. protein. B. carbohydrate. C. lipid. D. nucleic acid.
(Xem giải) Câu 11: Trong bảng tuần hoàn, nguyên tố copper (Cu, cấu hình electron: [Ar]3d104s1) thuộc
A. chu kì 4, nhóm IIA. B. chu kì 4, nhóm IA. C. chu kì 4, nhóm IB. D. chu kì 4, nhóm IIB.
(Xem giải) Câu 12: Cho hai phản ứng:
Fe(s) + Cu2+(aq) → Fe2+(aq) + Cu(s)
Fe2+(aq) + Ag+(aq) → Fe3+(aq) + Ag(s)
Số cặp oxi hóa – khử trong phản ứng trên là
A. 3. B. 2. C. 5. D. 4.
(Xem giải) Câu 13: Linalyl acetate là một ester tự nhiên được tìm thấy trong nhiều loại tinh dầu, đặc biệt là tinh dầu cam và tinh dầu oải hương (lavender). Đây là một hợp chất quan trọng trong công nghiệp nước hoa và mỹ phẩm nhờ mùi hương dễ chịu và dịu nhẹ của nó.
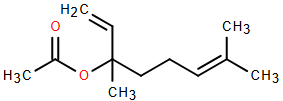
Cho các phát biểu sau về linalyl acetate:
(1) Linalyl acetate có đồng phân hình học.
(2) Linalyl acetate có số liên kết σ là 33.
(3) Thủy phân hoàn toàn linalyl acetate thu được một muối và một ketone.
(4) Hydrogen hóa hoàn toàn linalyl acetate (xt, t°, p) thu được ester có công thức phân tử là C12H24O2.
Phát biểu đúng là
A. (2), (4). B. (1), (3). C. (1), (2), (4). D. (2), (3), (4).
(Xem giải) Câu 14: Thủy ngân dễ bay hơi và rất độc. Khi nhiệt kế thủy ngân bị vỡ, dùng chất nào sau đây để khử độc?
A. Bột lưu huỳnh. B. Nước. C. Bột sắt. D. Bột than.
(Xem giải) Câu 15: “Đất chua” là loại đất có môi trường acid, pH của “đất chua” có giá trị
A. bằng 0. B. bằng 7. C. nhỏ hơn 7. D. lớn hơn 7.
(Xem giải) Câu 16: Một trong những vụ tai nạn nghiêm trọng trong ngành chế biến thực phẩm là vụ nổ tại nhà máy đường Imperial Sugar (Hoa Kỳ) ngày 7/2/2008 tại bang Georgia. Theo báo cáo của U.S. Chemical Safety and Hazard Investigation Board, nguyên nhân là do bụi đường tích tụ trong không gian kín, bị kích hoạt bởi nguồn nhiệt, gây cháy nổ lan rộng. Vụ việc làm 14 người tử vong, 38 người bị thương và phá hủy phần lớn nhà máy. Nổ bụi xảy ra khi hội tụ các yếu tố: bụi cháy được, oxygen, nguồn nhiệt, nồng độ bụi cao và không gian kín. Khi những yếu tố này cùng tồn tại, nguy cơ cháy nổ tăng mạnh và gây hậu quả rất nghiêm trọng. Một bạn học sinh đề xuất các biện pháp sau để phòng tránh nguy cơ nổ bụi trong tương lai:
(1) Lắp đặt hệ thống hút bụi để giảm lượng bụi trong không khí.
(2) Kiểm tra, bảo trì hệ thống điện định kỳ để tránh phát sinh tia lửa.
(3) Đóng kín toàn bộ cửa xưởng để tránh bụi phát tán ra ngoài.
(4) Lắp đặt hệ thống thông gió nhằm giảm sự tích tụ bụi trong không gian kín.
Theo em, những biện pháp nào là phù hợp nhất để giảm nguy cơ nổ bụi trong thực tế sản xuất?
A. (2), (3). B. (3), (4). C. (1), (2), (4). D. (1), (2), (3).
(Xem giải) Câu 17: Levodopa (L-dopa) là tiền chất của dopamine, thường được sử dụng như một chất thay thế dopamine để điều trị bệnh Parkinson.

Cho các phát biểu sau về L-dopa:
(1) L-dopa có khả năng phản ứng với nước bromine.
(2) L-dopa là một α-amino acid.
(3) Công thức phân tử của L-dopa là C8H11NO4.
(4) 1 mol L-dopa có thể phản ứng tối đa với 3 mol NaOH trong dung dịch.
Số phát biểu đúng là
A. 1. B. 4. C. 2. D. 3.
(Xem giải) Câu 18: Cho sơ đồ chuyển hóa sau:
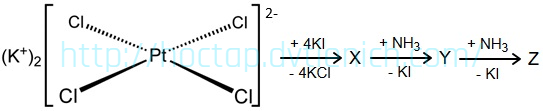
Biết rằng X, Y, Z đều là các phức chất đơn nhân. Cho các nhận định sau:
(1) Các phản ứng trên đều có sự thay thế phối tử trong phức chất.
(2) Trong phức chất Y, có hai phối tử NH3 và hai phối tử Cl-.
(3) Trong nước, dung dịch chất Z có khả năng dẫn điện tốt.
(4) Điện tích của phức Y là +2.
(5) Các phản ứng trong chuỗi trên đều kèm theo sự thay đổi số oxi hóa của nguyên tử trung tâm.
Số nhận định đúng là
A. 4. B. 1. C. 2. D. 3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Trong công nghiệp, kim loại Na được điều chế bằng cách điện phân NaCl nóng chảy trong bình điện phân Downs với điện áp khoảng 7V, cường độ dòng điện từ 25000A đến 40000A với các điện cực anode bằng than chì và cathode bằng Fe. Kim loại Na sinh ra ở trạng thái nóng chảy nhẹ hơn NaCl nóng chảy nên nổi lên, vì vậy hệ thống thu được lắp đặt ở phía trên. Lưới sắt giúp ngăn cho Na (ở trạng thái nóng chảy) không phản ứng lại với Cl2. Sơ đồ bình điện phân được mô tả như hình bên.

a) Khi sử dụng cường độ dòng điện là 25000A thì sau 12 giờ sản xuất được 206 kg sodium (hiệu suất của cả quá trình đạt 80%). Biết điện lượng q = I.t = ne.F, trong đó: q là điện lượng (C), ne là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian điện phân (giây), F = 96500 C/mol. (Kết quả cuối cùng làm tròn đến hàng đơn vị)
b) Nếu không có lưới sắt, Na và Cl2 vẫn được tách riêng hoàn toàn nên hiệu suất điện phân không thay đổi.
c) Hệ thống thu Na nóng chảy đặt trong khí trơ để tránh Na bị oxi hóa bởi không khí.
d) Có thể thay anode than chì bằng Fe vì Fe dẫn điện tốt.
(Xem giải) Câu 20: PMMA (polymethyl methacrylate) là một loại nhựa nhiệt dẻo trong suốt thường được sử dụng để làm kính, miếng nhựa mềm, hộp và có thể được dùng để thay thế cho kính và thủy tinh. PMMA được điều chế theo 2 giai đoạn: Methyl alcohol tác dụng với methacrylic acid tạo thành methyl methacrylate (giai đoạn 1). Trùng hợp methyl methacrylate tạo thành PMMA (giai đoạn 2).
a) Các thủy tinh được dùng trong phòng thí nghiệm có thành phần chủ yếu là poly (methyl methacrylate).
b) Để sản xuất 1000 hộp đựng thực phẩm hình hộp chữ nhật (không tính nắp) có chiều dài 9 cm, chiều rộng 6,5 cm, chiều cao 4 cm và độ dày 5 mm (khối lượng riêng của hộp là D = 1,2 g/cm³) người ta cần tối thiểu 74,304 kg methacrylic acid. Biết trong mỗi hộp khối lượng PMMA chiếm 90% và hiệu suất phản ứng của toàn bộ quá trình tính theo methacrylic acid là 80%.
c) Phản ứng thủy phân methyl methacrylate trong môi trường NaOH được gọi là phản ứng xà phòng hóa.
d) Trong giai đoạn 1, H2SO4 đặc vừa làm xúc tác vừa làm dịch chuyển cân bằng theo chiều tạo ester.
(Xem giải) Câu 21: Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Cho khoảng 5 mL dung dịch HNO3 đặc vào cốc thủy tinh (loại 100 mL) ngâm trong chậu nước đá. Thêm từ từ khoảng 10 mL dung dịch H2SO4 đặc và khuấy đều. Sau đó, lấy cốc ra khỏi chậu nước đá, cho một nhúm bông vào và dùng đũa thủy tinh ấn ngập hoàn toàn trong dung dịch.
• Bước 2: Ngâm cốc trong chậu nước nóng khoảng 10 phút. Để nguội, lấy sản phẩm thu được ra khỏi cốc, rửa nhiều lần với nước lạnh đến khi nước rửa không làm đổi màu quỳ tím, rồi tiếp tục rửa bằng dung dịch NaHCO3 loãng.
• Bước 3: Cho sản phẩm vào giữa 2 tờ giấy lọc, ép để hút nước và để khô tự nhiên.
a) Sau bước 3, lấy sản phẩm thu được đốt cháy thấy có nhiều khói trắng xuất hiện.
b) Ở bước 2, thêm từ NaHCO3 để phản ứng thủy phân diễn ra hoàn toàn.
c) Ở bước 3, có thể thay việc làm khô sản phẩm tự nhiên bằng cách sấy ở nhiệt độ cao.
d) Bước 1 cần làm lạnh vì trộn HNO3 và H2SO4 tỏa nhiệt mạnh, để đảm bảo an toàn và tăng hiệu quả phản ứng.
(Xem giải) Câu 22: Cho các loại nước được đánh dấu X, Y, Z, T có chứa các ion như sau:
| X | Y | Z | T |
| Ca2+, Mg2+ (nhiều); Cl-, SO42-, HCO3- | Ca2+, Mg2+ (nhiều); Cl-, SO42- | Ca2+, Mg2+ (nhiều); HCO3- | Na+, K+; HCO3- |
a) Đun sôi có thể loại bỏ hoàn toàn tính cứng của cả nước X và nước Z.
b) Có thể loại bỏ hoàn toàn tính cứng của nước Y bằng dung dịch Na2CO3 dư.
c) Thực hiện quy trình đun nóng từng mẫu đến khi không còn khí thoát ra, gạn bỏ kết tủa, sau đó thêm NaOH dư không thể nhận biết được đâu là X, Y, Z và T.
d) Nước Z là nước cứng tạm thời.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Phản ứng tổng hợp ammonia: N2(g) + 3H2(g) ⇋ 2NH3(g); ![]() = -92 kJ. Biết năng lượng liên kết (kJ/mol) của N≡N và H–H lần lượt là 946 và 436. Tính năng lượng liên kết (kJ/mol) của N-H trong ammonia.
= -92 kJ. Biết năng lượng liên kết (kJ/mol) của N≡N và H–H lần lượt là 946 và 436. Tính năng lượng liên kết (kJ/mol) của N-H trong ammonia.
(Xem giải) Câu 24: Cho các chất: (1) CH3[CH2]14COONa; (2) CH3[CH2]10CH2OSO3Na; (3) CH3[CH2]11C6H4SO3Na; (4) CH3OSO3Na. Liệt kê chất là thành phần chủ yếu của chất giặt rửa tổng hợp theo thứ tự tăng dần. (ví dụ: 1234, 24…)
(Xem giải) Câu 25: Một mẫu nước thải công nghiệp chứa ion Zn2+ được phân tích bằng phương pháp chuẩn độ gián tiếp như sau: Lấy chính xác 25,00 mL mẫu, cho phản ứng hoàn toàn với 30,00 mL dung dịch K4[Fe(CN)6] 0,02M tạo kết tủa Zn2[Fe(CN)6]. Sau khi phản ứng kết thúc, lọc bỏ kết tủa. Phần dung dịch lọc chứa [Fe(CN)6]4− dư, được chuẩn độ bằng dung dịch KMnO4 0,01M trong môi trường acid. Thể tích dung dịch KMnO4 0,01M đã dùng là 8,00 mL. Xác định nồng độ mol/L của Zn2+ trong dung dịch ban đầu. (Làm tròn kết quả cuối cùng đến hàng phần trăm). Biết: MnO4- + [Fe(CN)6]4- + H+ → Mn2+ + [Fe(CN)6]3- + H2O.
(Xem giải) Câu 26: Xét acquy chì gồm điện cực Pb (cực âm) và PbO2 (cực dương) trong dung dịch H2SO4. Khi phóng điện xảy ra phản ứng: Pb + PbO2 + 2H2SO4 → 2PbSO4 + 2H2O
Acquy ban đầu chứa 1 lít dung dịch H2SO4 33,5% (D = 1,25 g/mL). Sau một thời gian phóng điện, khối lượng điện cực Pb tăng 76,8 gam, nồng độ H2SO4 còn lại là x%. Hiệu suất phóng điện 90%, thể tích nước bay hơi không đáng kể, PbSO4 sinh ra bám hoàn toàn trên điện cực. Tính x (làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 27: Cho peptide X: Gly-Ala-Lys-Glu. Một mol X phản ứng tối đa với bao nhiêu mol KOH trong dung dịch?
(Xem giải) Câu 28: Khi nhỏ vài giọt sulfuric acid vào một xấp giấy ăn khô, giấy ăn sẽ hóa đen ở chỗ tiếp xúc, bốc cháy và tạo nhiều khói; khói này có thể làm đổi màu giấy quỳ tím ẩm. Xét các phát biểu sau:
(1) Giấy ăn hóa đen (than hóa) là do cellulose trong giấy bị khử thành carbon.
(2) Khí sinh ra (SO2) có tính oxi hóa nên làm mất màu dung dịch KMnO4.
(3) Khói sinh ra chủ yếu chứa sulfur trioxide là một acidic oxide.
Liệt kê các phát biểu sai theo thứ tự tăng dần.

Bình luận