[2026] Thi thử TN chuyên KHTN Hà Nội (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 029
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2B | 3D | 4C | 5A | 6D | 7B | 8D | 9C |
| 10B | 11C | 12C | 13A | 14C | 15B | 16C | 17B | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | S | Đ | 304 | 5 | 4321 |
| (b) | Đ | Đ | Đ | Đ | 26 | 27 | 28 |
| (c) | S | S | Đ | Đ | 6,27 | 203 | 145 |
| (d) | S | Đ | S | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Hợp chất nào sau đây thuộc loại protein?
A. Hemoglobin. B. Cocaine. C. Triglyceride. D. Cellulose.
(Xem giải) Câu 2: Kim loại tungsten (W) được sử dụng làm dây tóc bóng điện. Ứng dụng này được dựa trên cơ sở tính chất vật lí nào sau đây của tungsten?
A. Tính dẻo. B. Nhiệt độ nóng chảy cao.
C. Tính ánh kim. D. Tính dẫn nhiệt.
(Xem giải) Câu 3: Cho lượng dư methylamine vào dung dịch CuSO4 thì thu được
A. kết tủa màu đen. B. kết tủa màu xanh lam.
C. dung dịch không màu. D. dung dịch màu xanh lam.
(Xem giải) Câu 4: Trong sơ đồ của phương pháp sắc kí cột với pha tĩnh là chất hấp phụ silica gel và pha động là chloroform (CHCl3). Thứ tự đi ra khỏi cột hấp phụ lần lượt là các chất X, Y, Z, T. Chất có tương tác mạnh nhất với pha tĩnh là
A. chất Z. B. chất Y. C. chất T. D. chất X.
(Xem giải) Câu 5: Trong dãy các chất hydrogen fluoride (HF), hydrogen chloride (HCl), hydrogen bromide (HBr), hydrogen iodide (HI) thì hydrogen fluoride có nhiệt độ sôi cao nhất. Điều này được giải thích là do
A. giữa các phân tử HF có liên kết hydrogen.
B. tương tác Van der Waals trong HF mạnh nhất.
C. HF có tính acid mạnh nhất.
D. phân tử HF có độ dài liên kết ngắn nhất.
(Xem giải) Câu 6: Phản ứng chung trong pin Galvani X-Y là: X(s) + Y2+(aq) → Y(s) + X2+(aq)
Với X và Y là các kim loại. Quá trình xảy ra tại cathode (hay cực dương) của pin là
A. Y(s) → Y2+(aq) + 2e. B. X2+(aq) + 2e → X(s).
C. X(s) → X2+(aq) + 2e. D. Y2+(aq) + 2e → Y(s).
(Xem giải) Câu 7: Nhóm chức luôn có mặt trong các phân tử carbohydrate là nhóm nào?
A. -COOH (carboxyl). B. -OH (hydroxy).
C. C=O (ketone). D. -CHO (aldehyde).
(Xem giải) Câu 8: Phản ứng của methane với chlorine tạo thành methyl chloride theo phương trình hóa học: CH4 + Cl2 (as) → CH3Cl + HCl
Cơ chế của phản ứng như sau:
Giai đoạn 1: Khơi mào
Cl-Cl (ánh sáng) → Cl• + Cl•
Giai đoạn 2: Phát triển mạch
CH3-H + Cl• → •CH3 + HCl
•CH3 + Cl-Cl → CH3Cl + Cl•
CH3-H + Cl• → …
Giai đoạn 3: Kết thúc
Cl• + Cl• → Cl2
•CH3 + Cl• → CH3Cl
•CH3 + •CH3 → CH3CH3
Phát biểu nào sau đây sai?
A. Tiểu phân •CH3 chứa electron chưa ghép đôi nên được gọi là gốc tự do.
B. Nếu thay Cl2 bằng Br2 thì giai đoạn ba (kết thúc) cũng thu được ethane.
C. Sản phẩm CH3Cl được sinh ra chủ yếu ở giai đoạn hai (phát triển mạch).
D. Các góc liên kết trong phân tử CH3Cl đều bằng nhau và bằng 90°.
(Xem giải) Câu 9: Trong các hợp chất HCHO, CH3CHO, CH3COCH3 và CH3CH2CH2CHO, hợp chất có độ tan trong nước kém nhất là
A. CH3COCH3. B. HCHO. C. CH3CH2CH2CHO. D. CH3CHO.
(Xem giải) Câu 10: Cho các phản ứng sau:
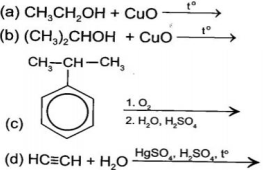
Những phản ứng có sản phẩm aldehyde là
A. (c). B. (a) và (d). C. (a). D. (b) và (c).
(Xem giải) Câu 11: Poly(methyl methacrylate) cho ánh sáng truyền qua trên 90%, được sử dụng làm thuỷ tinh hữu cơ. Thực hiện phản ứng trùng hợp monomer nào sau đây thu được poly(methyl methacrylate)?
A. CH2=CHCOOCH3. B. CH2=CHC6H5.
C. CH2=C(CH3)COOCH3. D. CH2=CHCl.
(Xem giải) Câu 12: Polymer nào sau đây có chứa nguyên tố nitrogen?
A. Polystyrene. B. Polyisoprene.
C. Nylon-6,6. D. Poly(vinyl chloride).
(Xem giải) Câu 13: Chất nào sau đây làm mềm được nước có tính cứng toàn phần?
A. Na2CO3. B. KCl. C. NaCl. D. KNO3.
(Xem giải) Câu 14: Protein tham gia phản ứng với dung dịch HNO3 đặc tạo thành hợp chất rắn có màu gì?
A. Tím. B. Xanh. C. Vàng. D. Trắng.
(Xem giải) Câu 15: Bơ thực vật (margarine) là loại được điều chế từ dầu thực vật. Để chuyển hoá dầu thực vật thành bơ thực vật người ta thực hiện phản ứng …(1)… nhằm chuyển chất béo không no thành chất béo no. Nội dung phù hợp với chỗ trống (1) là
A. oxi hoá. B. hydrogen hoá. C. xà phòng hoá. D. hydrate hoá.
(Xem giải) Câu 16: Những alcohol bền (có thể tồn tại độc lập) trên thực tế đều có đặc điểm là nhóm -OH liên kết với các nguyên tử carbon no và mỗi nguyên tử carbon chỉ liên kết tối đa với một nhóm -OH. Cho các hợp chất có công thức cấu tạo sau:
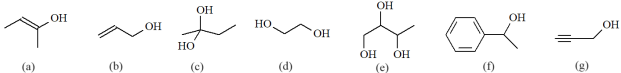
Số alcohol bền là
A. 4. B. 3. C. 5. D. 6.
(Xem giải) Câu 17: Khi nồng độ các chất dinh dưỡng như NO3-, PO43-,… tăng cao trong nước dẫn đến sự phát triển quá mức của các loại thực vật như tảo, bèo,… trong nước làm giảm nồng độ oxygen trong nước. Hiện tượng này được gọi là hiện tượng
A. thoái hoá đất. B. phú dưỡng. C. mưa acid. D. nhiễm phèn.
(Xem giải) Câu 18: Điện phân (với các điện cực trơ) dung dịch NaCl có màng ngăn giữa hai điện cực, sau điện phân thu được dung dịch chứa NaOH và NaCl, khí thoát ra từ bình điện phân là H2 và Cl2. Bán phản ứng xảy ra ở anode là
A. 4OH- → O2 + 2H2O + 4e B. 2H2O + 2e → H2 + 2OH-.
C. 2Na+ + 2e → 2Na. D. 2Cl- → Cl2 + 2e
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Một nhóm học sinh được yêu cầu xác định nồng độ mol/L của acetic acid có trong chai giấm (được đậy kín). Nhóm học sinh đó tiến hành theo các bước sau:
• Bước 1: Lấy 25,00 mL mẫu giấm cho vào bình định mức, sau đó thêm nước để được 500 mL dung dịch X. Lấy ra 25,00 mL dung dịch X vào bình nón, thêm vào đó 3 – 4 giọt chất chỉ thị phenolphthalein (điểm tương đương được nhận biết khi dung dịch có màu hồng nhạt bền).
• Bước 2: Dùng pipette lấy dung dịch NaOH 0,10M rồi cho vào burette đến vạch 0 trên burette.
• Bước 3: Mở khoá burette cho dung dịch NaOH từ từ vào dung dịch X. Khi có màu hồng xuất hiện và mất luôn, nhỏ chậm từng giọt dung dịch NaOH vào cho đến khi màu hồng nhạt bền thì dừng lại. Điểm tương đương của phép chuẩn độ ứng với acetic acid và sodium hydroxide đều đã hết.
Lặp lại thí nghiệm thêm 2 lần nữa. Kết quả của 3 lần chuẩn độ được thể hiện trong bảng sau:
| Lần thí nghiệm | Lần 1 | Lần 2 | Lần 3 |
| Vdd NaOH (mL) | 19,75 | 19,85 | 19,80 |
a) Giả thuyết của nhóm học sinh đưa ra là: nếu tiến hành chuẩn độ dung dịch CH3COOH bằng dung dịch NaOH thì có thể xác định được nồng độ CH3COOH trong mẫu giấm.
b) Phản ứng chuẩn độ trong phép chuẩn độ trên là CH3COOH + NaOH → CH3COONa + H2O.
c) Dung dịch thu được có môi trường trung tính.
d) Nếu khối lượng riêng của mẫu giấm đo được là D = 1,050 g/mL thì nồng độ % của CH3COOH trong mẫu giấm là 4,53%.
(Xem giải) Câu 20: Muối FeCl3 khan là những tinh thể có màu vàng nâu. Hoà tan một lượng muối này vào dung dịch H2SO4 loãng, thu được dung dịch X có màu vàng nhạt (màu của phức chất aqua). Nhỏ tiếp dung dịch KSCN vào dung dịch X, thu được dung dịch có màu đỏ máu. Hiện tượng trên được giải thích là do 1 phối tử H2O đã được thay thế bởi 1 phối tử SCN- để tạo thành phức chất Y. Các phức chất trong X và phức chất Y đều là phức bát diện.
a) Hiện tượng đổi màu trong thí nghiệm trên biểu diễn bởi phương trình hoá học sau:
[Fe(OH2)6]3+(aq) + SCN-(aq) → [Fe(SCN)(OH2)5]2+(aq) + H2O(l)
b) Trong phức chất aqua của iron(III), nguyên tử trung tâm liên kết với 6 phối tử H2O qua 6 nguyên tử oxygen.
c) Khi thay dung dịch H2SO4 loãng bằng dung dịch NaOH loãng dư, cũng thu được dung dịch có màu vàng.
d) Do sự đổi màu khi phản ứng với ion SCN-, nên có thể sử dụng dung dịch KSCN để nhận biết các muối iron(III) trong dung dịch.
(Xem giải) Câu 21: Một nhóm học sinh tiến hành xác định biến thiên enthalpy của phản ứng giữa kim loại Mg với hydrochloric acid theo phản ứng: Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g) (1)
Biến thiên enthalpy của phản ứng được xác định một cách gần đúng bởi công thức sau: ![]()
Trong đó: C là nhiệt lượng cần để tăng nhiệt độ của môi trường phản ứng lên 1°C; ∆T là nhiệt độ chênh lệch trong thí nghiệm; mMg là số gam Mg phản ứng. Nhóm học sinh tiến hành thí nghiệm theo các bước sau:
• Bước 1: Lấy 1000 gam nước cho vào bình cách nhiệt (nhiệt không thoát ra bên ngoài); cho tiếp 20 gam dung dịch HCl 14,6% vào ống đầu tròn và đặt nhiệt kế vào trong bình (xem hình vẽ). Dữ kiện được tính toán cho biết nhiệt lượng để nâng nhiệt độ của hệ phản ứng lên 1°C là 4205 J.
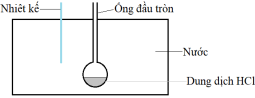
• Bước 2: Cho 0,5 gam bột Mg vào ống đầu tròn và ghi lại giá trị nhiệt độ cao nhất của nhiệt kế sau thí nghiệm. Thí nghiệm được lặp lại thêm hai lần nữa. Kết quả được thể hiện qua bảng sau:
| Thí nghiệm | 1 | 2 | 3 |
| Nhiệt độ ban đầu (°C) | 25,0 | 25,5 | 26,0 |
| Nhiệt độ cao nhất (°C) | 27,3 | 27,9 | 28,4 |
a) Dựa vào công thức và kết quả thí nghiệm, nhóm học sinh xác định được biến thiên enthalpy của phản ứng (1) là ΔrH° = 464 kJ (Kết quả được làm tròn đến hàng đơn vị).
b) Nhiệt độ của nước và nhiệt kế tăng lên là do nước nhận được lượng nhiệt sinh ra từ phản ứng (1).
c) Giả thuyết nhóm học sinh đưa ra là “Phản ứng giữa kim loại magnesium (Mg) và dung dịch hydrochloric acid (HCl) là phản ứng tỏa nhiệt và có thể xác định được biến thiên enthalpy của phản ứng dựa trên sự thay đổi nhiệt độ của nước và nhiệt kế”.
d) Chênh lệch nhiệt độ trung bình của các thí nghiệm được xác định theo biểu thức: ∆T = Tmax – Tmin; trong đó Tmax là nhiệt độ cao nhất của ba thí nghiệm sau phản ứng; Tmin là nhiệt độ ban đầu thấp nhất của ba thí nghiệm trước phản ứng.
(Xem giải) Câu 22: Phân tích nguyên tố hợp chất hữu cơ E cho kết quả phần trăm khối lượng carbon, hydrogen và oxygen lần lượt là 54,55%; 9,09% và 36,36%. Khối phổ (MS) của E cho giá trị m/z của mảnh ion phân tử [M+] bằng 88. Phổ hồng ngoại (IR) cho thấy phân tử E chứa nhóm C=O (peak hẹp, cường độ mạnh, có số sóng 1748 cm-1). Cho E tác dụng với dung dịch NaOH, thu được muối của carboxylic acid X và chất Y. Chất Y có nhiệt độ sôi (64,7 °C) nhỏ hơn nhiệt độ sôi của ethanol (78,3°C); (các nhiệt độ sôi đều được đo ở áp suất 1 bar).
a) Chất E không có phản ứng tạo iodoform
b) Dung dịch muối tạo bởi carboxylic acid X với NaOH có môi trường base.
c) Chất E có tên gọi là methyl propionate.
d) Thực hiện phản ứng giữa chất Y với khí carbon monoxide trong điều kiện thích hợp, thu được chất X.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Zeolite là vật liệu có thành phần dạng (NaAlO2)x(SiO2)y.zH2O. Khi cho nước cứng đi qua zeolite, các cation trong nước cứng như Mg2+, Ca2+ sẽ thay thế các ion Na+ trong zeolite theo sơ đồ:
2Na+(zeolite) + M2+(aq) → M2+(zeolite) + 2Na+(aq)
Zeolite X có công thức là (NaAlO2)2(SiO2)3.2H2O được sử dụng để làm mềm nước cứng. Khối lượng X (theo kg) cần lấy cho việc làm mềm 100 m³ nước chứa Ca2+ 9.10^-3 M, Cl- 4.10^-3M và HCO3- 1,4.10^-2M, để làm giảm 80% lượng ion Ca2+ có trong nước cứng là bao nhiêu? Biết rằng 90% lượng Na+ trong zeolite X tham gia quá trình trao đổi.
(Xem giải) Câu 24: Amine X có chứa vòng benzene và có công thức phân tử là C7H9N. Số công thức cấu tạo có thể có của X là bao nhiêu?
(Xem giải) Câu 25: Cho biết biến thiên enthalpy của các phản ứng đốt cháy các chất sau ở điều kiện chuẩn:
| Chất (kí hiệu) | CH4 (1) | C2H4 (2) | C2H2 (3) | C2H5OH (4) |
| ΔrH° (kJ) | -890 | -1411 | -1300 | -1367 |
Hãy sắp xếp các chất theo chiều tăng dần lượng nhiệt toả ra khi đốt cháy hoàn toàn cùng một khối lượng mỗi chất.
(Xem giải) Câu 26: Sơ đồ của phản ứng tổng hợp poly(methyl methacrylate) từ acetone như sau:
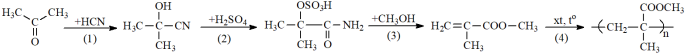
Hiệu suất của cả quá trình đạt 92,5%. Tính khối lượng acetone (theo tấn) cần lấy để sản xuất được 10 tấn poly(methyl methacylate). (Làm tròn kết quả đến hàng phần trăm).
(Xem giải) Câu 27: Xét phản ứng có phương trình hóa học: 2ClO2 + 2NaOH → NaClO3 + NaClO2 + H2O
Tốc độ phản ứng được viết như sau: ![]() ; trong đó C là nồng độ mol/L của chất. Thực hiện phản ứng với những nồng độ chất đầu khác nhau và đo tốc độ phản ứng tương ứng, thu được kết quả trong bảng dưới đây:
; trong đó C là nồng độ mol/L của chất. Thực hiện phản ứng với những nồng độ chất đầu khác nhau và đo tốc độ phản ứng tương ứng, thu được kết quả trong bảng dưới đây:
| STT | Nồng độ ClO2 (M) | Nồng độ NaOH (M) | Tốc độ phản ứng (mol/(L.s)) |
| 1 | 0,01 | 0,01 | 2.10-4 |
| 2 | 0,02 | 0,01 | 8.10-4 |
| 3 | 0,01 | 0,02 | 4.10-4 |
Tổng (x + y + k) trong biểu thức tốc độ phản ứng bằng bao nhiêu?
(Xem giải) Câu 28: Reforming alkane là quá trình chuyển các alkane mạch không phân nhánh thành các alkane mạch phân nhánh và các hydrocarbon mạch vòng nhưng không làm thay đổi số nguyên tử carbon trong phân tử và cũng không làm thay đổi đáng kể nhiệt độ sôi của chúng. Reforming làm tăng chỉ số octane của xăng hoặc tạo ra các hợp chất để làm nguyên liệu cho hóa dầu. Cho các phản ứng sau:
(1) Hexane → isohexane
(2) 2Methane → acetylene + 3H2
(3) Octane → Butane + But-1-ene
(4) Octane → 2,2,4-trimethylpentane
(5) Octane → p-Xylene + 4H2
Hãy lập thành bộ số theo thứ tự từ nhỏ đến lớn đối với các phản ứng thuộc loại reforming.


Bình luận