[2026] Thi thử TN cụm chuyên môn số 8 – Ninh Bình (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 090
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3C | 4B | 5B | 6B | 7B | 8D | 9A |
| 10D | 11C | 12D | 13B | 14B | 15B | 16B | 17B | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | S | Đ | S | S |
| (b) | Đ | S | Đ | Đ |
| (c) | Đ | Đ | S | Đ |
| (d) | Đ | S | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 1245 | 715 | 2314 | 13 | 28 | 18 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Công thức cấu tạo của đoạn mạch dưới đây mô tả cấu tạo của chất nào?
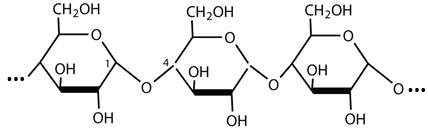
A. Saccharose. B. Cellulose. C. Amylose. D. Amylopectin.
(Xem giải) Câu 2. Nhỏ dung dịch X vào dung dịch Y thu được kết tủa trắng Z, biết Z tan trong dung dịch acid mạnh. Vậy X và Y lần lượt là
A. Na2CO3 và HCl. B. BaCl2 và H2SO4. C. CaCl2 và Na2CO3. D. Ca(OH)2 và H2SO4.
(Xem giải) Câu 3. Cho các chất sau: NaOH, Cu, CuO, CaCO3, CH3OH. Số chất phản ứng được với acetic acid trong điều kiện thích hợp là
A. 5. B. 2. C. 4. D. 3.
(Xem giải) Câu 4. Polypropylene (PP) là một polymer nhiệt dẻo, được dùng làm hộp đựng thực phẩm, bao gói, ống nước,… PP được điều chế từ monomer nào sau đây ?
A. Styrene. B. Propylene. C. Ethylene. D. Vinyl chloride.
(Xem giải) Câu 5. Cho các amino acid có công thức cấu tạo sau:
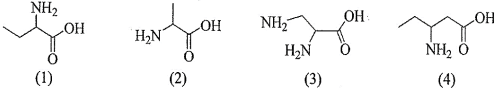
Có bao nhiêu chất thuộc loại α-amino acid?
A. 4. B. 3. C. 1. D. 2.
(Xem giải) Câu 6. Cầu chì là một thiết bị bảo vệ mạch điện bằng cách làm đứt mạch điện. Cầu chì được sử dụng nhằm phòng tránh các hiện tượng quá tải trên đường dây. Dây cầu chì thường được làm từ kim loại chì (Pb), thiếc trắng (Sn) hoặc cadmium (Cd). Ứng dụng này dựa trên tính chất nào của các kim loại trên?
A. Có độ cứng tương đối thấp.
B. Có nhiệt độ nóng chảy tương đối thấp.
C. Có tính dẻo cao.
D. Có độ dẫn điện cao.
(Xem giải) Câu 7. Cho thế điện cực chuẩn của các cặp oxi hóa – khử Fe3+/Fe2+ và Cu2+/Cu lần lượt là 0,771V và 0,340V. Nhận định nào sau đây đúng ?
A. Ở điều kiện chuẩn, ion Fe2+ có thể khử ion Cu2+ thành Cu.
B. Ở điều kiện chuẩn, ion Fe3+ có thể bị khử thành ion Fe2+ bởi kim loại Cu.
C. Tính oxi hóa của ion Cu2+ mạnh hơn tính oxi hóa của ion Fe3+.
D. Tính khử của Cu yếu hơn tính khử của ion Fe2+.
(Xem giải) Câu 8. Công thức cấu tạo nào sau đây mô tả amine bậc hai?
A. CH3CH2N(CH3)2. B. (CH3)2CHNH2. C. CH3CH2NH2. D. CH3NHCH2CH3.
(Xem giải) Câu 9. Cho sơ đồ gồm hai phản ứng hoá học xảy ra ở điều kiện thích hợp: X → NaOH → Na2CO3. Trong số các chất: Na, Na2SO4, Na2O, NaCl, số chất phù hợp với X là bao nhiêu?
A. 4. B. 2. C. 1. D. 3.
(Xem giải) Câu 10. Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane: CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ![]() = –890,3 kJ. Nếu đốt cháy hoàn toàn 9,916 L khí CH4 (g) ở điều kiện chuẩn thì nhiệt lượng sẽ biến đổi như thế nào?
= –890,3 kJ. Nếu đốt cháy hoàn toàn 9,916 L khí CH4 (g) ở điều kiện chuẩn thì nhiệt lượng sẽ biến đổi như thế nào?
A. Thu vào 356,12 kJ. B. Thu vào 890,3 kJ. C. Tỏa ra 890,3 kJ. D. Tỏa ra 356,12 kJ
(Xem giải) Câu 11. Một mẫu nước sinh hoạt chứa nhiều các ion: Ca2+, Mg2+, Cl-, SO42-. Nước sinh hoạt trên thuộc loại gì?
A. Nước có tính cứng tạm thời. B. Nước có tính cứng toàn phần.
C. Nước có tính cứng vĩnh cửu. D. Nước mềm.
(Xem giải) Câu 12. Ester no, đơn chức, mạch hở có công thức chung là
A. CnH2n-2O2 (n ≥ 2). B. CnH2n+2O2 (n ≥ 2). C. CnH2nO2 (n ≥ 1). D. CnH2nO2 (n ≥ 2).
(Xem giải) Câu 13. Cho các pin điện hoá và sức điện động chuẩn tương ứng :
| Pin điện hóa | Cu–X | Y–Cu | Z–Cu |
| Sức điện động chuẩn (V) | 0,46 | 1,1 | 1,47 |
(X, Y, Z là ba kim loại) Dãy các kim loại xếp theo chiều tăng dần tính khử từ trái sang phải là:
A. X, Cu, Z, Y. B. X, Cu, Y, Z. C. Z, Y, Cu, X. D. Y, Z, Cu, X.
(Xem giải) Câu 14. Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
A. Cu. B. Mg. C. Ag. D. Fe.
(Xem giải) Câu 15. Trong nước, thế điện cực chuẩn của kim loại Mn+/M càng lớn thì dạng khử có tính khử …(1)… và dạng oxi hoá có tính oxi hoá …(2)… Cụm từ cần điền vào (1) và (2) lần lượt là
A. càng mạnh và càng yếu. B. càng yếu và càng mạnh.
C. càng yếu và càng yếu. D. càng mạnh và càng mạnh.
(Xem giải) Câu 16. Hợp kim nào sau đây khi để trong không khí ẩm thì Fe không bị ăn mòn điện hoá?
A. Fe-Ni. B. Fe-Al. C. Fe-Cu. D. Fe-Ag.
(Xem giải) Câu 17. Kim loại có khối lượng riêng lớn nhất là
A. Pb. B. Os. C. Ag. D. Ba.
(Xem giải) Câu 18. Khi cho ethylene tác dụng với dung dịch nước bromine trong điều kiện thường, xảy ra phản ứng cộng electrophile theo sơ đồ sau:
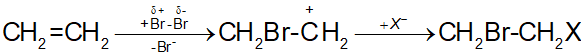
Ngoài sản phẩm chính là CH2Br-CH2Br, còn thu được một lượng nhỏ sản phẩm hữu cơ A, công thức cấu tạo của A là
A. CH3-CHBr-OH. B. CH2Br-CHBr-OH. C. CH2Br-CH2OH. D. CH2Br-CH3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Quặng sylvinite là một khoáng chất phổ biến có thành phần chính là NaCl.KCl. Một nhóm học sinh đưa ra giả thuyết: “Có thể dựa vào sự thay đổi độ tan khác nhau theo nhiệt độ để tách các chất ra khỏi nhau”.
Biết: độ tan (S) của một chất ở nhiệt độ xác định là khối lượng tối đa chất đó tan trong 100 gam nước để tạo dung dịch bão hòa. Nhóm học sinh đã tiến hành thí nghiệm để tách hai chất theo các bước sau:
• Bước 1: Hòa tan một lượng quặng synvinite được nghiền nhỏ vào 500 gam nước ở 100°C, lọc bỏ phần không tan thu được dung dịch bão hòa (X).
• Bước 2: Làm lạnh (X) đến 0°C thấy tách ra m gam chất rắn (Y).
• Bước 3: Tiếp tục cho m gam chất rắn (Y) vào 50 gam H2O ở 10°C, khuấy đều thì tách ra a gam chất rắn không tan (Z). (Giả thiết chất rắn thu được không chứa muối ngậm nước, các thao tác thí nghiệm coi như không làm hao hụt khối lượng chất, lượng nước bay hơi không đáng kể).
Bảng sự phụ thuộc của độ tan 2 muối được biểu diễn ở bảng sau:
| t°C | 10 | 20 | 30 | 50 | 70 | 90 | 100 | |
| S(NaCl) | 35,6 | 35,7 | 35,8 | 36,7 | 37,5 | 37,5 | 38,5 | 39,1 |
| S(KCl) | 28,5 | 32,0 | 34,7 | 42,8 | 48,3 | 48,3 | 53,8 | 56,6 |
a) Phương pháp tách các chất theo tiến trình trên được gọi là phương pháp chiết lỏng – rắn.
b) Độ tan của KCl giảm nhanh hơn của NaCl khi giảm nhiệt độ từ 100°C về 0°C.
c) Giả thiết của nhóm học sinh là đúng.
d) Nhóm học sinh thu được chất rắn Z chỉ chứa KCl.
(Xem giải) Câu 20. Phenol là nguyên liệu quan trọng trong công nghiệp hóa chất, như sản xuất nhựa phenol-formaldehyde, bisphenol A,… Biết ở 25°C, độ tan bão hòa của phenol trong nước là 84,2 g/L. Trong phương pháp chiết lỏng – lỏng để tách X khỏi dung dịch nước, người ta dùng một dung môi hữu cơ (không tan trong nước, dễ hòa tan X). Ở trạng thái cân bằng, hệ số phân bố được định nghĩa: K = Ch/Cn
– Ch: nồng độ mol/L của chất X trong pha hữu cơ.
– Cn: nồng độ mol/L của chất X trong pha nước.
a) Phổ khối lượng (MS) của phenol cho thấy peak ion phân tử có m/z bằng 94.
b) Dung dịch phenol và aniline đều không làm đổi màu quỳ tím nên có thể dùng dung dịch bromine để phân biệt ra 2 dung dịch này.
c) Phản ứng giữa phenol với methanal tạo nhựa phenol-formaldehyde trong môi trường acid, đun nóng là phản ứng trùng ngưng.
d) Thực hiện tách phenol trong 250 mL dung dịch phenol bão hoà ở 25°C trong nước bằng 50 mL dung môi ethylacetate với hệ số phân bố K = 90. Khối lượng phenol tối đa thu hồi được vào pha hữu cơ sau một lần chiết là 12,9 gam. (các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
(Xem giải) Câu 21. Disacharide X là thành phần chính của đường mạch nha. Trong dung dịch nước, X tồn tại chủ yếu ở hai dạng cấu tạo (1) và (2). Hai dạng này tồn tại cân bằng sau:
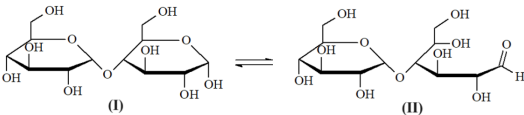
a) Liên kết giữa hai đơn vị monosaccharide trong phân tử X là liên kết β-1,4-glycoside
b) Dạng (1) có nhiều liên kết sigma hơn dạng (2).
c) Phản ứng thủy phân X trong dung dịch H2SO4 98% xảy ra nhanh hơn trong dung dịch H2SO4 50% vì nồng độ acid lớn hơn.
d) Enzyme maltase xúc tác đặc hiệu cho phản ứng thủy phân X.
(Xem giải) Câu 22. Bộ dụng cụ bên được sử dụng để điện phân nước với chất điện li là NaOH.
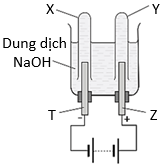
a) Điện cực T xảy ra quá trình oxi hoá anion OH-, điện cực Z xảy ra khử H2O.
b) Nếu thay NaOH bằng H2SO4 hoặc Na2SO4 thì các khí thu được ở các ống X, Y không thay đổi.
c) Mục đích thêm NaOH vào điện phân nước để tăng độ dẫn điện cho dung dịch do nước nguyên chất dẫn điện rất kém.
d) Nếu ở ống X thu được 100 mL khí thì ở ống Y sẽ thu được 50 mL khí (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất).
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Theo TCVN 5502/2003, dựa vào độ cứng của nước (được quy đổi về khối lượng CaCO3 trong 1 lít nước, coi tổng số mol Ca2+ và Mg2+ bằng số mol CaCO3) người ta phân chia nước thành các loại:
| Phân loại nước | Mềm | Hơi cứng | Cứng | Rất cứng |
| Độ cứng (mg CaCO3/lít) | 0 – dưới 50 | 50 – dưới 150 | 150 – 300 | > 300 |
Từ một mẫu nước có chứa các ion (Mg2+, Ca2+, SO42- 0,0004M, HCO3- 0,00042M, Cl- 0,0003M), người ta có thể tính được giá trị độ cứng của mẫu nước. Cho các nhận định sau:
(1) Dựa vào độ cứng của nước, người ta có thể phân chia nước thành 4 loại.
(2) Độ cứng của mẫu nước trên là 76 mg/L.
(3) Mẫu nước trên là nước cứng có tính cứng tạm thời.
(4) Khi đun sôi loại nước trên có xuất hiện kết tủa.
(5) Để loại bỏ tính cứng của mẫu nước trên, có thể dùng dung dịch Na3PO4 dư.
Hãy liệt kê theo các nhận định đúng theo số thứ tự tăng dần?
(Xem giải) Câu 24. Aniline được tổng hợp từ benzene theo sơ đồ chuyển hoá sau:
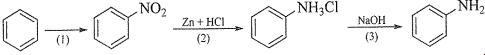
Theo sơ đồ trên, từ 1 tấn benzene sẽ điều chế được bao nhiêu kg aniline? Biết hiệu suất toàn bộ quá trình là 60%. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
(Xem giải) Câu 25. Cho sơ đồ các phản ứng sau:
(1) CH3CHO (NaBH4) → CH3CH2OH
(2) CH3CHO (thuốc thử Tollens) → CH3COONH4
(3) CH3CHO (HCN) → CH3CH(OH)CN
(4) CH3CHO (I2/NaOH) → HCOONa
Hãy lập thành bộ bốn số tương ứng theo trình tự các phản ứng: oxi hoá aldehyde, cộng hydrogencyanide, khử aldehyde, tạo iodoform?
(Xem giải) Câu 26. Tiến hành nghiên cứu phản ứng giữa glucose với methanol (xúc tác HCl khan) trong đó nguyên tử oxygen trong phân tử methanol là đồng vị 18O, các nguyên tử trong glucose là đồng vị 12C; 1H và 16O và trong methanol là đồng vị 12C; 1H. Sơ đồ phản ứng được mô tả như sau:
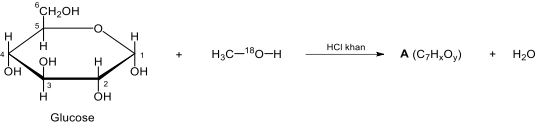
Cho các phát biểu sau:
(1) Phân tử glucose được biểu diễn ở phản ứng trên là dạng vòng α.
(2) Hợp chất A có khả năng tham gia phản ứng với thuốc thử Tollens.
(3) Khi phản ứng xảy ra, có sự phân cắt liên kết giữa nguyên tử carbon số 1 (1C) với nguyên tử oxygen trong nhóm -OH hemiacetal.
(4) Phân tử khối của A bằng 194.
(5) Glucose và hợp chất A đều tồn tại ở dạng mạch vòng và dạng mở vòng.
Hãy liệt kê các phát biểu đúng theo chiều số thứ tự tăng dần?
(Xem giải) Câu 27. Để tách Zn từ quặng sphalerite (chứa chủ yếu ZnS) người ta thực hiện theo sơ đồ sau:
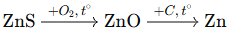
Tôn là một loại vật liệu được làm từ thép tấm mỏng, phủ thêm lớp kẽm bên ngoài thông qua quá trình nhúng nóng. Lượng kim loại Zn được tách ra từ 1 tấn quặng sphalerite (chứa 80% ZnS, tạp chất khác không chứa Zn, hiệu suất cả quá trình tách là 75%) được sử dụng hết để sản xuất tôn. Biết tổng diện tích bề mặt thép cần mạ là 2000 m², khối lượng riêng của Zn là 7,14 g/cm³ và 1 μm = 10-6 m. Độ dày trung bình của lớp mạ là x μm. Xác định giá trị của x. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
(Xem giải) Câu 28. Nguyên tố X thuộc chu kì 2 và nguyên tử ở trạng thái cơ bản có 3 electron độc thân. Nguyên tố Y thuộc chu kì 3 và ở nguyên tử trạng thái cơ bản có 1e ở lớp ngoài cùng. Tổng số hiệu nguyên tử của X và Y là bao nhiêu?


Bình luận