Bộ dụng cụ bên được sử dụng để điện phân nước với chất điện li là NaOH.
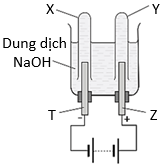
a) Điện cực T xảy ra quá trình oxi hoá anion OH-, điện cực Z xảy ra khử H2O.
b) Nếu thay NaOH bằng H2SO4 hoặc Na2SO4 thì các khí thu được ở các ống X, Y không thay đổi.
c) Mục đích thêm NaOH vào điện phân nước để tăng độ dẫn điện cho dung dịch do nước nguyên chất dẫn điện rất kém.
d) Nếu ở ống X thu được 100 mL khí thì ở ống Y sẽ thu được 50 mL khí (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất).
Câu trả lời tốt nhất
(a) Sai, điện cực T (cực âm, cathode) xảy ra quá trình khử H2O:
H2O + 2e —> H2 + 2OH-
Điện cực Z (cực dương, anode) xảy ra quá trình oxi hóa OH-:
4OH- —> O2 + 2H2O + 4e
(b) Đúng:
Nếu dùng H2SO4:
Anode: 2H2O —> O2 + 4e + 4H+
Cathode: 2H+ + 2e —> H2
Nếu dùng Na2SO4:
Anode: 2H2O —> O2 + 4e + 4H+
Cathode: 2H2O + 2e —> H2 + 2OH-
(c) Đúng, nước nguyên chất phân ly cực kỳ yếu:
H2O ⇋ H+ + OH-
Nồng độ H+, OH- quá nhỏ khiến nước nguyên chất dẫn điện rất kém. Để tăng độ dẫn điện người ta có thể thêm NaOH, một chất điện ly mạnh làm tăng độ dẫn điện của dung dịch lên gấp nhiều lần. Đặc biệt, NaOH không ảnh hưởng đến sản phẩm quá trình điện phân, không bị tiêu hao.
(d) Đúng, ống X là khí H2, ống Y là khí O2, theo tỷ lệ từ các bán phản ứng kể trên thì thể tích H2 gấp 2 lần thể tích O2.
