[2018 – 2019] Thi học sinh giỏi lớp 12 – Tỉnh Quảng Nam
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Thời gian làm bài: 90 phút
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2A | 3A | 4A | 5C | 6D | 7A | 8C | 9D | 10C |
| 11B | 12C | 13C | 14D | 15C | 16A | 17D | 18B | 19C | 20A |
| 21B | 22B | 23D | 24D | 25C | 26B | 27B | 28B | 29D | 30A |
| 31A | 32A | 33C | 34D | 35A | 36B | 37D | 38C | 39D | 40C |
| 41C | 42C | 43B | 44A | 45A | 46B | 47B | 48D | 49A | 50D |
Câu 1. Chất X được sử dụng để làm trắng bột giấy, chống nấm mốc cho lương thực, tẩy màu nước đường trong sản xuất đường mía. Chất X là
A. HClO. B. SO2. C. Cl2. D. O3.
(Xem giải) Câu 2. Có các dung dịch riêng biệt: Cu(NO3)2, AlCl3, FeCl3, AgNO3, Mg(NO3)2, NiSO4. Nhúng vào mỗi dung dịch một thanh sắt nguyên chất. Số trường hợp xảy ra ăn mòn điện hóa là
A. 3. B. 5. C. 4. D. 2.
Câu 3. Công thức cấu tạo nào sau đây là của triolein?
A. (CH3(CH2)7CH=CH(CH2)7COO)3C3H5. B. (CH3(CH2)16COO)3C3H5.
C. (CH3(CH2)14COO)3C3H5. D. (CH3(CH2)7CH=CH(CH2)5COO)3C3H5.
(Xem giải) Câu 4. Cho dung dịch Na2CO3 đến dư vào dung dịch chứa đồng thời AlCl3 và CaCl2 thu được kết tủa X. Trong X có
A. Al(OH)3, CaCO3. B. Al2(CO3)3, CaCO3. C. CaCO3. D. Al2(CO3)3.
Câu 5. Cho Fe3O4 vào dung dịch H2SO4 loãng, dư, sau phản ứng thu được dung dịch X. Dung dịch X không phản ứng được với dung dịch nào sau đây?
A. KMnO4. B. BaCl2. C. HCl. D. NaOH.
(Xem giải) Câu 6. Hai nguyên tố X và Y ở hai nhóm A liên tiếp nhau trong cùng một chu kỳ trong bảng hệ thống tuần hoàn. Trong các biểu thức liên hệ giữa số đơn vị điện tích hạt nhân của X (ZX) và Y (ZY) dưới đây, biểu thức liên hệ nào luôn không đúng?
A. ZY – ZX = 11. B. ZX – ZY = 1. C. ZX – ZY = 25. D. ZY – ZX = 8.
(Xem giải) Câu 7. Hiđro halogenua nào sau đây không được điều chế bằng cách cho muối halogenua tương ứng của nó phản ứng với dung dịch H2SO4 đặc?
A. HBr, HI. B. HBr, HCl. C. HF, HI. D. HCl, HF.
Câu 8. Độ dẫn điện của kim loại Cu kém hơn kim loại nào sau đây?
A. Fe. B. Au. C. Ag. D. Al.
Câu 9. Metyl acrylat không tác dụng với chất nào sau đây trong dung dịch?
A. Br2. B. H2SO4. C. NaOH. D. AgNO3/NH3.
Câu 10. Ion nào sau đây oxi hóa được ion Fe2+ thành Fe3+?
A. Cu2+. B. Pb2+. C. Ag+. D. Zn2+.
Câu 11. Chất X có công thức phân tử C5H8O2. Khi X tác dụng với dung dịch NaOH sinh ra chất Y có công thức phân tử C4H5O2Na. Chất X có thể là
A. Etyl propionat. B. Metyl metacrylat. C. Etyl acrylat. D. Vinyl propionat.
Câu 12. Nguyên tử Fe có Z = 26. Cấu hình electron của Fe2+ là
A. [Ar] 4s2 3d4. B. [Ar] 3d5 4s1. C. [Ar] 3d6. D. [Ar] 3d4 4s2.
(Xem giải) Câu 13. Cho các phát biểu sau:
(a) Cộng H2 (dùng dư, xúc tác Ni, t°C, phản ứng hoàn toàn) vào anđehit thì thu được ancol no, mạch hở, đơn chức.
(b) HCOOH có lực axit mạch hơn CH3COOH.
(c) Phản ứng giữa anđehit và O2 (xúc tác Mn2+, t°C) sinh ra axit cacboxylic.
(d) Trong số các anđehit no, mạch hở, chỉ có anđehit fomic phản ứng với dung dịch AgNO3/NH3 dư sinh ra Ag theo tỉ lệ mol giữa anđehit và Ag là 1 : 4.
(e) Giấm ăn là dung dịch axit axetic có nồng độ từ 15% đến 20%.
(g) Axit terephtalic (C6H4(COOH)2) được dùng trong tổng hợp tơ lapsan.
Số phát biểu đúng là
A. 2. B. 4. C. 3. D. 5.
Câu 14. Cho các phản ứng hóa học: 2FeCl2 + Cl2 → 2FeCl3; 2FeCl3 + 2KI → 2FeCl2 + 2KCl + I2. Dãy nào sau đây sắp xếp các tác nhân theo chiều tăng dần tính oxi hóa?
A. I2, Cl2, Fe2+, Fe3+. B. Fe2+, Fe3+, I2, Cl2. C. I2, Fe2+, Cl2, Fe3+. D. Fe2+, I2, Fe3+, Cl2.
(Xem giải) Câu 15. Tiến hành đồng trùng ngưng ε-amino hexanoic và ω-amino heptanoic thu được một loại tơ poliamit X có n mắt xích -NH-(CH2)5-CO- và m mắt xích -NH-(CH2)6-CO-. Lấy 24,35 gam tơ X đem đốt cháy hoàn toàn với O2 vừa đủ thu được hỗn hợp Y. Sục Y qua dung dịch NaOH dư thì còn lại 2,24 lít (đktc) một khí duy nhất. Tỉ số n : m là
A. 3:4. B. 5:3. C. 3:5. D. 2:1.
(Xem giải) Câu 16. Cho các phát biểu sau:
(a) Trong quá trình thép cacbon bị ăn mòn trong không khí ẩm, ở cực dương xảy ra quá trình khử oxi.
(b) Người ta tráng Zn lên sắt (thu được sắt tây) để làm chậm quá trình ăn mòn sắt.
(c) Quá trình ăn mòn kim loại là quá trình oxi hóa khử.
(d) Các kim loại tinh khiết thì không bị ăn mòn hóa học.
(e) Sắt cháy trong khí clo là quá trình ăn mòn hóa học.
Số phát biểu đúng là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 17. Cho dãy chuyển hóa sau: C2H2 → X (C, 600°C); X + Br2 → Y (Fe, t°C); Y + NaOH đặc dư → Z (t°C, áp suất). Z không thể là
A. Nước. B. Natri bromua. C. Natri phenolat. D. Phenol.
Câu 18. Cho các chất sau: (1) metyl fomat, (2) axit axetic, (3) propan-1-ol, (4) butan. Dãy nào sau đây sắp xếp theo chiều giảm dần nhiệt độ sôi?
A. (2)(1)(3)(4). B. (2)(3)(1)(4). C. (1)(2)(3)(4). D. (4)(3)(1)(2).
(Xem giải) Câu 19. Khối lượng riêng của kim loại X là 8,94 g/cm3. Giả thiết rằng trong tinh thể kim loại X, các nguyên tử là những hình cầu chiếm 76% thể tích tinh thể, phần còn lại là khe rỗng. Xác định bán kính nguyên tử X theo cm (Biết nguyên tử khối của X là 63,55)
A. 1,14.10^-8. B. 1,48.10^-8. C. 1,29.10^-8. D. 1,84.10^-8.
Câu 20. Cho các loại tơ sau: tơ tằm, sợi bông, len, tơ visco, tơ nilon-6, tơ axetat, tơ nitron. Số tơ thuộc loại tơ bán tổng hợp là
A. 2. B. 3. C. 4. D. 5.
(Xem giải) Câu 21. Có hai cốc thủy tinh đều chứa 100 ml dung dịch CH3COOH 0,01M. Thêm vào cốc thứ nhất 20 ml nước cất được dung dịch (1), thêm vào cốc thứ hai 20 ml dung dịch HCl 0,01M được dung dịch (2). So sánh với cốc CH3COOH 0,01M ban đầu, số mol phân tử CH3COOH chưa điện li trong dung dịch (1) và (2) lần lượt
A. bằng và lớn hơn. B. nhỏ hơn và lớn hơn. C. đều không đổi. D. lớn hơn và nhỏ hơn.
(Xem giải) Câu 22. Cho dãy chuyển hóa sau: Ca3(PO4)2 + SiO2 + than hoạt tính → Y; Y + O2 → Z (chất khí ở điều kiện thường). Chất Z phản ứng với dung dịch NaOH có thể tạo thành tối đa bao nhiêu muối?
A. 3. B. 2. C. 4. D. 1.
Câu 23. Phát biểu nào sau đây không đúng?
A. Ancol etylic nguyên chất bốc cháy khi tiếp xúc với CrO3.
B. Cr(OH)3 vừa tan được trong dung dịch KOH, vừa tan được trong dung dịch HCl.
C. Màu của dung dịch K2Cr2O7 thay đổi khi thêm vào dung dịch gồm FeSO4 và H2SO4.
D. Kim loại Zn khử được ion Cr3+ trong dung dịch về Cr.
(Xem giải) Câu 24. Cho các phát biểu sau:
(a) Hiđro hóa hoàn toàn glucozơ tạo ra axit gluconic.
(b) Ở điều kiện thường, glucozơ và saccarozơ đều là những chất rắn, dễ tan trong nước.
(c) Xenlulozơ trinitrat là nguyên liệu để sản xuất tơ nhân tạo và thuốc súng không khói.
(d) Amilopectin là pilime mạch không phân nhánh.
(e) Saccarozơ bị hóa đen khi tiếp xúc với dung dịch H2SO4 đặc.
(g) Tinh bột và xenlulozơ là đồng phân vì có cùng công thức (C6H10O5)n.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 2.
(Xem giải) Câu 25. Cho các dung dịch (dung môi là nước) có cùng nồng độ mol/lít: (1) NaHCO3, (2) Na2CO3, (3) CuSO4, (4) KNO3. Dãy nào sau đây sắp xếp các dung dịch trên theo chiều tăng dần độ pH (từ trái sang phải)?
A. (2)(1)(4)(3). B. (2)(4)(3)(1). C. (3)(4)(1)(2). D. (1)(3)(4)(2).
Câu 26. Tiến hành thí nghiệm với các dung dịch X, Y, Z, T. Kết quả được ghi lại ở bảng sau:
| Chất | Thuốc thử | Hiện tượng |
| X, T | Quỳ tím | Chuyển màu đỏ |
| X, Z, T | Cu(OH)2 | Tạo dung dịch xanh lam |
| Y, Z, T | Dung dịch AgNO3/NH3, t° | Tạo kết tủa bạc |
Các chất X, Y, Z, T lần lượt là
A. Axit fomic, etyl fomat, glucozơ, axit glutamic. B. Axit glutamic, etyl fomat, glucozơ, axit fomic.
C. Axit glutamic, glucozơ, etyl fomat, axit fomic. D. Axit fomic, axit glutamic, etyl fomat, glucozơ.
(Xem giải) Câu 27. Cho sơ đồ phản ứng sau (theo đúng tỉ lệ mol):
(1) X + 2NaOH → X1 + 2X2. (2) X1 + H2SO4 → X3 + Na2SO4.
(3) nX3 + nX4 → Poli(etilen terephtalat) + 2nH2O. (4) 2X2 → X5 + H2 + 2H2O
(5) nX5 + nX6 → Cao su Buna-S
Cho biết X là este có công thức phân tử C12H14O4. X1, X2, X3, X4, X5, X6 là các hợp chất hữu cơ khác nhau. Nhận định nào sau đây không đúng?
A. X4 tác dụng được với Cu(OH)2 trong môi trường kiềm.
B. X5 có nguyên tố C chiếm 85,71% khối lượng.
C. Từ 1,4-đimetyl benzen điều chế được X3 bằng 1 phản ứng hóa học.
D. Poli(etilen terephtalat) là polime tổng hợp.
(Xem giải) Câu 28. Hỗn hợp X gồm hai khí CO2 và SO2. Sục V lít X vào dung dịch H2S dư thì tạo thành 1,92 gam chất rắn màu vàng. Cho V lít X qua Mg dư, nung nóng thì thấy khối lượng chất rắn tăng thêm 2,16 gam (biết các phản ứng xảy ra hoàn toàn). Tỉ khối hơi của X so với H2 là
A. 29,5. B. 27. C. 28,35. D. 54.
(Xem giải) Câu 29. Hòa tan hoàn toàn m gam hỗn hợp X gồm Ba, Na và K vào nước dư, thu được 4,48 lít H2 (đktc) và dung dịch Y. Cô cạn Y thu được 16,2 gam chất rắn. Giá trị của m là
A. 16,2. B. 13,0. C. 12,8. D. 9,4.
(Xem giải) Câu 30. Đun nóng V lít hơi anđehit X với 3V lít khí H2 (xúc tác Ni) đến khi phản ứng xảy ra hoàn toàn chỉ thu được một hỗn hợp khí Y có thể tích 2V lít (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất). Ngưng tụ Y thu được chất Z; cho Z tác dụng với Na sinh ra H2 có số mol bằng số mol Z đã phản ứng. Chất X là anđehit
A. no, hai chức. B. no, đơn chức.
C. không no (chứa một nối đôi C=C), đơn chức.
D. không no (chứa một nối đôi C=C), hai chức.
(Xem giải) Câu 31. Hòa tan hết m gam Zn(OH)2 bằng một lượng vừa đủ dung dịch HCl 10% thu được dung dịch X. Thêm 125 ml dung dịch CuSO4 1,2M (D = 1,17 g/ml) vào 200 gam dung dịch X thu được dung dịch Y. Tổng giá trị nồng độ phần trăm của các chất tan trong dung dịch Y là
A. 16,41%. B. 8,21%. C. 24,62%. D. 32,82%.
(Xem giải) Câu 32. Cho m gam hỗn hợp Fe, Zn phản ứng với dung dịch CuSO4. Sau khi kết thúc phản ứng, thu được m gam chất rắn (chỉ chứa 1 kim loại) và dung dịch X chứa FeSO4 xM, ZnSO4 yM. Tỉ số x : y gần nhất với giá trị nào sau đây?
A. 0,15. B. 2,33. C. 1,50. D. 0,85.
(Xem giải) Câu 33. Thêm từ từ đến hết 250 ml dung dịch AgNO3 0,3M vào 100 ml dung dịch hỗn hợp CuBr2 0,1M và FeCl2 0,15M, sau khi phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
A. 4,305. B. 1,62. C. 9,685. D. 8,065.
(Xem giải) Câu 34. Hỗn hợp X gồm O2 và O3 có tỉ khối hơi so với H2 là x. Hỗn hợp Y gồm H2 và CO có tỉ khối hơi so với H2 là y. Để phản ứng với V lít hỗn hợp khí Y cần vừa đủ 0,45V lít hỗn hợp khí X (các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ số T = x : y nằm trong khoảng nào sau đây?
A. 1,43 < T < 17,78. B. 1,43 < T < 20,00. C. 1,27 < T < 20,00. D. 1,27 < T < 17,78.
(Xem giải) Câu 35. Có hai bình cầu, cho vào mỗi bình 20 ml etyl axetat, sau đó thêm vào bình thứ nhất 40 ml dung dịch H2SO4 20% (dư) và bình thứ hai 40 ml dung dịch NaOH 30% (dư), lắc đều, lắp ống sinh hàn hồi lưu (để không cho các chất lỏng hóa hơi thoát ra khỏi bình), đun cách thủy đến khi hệ thống đạt cân bằng. Hiện tượng nào sau đây đúng?
A. Chất lỏng trong bình thứ hai trở thành đồng nhất.
B. Chất lỏng trong cả hai bình có sự phân tách lớp.
C. Chất lỏng trong cả hai bình trở thành đồng nhất.
D. Chất lỏng trong bình thứ nhất trở thành đồng nhất.
(Xem giải) Câu 36. Hiđrocacbon X mạch hở, có công thức C3Hx. Cho m1 gam X và m2 gam O2 (dư) vào một bình kín (dung tích không đổi) ở 120°C thấy áp suất trong bình đạt 1,5 atm. Bật tia lửa điện để phản ứng cháy xảy ra hoàn toàn, đưa hệ về 120°C, thấy áp suất đạt 1,5 atm. Trộn 18,2 gam X với b gam H2 rồi dẫn qua xúc tác Ni, đun nóng đến xảy ra hoàn toàn thì thu được hỗn hợp Y. Tỉ khối hơi của Y so với H2 có thể là
A. 24,25. B. 21,25. C. 26,30. D. 22,30.
(Xem giải) Câu 37. Số đồng phân cấu tạo của C5H10O có phản ứng tráng bạc là
A. 6. B. 5. C. 3. D. 4.
(Xem giải) Câu 38. Cho 3,87 gam hỗn hợp gồm Mg và Al vào 200 ml dung dịch X gồm HCl 1,0M và H2SO4 0,5M thu được dung dịch B và 4,368 lít H2 (đktc). Phần trăm khối lượng của Mg trong hỗn hợp là
A. 72,09%. B. 62,79%. C. 37,21%. D. 27,91%.
(Xem giải) Câu 39. Đốt cháy hoàn toàn m gam một triglixerit E cần vừa đủ x mol O2, sau phản ứng thu được CO2 và y mol H2O. Biết m = 78x – 103y. Nếu cho 0,15 mol E tác dụng với dung dịch nước Br2 dư thì lượng Br2 phản ứng tối đa là
A. 0,15. B. 0,35. C. 0,90. D. 0,45.
(Xem giải) Câu 40. Hỗn hợp X gồm hai ancol đơn chức kế tiếp nhau trong dãy đồng đẳng. Cho m gam X tác dụng với CuO (dư) nung nóng, thu được hỗn hợp chất rắn và hỗn hợp hơi Y. Tỉ khối hơi của Y so với H2 là 14,10. Cho toàn bộ Y phản ứng với lượng dư AgNO3/NH3 đun nóng, sinh ra 181,44 gam Ag. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 23,04. B. 19,74. C. 24,24. D. 33,84.
(Xem giải) Câu 41. Hình vẽ dưới đây mô tả các giai đoạn của quá trình tổng hợp amoniac trong công nghiệp.
Giai đoạn 1: Nén hỗn hợp N2 và H2 theo tỉ lệ tương ứng 3 : 1
Giai đoạn 2: Đốt H2 trong N2 dư.
Giai đoạn 3: Hấp thụ khí NH3 bằng nước
Giai đoạn 4: Phát thải qua ống khói cao.
Trong các giai đoạn trên, có mấy giai đoạn sai:
A. 1. B. 2. C. 4. D. 3
Câu 42. Paclitaxel (tên thương mại là Taxol) là một loại thuốc hóa trị liệu được sử dụng để điều trị một số dạng ung thư, có công thức cấu tạo như sau:
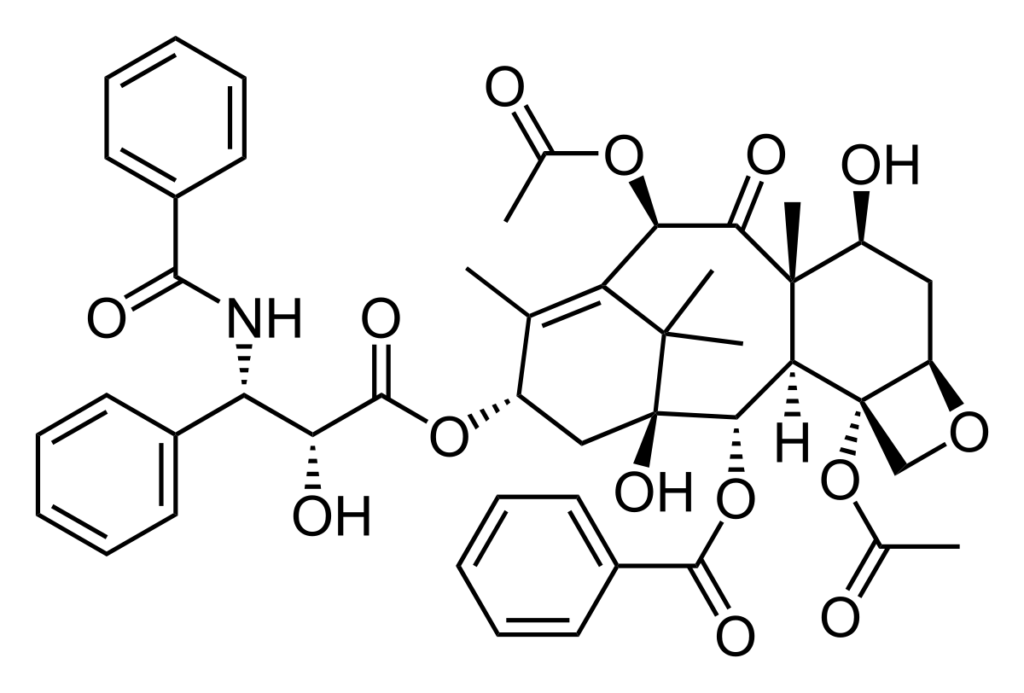
Công thức phân tử của Paclitaxel là
A. C45H49O14N. B. C44H55O14N. C. C47H51O14N. D. C46H53O14N.
(Xem giải) Câu 43. Hỗn hợp X gồm chất Y (C2H10O3N2) và chất Z (C2H7O2N). Cho 14,85 gam X phản ứng vừa đủ với dung dịch NaOH và đun nóng, thu được dung dịch M và 5,6 lít (đktc) hỗn hợp T gồm hai khí đều làm xanh quỳ ẩm. Cô cạn toàn bộ dung dịch M thu được m gam muối khan. Giá trị của m gần nhất với giá trị nào sau đây?
A. 16,2. B. 14,3. C. 15,8. D. 13,1.
(Xem giải) Câu 44. Hỗn hợp X gồm hai este đơn chức E1 và E2. Cho 0,05 mol X tác dụng vừa đủ với dung dịch NaOH thu được hỗn hợp sản phẩm hữu cơ Y. Đốt cháy hoàn toàn Y thu được 2,688 lít CO2 (đktc) và 3,18 gam Na2CO3. Khi làm bay hơi Y thu được chất rắn Z. Phần trăm khối lượng của muối có phân tử khối lớn hơn trong Z là
A. 25,438%. B. 35,620%. C. 56,841%. D. 74,562%.
(Xem giải) Câu 45. Hỗn hợp E gồm ba este mạch hở, đều có bốn liên kết pi (π) trong phân tử, trong đó có một este đơn chức là este của axit metacrylic và hai este hai chức là đồng phân của nhau. Đốt cháy hoàn toàn 12,22 gam E bằng O2, thu được 0,37 mol H2O. Mặt khác, cho 0,36 mol E phản ứng vừa đủ với 234 ml dung dịch NaOH 2,5M, thu đươc hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức có khối lượng m1 gam và một ancol no, đơn chức có khối lượng m2 gam. Tỉ lệ m1 : m2 có giá trị gần nhất với giá trị nào sau đây?
A. 2,9. B. 4,7. C. 1,1. D. 2,7.
(Xem giải) Câu 46. Cho X; Y; Z là 3 peptit mạch hở (phân tử có số nguyên tử cacbon tương ứng là 8; 9; 11; Z có nhiều hơn Y một liên kết peptit); T là este no, đơn chức, mạch hở. Chia 249,56 gam hỗn hợp E gồm X; Y; Z; T thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một, thu được a mol CO2 và (a – 0,11) mol H2O. Thủy phân hoàn toàn phần hai bằng dung dịch NaOH vừa đủ, thu được ancol etylic và 133,18 gam hỗn hợp G (gồm bốn muối của Gly; Ala; Val và axit cacboxylic). Đốt cháy hoàn toàn G, cần vừa đủ 3,385 mol O2. Phần trăm khối lượng của Y trong E là:
A. 1,61%. B. 4,17%. C. 2,08%. D. 3,21%.
(Xem giải) Câu 47. Điện phân dung dịch muối sunfat của một kim loại hóa trị II với điện cực trơ, cường độ dòng điện không đổi. Sau thời gian 4 phút 30 giây, thu được 0,02 mol khí ở anot. Nếu thời gian điện phân là 9 phút thì tổng số mol khí thu được ở cả hai điện cực là 0,05 mol, thể tích dung dịch lúc này là 0,5 lít. Giả sử hiệu suất điện phân là 100%, khí sinh ra không tan trong nước. Phát biểu nào sau đây không đúng?
A. Khối lượng muối sunfat trong dung dịch ban đầu lớn hơn 6,72 gam.
B. Tại thời điểm 9 phút, dung dịch có pH = 1.
C. Khi thu được 0,03 mol khí ở anot thì vẫn chưa xuất hiện khí ở catot.
D. Tại thời điểm 8 phút, ở catot đã có khí thoát ra.
(Xem giải) Câu 48. Hỗn hợp X gồm glyxin; axit glutamic và axit metacrylic. Hỗn hợp Y gồm etilen và đimetylamin. Đốt cháy a mol X và b mol Y thì tổng số mol khí oxi cần dùng vừa đủ là 2,625 mol, thu được H2O; 0,2 mol N2 và 2,05 mol CO2. Mặt khác, khi cho a mol X tác dụng với dung dịch NaOH dư thì lượng NaOH phản ứng là m gam. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 12. B. 16. C. 24. D. 20.
(Xem giải) Câu 49. Đồ thị dưới đây biểu diễn khối lượng kết tủa tạo thành theo thể tích dung dịch Ba(OH)2 0,75M khi thêm từ từ dung dịch này vào dung dịch hỗn hợp Al2(SO4)3 và AlCl3:
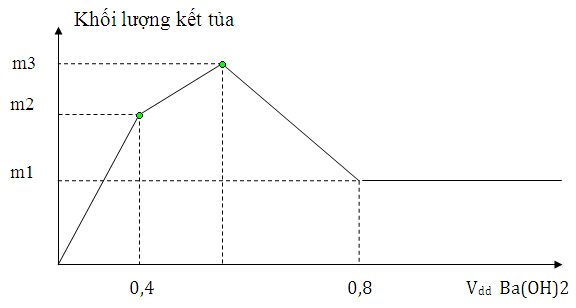
Giá trị của x = m1 + m2 + m3 là
A. 248,7. B. 178,8. C. 69,9. D. 155,4.
(Xem giải) Câu 50. Hỗn hợp R gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M hóa trị II. Cho 3,64 gam hỗn hợp R tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng thu được 0,448 lít khí (đktc) và dung dịch chỉ có một muối duy nhất, nồng độ 10,867% (khối lượng riêng là 1,093 g/ml, nồng độ mol là 0,545M. Trong hỗn hợp R, muối cacbonat trung hòa chiếm x% về khối lượng. Giá trị của x gần nhất với giá trị nào sau đây?
A. 45. B. 32. C. 22. D. 46.


Bình luận