[2022-2023][Hóa 10] Kiểm tra giữa kỳ 2 trường Nguyễn Tất Thành – Hà Nội
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Giải chi tiết và đáp án:
⇒ Mã đề: 041
| 1A | 2D | 3C | 4B | 5C | 6C | 7A | 8D | 9C | 10B |
| 11D | 12B |
I. TRẮC NGHIỆM (3 điểm)
(Xem giải) Câu 1: Phản ứng nào sau đây là phản ứng tỏa nhiệt?
A. 2S(s) + O2 (g) → 2SO2(g) ![]() = -296,8 kJ.
= -296,8 kJ.
B. CaCO3(s) → CaO(s) + CO2(g) ![]() = 178,29 kJ.
= 178,29 kJ.
C. H2(g) + I2(s) → 2HI(g) ![]() = 52,96 kJ.
= 52,96 kJ.
D. N2(g) + O2(g) → 2NO(g) ![]() = 180 kJ.
= 180 kJ.
(Xem giải) Câu 2: Phản ứng nào sau đây là phản ứng thu nhiệt?
A. C3H8(g) + 5O2(g) → 3CO2(g) + H2O(l) ![]() = – 2220 kJ.
= – 2220 kJ.
B. NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l) ![]() = – 57,9 kJ.
= – 57,9 kJ.
C. CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ![]() = – 890,36 kJ.
= – 890,36 kJ.
D. ZnSO4(s) → ZnO(s) + SO2(g) ![]() = 235,21 kJ.
= 235,21 kJ.
(Xem giải) Câu 3: Phản ứng nào sau đây cần phải cung cấp năng lượng dưới dạng nhiệt trong quá trình phản ứng?
A. Phản ứng tạo gỉ kim loại. B. Phản ứng quang hợp.
C. Phản ứng nhiệt phân. D. Phản ứng tạo oxit Na2O.
(Xem giải) Câu 4: Phản ứng nào sau đây không cần cung cấp năng lượng trong quá trình phản ứng?
A. Oxi hóa C bằng O2. B. Oxi hóa Hg bằng S.
C. Oxi hòa Fe bằng S. D. Oxi hóa S bằng O2.
(Xem giải) Câu 5: Phản ứng nào sau đây là phản ứng toả nhiệt?
A. Phản ứng nhiệt phân muối KNO3.
B. Phản ứng phân huỷ khí NH3.
C. Phản ứng oxi hoá glucose trong cơ thể.
D. Phản ứng hoà tan NH4Cl trong nước.
(Xem giải) Câu 6: Cho phản ứng: KMnO4 + HCl (đặc) → KCl + MnCl2 + Cl2 + H2O. Hệ số cân bằng phản ứng là các số tối giản. Số phân tử HCl đóng vai trò chất khử là:
A. 16. B. 9. C. 10. D. 11.
(Xem giải) Câu 7: Cho phương trình hoá học: aFe + bH2SO4 → cFe2(SO4)3 + dSO2 + eH2O. Tỉ lệ a : b là
A. 1 : 3. B. 1 : 2. C. 2 : 3. D. 2 : 9.
(Xem giải) Câu 8: Trong phản ứng: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O. Số phân tử nitric acid (HNO3) đóng vai trò chất oxi hóa là
A. 8. B. 6. C. 4. D. 2.
(Xem giải) Câu 9: Để m gam bột sắt ngoài không khí sau một thời gian thu được 6 gam hỗn hợp chất rắn X. Hoà tan hoàn toàn X bằng dung dịch HNO3, thu được 1,12 lít khí NO duy nhất (đktc). Giá trị của m là
A. 10,08. B. 1,08. C. 5,04. D. 0,504.
(Xem giải) Câu 10: Phương trình phản ứng nào sau đây không thể hiện tính khử ammonia (NH3)?
A. 4NH3 + 5O2 → 4NO + 6H2O. B. NH3 + HCl → NH4Cl.
C. 2NH3 + 3Cl2 → 6HCl + N2. D. 4NH3 + 3O2 → 2N2 + 6H2O.
(Xem giải) Câu 11: Xác định biến thiên enthalpy ( ) của phản ứng đốt cháy butane:
) của phản ứng đốt cháy butane:
C4H10(g) + O2(g) → CO2(g) + H2O(g)
Biết năng lượng liên kết trong các hợp chất cho trong bảng sau:
| Liên kết | Phân tử | Eb (kJ/mol) | Liên kết | Phân tử | Eb (kJ/mol) |
| C – C | C4H10 | 346 | C = O | CO2 | 799 |
| C – H | C4H10 | 418 | O – H | H2O | 467 |
| O = O | O2 | 495 |
A. +2356,5 kJ. B. -2356,5 kJ. C. +2626,5 kJ. D. -2626,5 kJ.
(Xem giải) Câu 12: Phát biểu nào sau đây sai?
A. Sự oxi hóa là sự nhường electron làm tăng số oxi hóa.
B. Trong quá trình oxi hóa, chất khử là chất nhận electron.
C. Sự khử là sự nhận electron làm giảm số oxi hóa.
D. Trong phản ứng oxi hóa – khử, sự oxi hóa và sự khử luôn xảy đồng thời.
II. TỰ LUẬN (7 điểm)
(Xem giải) Câu 13. (2,5 điểm): Cân bằng các phương trình hoá học sau theo phương pháp thăng bằng electron, xác định rõ chất khử, chất oxi hoá, quá trình khử, quá trình oxi hoá
1) Fe + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O
2) C + HNO3 đặc → CO2 + NO2 + H2O
3) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
4) KOH + Cl2 → KClO3 + KCl + H2O
5) Zn + HNO3 → Zn(NO3)2 + NO + N2O + H2O biết tỉ lệ thể tích 2 khí NO : N2O = 3:2
(Xem giải) Câu 14. (2 điểm): Hòa tan hoàn toàn 12 gam muối FeSO4.7H2O không nguyên chất trong nước thành 200 ml dung dịch. Lấy 20 ml dung dịch đó thêm dung dịch H2SO4 loãng rồi tiến hành chuẩn độ bằng dung dịch KMnO4 0,03M. Thể tích dung dịch KMnO4 đã dùng là 25 ml. Phản ứng hóa học xảy ra: FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
a. Xác định chất khử, chất oxi hóa và cân bằng phản ứng hóa học trên
b. Tính độ tinh khiết của muối FeSO4
(Xem giải) Câu 15. (1,5 điểm): Trong ngành công nghiệp lọc hóa dầu, các ankane thường được loại bỏ hydrogen trong các phản ứng dehydro hóa để tao ra những sản phẩm hydrocarbon không no có nhiều ứng dụng trong công nghiệp. Hãy tính biến thiên anthalpy chuẩn của phản ứng sau dựa vào năng lượng liên kết.
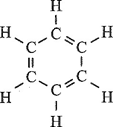
6CH4 → C6H6 (1,3,5-cyclohexatriene) + 9H2
Cho biết công thức cấu tạo 1,3,5-cyclohexatriene như sau:
Biết năng lượng liên kết:
C-H: 413 kJ/mol
C-C: 347 kJ/mol
C=C: 614 kJ/mol
H-H: 432 kJ/mol
(Xem giải) Câu 16. (1 điểm): Một hộ gia đình mua than đá làm nhiên liệu đun nấu và trung bình mỗi ngày dùng hết 1,8 kg than. Giả thiết loại than đá trên chứa 90% carbon và 1,2% sulfur về khối lượng, còn lại là các tạp chất trơ.
Cho các phản ứng:
C(s) + O2(g) → CO2(g)  = -393,5 kJ/mol
= -393,5 kJ/mol
S(s) + O2(g) → SO2(g)  = -296,8 kJ/mol
= -296,8 kJ/mol
Nhiệt lượng cung cấp cho hộ gia đình từ quá trình đốt than trong một ngày tương đương bao nhiêu số điện (1 số điện = 1 kWh = 3600 kJ)?

Bình luận