[2024 – 2025] Thi học sinh giỏi lớp 12 tỉnh Bắc Ninh (Đề minh họa)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề 026-H12A năm 2024-2025
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1C | 2D | 3C | 4D | 5C | 6C | 7C | 8C | 9C | 10A |
| 11D | 12B | 13B | 14A | 15B | 16C | 17D | 18C | 19D | 20D |
| 21A | 22C | 23D | 24B | 25B | 26A | 27B | 28D | 29A | 30B |
| 31 | 32 | 33 | 34 | 35 | 36 | 37 | 38 | |
| (a) | S | Đ | Đ | S | S | Đ | S | Đ |
| (b) | S | Đ | Đ | Đ | Đ | Đ | S | Đ |
| (c) | Đ | S | S | Đ | Đ | S | Đ | S |
| (d) | S | Đ | Đ | S | S | Đ | Đ | Đ |
| 39 | 40 | 41 | 42 | 43 | 44 |
| 32 | 219 | 9,6 | 13 | 245 | 0,8 |
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 30. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho mô hình tinh thể NaCl như hình dưới:
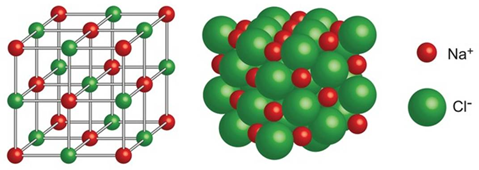
Số ion chloride (Cl-) bao quanh gần nhất với một ion sodium (Na+) là
A. 3. B. 5. C. 6. D. 4.
(Xem giải) Câu 2. Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
A. NH3. B. H2O. C. HF. D. CH4.
(Xem giải) Câu 3. Cho các phản ứng sau:
(a) Ca(OH)2 + Cl2 → CaOCl2 + H2O
(b) 2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
(c) O3 + 2Ag → Ag2O + O2
(d) 2H2S + SO2 → 3S + 2H2O
(e) 4KClO3 (°) → KCl + 3KClO4
Số phản ứng thuộc loại phản ứng oxi hóa – khử là
A. 2. B. 3. C. 5. D. 4.
(Xem giải) Câu 4. Theo dữ liệu về năng lượng liên kết (năng lượng giải phóng hoặc hấp thụ để hình thành hoặc phá vỡ 1 mol liên kết hóa học) được liệt kê trong bảng dưới đây:
| Liên kết hóa học | H-H | N≡N | Cl-Cl | Br-Br |
| Năng lượng liên kết ở đkc (kJ/mol) | 436 | 946 | 247 | 193 |
Phân tử bền nhất trong số các phân tử trên là
A. HCl. B. H2. C. Br2. D. N2.
(Xem giải) Câu 5. Ô nhiễm không khí có thể tạo ra mưa acid, gây tác hại rất lớn với môi trường. Hai khí nào sau đây đều là nguyên nhân gây ra mưa acid?
A. H2S và N2. B. CO2 và O2. C. SO2 và NO2. D. NH3 và HCl.
(Xem giải) Câu 6. Tổ chức Y tế thế giới (WHO) đưa ra một đơn vị uống chuẩn (ly tiêu chuẩn) sẽ chứa 10 gam cồn (ethanol). Ở người có cơ chế chuyển hóa bình thường, sau một giờ, gan sẽ dung nạp và chuyển hóa hết một đơn vị cồn trong 1 ly tiêu chuẩn. Anh A đi làm về trong thời tiết nóng bức có ghé qua 1 quán bia gần nhà và ngồi uống hết 6 lon bia có nồng độ cồn là 5°. Tính thời gian để anh A có thể chuyển hóa hết lượng cồn nằm trong bia mà anh A đã uống vào cơ thể. Biết rằng: 1 lon bia có thể tích 330mL và khối lượng riêng của ethanol là 0,8g/mL
A. 7h. B. 6h. C. 8h. D. 12h.
(Xem giải) Câu 7. Biết những chất lỏng có điểm chớp cháy thấp hơn 37,8°C là chất lỏng dễ cháy. Cho bảng số liệu về điểm chớp cháy của một số chất lỏng sau:
| Chất | Pentane | Ethanol | Formic acid | Ethylene glycol |
| Điểm chớp cháy (°C) | -49 | 13 | 50 | 111 |
Nhận định nào sau đây không đúng?
A. Trong số các chất trên, pentane có khả năng gây cháy, nổ cao nhất.
B. Trong số các chất trên, ethylene glycol có khả năng gây cháy nổ thấp nhất.
C. Pentane có điểm chớp cháy cao hơn ethanol.
D. Trong số các chất trên, có hai chất lỏng dễ cháy.
(Xem giải) Câu 8. Amphetamine (còn được gọi là hồng phiến) là một dạng chất ma túy có tác dụng gây kích thích thần kinh, tăng cường sức chịu đựng, tăng cảm giác hưng phấn, nếu sử dụng quá liều sẽ gây nghiện, ảnh hưởng xấu tới đến hệ thần kinh,… Amphetamine có cấu tạo như hình bên:
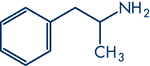
Phát biểu nào sau đây sai?
A. Amphetamine là amine bậc một.
B. Công thức phân tử của amphetamine là C9H13N.
C. Amphetamine thuộc loại arylamine.
D. Amphetamine tác dụng với hydrochloric acid theo tỉ lệ mol 1 : 1.
(Xem giải) Câu 9. Acetone được điều chế bằng cách oxi hóa cumene nhờ oxygen, sau đó thuỷ phân trong dung dịch H2SO4 loãng. Để thu được 87 gam acetone thì huợng cumene cần dùng (giả sử hiệu suất quá trình điều chế đạt 80%) là
A. 144 gam. B. 180 gam. C. 225 gam. D. 216 gam.
(Xem giải) Câu 10. Phổ khối lượng (MST) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của hợp chất hữu cơ X là 60. Chất X có thể là
A. methyl formate. B. ethyl formate. C. ethyl acetate. D. methyl acetate.
(Xem giải) Câu 11. Cho các phát biểu sau:
(a) Phân tử xà phòng, chất giặt rửa tổng hợp có cấu tạo gồm một phần ưa nước nối với một phần kị nước.
(b) Chất giặt rửa tổng hợp được sử dụng phổ biến hơn xà phòng do nó thân thiện với môi trường.
(c) Saponin trong bồ hòn và quả bồ kết là chất giặt rửa tự nhiên.
(d) Từ dầu mỏ có thể sản xuất được chất giặt rửa tổng hợp.
Số phát biểu đúng là
A. 1. B. 2. C. 4. D. 3.
(Xem giải) Câu 12. Chất béo là nguồn cung cấp năng lượng đáng kể cho cơ thể người. Trung bình 1 gam chất béo cung cấp năng lượng là 38 kJ và năng lượng từ chất béo đóng góp 20% tổng năng lượng cần thiết trong ngày. Một ngày, một học sinh trung học phổ thông cần năng lượng 9120 kJ thì cần ăn bao nhiêu gam chất béo cho phù hợp?
A. 50 gam. B. 48 gam. C. 80 gam. D. 72 gam.
(Xem giải) Câu 13. Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong cây mía, củ cải đường và hoa thốt nốt. Khi thuỷ phân chất X thu được chất Y và Z. Trong mẫu người trưởng thành, khoẻ mạnh vào lúc đói có một lượng nhỏ chất Y với nồng độ khoảng 4,4 – 7,2 mmol/L. Tên gọi của X và Y lần lượt là
A. glucose và fructose. B. saccharose và glucose.
C. glucose và saccharose. D. saccharose và sorbitol.
(Xem giải) Câu 14. Saccharose có trong nhiều loài thực vật, có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt. Công thức cấu tạo của saccharose được cho ở hình dưới đây
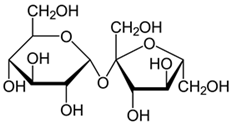
Cho các phát biểu sau:
(a) Saccharose cấu tạo từ một đơn vị α-glucose và một đơn vị β-fructose.
(b) Trong phân tử saccharose có chứa liên kết α-1,4-glycoside.
(c) Phân tử saccharose thuộc loại disaccharide.
(d) Phân tử saccharose thể hiện tính chất của polyalcohol.
Số phát biểu đúng là
A. 3. B. 2. C. 1. D. 4.
(Xem giải) Câu 15. Leucine có công thức cấu tạo (CH3)2CHCH2CH(NH2)COOH là α-amino acid có khả năng điều hoà sự tổng hợp protein của cơ. Tên theo danh pháp thay thế của leucine là
A. 2-aminoisohexanoic acid. B. 2-amino-4-methylpentanoic acid.
C. 4-amino-2-methylpentanoic acid. D. 2-amino-isohexanoic acid.
(Xem giải) Câu 16. Hình dưới đây biểu thị công thức của một peptide:
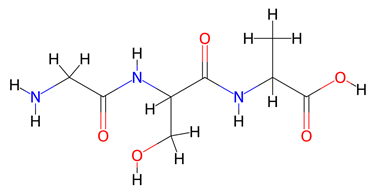
Phát biểu nào sau đây đúng?
A. X là tetrapeptide.
B. Peptide X có amino acid đầu N là Ala.
C. X tham gia phản ứng màu biuret.
D. Khối lượng phân tử của peptide X là 236.
(Xem giải) Câu 17. Việc lạm dụng nhựa trong cuộc sống dẫn đến một lượng nhựa khổng lồ được thải ra môi trường. Rác thải nhựa ảnh hưởng nghiêm trọng đến tất cả các sinh vật trong hệ sinh thái, nếu không được xử lí đúng cách sẽ ảnh hưởng trực tiếp đến môi trường. Cách xử lý rác thải nhựa nào sau đây là phù hợp nhất để giảm thiểu ảnh hưởng đến môi trường?
A. Đốt rác thải nhựa sau khi sử dụng.
B. Chôn lấp rác thải nhựa dưới đất.
C. Xả thải rác thải nhựa ra sông hồ, đại dương…
D. Tái chế và tái sử dụng đồ nhựa đã dùng.
(Xem giải) Câu 18. Polyisoprene là thành phần chính của cao su thiên nhiên, được sử dụng rộng rãi trong sản xuất các sản phẩm như lốp xe, găng tay và ống dẫn. Để cải thiện tính chất của polyisoprene, người ta cho polyisoprene phản ứng với khí HCl nhằm tạo ra một loại polymer mới có tính đàn hồi tốt hơn và khả năng kháng hóa chất cao. Sau phản ứng, sản phẩm thu được có chứa 14,76% chlorine về khối lượng. Trung bình một phân tử HCl phản ứng với k mắt xích trong mạch polymer. Giá trị của k là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 19. Pin Galvani được coi là nguồn điện hoá học đầu tiên mà con người phát minh ra, được biểu diễn ở hình bên.

Phát biểu nào sau đây đúng?
A. Cực âm (anode) là kim loại Cu được nhúng vào dung dịch muối CuSO4.
B. Cực dương (cathode) là kim loại Zn được nhúng vào dung dịch muối ZnSO4.
C. Có dòng electron chuyển dời từ điện cực Cu sang điện cực Zn.
D. Hai dung dịch được nối với nhau bằng một cầu muối.
(Xem giải) Câu 20. Phát biểu nào sau đây về hợp kim duralumin không đúng?
A. Duralumin là hợp kim của nhôm (aluminium).
B. Hợp kim duralumin có đặc điểm nhẹ, cứng, bền cơ học.
C. Hợp kim duralumin được sử dụng rộng rãi trong ngành không.
D. Hợp kim duralumin bền trong môi trường acid và môi trường kiềm.
(Xem giải) Câu 21. Một nhà máy gang thép sản xuất thép thành phẩm từ 400 tấn quặng hematite đỏ (chứa 84% Fe2O3 về khối lượng, còn lại là tạp chất không chứa sắt) với hiệu suất cả quá trình đạt 91% theo sơ đồ:
Quặng hematit đỏ (luyện gang) → Gang trắng (luyện thép) → Thép (gia công) → Thép thành phẩm
Biết thép thành phẩm chứa 98% sắt về khối lượng và có khối lượng riêng là 7,9 tấn/m³. Toàn bộ lượng thép thành phẩm được cán thành x cây thép hình trụ “phi 18 “(đường kính 18 mm) dài 11,7m. Cho π = 3,14, giá trị của x là
A. 9290. B. 9104. C. 18580. D. 18208.
(Xem giải) Câu 22. Giản đồ hình bên mô tả sự biến đổi độ tan trong nước của một số chất theo nhiệt độ:
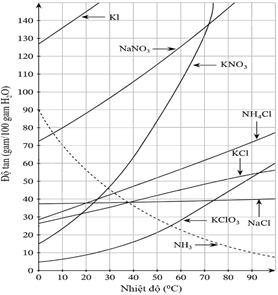
Cho các phát biểu sau:
(a) Ở nhiệt độ phòng, KNO3 là chất tan ít nhất, KI là chất tan nhiều nhất.
(b) Khi nhiệt độ tăng, độ tan của các muối sẽ tăng.
(c) Độ tan của NaCl ít phụ thuộc vào nhiệt độ nhất.
(d) Để tách riêng NaCl và KCl ra khỏi quặng sylvinite NaCl.KCl, người ta dựa vào độ tan khác nhau của chúng.
Số phát biểu đúng là
A. 1. B. 2. C. 3 D. 4.
(Xem giải) Câu 23. Dựa vào bảng thông tin sau:
| Chất | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 100,7 | 179,2 | 234,6 | 271,5 |
Hãy cho biết quá trình phân huỷ 1 mol muối carbonate của nguyên tố nhóm IIA nào sau đây cần hấp thu nhiều năng lượng nhất?
A. MgCO3. B. CaCO3. C. SrCO3. D. BaCO3.
(Xem giải) Câu 24. Tiến hành chuẩn độ 50 mL dung dịch CH3COOH chưa biết nồng độ cần dùng V mL dung dịch NaOH 0,05M. Giá trị của V được ghi lại sau mỗi lần chuẩn độ như sau:
| Lần chuẩn độ | Lần 1 | Lần 2 | Lần 3 |
| V (mL) | 75,1 | 74,9 | 75,0 |
Cho các phát biểu sau về quá trình chuẩn độ trên:
(a) Quá trình chuẩn độ acid-base trên không cần dùng thêm chất chi thị.
(b) Tại điểm tương đương, pH của dung dịch có giá trị bằng 7.
(c) Nồng độ của dung dịch cần chuẩn độ có kết quả là 0,075M.
(d) Thay dung dịch NaOH 0,05M bằng dung dịch KOH 0,05M thì không ảnh hưởng đến cách tiến hành và kết quả thí nghiệm.
Số phát biểu đúng là
A. 3. B. 2. C. 4. D. 1.
(Xem giải) Câu 25. Tiến hành các thí nghiệm sau:
(a) Cho kim loại Mg (dư) vào dung dịch Fe2(SO4)3.
(b) Dẫn khí H2 dư qua bột CuO nung nóng.
(c) Cho kim loại K vào dung dịch CuSO4 dư.
(d) Cho Al vào dung dịch Fe2(SO4)3 dư.
(e) Điện phân dung dịch AgNO3 với điện cực trơ.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
A. 2. B. 3. C. 4. D. 5.
(Xem giải) Câu 26. Chất nào sau đây không phản ứng với NaOH trong dung dịch?
A. Methylamine. B. Alanine. C. Ala-Val. D. Methylacetate.
(Xem giải) Câu 27. Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: CH3NH2, NH3, C6H5OH (phenol), C6H5NH2 (aniline) và các tính chất được ghi trong bảng sau:
| Chất | X | Y | Z | T |
| Nhiệt độ sôi (°C) | 182 | 184 | -6,7 | -33,4 |
| pH (0,001M) | 6,48 | 7,82 | 10,81 | 10,12 |
Nhận xét nào sau đây đúng?
A. Y là C6H5OH. B. Z là CH3NH2. C. T là C6H5NH2. D. X là NH3.
(Xem giải) Câu 28. Để đảm bảo năng suất cây trồng, mỗi hecta đất trồng cần cung cấp 103,25 kg N, 52,5 kg P2O5 và 58,03 kg K2O. Muốn có được lượng chất dinh dưỡng ở trên cho 1 hecta đất trồng, người nông dân cần trộn phân bón NPK (20-15-10) với phân đạm (chứa 95% NH4NO3) và phân kali (potassium, chứa 73,01% KCl) để thu được m kg phân bón hỗn hợp mới. Giá trị của m là
A. 350,0. B. 450,0. C. 575,0. D. 500,0.
(Xem giải) Câu 29. Hình sau đây mô tả dụng cụ dùng để tách hỗn hợp các chất.
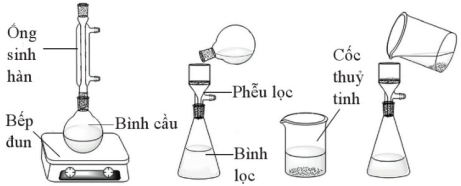
Phương pháp nào đã được sử dụng trong trường hợp này?
A. Kết tinh. B. Chưng cất. C. Bay hơi. D. Chiết.
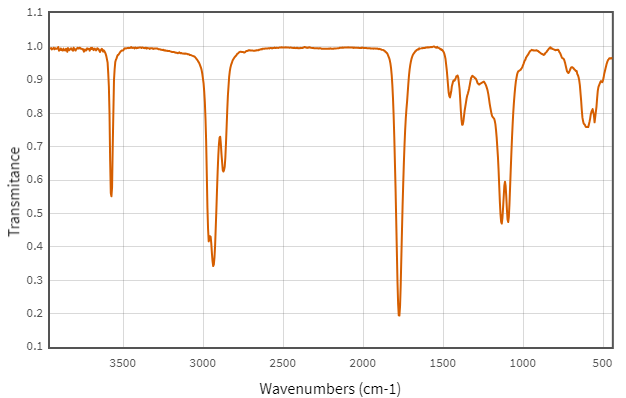
(Xem giải) Câu 30. Kết quả phân tích nguyên tố cho thấy thành phần phần trăm về khối lượng của các nguyên tố carbon, hydrogen, oxygen trong hợp chất hữu cơ X lần lượt là 64,62%; 10,77%; 24,61%. Phổ MS của X cho thấy chất này có phân tử khối là 130. X có mạch không phân nhánh và phổ hồng ngoại của X như sau:
 |
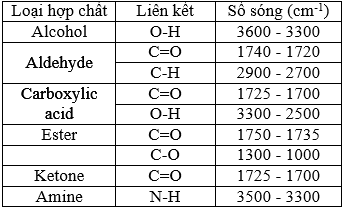 |
Cho các phát biểu sau:
(a) X có 6 nguyên tử carbon.
(b) X tác dụng được với NaHCO3.
(c) X thuộc loại hợp chất ester.
(d) Tỉ lệ số nguyên tử C và H trong X là 1 : 2
Số phát biểu đúng là:
A. 1. B. 2. C. 3. D. 4.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 31 đến câu 38. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 31. Ở một lò nung vôi công nghiệp sẽ xảy ra 2 phản ứng hóa học chính như sau:
(1) C(s) + O2(g) (t°) → CO2(g) ![]() = -393,5 kJ
= -393,5 kJ
(2) CaCO3(s) (t°) → CaO(s) + CO2(g) ![]() = 178,29 kJ
= 178,29 kJ
a) Đốt cháy hết 1 mol C tỏa ra 393,5 kJ nhiệt; phân hủy hết 1 mol đá vôi tỏa ra 178,29 kJ nhiệt.
b) Phản ứng (1) diễn ra khó khăn hơn phản ứng (2); nhiệt tỏa ra ở phản ứng (2) đã cung cấp cho quá trình đốt cháy than đá ở phản ứng (1).
c) Muốn cho phản ứng (1) và (2) xảy ra nhanh hơn thì than đá và đá vôi đều phải được tán thành những viên nhỏ nhưng không được tán quá nhỏ.
d) Để sản xuất được 500 kg vôi sống cần tối thiểu 101,136 kg than đá.
(Xem giải) Câu 32. Một số loại thực vật chỉ phát triển tốt ở môi trường có pH phù hợp, việc nghiên cứu pH của đất rất quan trọng trong nông nghiệp. Một số loại cây trồng phù hợp với đất có giá trị pH cho trong bảng sau:
| Cây trồng | pH thích hợp | Cây trồng | pH thích hợp |
| Bắp | 5,7 – 7,5 | Cây chè | 4,5 – 5,5 |
| Cà chua | 6,0 – 7,0 | Thanh long | 4,0 – 6,0 |
| Cải thảo | 6,5 – 7,0 | Lúa | 5,5 – 6,5 |
| Hành tây | 6,4 – 7,9 | Mía | 5,0 – 8,0 |
Một học sinh làm thí nghiệm xác định độ pH của đất như sau: Lấy một lượng đất cho vào nước rồi lọc lấy phần dung dịch. Dùng máy pH đo được giá trị pH là 4,52. Cho các phát biểu sau:
a) Vùng đất trên phù hợp trồng cây chè và thanh long.
b) Loại đất trên bị nhiễm chua, để trồng hành tây, cà chua, mía phát triển tốt ta cần khử chua cho đất bằng cách rắc vôi bột (chứa chủ yếu CaO) hoặc bón tro thực vật (tro đốt rơm rạ).
c) Để cây cải thảo và hành tây phát triển tốt, ta cần bón nhiều đạm hai lá (NH4NO3) qua nhiều vụ liên tiếp để đất có giá trị pH phù hợp.
d) Để cải tạo đất cằn cỗi thì một biện pháp hữu hiệu là sử dụng phân bón hữu cơ như phân chuồng, phân trùn quế.
(Xem giải) Câu 33. Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho khoảng 2 gam chất béo và khoảng 4 mL dung dịch NaOH 40% vào bát sứ. Đun hỗn hợp trong khoảng 10 phút và liên tục khuấy bằng đũa thủy tinh. Nếu thể tích nước giảm cần bổ sung thêm nước.
Bước 2: Kết thúc phản ứng đổ hỗn hợp vào cốc thuỷ tinh chứa khoảng 30 mL dung dịch NaCl bão hoà, khuấy nhẹ. Để nguội hỗn hợp. Quan sát hiện tượng của phản ứng xảy ra.
a) Sau bước 2 thấy có lớp chất rắn màu trắng chứa muối sodium của acid béo nổi lên.
b) Vai trò của dung dịch NaCl bão hòa ở bước 2 là để tách muối sodium của acid béo ra khỏi hỗn hợp.
c) Ở bước 1, nếu thay mỡ lợn bằng dầu nhớt thì hiện tượng thí nghiệm sau bước 2 vẫn xảy ra tương tự.
d) Trong công nghiệp, phản ứng ở thí nghiệm trên được ứng dụng để sản xuất xà phòng và glycerol.
(Xem giải) Câu 34. Khi thuỷ phân hoàn toàn 500 mg một loại protein, chỉ thu được các amino acid với khối lượng như sau:
| Công thức cấu tạo | Kí hiệu | Khối lượng (mg) |
| CH3CH(NH2)COOH | Ala | 178 |
| HOOC-CH2CH2CH(NH2)COOH | Glu | 44 |
| HS-CH2CH(NH2)COOH | Cys | 48 |
| HO-CH2CH(NH2)COOH | Ser | 105 |
| HOOC-CH2CH(NH2)COOH | Asp | 131 |
| (CH3)2CH-CH(NH2)-COOH | Val | 47 |
| H2N-[CH2]4-CH(NH2)-COOH | Lys | 44 |
a) Có thể dựa vào tính chất điện di để tách riêng từng amino acid trong bảng kết quả trên.
b) Trong các amino acid ở trên, Lysine (Lys) là một trong những amino acid đóng vai trò quan trọng cho quá trình xây dựng và tạo ra các mạch máu mới trong cơ thể. Ở pH = 6, Lysine tồn tại dạng cation.
c) Tỉ lệ số mol Ala : Ser trong hỗn hợp trên là 2 : 1.
d) Nếu phân tử khối của protein này là 50000 amu thì số mắt xích trong 1 phân tử protein ở trên là 200 Ala, 30 Glu, 40 Cys, 100 Ser, 100 Asp, 40 Val và 20 Lys.
(Xem giải) Câu 35. Trong công nghiệp, sản xuất aluminium từ quặng bauxite theo sơ đồ sau:
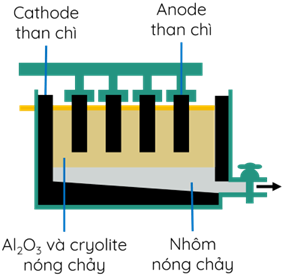
a) Aluminium thu được tại điện cực dương.
b) Quá trình điện phân, cực dương bằng than chì bị ăn mòn.
c) Cryolite có vai trò chính là hạ nhiệt độ nóng chảy của aluminium oxide.
d) Để thu được 2 tấn Al tinh khiết thì cần 5,95 tấn quặng bauxite chứa 40% Al2O3 về khối lượng (biết hiệu suất cả quá trình là 80%)
(Xem giải) Câu 36. Gói làm nóng thức ăn (FRH: Flameless Ration Heater) được phát minh nhằm hâm nóng các bữa ăn tiện lợi cho người lính trên chiến trường. Một số gói lẩu tự sôi cũng sử dụng công nghệ này. FRH có thành phần chính gồm bột kim loại Mg trộn với một lượng nhỏ bột Fe và NaCl. Khi sử dụng, chỉ cần cho khoảng 30 mL nước vào hỗn hợp FRH, hỗn hợp này phân ứng mãnh liệt theo phương trình Mg(s) + 2H2O(l) → Mg(OH)2(s) + H2(g) và tỏa rất nhiều nhiệt, đủ để làm nóng thức ăn nhanh chóng.
a) Magnesium phản ứng chậm với nước ở nhiệt độ thường, nhưng magnesium trong gói FRH lại có thể phản ứng nhanh chóng với nước.
b) Người ta chỉ dùng khoảng 30 mL nước mà không dùng lượng nước nhiều hơn.
c) Một gói FRH chứa khoảng 8 gam hỗn hợp (Mg (90%), Fe (4%), NaCl (6%) về khối lượng) có thể tỏa ra tối đa 642,6 kJ. Biết rằng enthalpy tạo thành chuẩn ![]() của Mg(OH)2 (s) và H2O(l) lần lượt là -928,4 kJ/mol và -285,8 kJ/mol.
của Mg(OH)2 (s) và H2O(l) lần lượt là -928,4 kJ/mol và -285,8 kJ/mol.
d) Gói FRH trên có đủ làm nóng 175 gam súp từ 30°C lên 100°C. Biết để nâng 1 gam súp lên 1°C cần tiêu tốn 4,2J, giả sử gói súp chỉ nhận được 50% lượng nhiệt tối đa tỏa ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
(Xem giải) Câu 37. Salbutamol là hoạt chất sử dụng để sản xuất thuốc điều trị bệnh cho người (làm giãn phế quản, giãn cơn co tử cung, …). Tuy nhiên salbutamol chỉ được sử dụng khi có chỉ định của bác sĩ. Trong chăn nuôi, salbutamol thúc cho gia súc, gia cầm lớn nhanh hơn, tỉ lệ nạc cao hơn, màu sắc thịt đỏ hơn. Nếu con người ăn phải thịt gia súc, gia cầm được nuôi có sử dụng salbutamol một thời gian dài thì sẽ làm cho tim đập nhanh, tăng huyết áp, run cơ, rối loạn tiêu hóa. Thậm chí, theo một số chuyên gia, đây là một trong những hoạt chất có khả năng gây ung thư nếu bị tích lũy nhiều trong cơ thể. Salbutamol có công thức cấu tạo thu gọn nhất như sau:
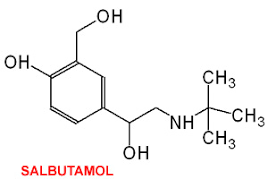
a) Salbutamol là hợp chất hữu cơ tạp chức, chứa đồng thời: 2 nhóm chức phenol, 1 nhóm chức alcohol và 1 nhóm chức amine bậc hai.
b) Cho a mol salbutamol có thể phản ứng tối đa với 3a mol NaOH.
c) Salbutamol có khả năng phản ứng với dung dịch Br2.
d) Cho 0,1 mol salbutamol phản ứng với 0,3 mol NaOH thu được dung dịch X. Cho dung dịch X phản với lượng vừa đủ dung dịch HCl thu được dung dịch Y. Khối lượng muối thu được trong dung dịch Y là 45,1 gam.
(Xem giải) Câu 38. Ammonium nitrate được dùng làm phân đạm. Năm 2020, một vụ nổ tại thủ đô Beirut, Lebanon đã cướp đi sinh mạng của hàng trăm người. Nguyên nhân của vụ nổ được do sự phân hủy 2750 tấn ammonium nitrate trên một tàu hàng bỏ hoang theo phương trình hoá học sau:
NH4NO3(s) → N2O(g) + 2H2O(g) ![]() = -36 kJ
= -36 kJ
a) Khi bón phân đạm ammonium nitrate nhiều sẽ gây hiện tượng chua đất.
b) Ammonium nitrate còn được dùng để sản xuất phân bón CAN (calcium ammonium nitrate) bằng cách cho dung dịch ammonium nitrate (chứa nitric acid dư) tác dụng với bột đá dolomite (CaCO3.MgCO3).
c) Phản ứng (1) là phản ứng thu nhiệt.
d) Nhiệt của vụ nổ trên tương đương với nhiệt toả ra 1062 tấn thuốc nổ TNT. (biết 1 kg thuốc nổ TNT phát nổ toả ra 1,165.10^6 J).
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 39 đến câu 44.
(Xem giải) Câu 39. Cho các chất có công thức sau: C2H6, CH3COOH, HCOOCH3, C2H5OH và các dữ liệu nhiệt độ sôi là 78,3°C, -88,6°C, 117,8°C, 32°C (không theo thứ tự). Nhiệt độ sôi của methyl formate là bao nhiêu?
(Xem giải) Câu 40. X là một peptide mạch hở, có công thức phân tử là C13H24N4O6. Thực hiện các phản ứng sau theo đúng tỉ lệ mol:
(1) X + 4NaOH → X1 + NH2CH2COONa + X2 + 2H2O
(2) X1 + 3HCl → C5H10NO4Cl + 2NaCl
(3) X2 + 3HCl → X4 + NaCl
Xác định phân tử khối của X4.
(Xem giải) Câu 41. Để tráng bạc một chiếc huy chương có bề dầy là 3 mm, bán kính 4 cm, người ta tiến hành điện phân dung dịch AgNO3 với cathode là tấm huy chương và anode bằng Ag. Biết cường độ dòng điện không đổi là 2,0A, hiệu suất điện phân là 90%, khối lượng riêng của tinh thể Ag là 10,8 g/cm³, hằng số Faraday F = 96485 C/mol). Cho biết thời gian điện phân để lớp mạ có độ dày đồng nhất 0,01 mm là bao nhiêu phút? (chỉ làm tròn ở phép tính cuối cùng, làm tròn kết quả đến hàng phần muời)
(Xem giải) Câu 42. Aspartame là một chất ngọt nhân tạo, có cấu trúc như sau:
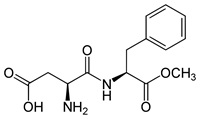
Cho các phát biểu sau:
(1) Thủy phân aspartame trong dung dịch NaOH đun nóng thu được methanol.
(2) Phân tử aminoacid đầu N có chứa vòng benzene trong phân tử.
(3) 1 mol aspartame tác dụng tối đa với 3 mol NaOH .
(4) Công thức phân tử của aspartame là C14H20O5N2.
Các phát biểu đúng gồm những phát biểu nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 123; 234; …).
(Xem giải) Câu 43. Một mẫu nước sinh hoạt được thử nghiệm định tính để xác định sự có mặt của một số ion. Mẫu nước được cho vào 4 ống nghiệm, sau đó tiến hành thí nghiệm nhỏ mỗi loại thuốc thử vào mỗi ống nghiệm và ghi nhận được hiện tượng như sau:
| Thí nghiệm | Thuốc thử | Hiện tượng |
| 1 | HCl | Sủi bọt khí không màu, không mùi |
| 2 | NaOH | Xuất hiện kết tủa trắng |
| 3 | BaCl2 | Xuất hiện kết tủa trắng |
| 4 | Na2CO3 | Xuất hiện kết tủa trắng |
Mẫu nước trên có thể chứa những ion nào trong số các ion sau đây: (1) NH4+; (2) Ca2+; (3) Ba2+; (4) SO42-; (5) HCO3-; (6) CO32-. (Liệt kê các ion theo thứ tự từ nhỏ đến lớn).
(Xem giải) Câu 44. Để xác định hàm lượng hydrogen sulfide (H2S) trong mẫu nước thải công nghiệp, ta tiến hành như sau: Hòa tan 6,50 gam KIO3 trong nước thành 1 lít dung dịch X. Lấy 10 mL dung dịch X, thêm 0,5 gam KI và 5 giọt hồ tinh bột vào, tiếp theo rót 10 mL mẫu nước thải công nghiệp, sau đó acid hóa dung dịch thu được bằng 10 mL dung dịch HCl 3,5M. Sau 5 phút, cho hỗn hợp phản ứng với dung dịch Na2S2O3 0,1M, đến khi màu xanh tím biến mất thì hết 13,5 mL dung dịch Na2S2O3. Biết các phản ứng diễn ra trong quy trình như sau:
IO3- + I- + H+ → I2 + H2O
H2S + I2 → S + HI
S2O32- + I2 → S4O62- + I-
Tính hàm lượng hydrogen sulfide trong mẫu nước theo g/L (chỉ làm tròn ở phép tính cuối cùng, làm tròn kết quả đến hàng phần mười)


Bình luận