[2024 – 2025] Thi học sinh giỏi lớp 12 – TP Hải Phòng
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Danh sách đề hsg năm 2024-2025
⇒ Tổng hợp đề hsg theo năm học
⇒ Mã đề 041-H12A năm 2024-2025
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1A | 2A | 3A | 4D | 5C | 6A | 7A | 8D | 9D | 10B |
| 11D | 12A | 13D | 14A | 15B | 16A | 17D | 18B | 19C | 20B |
| Câu 21 | Câu 22 | Câu 23 | Câu 24 | Câu 25 | |
| (a) | Đ | S | Đ | Đ | Đ |
| (b) | Đ | S | Đ | Đ | S |
| (c) | Đ | Đ | S | Đ | S |
| (d) | S | Đ | Đ | Đ | Đ |
| 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 |
| 3,5 | 2 | 80 | 428 | 38,4 | 1,5 | 29,4 | 290 | 82,2 | 30,1 |
PHẦN 1: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 20. Mỗi câu hỏi thí sinh chỉ lựa chọn một phương án.
(Xem giải) Câu 1: Khi nghiên cứu về tính chất của các halogen, một học sinh đề xuất 4 phương án thu khí chlorine trong phòng thí nghiệm như hình vẽ sau:
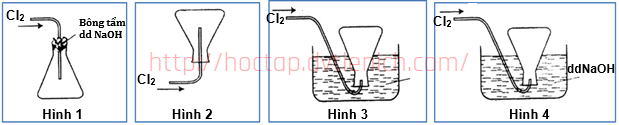
Hình vẽ nào mô tả đúng cách thu khí chlorine trong phòng thí nghiệm?
A. Hình 1 vì khí chlorine nặng hơn không khí.
B. Hình 2 vì khí chlorine nhẹ nên dễ bay lên.
C. Hình 3 vì khí chlorine chỉ tan một phần trong nước nhưng phản ứng với nước.
D. Hình 4 vì khí chlorine không tác dụng với dung dịch kiềm.
(Xem giải) Câu 2: Benzene là nguyên liệu quan trọng để sản xuất nhiều hợp chất hữu cơ đồng thời có thể là một dung môi quan trọng. Tuy nhiên, cũng như các hydrocarbon thơm khác, benzene cần được chú ý khi sử dụng, nên trên nhãn của chai chứa benzene thường có một số biểu tượng như hình bên.

Theo biểu tượng (1) và (2) ở trên, cần chú ý benzene là chất
A. dễ cháy, gây nguy hiểm cho sức khỏe.
B. khó cháy, có lợi cho sức khỏe.
C. được dùng làm nhiên liệu, gây hại môi trường.
D. dễ cháy, có lợi cho sức khỏe.
(Xem giải) Câu 3: Methadone là một loại thuốc dùng trong cai nghiện ma túy, dùng để cắt dần và kiểm soát cơn nghiện. Công thức cấu tạo thu gọn của methadone như hình dưới:
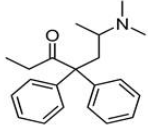
Công thức phân tử của methadone là
A. C21H27NO. B. C17H27NO. C. C17H22NO. D. C21H29N.
(Xem giải) Câu 4: Kết tinh là phương pháp quan trọng để tách biệt và tinh chế những chất hữu cơ ở dạng rắn thường được thực hiện qua các bước như mô tả ở hình dưới đây:
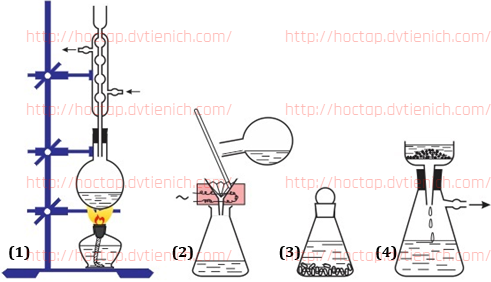
(1) Hòa tan hỗn hợp chất rắn ở nhiệt độ sôi của dung môi để tạo dung dịch bão hòa;
(2) Lọc nóng để loại bỏ phần chất rắn không tan;
(3) Để nguội phần dung dịch sau khi lọc;
(4) Lọc lấy chất rắn kết tinh.
Phương pháp kết tinh dùng để tách các chất rắn
A. có khối lượng riêng khác nhau. B. có nhiệt độ sôi khác nhau.
C. có nguyên tử khối khác nhau. D. có độ tan khác nhau.
(Xem giải) Câu 5: Xét phản ứng: O2(g) + 2H2(g) → 2H2O(g) (*). Theo dõi sự thay đổi nồng độ của các chất trong hệ phản ứng (*) theo thời gian được biểu đồ như hình vẽ dưới:

Phân tích biểu đồ trên, đường cong biểu thị sự thay đổi nồng độ theo thời gian của khí hydrogen là
A. đường số (1). B. đường số (2).
C. đường số (3). D. đường số (2) hoặc (3).
(Xem giải) Câu 6: Tùy theo đặc tính từng loại thực phẩm, mục đích, nhu cầu sử dụng, hiện có nhiều phương pháp bảo quản như: làm lạnh, hút chân không, dùng khí trơ,… Để vừa hạn chế sự oxi hóa, vừa giữ được độ giòn, độ khô và hình dạng sản phẩm trong quá trình vận chuyển ở ngay nhiệt độ thường, người ta có thể làm căng phồng bao bì bằng cách bơm loại khí nào sau đây vào gói bim bim?
A. N2. B. N2O. C. NO2. D. NH3.
(Xem giải) Câu 7: Ở điều kiện thường, calcium chloride (CaCl2) là chất rắn, khó nóng chảy, khó bay hơi. Liên kết trong phân tử CaCl2 là
A. liên kết ion. B. liên kết kim loại.
C. liên kết cộng hóa trị. D. liên kết hydrogen.
(Xem giải) Câu 8: Có 5 dung dịch: NH3, HCl, NH4Cl, Na2CO3 và CH3COOH cùng nồng độ được kí hiệu ngẫu nhiên là X, Y, Z, T, G. Giá trị pH và khả năng dẫn điện của các dung dịch trên được cho trong bảng sau:
| Dung dịch | X | Y | Z | T | G |
| pH | 5,25 | 11,53 | 3,01 | 1,25 | 11,00 |
| Khả năng dẫn điện | Tốt | Tốt | Kém | Tốt | Kém |
Biết: Khả năng dẫn điện của dung dịch tỉ lệ thuận với nồng độ ion trong dung dịch. Các dung dịch X, Y, Z, T, G lần lượt là
A. CH3COOH, NH3, NH4Cl, HCl, Na2CO3. B. NH4Cl, NH3, CH3COOH, HCl, Na2CO3.
C. Na2CO3, HCl, NH3, NH4Cl, CH3COOH. D. NH4Cl, Na2CO3, CH3COOH, HCl, NH3.
(Xem giải) Câu 9: Một trong các phương pháp dùng để loại bỏ sắt (iron) trong nguồn nước nhiễm sắt là sử dụng lượng vôi tôi (Ca(OH)2) vừa đủ để tăng pH của nước nhằm kết tủa ion sắt khi có mặt oxygen theo sơ đồ phản ứng:
(1) Fe3+ +3OH- → Fe(OH)3
(2) 4Fe2+ + 8OH- + O2 + 2H2O → 4Fe(OH)3
Theo QCVN 01-1:2018/BYT, hàm lượng sắt cho phép trong nước là 0,30 mg/L. Một mẫu nước có hàm lượng sắt cao gấp 28 lần so với ngưỡng cho phép trên. Biết sắt trong mẫu nước trên chỉ tồn tại ở hai dạng là Fe3+ và Fe2+ với tỉ lệ mol Fe3+ : Fe2+ = 1 : 4. Cần tối thiểu m gam Ca(OH)2 để kết tủa hoàn toàn lượng sắt trong 10 m³ mẫu nước trên. Giá trị của m là
A. 155,4. B. 222,0. C. 288,6. D. 122,1.
(Xem giải) Câu 10: Để tráng x chiếc gương soi (mỗi chiếc gương có diện tích bề mặt 0,35 m² và độ dày 0,1 µm), người ta sử dụng lượng bạc (sliver) thu được khi đun nóng dung dịch chứa 30,6 gam glucose với một lượng dư dung dịch silver nitrate trong ammonia. Biết khối lượng riêng của bạc là 10,49 g/cm³, hiệu suất phản ứng tráng gương là 80% (tính theo glucose). Giá trị của x là
A. 70. B. 80. C. 90. D. 100.
(Xem giải) Câu 11: Để nghiên cứu cấu tạo phân tử cellulose, tiến hành thí nghiệm với 5 bước như sau:
Bước 1: Cho lượng nhỏ bông vào cốc thủy tinh (cốc A), cho tiếp 5 mL dung dịch H2SO4 70%. Dùng đũa thủy tinh khuấy đều, sau đó đặt cốc thủy tinh vào chậu nước nóng và khuấy đều cho tới khi tạo thành dung dịch đồng nhất.
Bước 2: Để nguội, lấy khoảng 1 mL dung dịch trong cốc A cho vào ống nghiệm (ống nghiệm X). Thêm từ từ NaHCO3 vào ống nghiệm X cho đến khi dừng sủi bọt khí.
Bước 3: Cho vào ống nghiệm sạch (ống nghiệm Y) khoảng 3 mL dung dịch AgNO3. Cho tiếp dung dịch NH3 và lắc đều cho đến hòa tan hết kết tủa.
Bước 4: Cho dung dịch trong ống nghiệm X vào ống nghiệm Y, lắc đều.
Bước 5: Đặt ống nghiệm Y vào cốc nước nóng khoảng 60°C. Sau khoảng 5 phút, lấy ống nghiệm Y ra khỏi cốc.
Nhận định nào sau đây đúng?
A. Sau bước 1, trong cốc A thu được hai loại monosaccharide.
B. Sau bước 2, nhỏ dung dịch I2 vào ống nghiệm X được dung dịch có màu xanh tím.
C. Thí nghiệm trên dùng để chứng minh cellulose có chứa nhiều nhóm -OH.
D. Sau bước 5, trên thành ống nghiệm Y xuất hiện lớp kim loại màu trắng bạc.
(Xem giải) Câu 12: Salbutamol là chất cực kì nguy hiểm cho sức khỏe, nhiều hộ chăn nuôi nhỏ lẻ cố tình trộn các chất tăng trọng có chứa salbutamol vào thức ăn cho lợn trước thời kì bán thúc. Tồn dư salbutamol trong thịt gây độc hại cho người sử dụng. Salbutamol có công thức cấu tạo như hình bên.
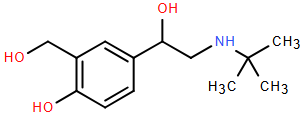
Cho các phát biểu sau:
(a) Công thức phân tử của salbutamol là C13H21NO3.
(b) Salbutamol là hợp chất hữu cơ đa chức vì có chứa nhiều nhóm chức.
(c) Nhóm amine trong phân tử salbutamol có bậc là 1.
(d) Salbutamol có khả năng phản ứng với Na ở điều kiện thường.
Số phát biểu đúng là
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 13: Từ xa xưa, con người đã có thể điều chế acetic acid bằng phương pháp lên men do có ưu điểm dễ thực hiện và sản phẩm thu được có mùi thơm đặc trưng. Nhược điểm của phương pháp này là thời gian lên men thường kéo dài, năng suất thấp và acetic acid thu được có nồng độ thấp. Hiện nay, phương pháp này chỉ được sử dụng để sản xuất một sản lượng nhỏ acetic acid và chủ yếu dùng làm giấm ăn. Từ 17,85 tấn bột sắn chứa 70% tinh bột sản xuất được 51,333 tấn dung dịch acetic acid có nồng độ a% theo sơ đồ chuyển hóa sau:
Tinh bột → Glucose → Ethanol → Acetic acid
Hiệu suất chung của cả quá trình sản xuất là 25%, giá trị của a là
A. 5,00. B. 4,75. C. 2,25. D. 4,51.
(Xem giải) Câu 14: Nitrogen là một nguyên tố dinh dưỡng chính đối với thực vật giúp tăng quá trình phát triển của cây và lá không bị vàng. Ammonium sulfate là thành phần chính của một loại phân đạm phổ biến, trong công nghiệp được điều chế từ nguyên liệu là NH3, CO2 và CaSO4.2H2O theo 2 giai đoạn chính sau:
Giai đoạn 1: Hấp thụ khí NH3 vào bể chứa nước và sục khí CO2 ở áp suất cao, thu được dung dịch (NH4)2CO3 theo phương trình phản ứng (1):
2NH3 + CO2 + H2O → (NH4)2CO3 (1)
Giai đoạn 2: Cho thạch cao CaSO4.2H2O vào dung dịch (NH4)2CO3 để thực hiện phản ứng theo phương trình (2):
(NH4)2CO3 + CaSO4.2H2O → (NH4)2SO4 + CaCO3 + 2H2O (2)
Tách lấy phần dung dịch, làm bay hơi nước thu được tinh thể (NH4)2SO4.
Hiệu suất của giai đoạn (1), (2) lần lượt là 80% và 90%.
Muốn điều chế được 2,64 tấn (NH4)2SO4 thì cần dùng ít nhất x tấn NH3; y tấn CO2 và z tấn CaSO4.2H2O (Kết quả làm tròn đến chữ số hàng phần trăm).
Giá trị x, y, z lần lượt là
A. 0,94; 1,22; 3,82. B. 0,76; 0,98; 3,44. C. 0,76; 0,98; 3,82. D. 0,94; 1,22; 3,44.
(Xem giải) Câu 15: X là chất rắn, vị ngọt, dễ tan trong nước. X có nhiều trong cây mía, củ cải đường …. Trong môi trường acid hoặc có enzyme làm xúc tác, X bị thủy phân thành chất Y và Z. Ở người trưởng thành, khỏe mạnh, lượng Y trong máu trước khi ăn khoảng 4,4 – 7,2 mmol/L (hay 80 – 130 mg/dL). Tên gọi của X và Y lần lượt là
A. glucose và fructose. B. saccharose và glucose.
C. glucose và saccharose. D. saccharose và sorbitol.
(Xem giải) Câu 16: Kết quả phân tích nguyên tố cho biết thành phần về khối lượng các nguyên tố trong hợp chất hữu cơ X là 54,54% carbon; 9,09% hydrogen, còn lại là oxygen.
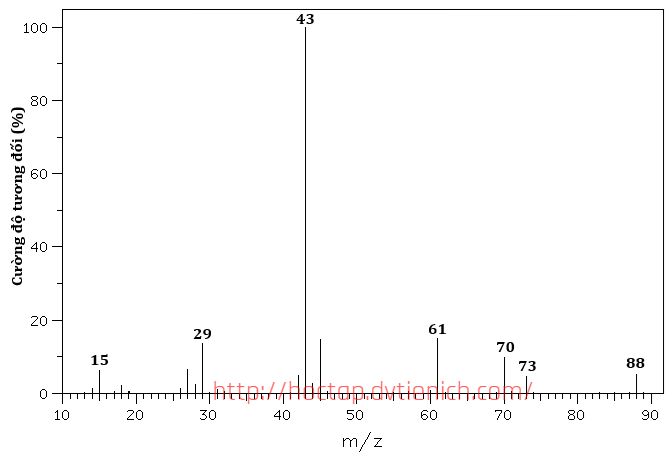
Dựa vào phổ khối lượng (MS) của X trong hình trên, công thức phân tử của X là
A. C4H8O2. B. C3H6O2. C. C5H8O2. D. C4H6O2.
(Xem giải) Câu 17: Một phần dầu thực vật (chất béo không no ở dạng lỏng) được chuyển hóa thành bơ thực vật (chất béo no ở dạng rắn) bởi quá trình
A. thủy phân. B. trùng hợp. C. ester hóa. D. hydrogen hóa.
(Xem giải) Câu 18: Alpha-linoleic acid (ALA) là một loại acid béo thuộc nhóm omega-3 cần thiết cho cơ thể người nhưng không thể tự tổng hợp được và cần phải dung nạp vào thông qua chế độ ăn uống. ALA đóng vai trò quan trọng trong việc duy trì sức khỏe tổng thể và có thể mang lại nhiều lợi ích. Công thức cấu tạo thu gọn của ALA như sau:
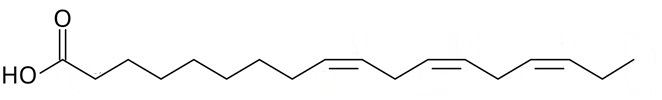
Trong công thức cấu tạo của ALA có bao nhiêu liên kết đôi?
A. 2. B. 4. C. 3. D. 1.
(Xem giải) Câu 19: Món ăn chế biến từ củ sắn (khoai mì) khá quen thuộc, rẻ tiền, phổ biến ở nhiều vùng quê và miền núi nước ta, vừa cung cấp năng lượng cho cơ thể do chứa nhiều tinh bột (carbohydrate), vừa cung cấp nguyên tố potassium (K) và chất xơ. Tuy nhiên, trong vỏ và nhựa củ sắn có nhiều hydrogen cyanide acid (HCN) – chất độc nguy hiểm khi sử dụng.
Phát biểu nào sau đây là sai?
A. Độc tố trong củ sắn là hydrogen cyanide acid (HCN).
B. Để loại bỏ độc tố trong khoai mì, cần gọt sạch vỏ, sau đó cắt khúc ngâm với nước có hòa tan muối ăn, cuối cùng luộc chín với nhiều nước và mở nắp khi luộc.
C. Nhỏ vài giọt dung dịch iodine lên mặt cắt của củ sắn tươi thấy xuất hiện màu vàng.
D. Tinh bột trong củ sắn sẽ chuyển hóa thành đường maltose và đường glucose trong cơ thể người.
(Xem giải) Câu 20: Methyl salicylate (C8H8O3) dùng làm chất giảm đau (có trong miếng dán giảm đau khi vận động hoặc chơi thể thao) được điều chế từ salicylic acid (hay 2–hydroxylbenzoic acid) theo phương trình hóa học sau:
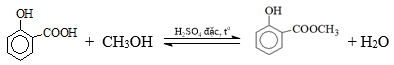
Phát biểu nào sau đây đúng?
A. Công thức phân tử của salicylic acid là C8H6O3.
B. 1 mol methyl salicylate phản ứng tối đa với 2 mol NaOH trong dung dịch.
C. Methyl salicylate thuộc loại hợp chất hữu cơ đa chức.
D. Methyl salicylate không thủy phân trong môi trường kiềm.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 21 đến câu 25. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 21: Muối Epsom (MgSO4.nH2O) có nhiều ứng dụng: vừa có thể dùng pha chế thuốc nhuận tràng, vừa như một loại phân bón cho cây, hay dung dịch khử khuẩn. Khi làm lạnh 440,0 gam dung dịch MgSO4 27,27% thì có 49,2 gam muối Epsom tách ra, phần dung dịch thu được có nồng độ 24,56%. Biết độ tan của MgSO4 tại 80°C và 20°C lần lượt là 54,80 gam và 35,10 gam. Khối lượng Epsom được tách ra khi làm lạnh 9288 gam dung dịch bão hoà MgSO4 từ 80°C xuống 20°C là b gam.
a) Để lâu Epsom trong không khí sẽ bị chảy rữa.
b) Giá trị của b là 3837 gam (kết quả làm tròn đến hàng đơn vị).
c) Epsom là một loại muối có ứng dụng trong y học.
d) Công thức của muối Epsom là MgSO4.6H2O.
(Xem giải) Câu 22: Saccharose monolaurate là một trong những chất phụ gia có chức năng kép do khả năng nhũ hóa và hoạt tính kháng khuẩn của nó. Saccharose monolaurate là hợp chất thu được khi cho saccharose tác dụng với lauric acid.
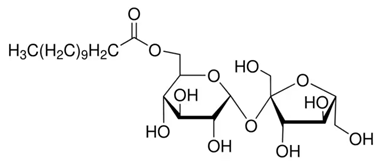
a) Saccharose monolaurate có phản ứng với thuốc thử Tollens.
b) Trong phân tử saccharose monolaurate có chứa hai nhóm chức ester.
c) Từ 400 gam saccharose và 80 gam lauric acid, với hiệu suất phản ứng đạt 47%, có thể điều chế được tối đa 98,512 gam saccharose monolaurate.
d) Lauric acid là một carboxylic acid no, đơn chức, mạch hở không phân nhánh.
(Xem giải) Câu 23: Một hồ chứa nước thải sinh hoạt có thể tích 4000 m³ bị nhiễm ammonium (NH4+) với nồng độ 30 mg/L gây hiện tượng phú dưỡng. Theo quy chuẩn về nước thải sinh hoạt hàm lượng NH4+ không được vượt quá 5 mg/L, thì nước trong hồ trên không đủ điều kiện cho phép. Để giảm hàm lượng trong hồ, người ta thực hiện 2 bước sau:
Bước 1: Dùng nước vôi trong để chuyển hóa NH4+ thành khí NH3; hiệu suất quá trình theo NH4+ là 90%.
Bước 2: Sử dụng khí chlorine để oxi hóa NH3 thành N2; hiệu suất quá trình theo NH3 là 85%.
a) Ở bước 1, khi tác dụng với nước vôi trong, ammonium (NH4+) thể hiện tính acid theo quan điểm của Bronsted – Lowry.
b) Hiện tượng phú dưỡng làm suy kiệt nguồn thủy sản do giảm oxygen.
c) Khối lượng khí chlorine đã dùng trong bước (2) là 534,15 kg.
d) Nước từ hồ trên, sau xử lý có nồng độ NH4+ đạt quy chuẩn về nước thải sinh hoạt.
(Xem giải) Câu 24: Eugenol là thành phần chính của tinh dầu hương nhu với các đặc điểm sau:
(1) Công thức phân tử của eugenol là: C10H12O2.
(2) Eugenol tác dụng được với Na và NaOH.
(3) Hydrogen hoá hoàn toàn eugenol, thu được sản phẩm 2-methoxy-4-propylcyclohexanol (gọi là sản phẩm P, nhóm methoxy có công thức là CH3O-).
(4) Eugenol không có đồng phân hình học.
Cho các phát biểu sau
a) Eugenol có 1 nhóm methylene (CH2) trong phân tử.
b) Eugenol làm nhạt màu nước bromine.
c) Eugenol thuộc loại hợp chất thơm.
d) Chất P không tác dụng với dung dịch NaOH.
(Xem giải) Câu 25: Bảng sau cung cấp một số thông tin của benzyl chloride, benzyl alcohol và o-cresol:
| Chất | Benzyl chloride | Benzyl alcohol | o-Cresol |
| Nhiệt độ sôi | 179°C | 205,3°C | 191°C |
| Nhiệt độ nóng chảy | -39°C | -15,2°C | 31°C |
| -352 kJ/mol | -204,3 kJ/mol | ||
| Độ tan trong nước (20°C) | Rất ít tan (0,05%) | 3,50 gam/100 mL | < 3,1 gam/100 mL |
Từ các thông tin trong bảng trên:
a) So với benzyl alcohol, benzyl chloride rất ít tan trong nước hơn do không tạo được liên kết hydrogen với nước.
b) Ở điều kiện thường (25°C), cả 3 chất trên tồn tại ở trạng thái lỏng.
c) Khi đốt cháy cùng lượng benzyl alcohol hoặc o-cresol đều cần lượng oxygen như nhau và phát sinh lượng nhiệt bằng nhau.
d) Nhiệt độ sôi của benzyl alcohol lớn hơn nhiệt độ sôi của benzyl chloride là do benzyl alcohol có liên kết hydrogen giữa các phân tử.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 26 đến câu 35. Chú ý: Trong các bài tính toán, chỉ làm tròn ở phép tính cuối cùng.
(Xem giải) Câu 26: Để xác định hàm lượng sulfur có trong một số mẫu than, người ta có thể chuyển hoàn toàn sulfur thành khí sulfur dioxide bằng cách oxi hóa rồi thực hiện thêm các bước sau:
Bước 1. Oxi hóa hoàn toàn sulfur dioxide bằng hydrogen peroxide:
H2O2 + SO2 → H2SO4
Bước 2. Chuẩn độ dung dịch H2SO4 thu được sau bước (1) bằng dung dịch NaOH:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Xử lý 1,302 gam mẫu than theo cách trên, ở bước (2) cần dùng vừa hết 28,44 mL dung dịch NaOH 0,1 M.
Hàm lượng sulfur có trong mẫu than là bao nhiêu %? (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 27: Tinh dầu chanh ngoài mùi thơm dễ chịu giúp thư dãn còn có thể diệt côn trùng (muỗi, rệp,..) và tương đối thân thiện với môi trường. Để thu tinh dầu từ lá chanh, có thể thực hiện theo các bước sau:
Bước 1. Cắt nhỏ lá chanh.
Bước 2. Cho hơi nước đi qua phần lá chanh đã cắt ở bước 1. Hơi nước chứa tinh dầu lá chanh sau đó được dẫn qua hệ thống sinh hàn làm lạnh và ngưng tụ lại thành dạng lỏng.
Bước 3. Để yên cho hỗn hợp thu được ở bước 2 tách thành 2 lớp dung dịch rõ ràng do tinh dầu không tan trong nước. Loại bỏ phần nước, thu lấy tinh dầu.
Trong quy trình này, người ta đã sử dụng bao nhiêu phương pháp trong những phương pháp sau đây để tách và tinh chế tinh dầu?
(1) Chưng cất. (2) Chiết. (3) Kết tinh. (4) Sắc kí.
(Xem giải) Câu 28: Một loại keo được sử dụng trong quá trình tạo gỗ công nghiệp là keo dán poly (urea-formaldehyde) được sản xuất từ urea và formaldehyde; phần dư formaldehyde trong quá trình sản xuất keo là một hoá chất độc hại đối với sức khoẻ con người. Tại các nước phát triển dư lượng formaldehyde được kiểm soát rất nghiêm ngặt. Một doanh nghiệp ở nước ta đã sử dụng 6,48.10^-5 gam keo dán poly (urea-formaldehyde) để tạo 300 kg gỗ (Khối lượng riêng của loại gỗ này là 800 kg/m³) và lô gỗ này đã đủ điều kiện để xuất khẩu sang các nước phát triển do dư lượng formaldehyde đạt mức cho phép (*). Tính lượng formaldehyde (μg) cần để tạo ra lượng keo dán 1m³ gỗ trên. (Kết quả làm tròn đến hàng đơn vị)
Biết: Quá trình sản xuất keo dán trên theo phương trình hóa học sau có hiệu suất đạt 90% (tính theo formaldehyde), bỏ qua khối lượng các tạp chất trong keo.
n(NH2)2CO + nHCHO (t°, p) → (-NH-CO-NH-CH2-)n + nH2O
(*) Các nước phát triển quy định tiêu chuẩn dư lượng formaldehyde trong gỗ công nghiệp là 120 μg/m³.
(Xem giải) Câu 29: Dung dịch glucose 5% (D = 1,1 g/mL) là dung dịch đường có thể dùng tiêm tĩnh mạch, là một loại thuốc thiết yếu, quan trọng của Tổ chức Y tế Thế giới (WHO) và hệ thống y tế cơ bản. Khi được truyền 1 chai 500 mL dung dịch glucose 5% người bệnh được cung cấp tối đa bao nhiêu năng lượng (kJ) theo phương trình phản ứng oxi hóa glucose xảy ra như sau:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l) ![]() = -2803,0 kJ
= -2803,0 kJ
(Kết quả làm tròn đến hàng đơn vị)
(Xem giải) Câu 30: Một loại thuốc có tác dụng điều trị triệu chứng rối loạn do tăng acid dạ dày – tá tràng trong các chứng: Viêm dạ dày, thoát vị hoành, khó tiêu, loét dạ dày – tá tràng chứa 2 hoạt chất chính, gồm: Aluminium hydroxide gel khô, magnesium hydroxide.
Thuốc bào chế dạng viên nén nhai, quy cách đóng gói gồm hộp 4 vỉ x 12 viên. Mỗi viên chứa tổng cộng 800 mg hoạt chất, trong đó:
+ Aluminium hydroxide gel khô chiếm 60% khối lượng hoạt chất.
+ Magnesium hydroxide chiếm 40% khối lượng hoạt chất.
Tính khối lượng (gam) hoạt chất có trong 1 hộp thuốc Maalox ở trên.
(Xem giải) Câu 31: Trong sản xuất phân bón, supephosphate kép chứa thành phần dinh dưỡng là Ca(H2PO4)2 và được sản xuất từ quặng phosphorite theo hai giai đoạn ứng với hai phương trình hóa học sau:
Ca3(PO4)2 + 3H2SO4 → 2H3PO4 + 3CaSO4
Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2
Để sản xuất được 1 tấn Ca(H2PO4)2 với hiệu suất của cả quá trình là 80% thì cần bao nhiêu tấn dung dịch H2SO4 70%? (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 32: Dầu gió dùng để trị cảm, ho, sổ mũi, nhức đầu, say nắng, trúng gió, say tàu xe, buồn nôn, đau bụng, sưng viêm, nhức mỏi, muỗi chích, kiến đốt, tê thấp tay chân,… Thành phần một chai dầu gió 12 mL gồm tinh dầu bạc hà (0,36 mL), menthol (2,52 gam), methyl salicylate (2,16 gam), eucalyptol (0,72 mL), tinh dầu đinh hương (0,24 mL), long não (0,36 gam). Methyl salicylate được điều chế theo phương trình hóa học sau:
HOC6H4COOH + CH3OH (H2SO4 đặc, t°) ⇋ HOC6H4COOCH3 + H2O
Để sản xuất một triệu hộp, mỗi hộp chứa 12 chai dầu gió trên cần tối thiểu m tấn salicylic acid, với hiệu suất cả quá trình là 80%. Giá trị của m là bao nhiêu? (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 33: Một vận động viên thể hình (Gymer) cần luyện tập với cường độ cao và bổ sung dinh dưỡng đầy đủ hơn để chuẩn bị cho một giải thi đấu. Một trong các thực phẩm bổ sung không thể thiếu là omega-3 để hỗ trợ tim mạch trong quá trình tập luyện. Vận động viên trước đây kết hợp các thực phẩm giàu omega-3 kèm theo sử dụng 5 viên “Now Omega-3 Fish Oil” mỗi ngày để cung cấp thêm omega-3 qua tổng hàm lượng EPA và DHA. Tuy nhiên, thương hiệu X đã sản xuất một sản phẩm với hàm lượng EPA và DHA cao hơn đó là “Now Ultra Omega-3 Fish Oil” với hàm lượng và giá thành của hai sản phẩm như sau:
| Loại sản phẩm | Tên sản phẩm | 1000 mg fish oil (dầu cá)/ viên | Giá thành 1 lọ | |
| EPA (mg) | DHA (mg) | |||
| Loại 1 | Now Omega-3 Fish Oil
(200 viên/ lọ) |
180 | 120 | 380.000 VNĐ |
| Loại 2 | Now Ultra Omega-3 Fish Oil
(180 viên/ lọ) |
500 | 250 | 850.000 VNĐ |
Vì lượng “body fat” (chỉ số mỡ trên cơ thể) của vận động viên tương đối cao nên thời gian luyện tập với cường độ cao và bổ sung dinh dưỡng đầy đủ suốt trong vòng 3 tháng (mỗi tháng coi như có 30 ngày). Nếu sử dụng viên uống dầu cá loại 2 thay cho loại 1 trong vòng 3 tháng thì vận động viên đó tiết kiệm được chi phí được bao nhiêu ngàn đồng Việt Nam (VNĐ)? (biết nhà phân phối, cửa hàng không bán lẻ từng viên và tỉ lệ chênh lệch EPA : DHA giữa mỗi loại sản phẩm không quan trọng)
(Xem giải) Câu 34: Urea ((NH2)2CO) là loại phân đạm có hàm lượng cao, được điều chế theo sơ đồ phản ứng sau:
(1) Nhiệt phân đá vôi với hiệu suất 80%: CaCO3 → CaO + CO2
(2) Tổng hợp NH3 với hiệu suất 18%: N2 + 3H2 ⇋ 2NH3
(3) Cho NH3 tác dụng với CO2 ở nhiệt độ 180 – 200°C, dưới áp suất khoảng 200 atm với hiệu suất 75%
CO2 + 2NH3 → (NH2)2CO + H2O
Từ nguồn nguyên liệu ban đầu gồm: 991,6 m³ (đo ở điều kiện chuẩn) hỗn hợp khí X (chứa: N2 và H2 với tỉ lệ mol tương ứng 1 : 3) và 400 kg đá vôi (chứa 80% CaCO3) có thể sản xuất được bao nhiêu kg phân urea có độ dinh dưỡng 46%? (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 35: Lactic acid hay acid sữa là hợp chất hóa học đóng vai trò quan trọng trong nhiều quá trình sinh hóa. Lactic acid lần đầu tiên được phân tách vào năm 1780 bởi nhà hóa học người Thụy Điển, Carl Wilhelm Scheele. Lactic acid có công thức phân tử là C3H6O3 và công thức cấu tạo như hình dưới.
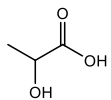
Khi vận động mạnh, không được cung cấp đủ oxygen, cơ thể sẽ chuyển từ hô hấp hiếu khí sang hô hấp kị khí tạo lactic acid (gây hiện tượng mỏi cơ) và năng lượng theo phương trình sau:
C6H12O6(aq) → 2C3H6O3(aq) ![]() = -150 kJ
= -150 kJ
Một người chạy bộ cần tiêu tốn 300 kcal (1 cal = 4,184 J) nhưng chỉ 98% năng lượng cho cơ thể được cung cấp nhờ oxygen qua hô hấp, phần còn lại nhờ vào sự chuyển hóa glucose thành lactic acid. Tính khối lượng lactic acid (gam) tạo ra từ glucose bằng cách hô hấp kị khí theo phương trình hóa học trên. (Kết quả làm tròn đến hàng phần mười)


Bình luận