[2025 – 2026] Thi học sinh giỏi lớp 12 cụm Phú Thọ
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Tổng hợp đề hsg theo năm học
⇒ Mã đề 015-H12B năm 2025-2026
⇒ Thời gian làm bài: 150 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1B | 2B | 3D | 4C | 5D | 6A | 7D | 8D |
| 9B | 10D | 11A | 12C | 13C | 14B | 15A | 16C |
| 17A | 18C | 19B | 20C | 21A | 22B | 23A | 24B |
| 25A | 26B | 27A | 28A | 29A | 30A | 31C | 32B |
| Câu 1 | Câu 2 | Câu 3 | Câu 4 | |
| (a) | S | S | S | S |
| (b) | Đ | Đ | Đ | S |
| (c) | Đ | S | Đ | Đ |
| (d) | S | Đ | S | S |
| Câu 1 | Câu 2 | Câu 3 | Câu 4 | Câu 5 | Câu 6 |
| 5 | 88,9 | 124 | 2 | 134 | 1238 |
I. PHẦN TRẮC NGHIỆM
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn (8,0 điểm). Thí sinh trả lời từ câu 1 đến câu 32. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho dãy các chất: Cu, S, FeO, SO2, N2, HCl, CH3CHO. Số chất có cả tính oxi hoá và tính khử là
A. 4. B. 6. C. 5. D. 7.
(Xem giải) Câu 2. Các hiện tượng cháy, nổ xảy ra hầu hết do các phản ứng hóa học gây nên, tỏa nhiều nhiệt, tốc độ phản ứng lớn. Do đó, hóa học đóng vai trò rất quan trọng trong việc nghiên cứu nguyên nhân, đưa ra các biện pháp phòng chống cũng như xử lí khi xảy ra hỏa hoạn một cách hiệu quả và an toàn nhất. Cho các phát biểu sau:
(a) Các đám cháy là chất rắn như gỗ, củi, rơm rạ ta có thể sử dụng nước làm giảm nhiệt độ của đám cháy xuống dưới nhiệt độ cháy, làm loãng khí cháy.
(b) Có thể dùng bột chữa cháy chứa NaHCO3 để dập tắt các đám cháy của kim loại magnesium.
(c) Sử dụng nước để dập tắt các đám cháy của các kim loại hoạt động hóa học mạnh như sodium (Na), aluminum (Al), …
(d) Trong một đám cháy do xăng, dầu, người ta có thể dùng nước để dập tắt đám cháy đó.
Các phát biểu sai là
A. (a), (b), (c). B. (b), (c), (d). C. (a), (c), (d). D. (a), (b), (d).
(Xem giải) Câu 3. Cho các phản ứng hóa học sau (ở điều kiện chuẩn):
(1) C(graphite) + O2(g) → CO2(g) ![]() = -393,5 kJ
= -393,5 kJ
(2) CaCO3(s) → CaO(s) + CO2(g) ![]() = +176 kJ
= +176 kJ
(3 C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l) ![]() = -1367 kJ
= -1367 kJ
Cho các phát biểu sau:
(a) Phản ứng (2) có ![]() > 0 là phản ứng tỏa nhiệt.
> 0 là phản ứng tỏa nhiệt.
(b) Đốt cháy 1 mol C(graphite) tỏa ra lượng nhiệt nhiều hơn đốt cháy 1 mol C2H5OH(l).
(c) Các phản ứng (1); (3) là phản ứng tỏa nhiệt.
(d) Trong phản ứng (2) khi 1 mol CO2 được tạo ra thì phản ứng thu vào lượng nhiệt là 176 kJ.
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 4. Khí oxygen được điều chế trong phòng thí nghiệm bằng cách nhiệt phân potassium chlorate. Để thí nghiệm thành công và rút ngắn thời gian tiến hành có thể dùng một số biện pháp sau:
(a) Dùng chất xúc tác manganese dioxide.
(b) Nung ở nhiệt độ cao.
(c) Dùng phương pháp dời nước để thu khí oxygen.
(d) Nghiền nhỏ potassium chlorate.
(e) Trộn đều bột potassium chlorate và xúc tác.
Số biện pháp dùng để tăng tốc độ phản ứng là
A. 2. B. 3. C. 4. D. 5.
(Xem giải) Câu 5. Urea là loại phân đạm có độ dinh dưỡng cao, được điều chế bằng cách cho ammonia tác dụng với carbondioxide ở nhiệt độ 180 – 200°C, áp suất khoảng 200 atm theo phương trình hóa học sau: CO2 + 2NH3 → (NH2)2CO + H2O.
Từ nguyên liệu ban đầu gồm 495,8 m³ hỗn hợp khí X (chứa N2 và H2 với tỉ lệ mol tương ứng là 1 : 3 ở điều kiện chuẩn) và 125 kg đá vôi chứa 80% CaCO3 thì thu được bao nhiêu kg urea (biết hiệu suất của các phản ứng tổng hợp ammonia, nung vôi và sản xuất phân urea lần lượt là 20%, 80% và 75%)?
A. 32. B. 48. C. 60. D. 36.
(Xem giải) Câu 6. Cho biết sức điện động chuẩn của các pin sau:
| Pin điện hóa | X – Y | M – Y | M – Z |
| Sức điện động chuẩn (V) | 0,20 | 0,60 | 0,30 |
Sắp xếp nào sau đây đúng với tính khử của các kim loại theo thứ tự tăng dần từ trái sang phải?
A. Y < X < Z < M. B. X < Y< M < Z. C. M < Z < Y < X. D. X < Y < Z < M.
(Xem giải) Câu 7. Cho pin điện hoá có cấu tạo như sau:
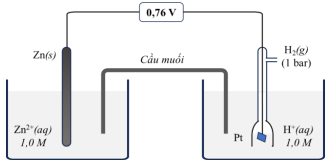
Cho các phát biểu sau:
(a) Thế điện cực chuẩn E°Zn2+/Zn = −0,76V.
(b) Khi pin hoạt động, ion âm trong cầu muối di chuyển về phía điện cực hydrogen.
(c) Tại điện cực dương xảy ra quá trình oxi hóa ion H+(aq) thành khí H2(g).
(d) Phản ứng xảy ra trong pin là: H2(g) + Zn2+(aq) → Zn(s) + 2H+(aq).
Số phát biểu đúng là
A. 3. B. 4. C. 2. D. 1.
(Xem giải) Câu 8. Để mạ đồng một vật dụng kim loại có tổng diện tích bề mặt là 10 cm², người ta tiến hành điện phân dung dịch CuSO₄ với cực âm là vật dụng cần mạ và cực dương là lá đồng thô. Biết cường độ dòng điện không đổi là 2 A, hiệu suất điện phân là 90%, khối lượng riêng của tinh thể Cu là 8,94 g/cm³ và lượng đồng tạo ra được tính theo công thức m = A.I.t/nF (với A là nguyên tử khối của Cu = 64; I là cường độ dòng điện, F là hằng số Faraday = 96485 C/mol, n là số electron mà 1 ion Cu²⁺ nhận, t là thời gian điện phân tính bằng giây). Thời gian điện phân để lớp mạ có độ dày đồng nhất 0,1 mm là bao nhiêu giây?
A. 1380,54. B. 1526,72. C. 1347,77. D. 1497,53.
(Xem giải) Câu 9. Chuẩn độ hàm lượng ion Fe2+ trong môi trường acid (chứa trong bình tam giác) bằng dung dịch KMnO4 đã biết nồng độ (chứa trên burette). Trong quá trình chuẩn độ, nếu dung dịch trên burette được thêm vào bình tam giác quá nhanh thì trong bình sẽ xuất hiện kết tủa nâu MnO2 theo quá trình hóa học dưới đây, dẫn đến sai lệch kết quả chuẩn độ: (aq) + H+(aq) + Fe2+(aq) → MnO2(s) + Fe3+(aq) + H2O(l)
Giả sử một học sinh thao tác sai, làm 60% lượng chuẩn độ chuyển thành MnO2 (phần còn lại vẫn phản ứng tạo Mn2+), tổng lượng Fe2+ bị oxi hóa là 2,2 mmol. Thể tích dung dịch KMnO4 0,020 M đã dùng tăng bao nhiêu mL so với khi chuẩn độ với thao tác phù hợp (chỉ tạo ra Mn2+)?
A. 6,72. B. 6,95. C. 5,85. D. 7,45.
(Xem giải) Câu 10. Đất chua là đất có độ pH dưới 6,5. Khi đất chua, các khoáng sét trong đất bị phá vỡ, giải phóng ra các ion Al3+ tự do gây bất lợi cho cây trồng. Nếu đất chua nhiều, ion Al3+ di động cao có thể gây độc cho hệ rễ cây, làm cho rễ bị bó và chùn lại không phát triển. Muốn sản xuất được trên nền đất này cần phải cải thiện độ chua đất trước khi gieo trồng. Một nông nhân đã làm thí nghiệm xác định độ pH của đất trồng của mình như sau: Lấy một lượng đất cho vào nước vừa lọc lấy phần dung dịch dùng máy pH đo được giá trị pH là 3,602.
Cho các phát biểu sau:
(a) Mẫu đất trên có môi trường acid, thuộc loại đất chua.
(b) Nồng độ [H+] trong mẫu đất trên khoảng 3.10-11M.
(c) Có thể cải tạo mẫu đất trên bằng cách bón đạm ammonium như NH4Cl.
(d) Nếu bón tro thực vật sẽ làm tăng pH của đất vì ion CO32- bị thuỷ phân tạo môi trường base.
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 11. Độ tan trong nước của MgSO4 ở 20°C và 80°C lần lượt là 33,7 gam và 55,8 gam (trong 100 gam nước). Làm lạnh 779 gam dung dịch bão hòa MgSO4 từ 80°C xuống 20°C thì thấy có 350,55 gam chất rắn MgSO4.nH2O kết tinh. Phần trăm khối lượng của nguyên tố oxygen trong chất rắn kết tinh là
A. 71,54%. B. 45,53%. C. 51,22%. D. 48,78%.
(Xem giải) Câu 12. Để xác định hàm lượng oxygen tan trong nước, người ta lấy 100,0 mL nước rồi cho ngay manganese(II) sulfate dư và sodium hydroxide vào nước. Sau khi lắc kĩ (không cho tiếp xúc với không khí), manganese(II) hydroxide bị oxygen oxi hóa thành manganese oxohydroxide (MnO(OH)2). Thêm acid dư và cho tiếp potassium iodide dư vào hỗn hợp, thì ion idodine bị MnO(OH)2 oxi hóa thành iodine. Lượng I2 sinh ra phản ứng vừa đủ với 10,5 mL dung dịch Na2S2O3 0,01M. Biết các phản ứng xảy ra theo sơ đồ sau:
Mn2+ + OH- → Mn(OH)2 (1)
Mn(OH)2 + O2 → MnO(OH)2 (2)
MnO(OH)2 + I- + H+ → Mn2+ + I2 + H2O (3)
I2 + Na2S2O3 → Na2S4O6 + NaI (4)
Hàm lượng O2 tan trong nước (tính theo mg O2/1L) là
A. 7,45. B. 0,84. C. 8,40. D. 6,25.
(Xem giải) Câu 13. Hai chất X và Y (chứa C, H, O) là đồng phân cấu tạo của nhau và đều có mạch carbon no, không phân nhánh, không tác dụng với NaOH. Từ phổ khối lượng, xác định được phân tử khối của Y là 72. Phát biểu nào sao đây là đúng về X và Y?
A. Trên phổ hồng ngoại của X và Y đều có tín hiệu đặc trưng trong khoảng 3600 – 3300 cm-1.
B. X là alcohol đơn chức còn Y là aldehyde đơn chức.
C. X và Y có 1 đồng phân cấu tạo Z mạch hở có tín hiệu đặc trưng trên phổ hồng ngoại từ 1740 – 1670 cm-1.
D. X và Y đều là alcohol đơn chức, không no.
(Xem giải) Câu 14. Cho các quá trình nào sau:
(1) Ethane (t°, xt) → Ethylene + hydrogen.
(2) Ethylbenzen (t°, xt) → 1,2-dimethylbenzene.
(3) Octane (t°, xt) → Butane + But-1-ene.
(4) Octane (t°, xt) → 2,2,4-trimethylpentane.
(5) Heptane (t°, xt) → isoheptan.
Có bao nhiêu quá trình là quá trình reforming?
A. 5. B. 3. C. 4. D. 2.
(Xem giải) Câu 15. Một học sinh tiến hành tổng hợp ethyl butyrate (thành phần chính tạo mùi dứa) từ butyric acid và ethanol theo phương trình hóa học sau: CH3CH2CH2COOH + C2H5OH ⇋ CH3CH2CH2COOC2H5 + H2O
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của butyric acid, ethanol và ethyl butyrate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O-H (alcohol) | O-H (carboxylic acid) | C=O (ester, carboxylic acid) |
| Số sóng (cm⁻¹) | 3650 – 3200 | 3300 – 2500 | 1780 – 1650 |
Cho các phát biểu sau:
(a) Phản ứng tổng hợp trong thí nghiệm này là phản ứng thủy phân ester.
(b) Phổ hồng ngoại có số sóng hấp thụ ở 3400 cm⁻¹ là phổ của ethanol.
(c) Phổ hồng ngoại có số sóng hấp thụ ở 1730 cm⁻¹ mà không có số sóng hấp thụ đặc trưng của liên kết -OH là phổ của ethyl butyrate.
(d) Dựa vào phổ hồng ngoại, phân biệt được butyric acid, ethanol và ethyl butyrate.
Số phát biểu đúng là
A. 3. B. 1. C. 4. D. 2.
(Xem giải) Câu 16. Aldehyde (X) no đơn chức mạch hở không nhánh. Phân tử khối của (X) được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất ở hình dưới đây:
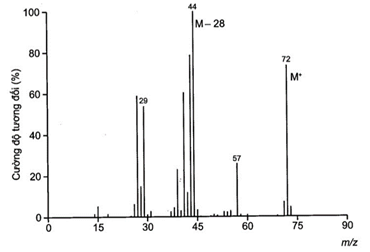
Trong phân tử X có số liên kết σ là
A. 10. B. 9. C. 12. D. 11.
(Xem giải) Câu 17. Bình “ga” loại 12 cân sử dụng trong hộ gia đình Thành Đạt có chứa 12 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 3 : 7 (thành phần khác không đáng kể). Khi được đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2500 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Trung bình, lượng nhiệt tiêu thụ từ đốt khí “ga” của hộ gia đình Y là 14283,15 kJ/ngày. Biết rằng hộ gia đình Thành Đạt sử dụng hết một bình ga trong vòng 30 ngày. Hiệu suất hấp thụ nhiệt là (kết quả làm tròn đến hàng đơn vị)
A. 70%. B. 60 %. C. 80%. D. 90%.
(Xem giải) Câu 18. Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Cho vào cốc thủy tinh chịu nhiệt khoảng 5 gam mỡ lợn và 10 mL dung dịch NaOH 40%.
• Bước 2: Đun sôi nhẹ hỗn hợp, liên tục khuấy đều bằng đũa thủy tinh khoảng 30 phút và thỉnh thoảng thêm nước cất để giữ cho thể tích hỗn hợp không đổi. Để nguội hỗn hợp.
• Bước 3: Rót vào hỗn hợp 15 – 20 mL dung dịch NaCl bão hòa, nóng, khuấy nhẹ rồi để yên.
Cho các phát biểu sau:
(a) Sau bước 3 thấy có lớp chất rắn màu trắng nổi lên là glycerol.
(b) Vai trò của dung dịch NaCl bão hòa ở bước 3 là để tách muối của acid béo ra khỏi hỗn hợp.
(c) Ở bước 2, nếu không thêm nước cất, hỗn hợp bị cạn khô thì phản ứng thủy phân không xảy ra.
(d) Ở bước 1, nếu thay mỡ lợn bằng dầu dừa thì hiện tượng thí nghiệm sau bước 3 xảy ra tương tự.
Số phát biểu đúng là
A. 4. B. 1. C. 3. D. 2.
(Xem giải) Câu 19. Xà phòng, chất giặt rửa được dùng để loại bỏ các vết bẩn bám trên quần áo, bề mặt các vật dụng. Cho công thức của chất giặt rửa:
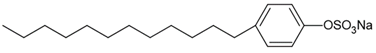
Cho các phát biểu sau:
(a) Chất giặt rửa này có thể dùng được với nước cứng.
(b) Hạn chế sử dụng chất giặt rửa tổng hợp vì phần kị nước chứa vòng benzene rất khó bị vi sinh vật phân huỷ gây ô nhiễm môi trường.
(c) Trong công nghiệp người ta tổng hợp chất trên từ alkane trong khí thiên nhiên qua nhiều giai đoạn.
(d) Khi giặt rửa vật liệu với nước, phần ưa nước quay đầu về phía dầu, mỡ và thâm nhập vào vết dầu mỡ.
(e) Phần ưu nước có 18 nguyên tử carbon.
Các phát biểu đúng là
A. a, b, d. B. a, b. C. a, c, d. D. a, d, e.
(Xem giải) Câu 20. Cho E và F là hai chất hữu cơ mạch hở có công thức phân tử lần lượt là C4H6O4 và C5H8O5 (đều tạo từ carboxylic acid và alcohol). Từ E và F thực hiện sơ đồ các phản ứng sau:
(1) E + NaOH (t°) → X + Y
(2) F + NaOH (t°) → X + Z
(3) X + HCl → T + NaCl
Biết X, Y, Z là các chất hữu cơ, trong đó phân tử Y không có nhóm -CH3. Cho các phát biểu sau:
(a) Chất T dùng làm nguyên liệu để điều chế khí CO trong công nghiệp.
(b) Chất Y có thể được điều chế trực tiếp từ ethylene.
(c) Đun nóng mỡ lợn hoặc dầu dừa trong môi trường kiềm đều thu được chất Z.
(d) Ở nhiệt độ thường, ba chất Y, Z và T đều hoà tan được Cu(OH)2.
(e) Chất F có hai công thức cấu tạo thỏa mãn.
Số phát biểu đúng là
A. 5. B. 3. C. 4. D. 2.
(Xem giải) Câu 21. Cho các phát biểu về saccharose và maltose:
(a) Ở dạng mạch vòng, số nhóm -OH trong saccharose và maltose bằng nhau.
(b) Hai gốc monosaccharide trong saccharose liên kết với nhau qua nguyên tử oxygen bằng liên kết α-1,2-glycoside.
(c) Hai gốc monosaccharide trong maltose liên kết với nhau qua nguyên tử oxygen bằng liên kết α-1,4-glycoside.
(d) Saccharose là hợp chất hữu cơ đa chức có công thức dạng C12(H2O)11.
Các phát biểu đúng là
A. a, b, c. B. a, b, c, d. C. b, c, d. D. a, c, d.
(Xem giải) Câu 22. X là chất rắn, tinh thể không màu, dễ tan trong nước, có vị ngọt nhưng không ngọt bằng đường mía. X có nhiều trong quả nho chín. Y là đồng phân của X và có nhiều trong quả ngọt như dứa, xoài,… Cho các phát biểu sau:
(a) X là chất dinh dưỡng và được dùng làm thuốc tăng lực cho người già, trẻ em và người ốm.
(b) Trong mật ong, X chiếm hàm lượng cao hơn Y khoảng 10%.
(c) X bị oxi hoá bởi AgNO3 trong NH3 và bị khử bởi Cu(OH)2 trong môi trường kiềm.
(d) Trong cơ thể người và động vật, tinh bột bị thuỷ phân thành X nhờ các enzyme.
Các phát biểu đúng là
A. b, c. B. a, d. C. a, c. D. b, d.
(Xem giải) Câu 23. Trong công nghiệp chế biến đường từ mía sẽ tạo ra sản phẩm phụ, gọi là rỉ đường hay rỉ mật (chứa 90% saccharose). Người ta sử dụng rỉ đường để lên men tạo ra ethanol trong điều kiện thích hợp với hiệu suất của cả quá trình là 40% (biết cả glucose và fructose đều bị lên men thành ethanol):
C12H22O11 + H2O → C6H12O6 + C6H12O6
C6H12O6 → 2C2H5OH + 2CO2
Khối lượng ethanol thu được từ 1 tấn rỉ đường mía theo 2 phương trình trên là
A. 193,7 kg. B. 484,21 kg. C. 184,2 kg. D. 96,84 kg.
(Xem giải) Câu 24. Tryptophan là amino acid thiết yếu có tác dụng duy trì cân bằng nitrogen cho cơ thể và là tiền chất của serotonin, một chất dẫn truyền thần kinh điều chỉnh cảm giác thèm ăn, cơn buồn ngủ và trạng thái tâm lý.

Phát biểu nào sau đây đúng?
A.Tryptophan là hợp chất amino acid chỉ chứa nhóm -COOH và -NH2.
B.Tryptophan có chứa 2 nhóm chức amine.
C.Tryptophan là amino acid mà cơ thể có thể tự tổng hợp được.
D.Tryptophan có công thức phân tử C11H10N2O2.
(Xem giải) Câu 25. Mỗi amino acid có một giá trị pH cụ thể mà tại đó amino acid tồn tại trong dung dịch ở dạng ion lưỡng cực, giá trị pH đó gọi là pH đẳng điện (pI). Giá trị pI của một số amino acid được cho ở bảng sau:
| Amino acid | Alanine | Lysine | Glutamic acid |
| pI | 6 | 9,8 | 3,2 |
Cho các phát biểu sau:
(a) Ở pH = 6 có thể tách alanine, lysine, glutamic acid ra khỏi hỗn hợp bằng phương pháp điện di.
(b) Ở pH = 12 cả ba amino acid trên đều di chuyển về cực dương của điện trường.
(c) Ở pH = 3,2 cả ba amino acid trên đều di chuyển về cực âm của điện trường.
(d) Glycine, valine có giá trị pI gần bằng giá trị pI của alanine.
Các phát biểu đúng là
A. a, b, d. B. a, c, d. C. b, c, d. D. a, b, c.
(Xem giải) Câu 26. Thyroxine là loại hormone được tiết ra từ tuyến giáp, tuyến nội tiết lớn nhất trong cơ thể. Đây là một loại thuốc được sử dụng trong điều trị bệnh thiếu hụt hormone tuyến giáp. Thyroxine không tồn tại trong protein. Hormone tuyến giáp được xem như một dạng ngôn ngữ chứa thông điệp di chuyển theo máu đến các cơ quan nhằm điều phối chức năng hoạt động của cơ thể. Hormone tuyến giáp chịu trách nhiệm chính trong việc kiểm soát và trao đổi chất. Đối với trẻ sơ sinh, hormone tuyến giáp có vai trò quan trọng cho sự phát triển của não. Thyroxine có công thức cấu tạo như hình dưới:
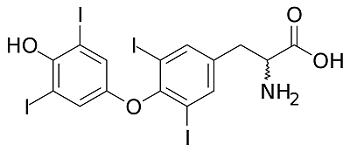
Cho các phát biểu sau:
(a) Thyroxine có hai nhóm chức có thể phân li ra proton trong nước.
(b) Số liên kết σ trong phân tử thyroxine là 36.
(c) Nếu thiếu hụt iodine dẫn đến tuyến giáp giảm sản xuất thyroxine, làm phình mô tuyến giáp và sẽ gây ra bệnh bứu cổ.
(d) Công thức phân tử của thyroxine là C15H11O4NI4.
(e) Thyroxine có 5 loại nhóm chức trong phân tử.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 2.
(Xem giải) Câu 27. Cho các polymer sau: poly(hexamethylene adipamide), polyacrylonitrile, poly(ethylene terephthalate), poly(methyl methacrylate), poly(vinylchloride), polyethylene. Số polymer có thành phần hóa học chứa nguyên tố nitrogen là
A. 2. B. 4. C. 3. D. 5.
(Xem giải) Câu 28. Tơ capron là polymer có tính dai, bền, mềm óng mượt, ít thấm nước, mau khô. Bên cạnh ứng dụng trong ngành may mặc, tơ capron còn được sử dụng làm dây cáp, dù, đan lưới, chế tạo các chi tiết máy. Một quy trình sản xuất tơ capron từ cyclohexanol được thực hiện theo sơ đồ sau:
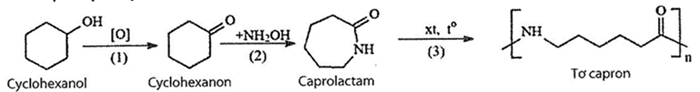
Cho các phát biểu sau:
(a) Tơ capron thuộc loại polypeptide.
(b) Phản ứng (3) là phản ứng trùng hợp.
(c) Phần trăm khối lượng của carbon trong tơ capron là 63,72%.
(d) Nếu hiệu suất chuyển hoá từ cyclohexanol đến tơ capron là 80%, thì cứ 1 tấn cyclohexanol thu được 1,13 tấn tơ capron.
(e) Oxi hóa cyclohexanon bởi LiAlH4 thu được cyclohexanol.
(g) Tơ capron không bền trong môi trường acid.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 2.
(Xem giải) Câu 29. Cho các phát biểu sau:
(a) Acid béo omega- 3 và omega-6 là các acid béo không no với liên kết đôi C=C đầu tiên ở vị trí số 3 và số 6 khi đánh số từ nhóm carboxyl.
(b) Số nguyên tử oxygen có trong một phân tử glucose là 6 .
(c) Dung dịch acetic acid CH3COOH có thể làm quỳ tím chuyển màu hồng.
(d) Acetaldehyde CH3CHO phản ứng với thuốc thử Tollens tạo kết tủa Ag.
(e) Trong phân tử xà phòng có đầu ưa nước và đuôi dài kị nước.
Số phát biểu đúng là
A. 4. B. 3. C. 2. D. 5.
(Xem giải) Câu 30. Phân tích nguyên tố hợp chất hữu cơ E cho kết quả phần trăm khối lượng carbon, hydrogen và oxygen lần lượt là 54,55%; 9,09% và 36,36%. Dựa vào phương pháp phân tích phổ khối (MS) xác định được phân tử khối của E là 88. Mặt khác, phổ hồng ngoại (IR) cho thấy phân tử E không chứa nhóm có số sóng từ 3600 – 3300 cm-1 nhưng lại chứa nhóm có số sóng 1740 – 1670 cm-1. Thủy phân hoàn toàn E trong dung dịch NaOH, thu được muối của carboxylic acid X và chất Y. Chất Y có nhiệt độ sôi (64,7°C) nhỏ hơn nhiệt độ sôi của ethanol (78,3°C). Cho các phát biểu sau:
(a) Nhiệt độ sôi của E, X và Y được xếp theo chiều giảm dần: X > E > Y.
(b) Chất E có thể được điều chế trực tiếp từ phản ứng ester hóa giữa chất Y với propanoic acid.
(c) Trong công nghiệp, chất Y được trộn với xăng RON 92 để tạo ra xăng sinh học.
(d) Dung dịch muối tạo bởi giữa carboxylic acid X và NaOH có pH = 7.
Các phát biểu đúng là
A. a, b. B. a, c, d. C. b, c, d. D. b, c.
(Xem giải) Câu 31. Cho sơ đồ các phản ứng (theo đúng tỉ lệ mol):
(1) X + 2NaOH → X1 + X2 + X3
(2) X1 + HCl → X4 + NaCl
(3) X2 + HCl → X5 + NaCl
(4) X3 + CuO → X6 + Cu + H2O
Biết X có công thức phân tử C5H8O4 và chứa hai chức ester. Phân tử khối X3 = X4 < X5. Cho các phát biểu sau:
(a) Dung dịch X3 hòa toàn được Cu(OH)2.
(b) X5 là hợp chất hữu cơ tạp chức.
(c) Khi có enzyme xúc tác, glucose bị lên men có thể thu được X3.
(d) Các chất X4 và X6 có phản ứng tráng bạc.
(e) X6 có phản ứng màu iodoform.
(g) X3 dùng để điều chế ethylene trong phòng thí nghiệm.
Số phát biểu đúng là
A. 4. B. 2. C. 5. D. 3.
(Xem giải) Câu 32. Phân tích nguyên tố trong phân tử ester mạch hở X cho kết quả phần trăm khối lượng carbon, hydrogen, oxygen lần lượt là 40,678%; 5,085%; 54,237%. Phổ MS của X xuất hiện peak của ion phân tử [M]+ có giá trị m/z = 118. Hợp chất hữu cơ Y, Z có cùng công thức phân tử với X. Từ X, Y, Z thực hiện sơ đồ các phản ứng sau theo đúng tỉ lệ mol:
(1) X + 2NaOH → 2X1 + X2
(2) Y + 2NaOH → X3 + X4 + H2O
(3) Z + 2NaOH → X5 + X6 + H2O
(4) X2 + 2CuO → X7 + 2Cu + 2H2O
(5) X7 + 4AgNO3 + 6NH3 + 2H2O → X8 + 4NH4NO3 + 4Ag
(6) X8 + 2NaOH → X3 + 2NH3 + 2H2O
(7) X4 + O2 → X9 + H2O
(8) X9 + NaOH → X5 + H2O
Biết X1, X2, X3, X4, X5, X6, X7, X8, X9 là các hợp chất hữu cơ khác nhau. Cho các phát biểu sau:
(a) Thực hiện phản ứng ester hoá 0,1 mol X4 và 0,125 mol X9 với hiệu suất 80% thu được 7,04 gam ester.
(b) Nhiệt độ sôi của Y cao hơn nhiệt độ sôi của X.
(c) X7 làm mất màu nước bromine.
(d) Có hai công thức cấu tạo thỏa mãn tính chất của Y.
(e) X6 là hợp chất hữu cơ tạp chức.
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
PHẦN II. Câu trắc nghiệm đúng sai (4,0 điểm). Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 1. Khí sulfur dioxide tham gia trong quá trình sản xuất sulfuric acid, oxi hóa sulfur dioxide bằng oxygen hoặc lượng dư không khí ở nhiệt độ 450°C – 500°C, xúc tác V2O5 tạo ra sulfur trioxide theo phương trình hóa học: 2SO2(g) + O2(g) ⇋ 2SO3(g)
Cho biết nồng độ ban đầu của SO2 và O2 tương ứng là 4M và 2M, khi phản ứng đạt trạng thái cân bằng thì có 80% lượng SO2 đã phản ứng.
a) Nếu duy trì ở nhiệt độ dưới 450°C thì cân bằng vẫn chuyển dịch theo chiều thuận với tốc độ không đổi so với tốc độ phản ứng ở 450°C.
b) Hằng số cân bằng của phản ứng là 40.
c) Để có 90% SO2 đã phản ứng khi hệ đạt trạng thái cân bằng thì ban đầu cần lấy O2 là 3,825M hoặc 1,6M.
d) Nếu tăng áp suất của hệ phản ứng lên 2 lần trong điều kiện nhiệt độ không đổi thì tốc độ phản ứng thuận tăng lên 8 lần.
(Xem giải) Câu 2. Bộ phận quan trọng nhất của máy tạo nhịp tim là một hệ pin điện hóa lithium – iodine (gồm hai cặp oxi hóa khử Li+/Li và I2/2I-). Hai điện cực được đặt vào tim, phát sinh dòng điện nhỏ kích thích tim đập ổn định. Cho biết: E°Li+/Li = -3,04V; E°I2/2I- = +0,54V; Nguyên tử khối của Li = 6,9; điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s), 1 năm = 365 ngày.
a) Khi pin hoạt động lithium đóng vai trò là anode, tại anode xảy ra quá trình khử.
b) Máy tạo nhịp tim có thể được đặt tạm thời hay vĩnh viễn trong cơ thể tùy theo tình trạng sức khỏe và các bệnh lý kèm theo của bệnh nhân.
c) Sức điện động chuẩn của pin bằng -3,58V.
d) Nếu pin tạo ra một dòng điện ổn định bằng 2,5.10–5 (A) thì một pin được chế tạo bởi 0,5 gam lithium có thể hoạt động tối đa trong thời gian 8,8695 năm.
(Xem giải) Câu 3. β-carotene có rất nhiều trong rau quả xanh và vàng đặc biệt là ở quả gấc, cà rốt, … β-carotene được cơ thể chuyển hóa thành vitamin A rất cần thiết cho cơ thể. Công thức cấu tạo của β-carotene như sau:
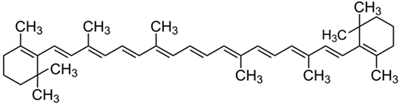
Thực hiện thí nghiệm tách β-carotene từ nước ép cà rốt như sau:
– Chuẩn bị: Nước ép cà rốt, hexane, cốc thuỷ tinh 100 mL, bình tam giác 100 mL, phễu chiết 60 mL, giá thí nghiệm.
– Tiến hành:
• Bước 1: Cho khoảng 20 mL nước ép cà rốt vào phễu chiết. Thêm tiếp khoảng 20 mL hexane, lắc đều khoảng 2 phút.
• Bước 2: Để yên phễu chiết trên giá thí nghiệm khoảng 5 phút để chất lỏng tách thành hai lớp.
• Bước 3: Mở khoá phễu chiết cho phần nước ở dưới chảy xuống, còn lại phần dung dịch là β-carotene hoà tan trong hexane.
a) Phân tử β-carotene có 9 nhóm methyl.
b) β-carotene tách ra khỏi nước dựa trên tính chất tan ít trong nước, tan nhiều trong dung môi hữu cơ.
c) Sau khi chiết lớp hexane trong phễu có màu vàng cam.
d) Phân tử carotene có công thức phân tử là C40H56 và có 13 liên kết π.
(Xem giải) Câu 4. Isopropyl myristate là một ester thường được sử dụng trong kem dưỡng da, dầu tẩy trang và sản phẩm chăm sóc tóc như một chất làm mềm, chất kết dính và chất tăng hương thơm vì khả năng thẩm thấu tốt mà không gây nhờn rít. Ester này được tạo ra từ phản ứng giữa acid béo bão hòa myristic và isopropyl alcohol. Công thức khung phân tử của isopropyl myristate như sau:
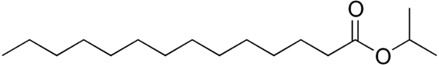
a) Độ nhớt thấp là do cấu trúc không phân nhánh của gốc acid béo bão hòa myristate mang lại cảm giác nhẹ, mượt và “không gây nhờn rít” khi thoa lên da.
b) Để điều chế 5,4 gam isopropyl myristate trong một sản phẩm mỹ phẩm cần 1,2 gam isopropyl alcohol (giả sử hiệu suất phản ứng là 80%).
c) Một lọ kem dưỡng da có thể tích thực là 100 mL cho biết thành phần có chứa 3% isopropyl myristate theo khối lượng. Giả sử khối lượng riêng của kem dưỡng da đã cho là 0,85 g/mL. Lượng ester cần dùng để sản xuất 500 lọ kem trên là 1,275 kg.
d) Isopropyl myristate (làm dung môi) và các thành phần chính trong mỹ phẩm (chất tan) đều là các chất phân cực cho nên isopropyl myristate dễ dàng hòa tan các loại sáp và dầu của chất trang điểm, giúp chúng bị rửa trôi khỏi da một cách hiệu quả.
PHẦN III. Câu trắc nghiệm trả lời ngắn (3,0 điểm). Thí sinh trả lời từ câu 1 đến câu 6.
(Xem giải) Câu 1. Tiến hành các thí nghiệm sau:
(a) Cho từ từ đến hết a mol HCl vào dung dịch chứa a mol Na2CO3.
(b) Hòa tan hết hỗn hợp Cu và Fe2O3 (tỉ lệ mol 1 : 1) vào dung dịch H2SO4 loãng dư.
(c) Cho NO2 vào dung dịch NaOH.
(d) Cho Fe3O4 vào dung dịch H2SO4 loãng, dư.
(e) Cho dung dịch NaOH dư vào dung dịch Ca(HCO3)2.
(g) Hấp thụ hoàn toàn x mol khí SO2 vào dung dịch chứa 1,2x mol NaOH.
(h) Cho hỗn hợp Cu và FeCl3 (tỉ lệ mol tương ứng là 1 : 2,5) vào H2O dư.
Sau khi kết thúc các phản ứng, có bao nhiêu thí nghiệm thu được dung dịch chứa hai muối?
(Xem giải) Câu 2. Nung nóng 20 gam một mẩu quặng malachite có thành phần chính là Cu(OH)2.CuCO3 (còn lại là tạp chất trơ) trong không khí. Hòa tan toàn bộ lượng CuO thu được bằng dung dịch H2SO4 20% vừa đủ, sau đó làm lạnh dung dịch đến 10°C thì có 24,6 gam tinh thể CuSO4.5H2O tách ra. Biết các phản ứng đều xảy ra hoàn toàn và độ tan của CuSO4 ở 10°C là 17,4 gam. Hàm lượng phần trăm của Cu(OH)2.CuCO3 có trong mẩu quặng bằng bao nhiêu? (làm tròn kết quả đến số hàng phần mười)
(Xem giải) Câu 3. Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn độ 3 lần thu được kết quả như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích dung dịch KMnO4 (mL) | 16 | 16,1 | 16 |
Cho các phát biểu sau:
(1) Theo kết quả chuẩn độ ở trên, trong số các giá trị: 93,32; 98,45; 97,36; 99,87, độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr có giá trị gần nhất với 99,87.
(2) Dung dịch H2SO4 được thêm vào dung dịch chuẩn độ để tạo môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn2+.
(3) Có thể thay dung dịch H2SO4 đã dùng bằng dung dịch acid mạnh như HCl, HNO3 nhưng phải đảm bảo lượng H+ dư sau phản ứng.
(4) Trong mỗi lần chuẩn độ, dung dịch KMnO4 được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch KMnO4 cuối cùng nhỏ vào dung dịch Y không bị mất màu sau 20 giây.
Liệt kê các phát biểu đúng theo thứ tự từ nhỏ đến lớn (1234,…)
(Xem giải) Câu 4. Tinh dầu chanh ngoài mùi thơm dễ chịu giúp thư dãn còn có thể diệt côn trùng (muỗi, rệp,…) và tương đối thân thiện với môi trường. Để thu tinh dầu từ lá chanh, có thể thực hiện theo các bước sau:
• Bước 1. Cắt nhỏ lá chanh.
• Bước 2. Cho hơi nước đi qua phần lá chanh đã cắt ở bước 1. Hơi nước chứa tinh dầu lá chanh sau đó được dẫn qua hệ thống sinh hàn làm lạnh và ngưng tụ lại thành dạng lỏng.
• Bước 3. Để yên cho hỗn hợp thu được ở bước 2 tách thành hai lớp dung dịch do tinh dầu không tan trong nước. Loại bỏ phần nước, thu lấy tinh dầu.
Trong quy trình này, người ta đã sử dụng bao nhiêu phương pháp trong những phương pháp sau đây để tách và tinh chế tinh dầu?
(1) Chưng cất. (2) Chiết. (3) Kết tinh. (4) Sắc kí.
(Xem giải) Câu 5. Khảo sát một số tính chất của 3 chất X, Y, Z được ghi lại trong bảng sau:
| Chất | Nhiệt độ nóng chảy (°C) | Quỳ tím |
| X | -6,3 | Không đổi màu |
| Y | 233 | Không đổi màu |
| Z | 247 | Màu hồng |
Biết X, Y, Z là một trong 3 chất: glycine, aniline, glutamic acid. Cho các phát biểu sau:
(1) Chất Y, Z là chất rắn ở nhiệt độ thường.
(2) Tên bán hệ thống của glutamic acid là α–amino pentane-1,5-dioic.
(3) X, Y, Z lần lượt là aniline, glycine, glutamic acid.
(4) Nếu hexapeptide T được tạo bởi Y và Z có phân tử khối là 504 thì số gốc Glu trong peptide là 2.
(5) Chất X để lâu trong không khí bị oxi hóa chuyển sang màu hồng.
(6) Nhỏ một ít nước vào dung dịch chứa chất X thì chất X ít tan và lắng xuống đáy ống nghiệm.
Liệt kê các phát biểu đúng theo thứ tự từ nhỏ đến lớn (1234,…)
(Xem giải) Câu 6. Một loại chất béo có chứa tristearin (C17H35COO)3C3H5, tripalmitin (C15H31COO)3C3H5, stearic acid, palmitic acid. Phần phần trăm khối lượng và hiệu suất phản ứng của các chất khi xà phòng hóa chất béo này bằng dung dịch NaOH như sau:
| Thành phần | Tristearin | Tripalmitin | Stearic acid | Palmitic acid | Tạp chất |
| Phần trăm khối lượng | 53,4% | 32,24% | 1,136% | 1,536% | 11,688% |
| Hiệu suất phản ứng với NaOH | 90% | 88% | 100% | 100% | 0% |
Một nhà máy cần sản xuất 15000 bánh xà phòng, khối lượng tịnh của mỗi bánh xà phòng là 90 gam (chứa 72% khối lượng muối sodium của các acid béo) bằng cách xà phòng hóa x kg chất béo nói trên với dung dịch NaOH. Biết trong quá trình đóng gói, lượng xà phòng bị hao hụt 4%. Giá trị của x là bao nhiêu? (làm tròn kết quả đến hàng đơn vị)
II. PHẦN TỰ LUẬN
Câu 1. (2,0 điểm).
(Xem giải) 1. Tinh thể muối ngậm nước FeSO4.xH2O được điều chế bằng cách cho muối iron(II) carbonate phản ứng với dung dịch sulfuric acid loãng theo quy trình sau: Thêm từng lượng nhỏ iron(II) carbonate đến dư vào dung dịch sulfuric acid loãng. Sau đó, lọc hỗn hợp phản ứng để thu lấy dung dịch. Đun nóng dung dịch đến khi thu được dung dịch bão hòa rồi để nguội. Lọc thu lấy tinh thể chất rắn và thấm khô bằng giấy lọc.
a) Cho biết dùng lượng dư iron(II) carbonate hay dùng dung dịch sulfuric acid? Giải thích.
b) Hãy chỉ ra dấu hiệu cho thấy lượng iron(II) carbonate đã dư.
c) Hãy cho biết hóa chất nào có thể thay thế iron(II) carbonate trong quy trình trên.
d) Biết Fe chiếm 20,14% khối lượng của FeSO4.xH2O. Hãy xác định x.
(Xem giải) 2. Ammonia được sản xuất trong công nghiệp dựa trên phản ứng sau đây: N2(g) + 3H2(g) ⇋ 2NH3(g)  = -92 kJ
= -92 kJ
a) Khi hỗn hợp phản ứng đang ờ trạng thái cân bằng, những thay đổi dưới đây sẽ làm cân bằng chuyển dịch theo chiểu nào? Giải thích.
– Tăng nhiệt độ.
– Tăng áp suất.
– Giảm nồng độ NH3.
– Thêm chất xúc tác.
b) Khi tăng nồng độ của khí hydrogen lên 3 lần thì tốc độ phản ứng thuận thay đổi như thế nào?
c) Hỗn hợp khí X gồm N2 và H2 có tỉ khối hơi so với He bằng 1,8. Đun nóng X một thời gian trong bình kin (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối hơi so với He bằng 2. Tính hiệu suất phản ứng tổng hợp NH3.
(Xem giải) 3. Đá vôi là loại đá trầm tích bao gồm các khoáng vật của calcium và các dạng kết tinh khác nhau của calcium carbonate. Để sản xuất 5,6 tấn vôi sống từ đá vôi cần bao nhiêu m³ khí CH4 và giải phóng bao nhiêu m³ khí CO2 vào khí quyển (thể tích các khí đo ở điều kiện chuẩn). Biết nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 1 mol CH4 là 890,5 kJ; có 80% lượng nhiệt đốt cháy được hấp thụ hiệu quả cho phản úng phân hủy CaCO3 theo phương trình nhiệt hóa học sau: CaCO3(s) → CaO(s) + CO2(g) ![]() = +179,2 kJ
= +179,2 kJ
Câu 2. (2,0 điểm).
(Xem giải) 1. Cho sơ đồ chuyển hóa sau: X → CH4 → Y → Z → T → Cao su Buna.
Cho biết: mỗi mũi tên là một phương trình hóa học, X là hợp chất chứa sodium, MX < 150 đvC. Xác định các chất X phù hợp và viết các phương trình hóa học theo sơ đồ trên.
(Xem giải) 2. Trong công nghiệp hương liệu, α-terpineol thường được tổng hợp nhân tạo từ limonene (có nhiều trong tinh dầu cam/chanh) bằng phản ứng hydrate hóa có xúc tác acid H2SO4 loãng.
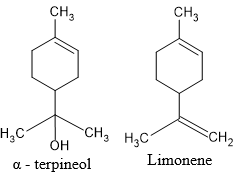
a) Dựa vào quy tắc Markovnikov và cấu tạo của limonene, hãy giải thích tại sao phản ứng này ưu tiên tạo ra α-terpineol (chỉ cộng nước vào nối đôi ở nhánh, nối đôi trong vòng không phản ứng).
b) Cho α-terpineol phản ứng với dung dịch KMnO4 loãng, lạnh. Nêu hiện tượng, viết phương trình phản ứng. Cho biết ý nghĩa của phản ứng này.
(Xem giải) 3. Dung dịch sát khuẩn (thành phần chính là ethanol) là một trong những cách để phòng dịch Covid-19. Ngoài ra, ethanol được pha vào xăng làm nhiên liệu cho động cơ đốt trong. Xăng E5 (xăng sinh học) bán ngoài thị trường là xăng có 5% ethanol theo thể tích. Một nhà máy sản xuất ethanol để pha dung dịch sát khuẩn dùng nguyên liệu là hạt ngô khô để lên men rượu theo sơ đồ sau (hiệu suất phản ứng lần lượt là 55% và 65%): (C6H10O5)n → C6H12O6 → C2H5OH.
Cho biết trong hạt ngô khô có 64,8% khối lượng tinh bột, ethanol có khối lượng riêng là 0,8 g/mL.
a) Viết phương trình hóa học của quá trình chuyển hóa trên.
b) Tính thể tích ethanol 96° điều chế được từ 6 tấn hạt ngô khô trên.
c) Giả thiết 20% lượng ethanol 96° thu được từ 6 tấn hạt ngô khô này được dùng để pha chế dung dịch sát khuẩn. Tính thể tích dung dịch sát khuẩn được tạo ra, biết rằng trong 10 lít dung dịch sát khuẩn sử dụng trong phòng dịch Covid-19, có thành phần như bảng sau:
| Dung dịch ethanol 96o | 8333 mL |
| Dung dịch hydrogen peoxide 3% | 417 mL |
| Dung dịch glycerol 98% | 145 mL |
| Nước cất đã đun sôi, để nguội | Phần còn lại |
Câu 3. (1,0 điểm).
(Xem giải) 1. Tiến hành thí nghiệm điều chế và thử tính chất của hydrocarbon X như hình vẽ và các bước sau đây:
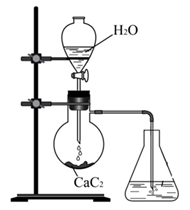
• Bước 1: Mở khoá phễu cho H2O chảy từ từ xuống bình cầu đựng CaC2.
• Bước 2: Dẫn X vào bình 1 đựng dung dịch Br2.
• Bước 3: Dẫn X vào bình 2 đựng dung dịch AgNO3 trong NH3.
• Bước 4: Dẫn X vào bình 3 đựng dung dịch KMnO4.
a) Nêu hiện tượng, viết các phương trình phản ứng hoã học đã xảy ra ở bước 1, 2, 3 và 4.
b) Khí X sinh ra thường lẫn một số khí có mùi khó chịu. Trình bày cách loại bỏ khí này bằng phương pháp hóa học. Viết phương trình phản ứng.
(Xem giải) 2. Do có kết quả học tập tốt, Lan được bố cho đi tham quan Hà Giang, khi về hai bố con mua một can to mật ong bạc hà Mèo Vạc nổi tiếng của tỉnh này để làm quà cho người thân. Lan rất vui giúp bố chia mật ong ra các chai. Bố dặn Lan “Con phải nhớ đổ đầy mật ong vào các chai sạch, khô, đậy nút thật chặt và để ở nơi khô ráo, như vậy mật ong mới không bị biến chất”.
a) Lan không hiểu tại sao bố lại nói như vậy. Em hãy giải thích giúp bạn Lan.
b) Lan muốn bảo quản mật ong được lâu nên đã cho chai mật ong vào tủ lạnh. Sau một thời gian thấy có cặn ở đáy chai. Hãy giải thích hiện tượng trên.


Bình luận