[2025] Thi thử TN chuyên ĐH Vinh – Nghệ An (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 153
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2D | 3C | 4C | 5D | 6B | 7A | 8A | 9A |
| 10D | 11A | 12B | 13A | 14B | 15A | 16B | 17B | 18A |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | S | Đ | S | 4 | 28,6 | 1,7 |
| (b) | S | Đ | Đ | S | 26 | 27 | 28 |
| (c) | Đ | S | S | Đ | 76,5 | 12 | 4123 |
| (d) | S | Đ | S | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Số nhóm –NH2 trong phân tử Gly-Ala-Lys-Gly-Ala là
A. 2. B. 6. C. 3. D. 5.
(Xem giải) Câu 2. Hợp chất hữu cơ X mạch hở có công thức phân tử là C3H6O. X có phản ứng iodoform. Phát biểu nào sau đây đúng?
A. X là hợp chất không no. B. X có 2 đồng phân cấu tạo thỏa mãn.
C. X có phản ứng với thuốc thử Tollens. D. X thuộc loại hợp chất carbonyl.
(Xem giải) Câu 3. Chất nào sau đây được sử dụng làm xà phòng?
A. CH3COOK. B. CH3[CH2]11OSO3Na.
C. C17H35COONa. D. CH3[CH2]11C6H4SO3Na.
(Xem giải) Câu 4. Khi cho phức chất [Zn(H2O)6]2+ tác dụng với dung dịch NH3 đặc, thu được phức chất bát diện M. Trong phức chất M, số phối tử NH3 chiếm 2/3 tổng số phối tử. Có bao nhiêu phối tử H2O đã được thay thế bởi phối tử NH3?
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 5. X là một carboxylic acid đơn chức. Y là triester mạch hở tạo bởi X và glycerol. Trong phân tử Y có số nguyên tử carbon gấp 1,5 lần số nguyên tử oxygen. Thủy phân hoàn toàn m gam Y cần dùng vừa đủ 300 mL dung dịch KOH 1 M. Giá trị của m là
A. 32,7. B. 17,6. C. 65,4. D. 21,8.
(Xem giải) Câu 6. Nguồn điện nào sau đây không dựa vào năng lượng từ các phản ứng hoá học?
A. Pin Galvani. B. Pin mặt trời. C. Pin nhiên liệu. D. Acquy.
(Xem giải) Câu 7. Phân tử polymer nào sau đây chứa ba nguyên tố hóa học?
A. Poly(vinyl chloride). B. Polybuta-1,3-diene.
C. Popypropylene. D. Polystyrene.
(Xem giải) Câu 8. Phản ứng của 2-methylpropene với hydrogen bromide diễn ra theo cơ chế như sau:
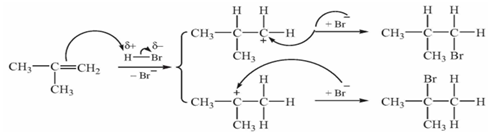
Các sản phẩm trung gian là các ion có nguyên tử carbon mang điện tích dương, được gọi là carbocation. Độ bền tương đối của carbocation tăng khi bậc của nguyên tử carbon mang điện tích dương tăng. Phát biểu nào sau đây sai?
A. Hàm lượng phần trăm sản phẩm: 1-bromo-2-methylpropane > 2-bromo-2-methylpropane.
B. Carbocation (CH3)2CHCH2⁺ có độ bền kém hơn carbocation (CH3)3C⁺.
C. Phản ứng trên là phản ứng cộng AE diễn ra qua hai giai đoạn.
D. Liên kết π trong 2-methylpropene bị phá vỡ theo kiểu phân cắt dị li trong giai đoạn đầu tiên.
(Xem giải) Câu 9. Ở môi trường pH = x, khi đặt trong một điện trường, glycine di chuyển về cực dương. Giá trị của x có thể là
A. 13. B. 6. C. 3. D. 1.
(Xem giải) Câu 10. Catechin là một chất chống oxi hóa mạnh, được tìm thấy rất nhiều trong lá chè xanh. Đây là dưỡng chất rất an toàn cho cơ thể và mang đến nhiều tác dụng tuyệt vời đối với sức khỏe con người như ức chế hoạt động của các gốc tự do nên có khả năng phòng chống bệnh ung thư, nhồi máu cơ tim. Ngoài ra, catechin còn có trong táo, lê, nho,… Công thức cấu tạo của catechin cho như hình sau:
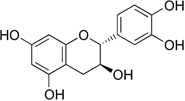
Phát biểu nào sau đây sai?
A. Công thức phân tử của catechin là C15H14O6.
B. Catechin thuộc loại hợp chất thơm và tạp chức.
C. Cho 1 mol catechin tác dụng tối đa với 5 mol Na.
D. Catechin không tác dụng với CH3COOH (xúc tác H2SO4 đặc, đun nóng).
(Xem giải) Câu 11. Cho các cân bằng hóa học:
(1) H2(g) + I2(g) ⇋ 2HI(g)
(2) Fe2O3(s) + 3CO(g) ⇋ 2Fe(s) + 3CO2(g)
(3) 2NO2(g) ⇋ N2O4(g)
Yếu tố áp suất làm cân bằng nào chuyển dịch (giữ nguyên các yếu tố khác)?
A. (3). B. (2). C. (2); (3). D. (1).
(Xem giải) Câu 12. Phát biểu nào sau đây sai?
A. Saccharose và cellulose đều có chứa liên kết glycoside.
B. Tinh bột và cellulose đều là polymer mạch không nhánh.
C. Saccharose và maltose đều thuộc loại disaccharide.
D. Glucose và fructose đều tác dụng với Cu(OH)2 trong dung dịch.
(Xem giải) Câu 13. Cho câu ca dao sau:
“Lúa chiêm lấp ló đầu bờ
Hễ nghe tiếng sấm phất cờ mà lên”
Theo câu ca dao trên, lúa chiêm đã được cung cấp loại phân bón nào sau đây?
A. Phân đạm. B. Phân hữu cơ. C. Phân lân. D. Phân kali.
(Xem giải) Câu 14. Nước có tính cứng tạm thời (chỉ chứa các ion Ca2+, Mg2+, HCO3-) không tác dụng với chất nào sau đây trong dung dịch?
A. HCl. B. BaCl2. C. NaOH. D. Na2CO3.
(Xem giải) Câu 15. Một học sinh tiến hành thí nghiệm sau:
• Bước 1: Lấy 10 mL dung dịch Fe(NO3)3 0,1 M cho vào cốc (1) và 10 mL dung dịch AgNO3 0,1 M cho vào cốc (2).
• Bước 2: Cho vào cốc (1) một lá Fe dư và cốc (2) một lá Cu dư.
Biết kim loại mới sinh ra bám vào lá kim loại cũ. Sau khi các phản ứng xảy ra hoàn toàn, học sinh đưa ra một số phát biểu.
Phát biểu nào sau đây đúng?
A. Ở cốc (1) chỉ xảy ra ăn mòn hóa học, ở cốc (2) xảy ra cả ăn mòn hóa học và ăn mòn điện hóa.
B. Khối lượng lá Fe ở cốc (1) tăng lên, khối lượng lá Cu ở cốc (2) giảm xuống.
C. Sau phản ứng, nồng độ mol/L của chất tan trong hai dung dịch ở hai cốc bằng nhau.
D. Dung dịch ở cốc (1) mất màu vàng nhạt, dung dịch ở cốc (2) từ màu xanh chuyển thành không màu.
(Xem giải) Câu 16. Benzyl benzoate được sử dụng rộng rãi dưới dạng bôi ngoài da trong điều trị bệnh ghẻ. Số nguyên tử carbon trong phân tử benzyl benzoate là
A. 12. B. 14. C. 13. D. 10.
(Xem giải) Câu 17. Ứng với công thức phân tử C4H11N có bao nhiêu đồng phân amine mà khi phản ứng với HNO2 ở điều kiện thường giải phóng khí nitrogen?
A. 2. B. 4. C. 5. D. 3.
(Xem giải) Câu 18. Một pin điện hoá Ni – H2 được thiết lập ở điều kiện chuẩn (vôn kế có điện trở rất lớn) như hình sau:
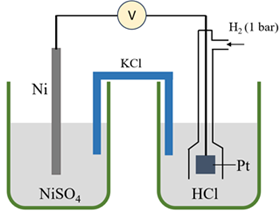
Biết thế điện cực chuẩn của cặp oxi hóa – khử Ni2+/Ni bằng -0,257 V.
Cho các nhận định sau khi pin hoạt động:
(a) Dung dịch NiSO4 và HCl đều có nồng độ ban đầu bằng 1 M.
(b) Ở anode xảy ra quá trình oxi hoá Ni, ở cathode xảy ra quá trình khử cation H+.
(c) Từ cầu muối, ion K+ đi vào dung dịch NiSO4, ion Cl- đi vào dung dịch HCl.
(d) Khối lượng điện cực Ni giảm dần, khối lượng điện cực Pt không đổi.
(e) Giá trị hiện thị trên vôn kế là 0,257 V.
Trong các nhận định trên, có bao nhiêu nhận định đúng?
A. 4. B. 3. C. 5. D. 6.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Điện phân có nhiều ứng dụng trong sản xuất và đời sống thực tiễn như luyện kim, tinh chế kim loại, mạ điện,…
a) Sau quá trình điều chế copper bằng phương pháp điện phân dung dịch CuSO4 với điện cực than chì thì pH của dung dịch sẽ giảm.
b) Trong quá trình điện phân dung dịch, khối lượng dung dịch thu được sau điện phân luôn giảm.
c) Người ta cần mạ đồng lên 100 chiếc chìa khóa giống nhau (mỗi chiếc có tổng diện tích cần mạ là 30 cm² và độ dày trung bình lớp mạ là 0,006 cm) bằng cách điện phân dung dịch CuSO4 với anode làm bằng thanh đồng nguyên chất, cathode là các chìa khóa cần mạ. Nếu quá trình điện phân được cung cấp nguồn điện một chiều có hiệu điện thế không đổi 110 V thì điện năng mà bình điện phân tiêu thụ là 14,861 kWh.
Biết: khối lượng riêng của Cu là 8,96 g/cm³, hiệu suất điện phân là 100%, 1 kWh = 3,6.10^6 J.
Điện lượng : q = It = ne.F.
Điện năng tiêu thụ: A = UIt (J).
Trong đó: q là điện lượng (C), I là cường độ dòng điện (A); ne là số mol electron trao đổi (mol), t là thời gian điện phân (s); F = 96500 C/mol; A là điện năng tiêu thụ (J hay Ws), U là hiệu điện thế (V).
d) Do tính oxi hoá của H2O yếu hơn ion Na+ nên khi điện phân dung dịch NaCl (điện cực trơ) ở cathode (cực âm) xảy ra quá trình khử: 2H2O + 2e → H2 + 2OH-.
(Xem giải) Câu 20. Công thức cấu tạo thu gọn của một loại triglyceride (X) được biểu diễn như sau:
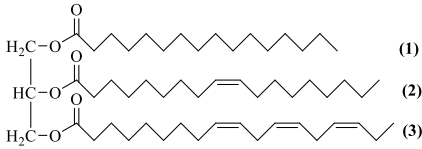
a) Để chuyển 6,405 tấn X thành chất béo no (bơ nhân tạo) thì thể tích H2 (đkc) cần dùng là 929,625 m³. Biết lượng H2 cần dùng dư 20% so với lượng cần phản ứng.
b) Khi thủy phân hoàn toàn X trong môi trường acid, đun nóng thu được sản phẩm có chứa các acid béo omega-3 và omega-9.
c) X có nhiệt độ nóng chảy cao hơn tristearin vì trong phân tử có chứa hai gốc acid béo không no.
d) Khi để lâu trong không khí, X bị oxi hoá chậm bởi oxygen tạo thành hợp chất có mùi khó chịu.
(Xem giải) Câu 21. Polymer A thuộc loại poly(ester amide) được sử dụng trong dược phẩm để giải phóng thuốc có kiểm soát. Sau khi uống, các enzyme của cơ thể nhận biết các gốc amino acid tự nhiên trong mạch polymer và phân cắt tại các vị trí này làm thuốc được giải phóng một cách từ từ. Polymer A chỉ được tổng hợp từ bốn monomer gồm X, Y (MX < MY) là hai hợp chất đa chức, Z là amino acid và T là dẫn xuất của amino acid. Công thức một mắt xích của polymer A như hình sau:

a) Chất T là dẫn xuất của Lys.
b) Tổng phân tử khối của T và X là 298.
c) Thủy phân hoàn toàn polymer A trong dung dịch NaOH dư thu được 5 sản phẩm hữu cơ trong đó có 2 muối.
d) Trong một mắt xích của polymer A có chứa hai liên kết ester.
(Xem giải) Câu 22. Thuốc eloxatin có thành phần chính là phức chất oxaliplatin thuộc nhóm chống ung thư, sử dụng trong điều trị ung thư đại tràng, trực tràng giai đoạn ba hoặc di căn. Cho biết cấu tạo của phức chất oxaliplatin như hình sau:

a) Trong phân tử phức chất oxaliplatin, nguyên tử nitrogen trên nhóm amine còn một cặp electron chưa tham gia liên kết.
b) Trong phân tử phức chất oxaliplatin có chứa phối tử oxalic acid.
c) Nguyên tử trung tâm của phức chất oxaliplatin là ion Pt2+.
d) Trong phân tử phức chất oxaliplatin, mỗi phối tử tạo hai liên kết cho – nhận với nguyên tử trung tâm.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho dung dịch các chất sau: NaHCO3; CuSO4; (NH4)2CO3; NaNO3; MgCl2; KCl. Khi cho Ba vào dung dịch các chất trên thì có bao nhiêu dung dịch xuất hiện kết tủa?
(Xem giải) Câu 24. Trong phòng thí nghiệm, soda (Na2CO3) khi để lâu ngày bị hút ẩm và chuyển hóa tạo thành hỗn hợp X gồm Na2CO3, NaHCO3 và H2O. Hòa tan hoàn toàn một lượng X trong nước thu được 100 mL dung dịch Y. Tiến hành các thí nghiệm sau:
• Thí nghiệm 1: Cho 76 mL dung dịch HCl 1 M vào 10 mL dung dịch Y, thu được dung dịch Z. Trung hoà Z bằng dung dịch NaOH 1 M thấy hết 20 mL dung dịch NaOH.
• Thí nghiệm 2: Cho 10 mL dung dịch NaOH 1 M vào 10 mL dung dịch Y, sau đó thêm tiếp dung dịch BaCl2 dư vào, thu được 5,91 gam kết tủa và dung dịch T. Nếu đun nóng dung dịch T thì thấy xuất hiện thêm kết tủa.
Phần trăm Na2CO3 đã bị chuyển hóa thành NaHCO3 là a%. Tính giá trị của a. (làm tròn đến hàng phần mười). Biết các phản ứng đều xảy ra hoàn toàn, khí sinh ra không tan trong nước.
(Xem giải) Câu 25. Trong công nghiệp, người ta điều chế Al bằng phương pháp điện phân Al2O3 nóng chảy với điện cực bằng than chì. Để sản suất 5,4 tấn Al thì khối lượng anode bị tiêu hao m tấn. Biết rằng hỗn hợp khí thu được ở anode chứa 10% O2; 10% CO và 80% CO2 về thể tích; hiệu suất của quá trình điện phân là 100%. Tính giá trị của m. (làm tròn đến hàng phần mười).
(Xem giải) Câu 26. Trong công nghiệp, lượng lớn soda được sản xuất theo phương pháp Solvay theo sơ đồ sau:
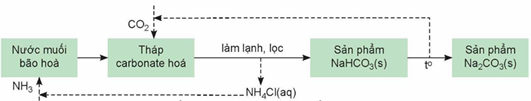
Muối NaHCO3 được tạo thành từ “tháp carbonate hóa” được làm lạnh, lọc rồi đem phân hủy một phần tạo thành soda theo phương trình hóa học (1) như sau:
(1) 2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l)
Phản ứng (1) là phản ứng thu nhiệt. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí methane theo phương trình hóa học (2):
(2) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Xét các phản ứng ở điều kiện chuẩn, chỉ có 60% nhiệt lượng tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1). Tính khối lượng khí methane (theo kg, làm tròn đến hàng phần mười) cần tiêu thụ (đốt cháy hoàn toàn) để sản xuất được 3 tấn soda (có độ tinh khiết 98,56% về khối lượng).
Biết giá trị nhiệt tạo thành chuẩn của các chất được cho trong bảng sau:
| Chất | H2O(l) | CO2(g) | NaHCO3(s) | Na2CO3(s) | CH4(g) |
| -285,8 | -393,5 | -950,8 | -1130,7 | -74,6 |
(Xem giải) Câu 27. Hợp chất E mạch hở, có công thức phân tử là C4H6O5 được tạo thành carboxylic acid và alcohol. Khi cho E tác dụng với Na hoặc NaHCO3 đều thu được số mol khí bằng số mol E đã phản ứng. Từ E thực hiện các sơ đồ sau (theo đúng tỉ lệ mol):
(1) E + 2NaOH (t°) → X + Y + H2O
(2) X + H2SO4 → Z + Na2SO4
(3) 3Z + 2Y (H2SO4 đặc, t°) ⇋ T + 4H2O
Số nguyên tử oxygen trong phân tử T (mạch hở) là bao nhiêu?
(Xem giải) Câu 28. Cho các chất được kí hiệu tương ứng như sau:
(1) HOOC-CH2-CH2-CH(NH2)-COOH (2) HOOC-CH2-CH2-CH(NH2)-COONa
(3) NaOOC-CH2-CH2-CH(NH2)-COONa (4) HOOC-CH2-CH2-CH(NH3Cl)-COOH
Sắp xếp dung dịch các chất trên (cùng nồng độ) theo thứ tự pH tăng dần?


Bình luận