[2025] Thi thử TN sở GDĐT Vĩnh Phúc (Lần 3 – Đề 4)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 101
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2D | 3D | 4C | 5D | 6C | 7C | 8D | 9C |
| 10B | 11D | 12D | 13A | 14C | 15D | 16D | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | Đ | Đ | 5 | 0,98 | 600 |
| (b) | S | S | Đ | S | 26 | 27 | 28 |
| (c) | S | Đ | S | Đ | 2 | 6 | 256 |
| (d) | Đ | Đ | S | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. PE là một polymer thông dụng, dùng làm chất dẻo (chất dẻo chứa PE chiếm gần 1/3 tổng lượng chất dẻo được sản xuất hàng năm). Trong đời sống, PE được dùng làm màng bọc thực phẩm, túi nylon, bao gói, chai lọ đựng hoá mĩ phẩm,… PE được điều chế từ monomer có tên gọi là
A. propylene. B. vinyl chloride. C. styrene. D. ethylene.
(Xem giải) Câu 2. Chất X có công thức H2NCH2COOH. Tên gọi của X là
A. valine. B. alanine. C. lysine. D. glycine.
(Xem giải) Câu 3. Điện phân 500 mL dung dịch CuSO4 0,2 M (điện cực trơ) cho đến khi ở cathode thu được 3,2 gam kim loại thì thu được V (L) khí (đkc) ở anode. Giá trị của V là
A. 1,24. B. 3,72. C. 2,48. D. 0,62.
(Xem giải) Câu 4. Hợp chất của nguyên tố nhóm IIA nào sau đây thường được sử dụng để khử chua đất và loại bỏ sulfur dioxide khỏi khí thải?
A. Sr. B. Be. C. Ca. D. Mg.
(Xem giải) Câu 5. Cho các phát biểu sau:
(a) Phân đạm ammonium chỉ phù hợp với đất chua.
(b) Khi bón quá nhiều phân bón NH4NO3 cây trồng không hấp thụ hết làm cho đất bị kiềm hoá.
(c) Người ta dùng phân bón kali để tăng cường sức chống rét, chống bệnh và chịu hạn cho cây.
(d) Urea là một hợp chất vô cơ có công thức (NH2)2CO.
(e) Nguyên liệu để sản xuất phân lân là quặng phosphorite hoặc apatite.
Số phát biểu không đúng là
A. 2. B. 5. C. 4. D. 3.
(Xem giải) Câu 6. Ăn mòn kim loại là hiện tượng phổ biến trong đời sống hàng ngày. Phương pháp nào sau đây có thể góp phần hạn chế sự ăn mòn kim loại?
A. Cuốn sợi dây đồng vào thanh sắt hoặc thanh nhôm.
B. Sử dụng giấy ráp đánh sạch bề mặt kim loại sau mỗi khoảng thời gian nhất định.
C. Phủ một lớp sơn hoặc lớp dầu mỡ lên bề mặt của vật dụng kim loại.
D. Dùng nước muối ăn để diệt các vi khuẩn bám trên bề mặt của các vật dụng kim loại.
(Xem giải) Câu 7. Thêm chromium vào thép thì tính chất nào sau đây được tăng cường?
A. Tính dễ kéo sợi. B. Tính chất từ. C. Chống ăn mòn. D. Tính dẫn điện.
(Xem giải) Câu 8. Nguyên tắc làm mềm nước là làm giảm nồng độ của ion
A. Cl-, SO42-. B. Ba2+. C. HCO3-. D. Ca2+, Mg2+.
(Xem giải) Câu 9. So sánh với nguyên tử phi kim cùng chu kì, nguyên tử kim loại
A. thường có số electron ở lớp ngoài cùng nhiều hơn.
B. thường có độ âm điện lớn hơn.
C. thường có bán kính của nguyên tử lớn hơn.
D. thường dễ nhận electron trong phản ứng hóa học.
(Xem giải) Câu 10. Cho các cặp oxi hoá-khử của các kim loại và thế điện cực chuẩn tương ứng:
| Cặp oxi hoá-khử | Li+/Li | Mg2+/Mg | Zn2+/Zn | Ag+/Ag |
| Thế điện cực chuẩn,V | -3,040 | -2,356 | -0,762 | +0,799 |
Trong số các kim loại trên, kim loại có tính khử mạnh nhất là
A. Mg. B. Li. C. Zn. D. Ag.
(Xem giải) Câu 11. Phản ứng chlorine hóa methane khi chiếu sáng xảy ra theo cơ chế gốc gồm ba giai đoạn: khơi mào, phát triển mạch và tắt mạch. Trong đó, giai đoạn phát triển mạch diễn ra như sau:
Cl• + CH4 → CH3• + HCl
CH3• + Cl2 → CH3Cl + Cl•
Nhận định nào sau đây không đúng về giai đoạn này?
A. Có sự phân cắt liên kết C–H. B. Có sự hình thành liên kết H–Cl.
C. Có sự hình thành liên kết C–Cl. D. Có sự hình thành liên kết π.
(Xem giải) Câu 12. Phát biểu nào sau đây sai?
A. Protein bị thủy phân nhờ xúc tác acid, base hoặc enzyme.
B. Protein là cơ sở tạo nên sự sống.
C. Dung dịch protein có phản ứng màu biuret.
D. Protein đơn giản là những chất có tối đa 10 liên kết peptide.
(Xem giải) Câu 13. Sulfur dioxide và các oxide của nitrogen trong khí quyển hòa tan trong nước tạo thành mưa acid. Phát biểu nào sau đây đúng?
A. Thu hồi sulfur từ các khí thải như H2S, SO2….có thể làm giảm sự hình thành mưa acid.
B. Thành phần chính của mưa acid là H2SO3 và HNO3.
C. Nước mưa có pH > 5,6 được xem là mưa acid.
D. Công thức hóa học của NOx trong khí thải ô tô luôn là NO2.
(Xem giải) Câu 14. Chất nào sau đây không phải là ester?
A. CH3COO[CH2]7CH3. B. CH3COOCH2C6H5.
C. CH3COOH. D. CH3[CH2]14COO[CH2]29CH3.
(Xem giải) Câu 15. Ethylamine (C2H5NH2) tác dụng được với chất nào sau đây tạo thành alcohol?
A. CuSO4. B. HCl. C. FeCl3. D. HNO2.
(Xem giải) Câu 16. Thủy phân ester nào sau đây trong dung dịch NaOH thu được sodium formate?
A. CH3COOC2H5. B. CH3COOC3H7. C. CH3COOCH3. D. HCOOC2H5.
(Xem giải) Câu 17. Nước ép chanh chứa khoảng 5% citric acid (X) nên chanh có vị chua và độ pH khoảng 2 – 3. Công thức X được cho như sau:
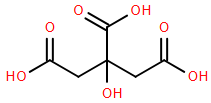
Khi cho 1 mol X tác dụng với kim loại Na dư thu được a mol H2. Giá trị của a là
A. 3. B. 4. C. 2. D. 1.
(Xem giải) Câu 18. Carbohydrate X là một polysaccharide được tạo thành từ các gốc β-glucose. Carbohydrate X là
A. saccharose. B. tinh bột. C. cellulose. D. glucose.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Heme là phức chất của pophirin với sắt có công thức như sau:
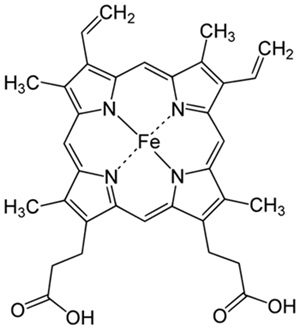
Hemoglobin là chất hồng cầu có trong máu người và hầu hết động vật. Nó có mạch protein liên kết với nguyên tử trung tâm của 4 nhóm heme qua nguyên tử N của phân tử histidine. Trong quá trình hô hấp của người, hemoglobin (Hb) theo máu đi đến phổi, kết hợp với oxygen tạo thành oxygen hemoglobin (HbO2) theo cân bằng sau (được đơn giản hóa rất nhiều):
Hb (màu đỏ thẫm) + O2 ⇋ HbO2 (màu đỏ tươi)
Nhóm heme trong Hb kết hợp với phân tử O2 nhờ cặp electron tự do ở một trong hai nguyên tử O của phân tử tạo liên kết cho nhận với orbital trống của nguyên tử trung tâm.
a) Máu người trước khi đi đến phổi có màu đỏ tươi.
b) Trong heme, nguyên tử trung tâm là Fe3+.
c) Phản ứng của Hb với O2 là phản ứng oxi hóa khử.
d) Liên kết giữa nguyên tử N trong phân tử histidine với heme là liên kết cho nhận.
(Xem giải) Câu 20. Enzyme amylase là một protein có khả năng xúc tác cho phản ứng thủy phân tinh bột. Hoạt tính xúc tác của enzyme càng cao thì phản ứng thủy phân tinh bột diễn ra càng nhanh. Hoạt tính xúc tác của enzyme phụ thuộc vào các yếu tố như nhiệt độ, pH … Một nhóm học sinh đưa ra giả thuyết “nhiệt độ càng tăng thì tốc độ phản ứng thủy phân tinh bột nhờ xúc tác của enzyme amylase xảy ra càng nhanh”. Từ đó, học sinh tiến hành thí nghiệm ở pH không đổi (pH = 7) tại các nhiệt độ 20°C; 30°C; 40°C; 50°C; 60°C; 70°C để kiểm tra dự đoán trên như sau:
• Bước 1: Thêm 2 mL dung dịch enzyme amylase vào ống nghiệm chứa dung dịch có vai trò duy trì pH = 7 ở 20°C.
• Bước 2: Thêm tiếp 2 mL dung dịch tinh bột vào ống nghiệm trên, lắc đều.
• Bước 3: Sau khoảng mỗi 10 giây, dùng ống hút lấy 1 – 2 giọt hỗn hợp phản ứng trong ống nghiệm và cho vào đĩa sứ chứa sẵn dung dịch iodine (màu vàng), quan sát để từ đó xác định thời gian tinh bột thủy phân hết.
Lặp lại thí nghiệm theo ba bước trên, chỉ thay đổi nhiệt độ trong bước 1 lần lượt là 30°C; 40°C; 50°C; 60°C; 70°C. Kết quả thí nghiệm được biểu diễn theo đồ thị sau:
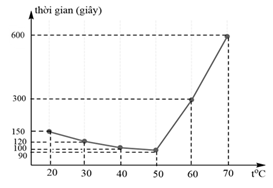
a) Ở bước 3, dung dịch iodine chuyển sang màu xanh tím nghĩa là tinh bột chưa thủy phân hết.
b) Ở nhiệt độ bằng nhiệt độ cơ thể (37°C), tốc độ phản ứng thủy phân tinh bột nhờ xúc tác enzyme amylase trên xảy ra nhanh nhất.
c) Theo số liệu phản ứng, phản ứng thủy phân tinh bột ở 50°C diễn ra nhanh hơn ở 40°C.
d) Kết quả thí nghiệm chứng minh giả thuyết nghiên cứu ở trên của nhóm học sinh trong khoảng từ 20°C đến 70°C là sai.
(Xem giải) Câu 21. Soda (Na2CO3) là một trong những chất có nhiều ứng dụng quan trọng. Để “tối ưu hóa” quy trình sản xuất soda (quy trình Solvay), nhà hóa học Hou Debang đã sử dụng sodium chloride làm nguyên liệu thô và thực hiện theo sơ đồ được mô tả ngắn gọn dưới đây.
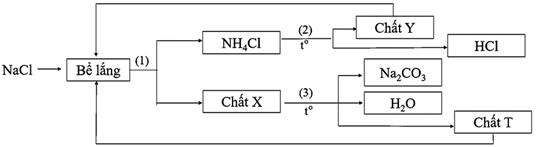
a) Trong sơ đồ trên hai chất được tái sử dụng là T và Y.
b) Phương trình phản ứng ở (1) là NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl.
c) Các chất X, Y, T lần lượt là NaHCO3, CO2, NH3.
d) Từ 17,55 kg NaCl điều chế theo phương pháp solvay thu được 25,20 kg NaHCO3 (hiệu suất toàn bộ quá trình là 90%).
(Xem giải) Câu 22. Nhựa ABS được làm từ polymer có tên đầy đủ là poly(acrylonitrile butadiene styrene), nhựa ABS có đặc tính cứng, rắn nhưng không giòn, cách điện, không thấm nước, bền với nhiệt độ và hóa chất. Nhựa này được sử dụng khá rộng rãi để làm vật liệu xây dựng, đồ chơi trẻ em, đồ gia dụng, mũ bảo hiểm,… Công thức cấu tạo của ABS được trình bày dưới đây:
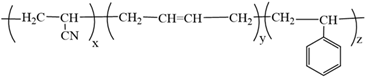
a) Các monomer tạo nên polymer là CH2=CH-CN, CH2=CH-CH=CH2, CH2=CH-C6H5.
b) Một mẻ thành phẩm ABS có tỉ lệ khối lượng acrylonitrile (15,41%), butadiene (39,24%) còn lại là styrene thì tỉ lệ giữa các mắt xích x : y : z là 1 : 5 : 3.
c) ABS là vật liệu polymer có tính dẻo.
d) Nhựa ABS dễ phân hủy sinh học, có thể xử lý bằng cách chôn lấp.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Trong một đề tài khôi phục nước trên sao hỏa của NASA. Tiến hành sấy các mẫu iron(II) sulfate heptahydrate (FeSO4.7H2O) với độ tinh khiết 99,99% với các khoảng nhiệt độ tăng dần và xử lý số liệu thu được đồ thị như sau:

Tính tổng giá trị x + y + z (Kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 24. Trong công nghiệp, PVC dùng làm chất dẻo được sản xuất từ ethylene với hiệu suất giả định cho từng bước theo sơ đồ sau:
![]()
Cần bao nhiêu tấn ethylene để sản xuất 1 tấn PVC theo sơ đồ và hiệu suất trên? (Kết quả làm tròn đến hàng phần trăm)
(Xem giải) Câu 25. Calcium là nguyên tố cần thiết đối với cơ thể con người, là thành phần chủ yếu cấu tạo nên xương và răng, không thể thiếu trong quá trình đông máu. Theo khuyến cáo của Viện Dinh dưỡng Quốc gia Việt Nam, mỗi ngày người lớn cũng như trẻ em cần khoảng 500 mg calcium dưới dạng ion Ca2+. Hãy tính số mg calcium được đưa vào cơ thể khi một người uống 300 gam sữa bò, biết nồng độ ion calcium trong sữa bò là 0,2%.
(Xem giải) Câu 26. Để xác định độ tinh khiết của mẫu muối Mohr (NH4)2Fe(SO4)2.6H2O, tiến hành chuẩn độ Fe2+ bằng phương pháp chuẩn độ dichromate Cr2O72- trong môi trường acid theo các bước sau:
• Bước 1: Cân chính xác 1,9 gam muối Mohr, hoà tan với khoảng 5 mL nước cất. Chuyển hết vào bình định mức 100 mL và thêm nước đến vạch được dung dịch X.
• Bước 2: Dùng pipet hút chính xác 10,00 mL dung dịch X cho vào bình nón, thêm 20,00 mL dung dịch H2SO4 2M với 2 – 3 giọt chỉ thị diphenylamine.
• Bước 3: Tiến hành chuẩn độ bằng dung dịch K2Cr2O7 0,005 M cho đến khi dung dịch chuyển sang màu xanh lam đậm thì dừng lại.
Biết phản ứng và màu sắc của ion trong dung dịch như sau:
6Fe2+ (lục nhạt) + Cr2O72-(da cam) + 14H+ → 6Fe3+(vàng nhạt) + 2Cr3+(lục) + 7H2O
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích dung dịch K2Cr2O7 (mL) | 15,9 | 16,0 | 16,0 |
a) Trong phản ứng trên, K2Cr2O7 đóng vai trò chất khử.
b) Để phản ứng chuẩn độ diễn ra nhanh chóng có thể thay dung dịch H2SO4 2M bằng dung dịch H2SO4 đặc.
c) Có thể dự đoán màu xanh lam đậm xuất hiện ở cuối chuẩn độ là do tương tác giữa chỉ thị diphenylamine với ion Fe3+ tạo thành.
d) Độ tinh khiết của mẫu muối Mohr là 98,8% (kết quả làm tròn đến hàng phần mười).
Số phát biểu đúng là bao nhiêu?
(Xem giải) Câu 27. Từ 3 α-amino acid X, Y, Z (phân tử chỉ có 1 nhóm -NH2 và 1 nhóm -COOH) có thể tạo bao nhiêu dipeptide cấu tạo bởi hai gốc amino acid khác nhau?
(Xem giải) Câu 28. Có các phát biểu sau đây:
(1) Amylose có cấu trúc mạch phân nhánh.
(2) Glucose bị oxi hóa bởi thuốc thử Tollens.
(3) Cellulose có cấu trúc mạch phân nhánh.
(4) Saccharose làm mất màu nước bromine.
(5) Fructose có nhiều trong mật ong.
(6) Trong dung dịch, glucose tồn tại chủ yếu ở dạng mạch vòng và một phần nhỏ ở dạng mạch hở.
Hãy liệt kê các phát biểu đúng theo thứ tự tăng dần (ví dụ: 1234, 4321, 235…).

Bình luận