[2026] Thi thử TN sở GDĐT Hải Phòng (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 093
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2B | 3A | 4D | 5C | 6D | 7D | 8A | 9A |
| 10D | 11B | 12D | 13B | 14B | 15B | 16C | 17D | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | S | Đ | Đ | S |
| (b) | Đ | Đ | S | Đ |
| (c) | Đ | S | Đ | Đ |
| (d) | S | S | Đ | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 3 | 3 | 45,7 | 3 | 1108 | 5,92 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Thực hiện các thí nghiệm sau:
(1) Điện phân dung dịch NaCl bằng điện cực trơ, không có màng ngăn xốp.
(2) Cho BaO vào dung dịch CuSO4.
(3) Nhiệt phân AgNO3.
(4) Điện phân hỗn hợp nóng chảy của Al2O3 và Na3AlF6.
(5) Cho dung dịch FeCl2 vào dung dịch AgNO3 (dư).
(6) Cho Al vào dung dịch FeCl3 (dư).
(7) Cho K vào dung dịch CuSO4 (dư).
Số thí nghiệm thu được đơn chất là
A. 4. B. 5. C. 3. D. 6.
(Xem giải) Câu 2. Để khử nhanh mùi tanh của cá do các amine gây ra người ta thường rửa cá bằng
A. nước muối. B. giấm ăn. C. nước vôi. D. nước lạnh.
(Xem giải) Câu 3. Cho pin điện hoá tạo bởi hai cặp oxi hoá – khử ở điều kiện chuẩn: Pb2+/Pb và Zn2+/Zn với thế điện cực chuẩn tương ứng là a V và -0,762V. Sức điện động chuẩn của pin là 0,636V. Giá trị của a là:
A. -0,126. B. 1,398. C. 0,126. D. -1,398.
(Xem giải) Câu 4. Vàng (Au) có thể bị dát mỏng để tạo ra các vật dụng làm đồ trang sức có kích thước lớn nhưng khối lượng nhỏ hoặc bị kéo thành sợi chỉ nhỏ. Khả năng dễ bị dát mỏng hoặc dễ kéo thành sợi nhỏ của vàng dựa trên tính chất nào sau đây?
A. Tính cứng. B. Tính ánh kim. C. Tính khử. D. Tính dẻo.
(Xem giải) Câu 5. Sắc tố quang học trong võng mạc giúp mắt chuyển đổi ánh sáng thành tín hiệu thần kinh để truyền đến não, cho phép chúng ta nhìn thấy thế giới xung quanh. Hợp chất A là một phần của thành phần sắc tố quang học quan trọng trong tế bào võng mạc. Hợp chất A có thể chuyển hóa thành hợp chất B sau khi hấp thụ ánh sáng (phương trình mô tả cho dưới đây):
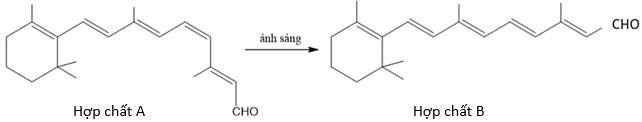
Cho các phát biểu sau:
(a) Tất cả các liên kết đôi trong hợp chất A đều ở dạng trans.
(b) Hợp chất A và hợp chất B có cùng công thức phân tử và cùng nhiệt độ nóng chảy.
(c) Chỉ có chất A phản ứng với thuốc thử Tollens, còn chất B thì không phản ứng với thuốc thử Tollens.
(d) Tổng số nguyên tử trong phân tử chất A là 49.
Số phát biểu sai là
A. 4. B. 1 C. 3. D. 2.
(Xem giải) Câu 6. Phosphorus(V) chloride bị phân hủy ở nhiệt độ cao thành phosphorus(III) chloride và chlorine theo phương trình: PCl5(g) ⇋ PCl3(g) + Cl2(g). Trong các đồ thị sau đây thì đồ thị nào biểu diễn đúng sự biến đổi sản lượng chlorine khi tăng áp suất ở trạng thái cân bằng?
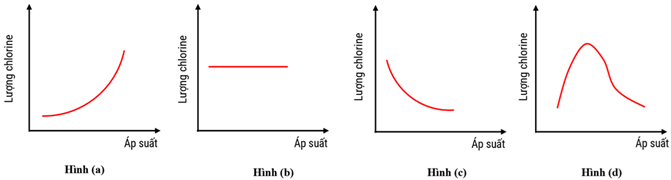
A. Hình (b). B. Hình (d). C. Hình (a). D. Hình (c).
(Xem giải) Câu 7. Cho các chất: HCOOCH3, CH3COOCH3, C2H5OH và CH3COOH và nhiệt độ sôi các chất không theo thứ tự là 118°C, 32°C; 57°C, 78,3°C. Chất có nhiệt độ sôi 118°C là
A. C2H5OH. B. HCOOCH3. C. CH3COOCH3. D. CH3COOH.
(Xem giải) Câu 8. Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Cho khoảng 2 mL dung dịch NaOH 10% vào ống nghiệm. Sau đó, thêm khoảng 0,5 mL dung dịch CuSO4 5% vào, lắc nhẹ.
• Bước 2: Cho tiếp khoảng 3 mL dung dịch glucose 2% vào ống nghiệm và lắc đều ở nhiệt độ thường.
Thí nghiệm trên chứng tỏ glucose có tính chất của
A. Polyalcohol. B. Aldehyde. C. Carboxylic acid. D. Amine.
(Xem giải) Câu 9. Cao su lưu hóa là vật liệu đàn hồi, bền bỉ, chịu nhiệt, cách âm vượt trội và tăng tuổi thọ cao cho các sản phẩm công nghiệp. Cho sơ đồ lưu hóa cao su:
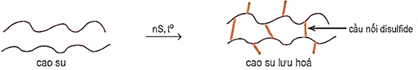
Quá trình lưu hóa cao su thuộc loại phản ứng
A. tăng mạch polymer. B. phân hủy polymer.
C. cắt mạch polymer. D. giữ nguyên mạch polymer.
(Xem giải) Câu 10. Aluminium (![]() ) là kim loại nhẹ, bền, dẫn điện, dẫn nhiệt tốt. Trong công nghiệp, aluminium được sử dụng rộng rãi trong việc chế tạo khung máy, vỏ ô tô, máy bay, hệ thống tản nhiệt… Số hạt proton và neutron trong một nguyên tử aluminium lần lượt là
) là kim loại nhẹ, bền, dẫn điện, dẫn nhiệt tốt. Trong công nghiệp, aluminium được sử dụng rộng rãi trong việc chế tạo khung máy, vỏ ô tô, máy bay, hệ thống tản nhiệt… Số hạt proton và neutron trong một nguyên tử aluminium lần lượt là
A. 13 và 27. B. 14 và 27. C. 14 và 13. D. 13 và 14.
(Xem giải) Câu 11. Trong phản ứng tách kim loại Al từ Al2O3 theo phương trình hoá học: 2Al2O3(l) → 4Al(l) + 3O2(g). Phương pháp tách kim loại nào sau đây đã được áp dụng?
A. Nhiệt luyện. B. Điện phân nóng chảy.
C. Thủy luyện. D. Điện phân dung dịch.
(Xem giải) Câu 12. Ethyl acetate (EA) là dung môi hữu cơ phổ biến, ứng dụng rộng rãi nhất trong sơn, mực in, keo dán nhờ đặc tính bay hơi nhanh và mùi dễ chịu. Nó còn dùng trong dược phẩm (chiết xuất), thực phẩm (khử caffeine, hương liệu), mỹ phẩm (sơn móng tay) và ngành bảo quản côn trùng nghiên cứu. Ethyl acetate có công thức cấu tạo là
A. CH3COOCH3. B. HCOOC2H5. C. HCOOCH3. D. CH3COOC2H5.
(Xem giải) Câu 13. Ngâm bột củ nghệ với ethanol nóng, sau đó lọc bỏ bã, lấy dung dịch đem cô để làm bay hơi bớt dung môi. Phần dung dịch còn lại sau khi cô được làm lạnh, để yên một thời gian rồi lọc lấy chất rắn curcumin màu vàng. Từ mô tả ở trên, hãy cho biết, người ta đã sử dụng các kĩ thuật tinh chế nào để lấy được curcumin từ củ nghệ?
A. Chưng cất và sắc kí. B. Chiết và kết tinh.
C. Chiết và chưng cất. D. Kết tinh và sắc kí.
(Xem giải) Câu 14. Phức chất được dùng làm thuốc chữa bệnh ung thư với tên gọi thương phẩm cisplatin có công thức [PtCl2(NH3)2]. Số phối tử của phức chất cisplatin bằng
A. 1. B. 4. C. 2. D. 3.
(Xem giải) Câu 15. Phương trình hóa học của phản ứng thủy phân 2-chloro-2-methylpropane trong môi trường kiềm là: (CH3)3CCl + NaOH → (CH3)3COH + NaCl. Trong cơ chế của phản ứng trên có hai giai đoạn như sau:
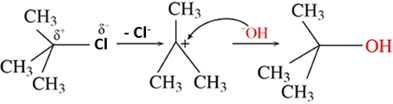
Cho các nhận định sau:
(1) Trong giai đoạn (2) ion OH- hình thành liên kết σ với nguyên tử carbon mang điện tích dương.
(2) Trong giai đoạn (1) có sự phân cắt liên kết σ.
(3) Phản ứng thủy phân 2-chloro-2-methylpropane trong môi trường kiềm là phản ứng trao đổi.
(4) Trong phân tử 2-chloro-2-methylpropane có 14 liên kết σ.
Số nhận định đúng là
A. 4. B. 2. C. 1. D. 3.
(Xem giải) Câu 16. Một mẫu nước cứng chứa các ion: Ca2+, Mg2+, HCO3-, Cl-, SO42-. Hóa chất phù hợp được dùng để làm mềm mẫu nước cứng là
A. NaHCO3. B. H2SO4. C. Na2CO3. D. HCl.
(Xem giải) Câu 17. Trong công nghiệp, sodium hydrogencarbonate (baking soda) và sodium carbonate (soda) được sản xuất bằng phương pháp Solvay. Trong đó, có giai đoạn làm lạnh để tách NaHCO3 ra khỏi dung dịch. Người ta làm lạnh 30 m³ dung dịch NaHCO3 (d = 1,05 g/mL) bão hòa ở 35°C có độ tan 10,3 gam NaHCO3 /100 gam nước về 0°C có độ tan 6,9 gam NaHCO3 /100 gam nước thì có m kg NaHCO3 kết tinh tách ra. Giá trị gần nhất của m là:
A. 986. B. 999. C. 842. D. 971.
(Xem giải) Câu 18. Số oxi hóa của manganese trong KMnO4, MnO2, MnCl2 lần lượt là
A. +8, +4, +3. B. +7, +4, +2. C. +7, +2, +2. D. +7, 0, +3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Pin Galvani được coi là nguồn điện hóa học đầu tiên mà con người phát minh ra. Pin Galvani Zn-Cu được biểu diễn ở hình vẽ và cầu muối chứa NaNO3:

a) Khi pin hoạt động thì nồng độ ion Na+ ở dung dịch chứa điện cực Zn tăng dần.
b) Khi pin hoạt động, khối lượng thanh Zn giảm dần.
c) Khi pin hoạt động dòng Electron chuyển từ thanh Zn qua dây dẫn đến thanh Cu. Cầu muối đóng vai trò khép kín mạch và trung hoà điện tích của dung dịch ở hai điện cực.
d) Khi pin hoạt động, điện cực âm xảy ra quá trình khử Zn, điện cực dương xảy ra quá trình oxi hoá ion Cu2+.
(Xem giải) Câu 20. Năng lượng hoạt hoá (kí hiệu là Ea) là năng lượng tối thiểu mà các chất tham gia cần phải có để phản ứng có thể xảy ra. Enzyme đóng vai trò xúc tác cho nhiều phản ứng, phổ biến trong phản ứng hữu cơ, môi trường hoạt động ở nhiệt độ không cao. Chất xúc tác làm giảm năng lượng hoạt hóa (Ea) của phản ứng dẫn đến tốc độ phản ứng tăng. Sự khác nhau về năng lượng hoạt hoá của phản ứng có sử dụng và không sử dụng enzyme xúc tác được biểu thị như hình vẽ.
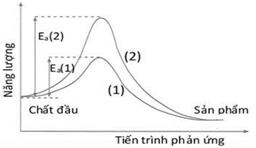
a) Đường (2) có năng lượng hoạt hóa cao hơn đường (1).
b) Phản ứng hóa học ứng với đồ thị đã cho là phản ứng tỏa nhiệt
c) Đường (1) biểu diễn cho phản ứng không sử dụng enzyme làm xúc tác.
d) Trong điều kiện không có enzyme, phản ứng sẽ không thể xảy ra dù có cung cấp đủ năng lượng.
(Xem giải) Câu 21. Có hai học sinh (Bình và An) đều tiến hành thí nghiệm chuẩn độ dung dịch FeSO4 nồng độ xM theo các bước sau:
• Bước 1: Dùng pipette lấy chính xác 10,00mL dung dịch FeSO4 nồng độ xM cho vào bình định mức loại 50 mL, dùng nước cất rửa pipette vừa sử dụng, nước rửa đều cho vào bình định mức. Thêm tiếp nước cất vào định mức đến vạch, lắc đều, thu được 50 mL dung dịch Y.
• Bước 2: Lấy 10,00mL dung dịch Y cho vào bình tam giác, thêm H2SO4 loãng dư. Tiến hành chuẩn độ.
Học sinh Bình: Tiến hành chuẩn độ đúng theo thao tác giáo viên hướng dẫn, kết quả thấy thể tích trung bình dung dịch KMnO4 0,01M sau 03 lần chuẩn độ là 4,0mL và xảy ra theo sơ đồ phản ứng sau:
MnO4-(aq) + H+(aq) + Fe2+(aq) → Mn2+(aq) + Fe3+(aq) + H2O(l) (1)
Học sinh An: Trong quá trình chuẩn độ tiến hành không đúng thao tác. Dung dịch trên burette được thêm vào bình tam giác quá nhanh, trong bình sẽ xuất hiện kết tủa nâu MnO2 xảy ra theo sơ đồ phản ứng sau: MnO4-(aq) + H+(aq) + Fe2+(aq) → MnO2(s) + Fe3+(aq) + H2O(l) (2)
Kết quả thấy thể tích trung bình dung dịch KMnO4 0,01M sau 03 lần chuẩn độ là 5,5 mL và có a% lượng MnO4- chuẩn độ chuyển thành MnO2 phần còn lại vẫn phản ứng tạo Mn2+.
a) Theo học sinh Bình chuẩn độ, giá trị của x bằng 0,10.
b) Tổng hệ số cân bằng nguyên, tối giản nhất của chất trong phản ứng (2) là 16.
c) Thời điểm kết thúc chuẩn độ là lúc dung dịch xuất hiện màu hồng nhạt, bền trong 20s.
d) Nếu dùng kết quả x thu được của học sinh Bình chuẩn độ thì giá trị a bằng 68,18 (Kết quả làm tròn tới phần trăm).
(Xem giải) Câu 22. Vitamin C được phát hiện vào năm 1912 và được phân lập vào năm 1928, là loại vitamin đầu tiên được sản xuất bằng phương pháp hóa học. Walter N. Haworth đã xác định cấu trúc hóa học của vitamin C vào năm 1933. Ông và Szent-Györgyi đã đề xuất và đặt tên nó là ascorbic acid. Người ta xác định được phân tử khối của acid ascorbic là 176 bằng phổ khối lượng MS. Trong ascorbic acid thì thành phần các nguyên tố như sau:
| Nguyên tố | C | H | O |
| Thành phần về khối lượng (%) | 40,91 | 4,55 | 54,54 |
Bằng các phương pháp phổ hồng ngoại IR và phổ cộng hưởng từ NMR, người ta xác định được trong phân tử của acid ascorbic có đặc điểm như sau:
– Trên phổ IR xuất hiện các peak: 3410 cm-1 (to, rộng), 1716 cm-1 (nhọn), 1612 cm-1 (nhọn).
– Có chứa vòng năm cạnh chứa O như sau:
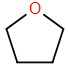
– Trong phân tử chứa 2 loại nhóm -OH khác nhau và tổng số nhóm -OH là 4.
Bảng thông tin các liên kết trên phổ IR.
| Hợp chất | Liên kết hấp thụ | Số sóng hấp thụ (cm-1) |
| Alcohol | O-H | 3500 – 3200 |
| Aldehyde | C-H | 2830 – 2695 |
| C=O | 1740 – 1685 | |
| Ketone | C=O | 1715 – 1666 |
| Carboxylic acid | C=O | 1715 – 1690 |
| O-H | 3300 – 2500 | |
| Ester | C=O | 1750 – 1715 |
| C-O | 1300 – 1000 | |
| Amine | N-H | 3300 – 3000 |
| C=C | 1680 – 1640 | |
| C≡N | 2250 – 2220 | |
| C≡C | 2250 – 2100 |
a) Để xác định hàm lượng vitamin C trên thị trường thì người ta thực hiện như sau: thêm nước vào vitamin C có bán trên thị trường để hòa tan hoàn toàn và pha thành 100 mL dung dịch. Lấy 20 mL dung dịch này cho vào bình nón, thêm một lượng hồ tinh bột thích hợp làm chất chỉ thị, và chuẩn độ bằng dung dịch I2 0,10 M thì hết 12 mL để đạt đến điểm cuối chuẩn độ (đến khi xuất hiện màu xanh tím). Phương trình hóa học của phản ứng giữa và I2 theo đúng hệ số cân bằng sau như sau: vitamin C(aq) + I2(aq) → X(aq) + 2H+(aq) + 2I-(aq). Người ta xác định loại vitamin C thị trường này chứa khoảng 500 mg vitamin C.
b) Công thức phân tử của ascorbic acid là C6H8O6.
c) Vitamin C rất dễ tan trong nước do tạo liên kết hydrogen với nước.
d) Trong ascorbic acid có chứa nhóm chứa ester và liên kết ba.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Trong những cơn mưa giông kèm theo sấm sét, khí nitrogen trong khí quyển được chuyển hóa thành phân đạm theo sơ đồ sau:
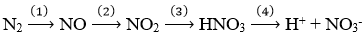
Xác định số phản ứng hoá học trong đó nguyên tố nitrogen đóng vai trò chất khử.
(Xem giải) Câu 24. Retigeranic acid có các đặc tính như kháng khuẩn và kháng viêm. Để tổng hợp được retigeranic acid, người ta cần phải tổng hợp được chất trung gian X có cấu tạo như hình vẽ:
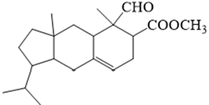
Xác định số liên kết π có trong một phân tử X.
(Xem giải) Câu 25. Isoamyl acetate thường được làm hương liệu nhân tạo. Một học sinh tiến hành điều chế isoamyl acetate theo các bước sau:
• Bước 1: Cho vào bình cầu 44 mL isoamyl alcohol (d = 0,81 g/mL), 40 mL acetic acid (d = 1,049 g/mL) và 2,5 mL dung dịch H2SO4 đậm đặc, cho thêm vào bình viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng đứng vào miệng bình cầu và đun nóng nhẹ trong khoảng 1,5 giờ.
• Bước 2: Sau khi đun, để nguội rồi rót vào phễu chiết, thêm 50 mL nước cất vào phễu, lắc đều rồi để yên khoảng 5 phút, lúc đó chất lỏng tách thành 2 lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
• Bước 3: Cho từ từ dung dịch Na2CO3 10% vào phần chất lỏng thu được ở bước 2 và lắc đều đến khi không còn khí thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hòa rồi để yên cho đến khi chất lỏng đó tách thành hai lớp. Chiết lấy phần chất lỏng phía trên, thu được V mL isoamyl acetate (d = 0,876 g/mL). Biết tổng lượng isoamyl acetate bị thất thoát ở bước 2 và 3 là 5% so với lượng thu được ban đầu, hiệu suất phản ứng ester hóa ở bước 1 bằng 80%. Giá trị của V là bao nhiêu? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn tới hàng phần mười).
(Xem giải) Câu 26. Để bảo vệ vật bằng thép khỏi bị ăn mòn, trong thực tế người ta đã thực hiện một số cách sau:
(1) Sơn kín bề mặt cánh cổng làm bằng thép.
(2) Tráng thiếc lên lá thép (sắt tây).
(3) Để bảo vệ vỏ tàu làm bằng thép, người ta gắn các tấm kẽm lên vỏ tàu (phần chìm dưới nước).
(4) Mạ chromium lên bề mặt thép để làm vật liệu chế tạo các dụng cụ y tế.
Trong số các cách trên, có bao nhiêu cách sử dụng phương pháp phủ bề mặt?
(Xem giải) Câu 27. Khi điều chế gang từ quặng hematite (thành phần chính Fe2O3), người ta sử dụng phương pháp nhiệt luyện trong lò cao. Iron (Fe) thu được ở dạng lỏng có hòa tan carbon (C) và một số nguyên tố khác gọi là gang. Từ 2000 tấn quặng chứa 80% Fe2O3 (còn lại tạp chất không chứa Fe) điều chế được m tấn gang chứa 96% Fe. Biết hiệu suất cả quá trình là 95%. Giá trị của m là bao nhiêu? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng làm tròn tới hàng đơn vị).
(Xem giải) Câu 28. Các nhiên liệu hóa thạch thường chứa sulfur với hàm lượng khác nhau (0,05 – 6,0% với dầu thô, 0,5 – 3% với than và khoảng 10 ppm với khí thiên nhiên, về khối lượng). Dù đã trải qua quá trình loại bỏ sulfur khỏi các nhiên liệu hóa thạch nhưng cặn sulfur còn lại (tối đa là 10 ppm sulfur trong xăng và dầu diesel theo tiêu chuẩn Châu Âu V) vẫn gây ra nhiều vấn đề vì sản phẩm cháy của nó chứa SO2, là chất làm ô nhiễm không khí chính. Người ta đã ước tính tổng mức tiêu thụ năng lượng toàn cầu hàng năm 4,8.10^22 J, trong đó 30,6% đến từ các sản phẩm dầu. Lượng SO2 sinh ra từ các sản phẩm dầu trong một năm là a triệu tấn. Giả sử rằng thành phần chính các sản phẩm dầu là Octane (C8H18) và hàm lượng sulfur là 8 ppm. Biết 90% năng lượng từ sự đốt cháy hoàn toàn octane đã được sử dụng và lượng sulfur trong dầu chuyển hết thành SO2. Biết 1 ppm = 10-6, một số giá trị năng lượng liên kết (E, tính theo kJ/mol) dưới đây:
| Liên kết | C-H | C-C | C=O | O=O | H-O |
| Eb (kJ/mol) | 414 | 347 | 799 | 498 | 464 |
Xác định giá trị của a. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn tới hàng phần trăm)

Bình luận