[2026] Thi thử TN sở GDĐT Nghệ An (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 104
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2A | 3B | 4B | 5D | 6A | 7A | 8D | 9A |
| 10A | 11C | 12A | 13D | 14D | 15A | 16D | 17B | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | S | S | S | Đ |
| (b) | Đ | Đ | Đ | S |
| (c) | Đ | S | S | Đ |
| (d) | S | Đ | S | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 2 | 3 | 1245 | 134 | 77,1 | 65,6 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Trong dãy hydrohalic acid, chất có tính acid mạnh nhất là
A. HCl. B. HF. C. HBr. D. HI.
(Xem giải) Câu 2. Carboxylic acid nào sau đây không no?
A. Propenoic acid. B. Propanoic acid. C. Ethanoic acid. D. Methanoic acid.
(Xem giải) Câu 3. Chất nào sau đây là chất điện li yếu?
A. NaOH. B. CH3COOH. C. Na2CO3. D. HCl.
(Xem giải) Câu 4. Cho dung dịch HCl 0,5M (dư) vào bình tam giác chứa 2 gam đá vôi. Khi thay đổi một trong các yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng trên?
A. Diện tích bề mặt đá vôi. B. Thể tích dung dịch HCl 0,5 M.
C. Nồng độ dung dịch HCl. D. Nhiệt độ của dung dịch HCl 0,5M.
(Xem giải) Câu 5. Điểm chớp cháy của chất cháy là nhiệt độ thấp nhất ở áp suất khí quyển mà chất cháy bị đốt nóng tới mức tạo ra lượng hơi đủ lớn để bốc cháy trong không khí khi gặp nguồn lửa. Cho điểm chớp cháy của một số nhiên liệu lỏng như bảng sau:
| Nhiên liệu | Xăng | Dầu hỏa | Acetone | Ethanol (cồn) | Biodiesel |
| Điểm chớp cháy (°C) | -43 | 38 – 72 | -18 | 13 | 130 |
Chất lỏng có điểm chớp cháy nhỏ hơn 37,8°C gọi là chất lỏng dễ cháy, chất lỏng có điểm chớp cháy lớn hơn 37,8°C gọi là chất lỏng có thể gây cháy. Cho các phát biểu sau:
(a) Nguy cơ gây hỏa hoạn của cồn thấp hơn xăng và acetone.
(b) Xăng dễ bắt cháy hơn so với dầu hỏa.
(c) Biodiesel là chất lỏng có thể gây cháy.
(d) Xăng, acetone, cồn và dầu hỏa là những chất lỏng dễ cháy.
Những phát biểu đúng là
A. (b), (c), (d). B. (a), (b), (d). C. (a), (c), (d). D. (a), (b), (c).
(Xem giải) Câu 6. Carbohydrate nào sau đây không có phản ứng thuỷ phân?
A. Fructose. B. Cellulose. C. Tinh bột. D. Saccharose.
(Xem giải) Câu 7. Hydrocarbon nào sau đây làm mất màu dung dịch KMnO4 ở nhiệt độ thường?
A. Ethene. B. Ethane. C. Benzene. D. Methane.
(Xem giải) Câu 8. Trong kỹ thuật mạ điện, để mạ một lớp đồng lên chiếc chìa khóa bằng thép, người ta tiến hành điện phân dung dịch copper(II) sulfate với anode là thanh đồng, cathode là chiếc chìa khóa. Quá trình chính xảy ra tại cathode là
A. 2H2O + 2e → H2 + 2OH-. B. Cu → Cu2+ + 2e.
C. Fe2+ + 2e → Fe. D. Cu2+ + 2e → Cu.
(Xem giải) Câu 9. Tiến hành các thí nghiệm sau:
– Thí nghiệm 1: Cho khoảng 2 mL dung dịch lòng trắng trứng vào ống nghiệm sau đó đun nóng.
– Thí nghiệm 2: Cho khoảng 2 mL dung dịch lòng trắng trứng vào ống nghiệm sau đó thêm vài giọt dung dịch HNO3 đặc.
– Thí nghiệm 3: Cho khoảng 1 mL dung dịch NaOH 30% vào ống nghiệm, nhỏ 2-3 giọt dung dịch CuSO4 2% vào, lắc đều, cho tiếp khoảng 4 mL dung dịch lòng trắng trứng vào, lắc đều.
Phát biểu nào sau đây không đúng?
A. Ở thí nghiệm 3 thu được dung dịch màu xanh lam.
B. Ở thí nghiệm 3 có xảy ra phản ứng màu biuret.
C. Ở thí nghiệm 2 thu được kết tủa màu vàng.
D. Ở thí nghiệm 1 lòng trắng trứng bị đông tụ.
(Xem giải) Câu 10. Kim loại cơ bản trong hợp kim gang là
A. Fe. B. Al. C. Cr. D. Mn.
(Xem giải) Câu 11. Cho khoảng 2 – 3 giọt dung dịch NaOH 1M vào ống nghiệm đựng 2 mL dung dịch FeCl3 1 M thấy xuất hiện
A. kết tủa màu xanh. B. kết tủa màu tím.
C. kết tủa màu nâu đỏ. D. kết tủa màu trắng.
(Xem giải) Câu 12. Phát biểu nào sau đây đúng khi nói về polymer?
A. Phản ứng thuỷ phân tinh bột là phản ứng cắt mạch polymer.
B. Polymer dùng làm tơ nylon-6,6 được điều chế bằng phản ứng trùng hợp.
C. Polymer dùng làm tơ olon (nitron) chứa bốn nguyên tố C, H, O, N.
D. Tơ tằm, tơ acetate đều thuộc loại tơ thiên nhiên.
(Xem giải) Câu 13. Cho các phát biểu sau về kim loại nhóm IA:
(a) Trong các phản ứng hóa học, kim loại nhóm IA dễ nhường 1 electron, thể hiện tính khử mạnh.
(b) Nhiệt độ nóng chảy và nhiệt độ sôi của các kim loại nhóm IA có xu hướng giảm dần từ Li đến Cs.
(c) Các kim loại nhóm IA có tính khử tăng dần từ Li đến Cs.
(d) Phương pháp chung để tách kim loại nhóm IA là điện phân dung dịch muối chloride.
Số phát biểu đúng là
A. 2. B. 1. C. 4. D. 3.
(Xem giải) Câu 14. Cặp chất nào sau đây là đồng đẳng của nhau?
A. C3H5OH và C3H5(OH)3. B. C6H5OH và C2H5OH.
C. CH3OCH3 và C2H5OH. D. CH3OH và C2H5OH.
(Xem giải) Câu 15. Khí NO2 là một trong các tác nhân gây mưa acid, sương mù quang hóa,… Tên gọi của NO2 là
A. nitrogen dioxide. B. dinitrogen oxide.
C. dinitrogen tetroxide. D. nitrogen monoxide.
(Xem giải) Câu 16. Amine nào sau đây là amine bậc hai?
A. Trimethylamine. B. Methylamine. C. Ethylamine. D. Dimethylamine.
(Xem giải) Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Methyl salicylate thường được phối hợp với các loại tinh dầu khác dùng làm thuốc bôi ngoài da, thuốc xoa bóp, cao dán giảm đau, chống viêm. Methyl salicylate có công thức cấu tạo như bên:
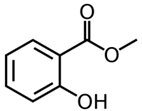
Câu 17. Để sản xuất 3,8 triệu tuýp thuốc xoa bóp giảm đau cần tối thiểu m tấn salicylic acid. Biết mỗi tuýp thuốc chứa 2,7 gam methyl salicylate và hiệu suất phản ứng tính theo salicylic acid là 75%; phương trình hóa học của phản ứng điều chế methyl salicylate:
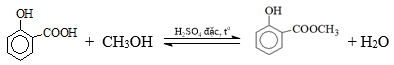
Giá trị m là
A. 6,99. B. 12,42. C. 16,56. D. 9,32.
Câu 18. Phát biểu nào sau đây không đúng khi nói về methyl salicylate?
A. Phản ứng được với dung dịch NaOH. B. Chứa chức ester.
C. Chứa chức alcohol. D. Công thức phân tử là C8H8O3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Một nhóm học sinh nghiên cứu thí nghiệm lên men giấm và đưa ra giả thuyết “Nồng độ C2H5OH càng lớn thì hiệu suất lên men giấm càng cao”. Để kiểm chứng giải thuyết, học sinh tiến hành thí nghiệm theo các bước sau:
• Bước 1: Chuẩn bị 5 cốc giống nhau, mỗi cốc đựng 100 mL dung dịch có nồng độ C2H5OH khác nhau (dung dịch nghiên cứu) được pha từ nước cất, C2H5OH với 10 mL dung dịch men giấm tươi. Các miệng cốc đều được che bằng tấm vải màn giống nhau nhằm ngăn bụi rồi để cả 5 cốc trong phòng thí nghiệm.
• Bước 2: Tiến hành xác định nồng độ CH3COOH trong dung dịch các cốc ở cùng thời điểm bằng phương pháp chuẩn độ với dung dịch chuẩn là NaOH 0,1M và chỉ thị phenolphthalein. Kết quả các lần chuẩn độ xác định được nồng độ phần trăm của CH3COOH ghi trong bảng sau.

a) Khi tiến hành chuẩn độ, chỉ thị phenolphthalein phải được cho vào dung dịch chuẩn NaOH ở trên burette.
b) Kết quả thí nghiệm không phù hợp với giả thuyết của nhóm học sinh đưa ra ở trên.
c) Nếu coi trong quá trình lên men các chất bay hơi không đáng kể thì hiệu suất lên men giấm đến ngày thứ 15 ở cốc 2 là 54,69% (chỉ làm tròn số ở phép tính cuối cùng và kết quả làm tròn số đến hàng phần trăm).
d) Từ kết quả thí nghiệm cho thấy với mọi nồng độ C2H5OH, thời gian lên men càng lâu thì tốc độ phản ứng lên men giấm càng lớn.
(Xem giải) Câu 20. Magnesium (Mg) là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau:
– Giai đoạn 1: Nung quặng dolomite ở 1100 – 1200°C thu được dolomite nung:
MgCO3.CaCO3(s) ⟶ MgO(s) + CaO(s) + 2CO2(g)
– Giai đoạn 2: Dolomite nung được nghiền nhỏ, trộn với chất khử (bột ferrosilicon Fe, Si) và chất xúc tác fluorite (CaF2), sau đó ép thành viên.
– Giai đoạn 3: Viên nguyên liệu được đưa vào lò thép không gỉ, nung chân không ở 1200°C:
2MgO(s) + 2CaO(s) + Si(s) ⟶ 2Mg(g) + Ca2SiO4(s)
– Giai đoạn 4: Hơi magnesium được dẫn qua bộ ngưng tụ chuyển thành dạng tinh thể, sau đó nấu chảy và đúc thành thỏi.
Một nhà máy sản xuất magnesium theo quy trình trên với hiệu suất toàn bộ quá trình là 90%, khối lượng mỗi thỏi thành phẩm chứa 7,5 kg magnesium.
a) Trong phản ứng ở giai đoạn 3, MgO dễ bị oxi hóa bởi Si hơn CaO.
b) Giai đoạn 3 tiến hành trong môi trường chân không nhằm giúp hơi magnesium thoát ra dễ dàng hơn và tránh bị oxi hóa bởi không khí ở nhiệt độ cao.
c) Quá trình hơi magnesium chuyển thành tinh thể là quá trình thu nhiệt.
d) Từ 10 tấn quặng dolomite (chứa 92% MgCO3.CaCO3 về khối lượng, còn lại là tạp chất không chứa magnesium) nhà máy trên sản xuất được 144 thỏi magnesium thành phẩm.
(Xem giải) Câu 21. Trong không khí ẩm, trên bề mặt của gang thép luôn có một lớp nước mỏng đã hòa tan khí oxygen, carbon dioxide và một số chất khác tạo thành dung dịch chất điện li. Khi đó tại bề mặt của gang thép xảy ra sự ăn mòn kim loại.
a) Trong quá trình ăn mòn sắt đóng vai trò anode, tại bề mặt xảy ra quá trình: Fe(s) → Fe3+(aq) + 3e.
b) Thành phần gỉ sắt có chứa hợp chất dạng Fe2O3.nH2O.
c) Thiếc có tính khử yếu hơn sắt nên người ta gắn các lá thiếc vào vỏ tàu để bảo vệ vỏ tàu biển bằng thép.
d) Quá trình ăn mòn kim loại ở trên chủ yếu là ăn mòn hóa học.
(Xem giải) Câu 22. Cao sư thiên nhiên là một loại polymer được tạo bởi các mắt xích isoprene. Cấu trúc của một đoạn mạch cao su thiên nhiên như sau:
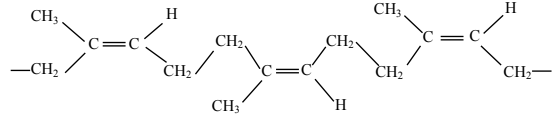
Muốn sử dụng được trong thực tế, người ta phải thực hiện quá trình lưu hóa cao su thiên nhiên để tạo ra cao su lưu hóa theo sơ đồ sau:
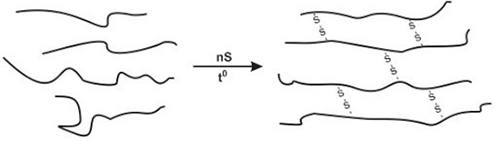
Quá trình lưu hóa cao su là quá trình thay thế hai nguyên tử H ở hai nhóm CH2 trong các mạch polymer bằng cầu disulfide (-S-S-).
a) Các liên kết đôi trong đoạn mạch cao su thiên nhiên ở trên đều ở dạng cis.
b) Phản ứng lưu hóa cao su thuộc loại phản ứng giữ nguyên mạch polymer.
c) So với cao su thiên nhiên thì cao su lưu hóa có độ bền nhiệt, độ đàn hồi cao hơn.
d) Một loại cao su lưu hóa có 2,3% sulfur về khối lượng thì trung bình 46 mắt xích isoprene có một cầu disulfide (-S-S-) (chỉ làm tròn số ở phép tính cuối cùng và số mắt xích làm tròn số đến phần nguyên).
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho các chất: ethane, ethyne, toluene, styrene. Cho lần lượt lượng dư từng chất trên vào dung dịch bromine ở nhiệt độ thường. Có bao nhiêu chất làm mất màu dung dịch bromine?
(Xem giải) Câu 24. Cho bảng giá trị thế điện cực chuẩn (E°) của một số cặp oxi hóa – khử sau:
| Cặp oxi hóa – khử | Na+/Na | Zn2+/Zn | Fe2+/Fe | 2H+/H2 | Cu2+/Cu |
| E° (V) | -2,713 | -0,763 | -0,44 | 0,00 | +0,34 |
Trong số các kim loại: Na, Zn, Fe và Cu, có bao nhiêu kim loại phản ứng được với HCl trong dung dịch ở điều kiện chuẩn?
(Xem giải) Câu 25. Cho các phát biểu về dãy kim loại chuyển tiếp thứ nhất:
(1) Ở trạng thái cơ bản, lớp ngoài cùng của nguyên tử kim loại chuyển tiếp dãy thứ nhất có một hoặc hai electron.
(2) Trong dãy kim loại chuyển tiếp dãy thứ nhất thì chromium có độ cứng lớn nhất.
(3) Ở trạng thái cơ bản, phân lớp 3d trong nguyên tử các kim loại chuyển tiếp dãy thứ nhất đều chưa bão hoà.
(4) Các kim loại chuyển tiếp dãy thứ nhất đều là các nguyên tố thuộc nhóm B trong bảng tuần hoàn.
(5) Các kim loại chuyển tiếp dãy thứ nhất đều có nhiệt độ nóng chảy cao hơn kim loại Ca, K.
Hãy liệt kê các phát biểu đúng theo số thứ tự tăng dần.
(Xem giải) Câu 26. Từ cây chùm ngây (Moringa oleifera), người ta phân lập được hợp chất hữu cơ E. Chất E có vai trò như một chất ức chế, chất chuyển hóa thực vật và còn là chất gây dị ứng. Kết quả phân tích nguyên tố của E cho phần trăm khối lượng các nguyên tố như sau: %C = 78,505%; %H = 8,411%; còn lại là %N. Bằng các phương pháp khác, người ta xác định được E có chứa vòng benzene, chỉ có 1 nguyên tử N và không có nhóm -CH3. Cho các phát biểu sau về E:
(1) Công thức phân tử của E là C7H9N.
(2) E là một arylamine.
(3) Ở nhiệt độ thường, E tác dụng với dung dịch nitrous acid tạo alcohol.
(4) E tác dụng với dung dịch HCl tạo ra muối có dạng RNH3Cl.
(5) E là một amine bậc 2.
Hãy liệt kê các phát biểu đúng theo số thứ tự tăng dần.
(Xem giải) Câu 27. Gói làm nóng thức ăn (FRH: Flameless Ration Heater) được sử dụng để hâm nóng các bữa ăn tiện lợi. Thành phần chính của FRH là bột Mg, ngoài ra có một lượng nhỏ Fe và NaCl đóng vai trò tạo pin điện hoá, giúp tăng tốc độ phản ứng của Mg với nước. Khi sử dụng, cho khoảng 30 mL nước vào hỗn hợp FRH thì chỉ xảy ra phản ứng: Mg(s) + 2H2O(l) → Mg(OH)2(s) + H2(g)
Một gói FRH chứa 8,0 gam hỗn hợp gồm Mg 92,0%, Fe 4,0% và NaCl 4,0% theo khối lượng được sử dụng để làm nóng 300 gam súp từ 25°C lên t°C. Biết: để 1,0 gam súp tăng 1°C thì cần 4,2 J, chỉ có 60% nhiệt tỏa ra từ phản ứng trên làm nóng súp và enthalpy tạo thành chuẩn của các chất cho ở bảng sau:
| Chất | Mg(OH)2(s) | H2O(l) | Mg(s) | H2(g) |
| -928,4 | -285,8 | 0,0 | 0,0 |
Giá trị của t bằng bao nhiêu? (Không làm tròn các kết quả trung gian, làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 28. Cho 30,0 mL isoamyl alcohol (d = 0,810 g/mL) phản ứng với 20,0 mL acetic acid (d = 1,049 g/mL) có xúc tác H2SO4 đặc và đun nóng. Sau phản ứng thu được 26,9 mL isoamyl acetate (d = 0,876 g/mL). Cho biết hiệu suất của quá trình điều chế isoamyl acetate ở trên là h%. Giá trị của h bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).

Bình luận