[2026] Thi thử TN trường Phan Châu Trinh – Đà Nẵng
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 103
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2D | 3A | 4C | 5A | 6D | 7C | 8A | 9A |
| 10D | 11B | 12D | 13B | 14D | 15B | 16C | 17D | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | Đ | Đ |
| (b) | S | Đ | Đ | Đ |
| (c) | S | Đ | Đ | Đ |
| (d) | Đ | Đ | S | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 4 | 109 | 8731 | 499 | 1 | 34 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Phức chất [Co(NH3)6]3+ có nguyên tử trung tâm là
A. NH3+. B. Co3+. C. Co. D. NH3.
(Xem giải) Câu 2. FGD là quy trình khử SO2 trong khí thải phổ biến nhất tại Việt Nam. Khí SO2 được hấp thụ bằng Ca(OH)2 tạo thành CaSO3. Sau đó CaSO3 bị oxi hóa hoàn toàn thành CaSO4 khi cho tác dụng liên tục với O2. CaSO4 được lọc tách, làm sạch, nung và thu hồi dưới dạng thạch cao thương phẩm là 2CaSO4.H2O có thể sử dụng để sản xuất xi măng. Một nhà máy nhiệt điện sử dụng quy trình trên để xử lí trung bình 1,2 triệu m³ khí thải mỗi ngày, nồng độ SO2 trong khí thải là 3200 mg/m³, biết hiệu suất của cả hệ thống là 95% thì khối lượng 2CaSO4.H2O thu được trong một ngày là (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần mười)
A. 9,8 kg. B. 8,3 kg. C. 9,8 tấn. D. 8,3 tấn.
(Xem giải) Câu 3. Chất nào sau đây thuộc loại polymer thiên nhiên?
A. Amylopectin. B. Cellulose triacetate.
C. Poly(methyl methacrylate). D. Polybutadiene.
(Xem giải) Câu 4. Xét các biện pháp sau:
(a) Sử dụng nồi áp suất khi nấu các món hầm.
(b) Bảo quản thực phẩm trong tủ lạnh để giữ thực phẩm tươi lâu.
(c) Nghiền nguyên liệu trước khi nung trong sản xuất clinker xi măng.
(d) Dùng men làm chất xúc tác để chuyển hóa cơm nếp thành rượu.
Số biện pháp được sử dụng để tăng tốc độ phản ứng là
A. 2. B. 4. C. 3. D. 1.
(Xem giải) Câu 5. Vật liệu X có thành phần chính là polymer cấu tạo như hình bên. X là
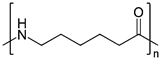
A. tơ nylon-6. B. tơ nylon-7. C. nhựa PP. D. cao su buna.
(Xem giải) Câu 6. Phát biểu nào sau đây không đúng về pin Galvani Zn-Cu?
A. Dòng electron chạy từ Zn sang Cu.
B. Zn đóng vai trò anode, Cu đóng vai trò cathode.
C. Ở anode xảy ra quá trình oxi hóa Zn.
D. Ở cathode xảy ra quá trình khử Cu.
(Xem giải) Câu 7. Cetyl alcohol (X) là một chất nhũ hóa có nguồn gốc tự nhiên và công thức cho ở hình bên. X có đặc tính làm mướt, giữ ẩm, làm mềm, được sử dụng phổ biến trong các sản phẩm kem dưỡng, dầu xả tóc.
![]()
X là alcohol thuộc loại nào sau đây?
A. Không no, bậc hai. B. No, bậc hai.
C. No, bậc một. D. Không no, bậc một.
(Xem giải) Câu 8. Fumaric acid (X) là một loại acid thực phẩm được sử dụng lâu đời vì không độc, có công thức cho ở hình bên. X thường sử dụng làm chất điều chỉnh độ acid, chất phụ trợ chống oxi hóa nhiệt, chất tăng tốc đóng rắn và gia vị trong thực phẩm.

Phát biểu nào sau đây không đúng?
A. X tác dụng với dung dịch NaOH dư theo tỉ lệ mol 1 : 1.
B. Dung dịch của X có pH < 7 và có cấu hình trans.
C. X là acid đa chức, có công thức phân tử C4H4O4.
D. X làm mất màu dung dịch Br2.
(Xem giải) Câu 9. Chất nào sau đây tan tốt trong nước?
A. MgSO4. B. MgCO3. C. BaSO4. D. CaCO3.
(Xem giải) Câu 10. Tiến hành các thí nghiệm sau:
(a) Đun sôi một mẫu nước có tính cứng tạm thời.
(b) Cho dung dịch KHSO4 vào dung dịch Ba(OH)2.
(c) Cho dung dịch NaOH đến dư vào dung dịch AlCl3.
(d) Cho dung dịch NaOH đến dư vào dung dịch Ba(HCO3)2.
Khi kết thúc phản ứng, số thí nghiệm thu được kết tủa là
A. 4. B. 1. C. 2. D. 3.
(Xem giải) Câu 11. Cho các phát biểu sau:
(a) Dung dịch aniline tạo được kết tủa trắng với nước bromine.
(b) Đun nóng dung dịch lòng trắng trúng có hiện tượng đông tụ protein.
(c) Tất cả các peptide đều phản ứng với thuốc thử biuret.
(d) Protein dễ bị thủy phân bởi acid, base hoặc enzyme.
(e) Hầu hết enzyme là xúc tác và có tính chọn lọc cao.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 2.
(Xem giải) Câu 12. PVC là loại nhựa được sử dụng phổ biến thứ ba trên thế giới. Nhờ khả năng kết hợp với các chất phụ gia, PVC có thể biến đổi linh hoạt từ dạng cứng (khung cửa, ống nước) đến dạng dẻo (màng bọc, dây điện), phục vụ đa dạng ngành công nghiệp và đời sống. Hiện nay, PVC được điều chế chủ yếu từ ethylene theo sơ đồ: Ethylene → dichloroethane → vinyl chloride → PVC. Hiệu suất mỗi quá trình trong sơ đồ trên tương ứng là 55%, 65% và 62% thì khối lượng PVC sản xuất được từ 500 m³ khí ethylene (đkc) gần nhất với
A. 5687 kg. B. 558 kg. C. 2844 kg. D. 279 kg.
(Xem giải) Câu 13. Thực hiện quá trình điện phân để mạ đồng lên một chiếc chìa khóa được làm từ thép không gỉ. Phát biểu nào sau đây không đúng?
A. Dung dịch điện phân là CuSO4. B. Chiếc chìa khóa được treo ở cực dương.
C. Điện cực anode tan dần. D. Anode được làm bằng kim loại đồng.
(Xem giải) Câu 14. Tiến hành thí nghiệm điều chế và thử tính chất của khí X theo các bước sau:
• Bước 1: Cho vài mẩu nhỏ CaC2 vào ống nghiệm đã đựng 2 mL nước và đậy nhanh bằng nút có ống dẫn khí đầu vuốt nhọn.
• Bước 2: Đốt khí X sinh ra ở đầu ống vuốt nhọn.
• Bước 3: Dẫn khí X qua ống nghiệm đựng dung dịch KMnO4.
Cho các phát biểu sau:
(a) Khi thay CaC2 bằng Al4C3 thì sản phẩm thu được giống nhau.
(b) Khí X được ứng dụng rộng rãi để hàn cắt kim loại.
(c) Phân tử khí X làm nhạt màu dung dịch KMnO4.
(d) Trong phòng thí nghiệm có thể điều chế khí X từ ethanol bằng một phản ứng.
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 15. Sodium carbonate (Na2CO3) là một trong những hóa chất được sử dụng rộng rãi trong công nghiệp sản xuất thủy tinh, bột giặt, xà phòng, giấy, sợi, chất tẩy rửa. Phát biểu nào sau đây không đúng về Na2CO3?
A. Là chất rắn màu trắng, tan tốt trong nước.
B. Là thành phần chính trong bình chữa cháy dạng bột.
C. Có thể làm mềm nước có tính cứng toàn phần.
D. Được sản xuất chủ yếu bằng phương pháp Solvay.
(Xem giải) Câu 16. Cho các cặp oxi hóa – khử và thế điện cực chuẩn tương ứng:
| Cặp oxi hóa – khử | Cr2+/Cr | Zn2+/Zn | Cr3+/Cr2+ | Ni2+/Ni |
| Thế điện cực chuẩn (V) | -0,91 | -0,76 | -0,41 | -0,26 |
Phản ứng nào sau đây đúng?
A. Ni + 2Cr3+ → Ni2+ + 2Cr2+. B. Zn + Cr2+ → Zn2+ + Cr.
C. Zn + 2Cr3+ → Zn2+ + 2Cr2+. D. 3Zn + 2Cr3+ → 3Zn2+ + 2Cr.
(Xem giải) Câu 17. Phát biểu nào sau đây không đúng với ammonia?
A. Làm nguyên liệu để sản xuất HNO3 theo phương pháp Ostwald.
B. Được dùng để sản xuất các loại phân đạm.
C. Trong công nghiệp được sử dụng như chất làm lạnh (chất sinh hàn).
D. Hầu như không tan trong nước do phân tử không phân cực.
(Xem giải) Câu 18. Chất nào sau đây chiếm khoảng 90% khối lượng sợi bông?
A. Tinh bột. B. Glucose. C. Cellulose. D. Fructose.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Glycine là chất rắn kết tinh, không màu, được tìm thấy với nồng độ cao trong da, mô cơ, mô liên kết của các khớp. Glycine còn được sử dụng làm chất phụ gia cho thực phẩm, thuốc, mỹ phẩm. Hiện nay, glycine được sản xuất chủ yếu bằng cách cho chloroacetic acid tác dụng với ammonia theo phương trình hóa học:
ClCH2COOH + 2NH3 → H2NCH2COOH + NH4Cl.
Chloroacetic acid Glycine
a) NH4Cl được thu hồi sau quá trình sản xuất có thể dùng làm phân đạm, giup tối ưu chi phí và giảm thiểu đáng kể tình trạng ô nhiễm nitrogen gây hiện tượng phú dưỡng.
b) Một kỹ sư hóa chất cho 18,9 kg chloroacetic acid tác dụng với dung dịch ammonia 25% (D = 0,91 g/mL, dùng dư). Thêm methanol vào sản phẩm để glycine kết tinh khỏi dung dịch (phụ phẩm vẫn tan phần lớn trong hỗn hợp). Lọc và sấy khô, thu được 12,8 kg sản phẩm glycine thô. Phân tích mẫu glycine thô này bằng phương pháp chuẩn độ, kết quả cho thấy hàm lượng glycine nguyên chất trong mẫu đạt 94,12%. Hiệu suất của quá trình sản xuất glycine là 90,2%. (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần mười).
c) Dung dịch của glycine làm quỳ tím hóa đỏ.
d) Glycine là α–amino acid đơn giản nhất có công thức phân tử C2H5NO2.
(Xem giải) Câu 20. Nhiên liệu hóa thạch hiện nay đang khủng hoảng do nguồn cung dần cạn kiệt, xung đột địa chính trị và gây ô nhiễm môi trường. Bên cạnh các nguồn năng lượng tái tạo đang được phát triển mạnh (gió, mặt trời…) thì pin nhiên liệu, đặc biệt là pin hydrogen đang là hướng nghiên cứu đầy triển vọng, chuyển đổi năng lượng hóa học từ hydrogen và oxygen thành điện thông qua phản ứng điện hóa mà không cần xảy ra sự cháy.

Quá trình xảy ra tại một tế bào pin hydrogen điển hình là:
• Tại anode: Hydrogen được cung cấp và tiếp xúc với chất xúc tác platinum (Pt): H2 → 2H+ + 2e.
• Tại cathode: Oxygen từ không khí kết hợp với proton và electron tạo thành nước: O2 + 4H+ +4e → 2H2O.
a) Các proton (H+) và các electron đi qua màng trao đổi proton (PEM) từ anode đến cathode.
b) Phản ứng hóa học xảy ra trong pin hydrogen là: 2H2 + O2 → 2H2O, sản phẩm không phát thải khí CO2 nên đây là giải pháp hiệu quả hướng tới mục tiêu “Net Zero” (Phát thải ròng bằng 0).
c) Một mẫu xe ô tô điện sử dụng công nghệ pin hydrogen, bình chứa nhiên liệu của xe có dung tích 120 L chứa khí H2 được nén ở áp suất 700 atm và nhiệt độ 27°C. Biết định mức tiêu hao nhiên liệu trung bình của pin là 56 gam H2/kWh, phương trình trạng thái khí lí tưởng là P.V = n.R.T, với T là nhiệt độ (K), P là áp suất (atm), V là thể tích (L), n là lượng chất (mol), R = 0,082 (L.atm.mol-1.K-1). Nếu động cơ chạy liên tục trên cao tốc với công suất trung bình là 40 kW, xe chứa đầy nhiên liệu thì thời gian tối đa xe có thể hoạt động liên tục là 3 h. (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị).
d) Có một ít khí hydrogen không bị oxi hóa hết sẽ được dẫn ra ngoài và tái sử dụng.
(Xem giải) Câu 21. Ethyl cinnamate (D = 1,049 g/cm³, t°s = 271°C) là một ester sở hữu mùi hương rất độc đáo, ấm nồng giống hương quế kết hợp cùng các nốt hương trái cây dịu nhẹ. Hợp chất này chủ yếu được sản xuất thông qua hai phương pháp:
• Phản ứng ester hóa trực tiếp:
C6H5-CH=CH-COOH + C2H5OH ⇋ C6H5-CH=CH-COOC2H5 + H2O (H2SO4 đặc, t°)
• Phản ứng ngưng tụ Claisen:
C6H5-CHO + CH3COOC2H5 → C6H5-CH=CH-COOC2H5 + H2O (Na/C2H5ONa)
a) Ethyl cinnamate khó tan trong nước, để tách nó ra khỏi hỗn hợp có thể dùng phương pháp chiết hoặc ngưng tụ, sau đó làm khô bằng CaCl2 khan.
b) Ethyl cinnamate có phản ứng xà phòng hóa.
c) Ethyl cinnamate là ester đơn chức, có đồng phân hình học cis – trans.
d) Trong phương pháp ester hóa, phản ứng xảy ra không hoàn toàn nên hiệu suất cao hơn phương pháp ngưng tụ Claisen.
(Xem giải) Câu 22. Chromium (Z = 24) được biết đến là kim loại cứng nhất trong tự nhiên. Khoảng 80% sản lượng chromium toàn thế giới được sử dụng cho việc sản xuất thép không gỉ (inox). Quy trình sản xuất chromium từ quặng chromite (thành phần chính là FeCr2O4) qua các giai đoạn sau:
• Giai đoạn 1: Quặng chromite được nghiền nhỏ, trộn với Na2CO3 và nung trong lò ở nhiệt độ trên 1000°C với sự có mặt của không khí: 4FeCr2O4 + 8Na2CO3 + 7O2 → 8Na2CrO4 + 2Fe2O3 + 8CO2.
• Giai đoạn 2: Hỗn hợp thu được sau khi nung được hòa tan vào nước thu được dung dịch màu vàng, trong khi các tạp chất không tan bị loại bỏ. Thêm dung dịch H2SO4 vào dung dịch màu vàng tạo thành dung dịch màu da cam: 2Na2CrO4 + H2SO4 → Na2Cr2O7 + Na2SO4 + H2O.
• Giai đoạn 3: Khử muối Na2Cr2O7 bằng than cốc ở nhiệt độ cao: Na2Cr2O7 + 2C → Cr2O3 + Na2CO3 + CO.
• Giai đoạn 4: Cr2O3 được trộn với bột Al rồi kích hoạt phản ứng bằng mồi cháy (Mg + KClO3) để xảy ra phản ứng nhiệt nhôm: Cr2O3(s) + 2Al(s) → Al2O3(s) + 2Cr(s). Cho biết nhiệt tạo thành chuẩn của Cr2O3(s) và Al2O3(s) lần lượt là –1128,6 kJ/mol và –1676,0 kJ/mol.
a) Từ 2,24 tấn quặng chromite (chứa 52% FeCr2O4, còn lại là các tạp chất trơ), hiệu suất cả quá trình đạt 85% thì thu được 460 kg chromium. (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị).
b) Chromium thường dùng để sản xuất thép không gỉ do tạo lớp màng Cr2O3 mỏng, bền, giúp ngăn chặn quá trình oxi hóa và ăn mòn điện hóa.
c) Nguyên tử Cr ở trạng thái cơ bản có 6 electron độc thân, có số oxi hóa cao nhất là +6 trong hợp chất.
d) Biến thiên enthalpy chuẩn của phản ứng nhiệt nhôm ở giai đoạn 4 bằng +547,4 kJ, là phản ứng thu nhiệt mạnh nên cần phải cung cấp nhiệt suốt quá trình xảy ra.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho phương trình hóa học của các phản ứng sau:
(a) N2(g) + 3H2(g) ⇋ 2NH3(g)
(b) H2(g) + I2(g) ⇋ 2HI(g)
(c) 2NO2(g) ⇋ N2O4(g)
(d) 2SO2(g) + O2(g) ⇋ 2SO3(g)
(e) 2NO(g) + O2(g) ⇋ 2NO2(g)
Khi tăng áp suất, số phản ứng hóa học chuyển dịch cân bằng theo chiều thuận là bao nhiêu?
(Xem giải) Câu 24. Trên thế giới, kẽm (Zn) được sản xuất chủ yếu từ quặng sphalerite có thành phần chính là ZnS. Một nhà máy luyện kim sản xuất Zn từ 100 tấn quặng sphalerite (chứa 92% ZnS về khối lượng, còn lại là tạp chất không chứa kẽm) với hiệu suất cả quá trình đạt 95% theo các giai đoạn:
• Đốt quặng sphalerite: 2ZnS(s) + 3O2(g) → 2ZnO(s) + 2SO2(g).
• Khử ZnO ở nhiệt độ cao bằng than cốc: ZnO(s) + C(s) → Zn(g) + CO(g).
Toàn bộ lượng kẽm tạo ra được đúc thành x thanh kẽm hình hộp chữ nhật: chiều dài 150 cm, chiều rộng 20cm và chiều cao 25 cm. Biết khối lượng riêng của kẽm là 7,14 g/cm³. Giá trị của x là bao nhiêu? (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 25. Biodiesel B10 là hỗn hợp gồm 10% biodiesel và 90% dầu diesel truyền thống về thể tích. Biodiesel được sản xuất từ các nguồn tài nguyên sinh học như dầu thực vật hoặc mỡ động vật đã qua sử dụng thông qua phản ứng giữa chất béo với các alcohol mạch ngắn (thường là methyl alcohol) với xúc tác là kiềm, thu được biodiesel (ester của acid béo) và glycerol: (RCOO)3C3H5 + 3CH3OH → 3RCOOCH3 + C3H5(OH)3. Một nhà máy sử dụng 1 tấn dầu ăn đã qua sử dụng chứa 91% chất béo (phân tử khối trung bình của chất béo là 860, các tạp chất không có khả năng chuyển hóa thành biodiesel) với hiệu suất của quá trình sản xuất là 85% thì sản xuất được bao nhiêu L biodiesel B10 (biết D biodiesel = 890 g/L)? (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Một nhóm học sinh tiến hành thí nghiệm xác định hàm lượng calcium có trong một viên khoáng chất bổ sung (1,25 g/1 viên) như sau:
• Hòa tan viên khoáng chất trong môi trường acid yếu hoặc trung tính, sau đó cho ion Ca2+ kết tủa hoàn toàn dưới dạng CaC2O4: Ca2+ + C2O42- → CaC2O4.
• Kết tủa được lọc, rửa sạch và hòa tan lại bằng sulfuric acid loãng. Lúc này, ion C2O42- giải phóng ra sẽ được chuẩn độ bằng dung dịch chuẩn KMnO4: 2MnO4- + 5C2O42- + 16H3O+ → 2Mn2+ + 10CO2 + 24H2O. Kết quả chuẩn độ được cho ở bảng sau:
| Thí nghiệm | Lần 1 | Lần 2 | Lần 3 |
| Thể tích dung dịch KMnO4 0,2 M đã dùng (mL) | 24,9 | 25,0 | 24,9 |
Khối lượng calcium (mg) trong mỗi viên khoáng chất trên là bao nhiêu? (Chi làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 27. Thực hiện phản ứng của glucose với thuốc thử Tollens qua các bước sau:
• Bước 1: Nhỏ từ từ đến dữ dung dịch NH3 vào ống nghiệm chứa 2 mL dung dịch AgNO3 đến khi kết tủa tan hết.
• Bước 2: Nhỏ tiếp vào ống nghiệm 2 mL dung dịch glucose và lắc đều.
• Bước 3: Ngâm ống nghiệm trong cốc nước nóng ở nhiệt độ khoảng 70°C – 80°C vài phút.
Cho các phát biểu sau:
(a) Sau bước 3 quan sát thấy thành ống nghiệm sáng bóng như gương.
(b) Ở bước 3 xảy ra phản ứng oxi hóa – khử trong đó glucose là chất oxi hóa.
(c) Trong bước 3, để kết tủa bạc nhanh bám vào thành ống nghiệm ta phải luôn lắc đều và liên tục hỗn hợp phản ứng.
(d) Ở bước 1 có thể thay dung dịch NH3 bằng dung dịch NaOH.
(e) Ở bước 3 nếu thay glucose bằng saccharose vào ống nghiệm thì thu được hiện tượng tương tự.
Số phát biểu đúng là bao nhiêu?
(Xem giải) Câu 28. Cao su tự nhiên lấy từ mủ cây cao su là một polymer có chứa các mắc xích isoprene. Khi cho cao su tự nhiên tác dụng với lưu huỳnh thu được cao su lưu hóa có các cầu nối disulfide –S–S– tạo mạng lưới không gian nên các tính chất lí hóa nổi trội hơn so với cao su tự nhiên. Cho các phát biểu sau:
(1) Bản chất của quá trình lưu hóa cao su là phản ứng giữ nguyên mạch polymer.
(2) Cao su tự nhiên là polymer của isoprene có cấu hình trans.
(3) Cao su tự nhiên có thể tham gia phản ứng cộng H2, HCl, Cl2 do phân tử polymer còn liên kết đôi.
(4) Một loại cao su lưu hóa có 3,0% lưu huỳnh về khối lượng, nguyên tử lưu huỳnh đã thay thế cho nguyên tử hydrogen ở cầu methylene trong mạch cao su, số mắt xích isoprene tương ứng với một cầu disulfide là 30. (Chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị).
Liệt kê các phát biểu đúng theo thứ tự tăng dần (ví dụ 123, 14,…).

Bình luận