[2026] Thi thử TN sở GDĐT Sơn La (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 059
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2B | 3D | 4A | 5A | 6A | 7B | 8D | 9B |
| 10D | 11A | 12A | 13C | 14D | 15C | 16B | 17A | 18A |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | S | Đ | S | 30 | 8 | 4 |
| (b) | S | S | Đ | Đ | 26 | 27 | 28 |
| (c) | Đ | Đ | S | S | 234 | 135 | 64,3 |
| (d) | Đ | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Điện phân là một ứng dụng quan trọng của dòng điện trong việc biến đổi điện năng và hóa năng. Điện phân dung dịch NaCl có màng ngăn là phương pháp chủ đạo để sản xuất các hóa chất cơ bản như NaOH và chlorine (Cl2). Cho các phát biểu sau về quá trình điện phân dung dịch NaCl có màng ngăn, sử dụng các điện cực trơ:
(a) Tại cực dương (anode), xảy ra quá trình oxi hóa ion chloride thành khí chlorine.
(b) Tại cực âm (cathode), xảy ra quá trình khử nước tạo thành khí hydrogen và ion OH-.
(c) Dung dịch thu được trong quá trình điện phân có khả năng làm quỳ tím chuyển sang màu xanh.
(d) Màng ngăn xốp có tác dụng ngăn không cho khí Cl2 tiếp xúc và phản ứng với dung dịch NaOH.
Số phát biểu đúng là
A. 2. B. 4. C. 3. D. 1.
(Xem giải) Câu 2. Phản ứng oxi hóa không hoàn toàn ethanol bằng CuO (đun nóng) tạo ra sản phẩm hữu cơ thuộc loại
A. ketone. B. aldehyde. C. carboxylic acid. D. ester.
(Xem giải) Câu 3. Tên gọi của ester có công thức cấu tạo CH3COOCH3 là
A. methyl formate. B. vinyl acetate. C. ethyl acetate. D. methyl acetate.
(Xem giải) Câu 4. Tên gọi theo danh pháp thay thế của amino acid có công thức H2NCH2COOH là
A. aminoethanoic acid. B. glycine.
C. 2-aminopropanoic acid. D. alanine.
(Xem giải) Câu 5. Cùng với điện phân, mạ điện cũng là ứng dụng quan trọng của dòng điện trong việc biến đổi hóa năng và điện năng. Mạ điện được ứng dụng rộng rãi để bảo vệ kim loại khỏi sự ăn mòn hoặc tăng tính thẩm mỹ bằng cách phủ một lớp kim loại mỏng lên bề mặt vật dụng. Để mạ một lớp bạc (silver, Ag) lên một chiếc nhẫn bằng đồng (copper, Cu), một học sinh đề xuất sơ đồ lắp đặt: “Gắn chiếc nhẫn vào cực dương (anode) và thanh bạc nguyên chất vào cực âm (cathode) của nguồn điện một chiều, sau đó nhúng cả hai vào dung dịch silver nitrate (AgNO3)”.
Một số nhận định về đề xuất này được đưa ra như sau:
(1) Có thể thực hiện theo đề xuất này do bạc có thế điện cực chuẩn lớn hơn đồng.
(2) Có thể thực hiện theo đề xuất này vì thanh bạc ở cathode sẽ hút các ion Ag+ để tạo lớp mạ.
(3) Không thể thực hiện theo đề xuất này vì tại anode, chiếc nhẫn đồng sẽ bị oxi hóa và tan vào dung dịch thay vì được phủ lớp bạc.
(4) Không thể thực hiện theo đề xuất này do dung dịch AgNO3 sẽ phản ứng trực tiếp với chiếc nhẫn đồng tại anode.
Nhận định đúng về lỗi sai kỹ thuật trong đề xuất của học sinh là
A. nhận định (3). B. nhận định (1). C. nhận định (4). D. nhận định (2).
(Xem giải) Câu 6. Nhôm (aluminium, số hiệu nguyên tử 13) là kim loại màu trắng bạc, nhẹ (khối lượng riêng 2,7 g/cm³), dẻo, dẫn nhiệt, điện tốt và chống ăn mòn cao do có lớp oxit bảo vệ. Ở trạng thái cơ bản, cấu hình electron của nguyên tử nhôm là
A. 1s2 2s2 2p6 3s2 3p1. B. 1s2 2s2 2p6 3s3 3p1.
C. 1s2 2s2 2p6 3s2 3p2. D. 1s2 2s2 2p6 3p1 3s2.
(Xem giải) Câu 7. Cho phản ứng: H2(g) + Cl2(g) → 2HCl(g). Biết năng lượng liên kết (Eb) của H-H là 436 kJ/mol; Cl-Cl là 243 kJ/mol và H-Cl là 432 kJ/mol. Biến thiên enthalpy chuẩn của phản ứng là
A. +185 kJ. B. -185 kJ. C. -247 kJ. D. +247 kJ.
(Xem giải) Câu 8. Phản ứng nào sau đây không có sự thay thế phối tử?
A. [Fe(OH2)6]3+(aq) + 3F-(aq) → [Fe(OH2)3F3](aq) + 3H2O(l)
B. [Cr(OH2)6]3+(aq) + 6OH-(aq) → [Cr(OH)6]3-(aq) + 6H2O(l)
C. [Co(OH2)6]2+(aq) + 6NH3(aq) ⇋ [Co(NH3)6]2+(aq) + 6 H2O(l)
D. 2[Fe(CN)6]4-(aq) + Cl2(g) → 2[Fe(CN)6]3-(aq) + 2Cl-(aq)
(Xem giải) Câu 9. Các loại hợp chất hữu cơ như: aldehyde, ketone, carboxylic acid đều có nhóm nào sau đây?
A. Carboxyl. B. Carbonyl. C. Ketone. D. Aldehyde.
(Xem giải) Câu 10. Kim loại nào sau đây có độ cứng lớn nhất?
A. Al. B. Fe. C. Cu. D. Cr.
(Xem giải) Câu 11. Trong công nghiệp, hợp chất nào sau đây của kim loại kiềm được sử dụng phổ biến để làm thuốc súng, pháo hoa?
A. KNO3. B. NaOH. C. K2CO3. D. NaCl.
(Xem giải) Câu 12. Để điều chế kim loại barium (Ba) từ hợp chất BaCl2, phương pháp nào sau đây là phù hợp nhất?
A. Điện phân nóng chảy. B. Điện phân dung dịch. C. Nhiệt luyện. D. Thủy luyện.
(Xem giải) Câu 13. Cho các phát biểu sau về tính chất của amino acid:
(a) Amino acid là những hợp chất hữu cơ tạp chức.
(b) Ở điều kiện thường, các amino acid là những chất lỏng, dễ tan trong nước.
(c) Amino acid có tính chất lưỡng tính.
(d) Dung dịch glycine làm quỳ tím hóa xanh.
Số phát biểu đúng là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 14. Cho thế điện cực chuẩn của Cu2+/Cu và Zn2+/Zn lần lượt là +0,340 V và -0,763 V. Sức điện động chuẩn của pin Galvani (Zn-Cu) là
A. -0,423 V. B. 1,526 V. C. 0,423 V. D. 1,103 V.
(Xem giải) Câu 15. Cho phản ứng thuận nghịch: N2(g) + 3H2(g) ⇋ 2NH3(g) có ΔH < 0. Yếu tố nào sau đây làm cân bằng chuyển dịch theo chiều thuận?
A. Giảm áp suất. B. Tăng nhiệt độ. C. Giảm nhiệt độ. D. Giảm nồng độ N2.
(Xem giải) Câu 16. Phản ứng thuỷ phân dẫn xuất halogen có thể xảy ra theo cơ chế SN1 hoặc SN2. Đối với dẫn xuất halogen bậc 1, phản ứng xảy ra theo cơ chế SN2 là chủ yếu. Ví dụ, cơ chế phản ứng SN2 như sau:
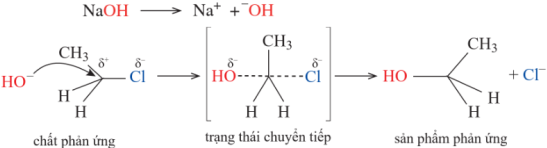
Trong các dẫn xuất halogen sau: CH3Cl, (CH3)3CCl, (CH3)2CHCH2Cl, CH3CH2CH2Cl, CH3CHClCH3, có bao nhiêu dẫn xuất khi thuỷ phân xảy ra theo cơ chế SN2 là chủ yếu?
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 17. Kim loại nào sau đây thuộc nhóm kim loại chuyển tiếp dãy thứ nhất?
A. Cu. B. K. C. Ba. D. Al.
(Xem giải) Câu 18. Phát biểu nào sau đây về saccharose là không đúng?
A. Saccharose có phản ứng tráng bạc.
B. Saccharose có phản ứng thủy phân trong môi trường acid.
C. Saccharose là một disaccharide.
D. Dung dịch saccharose hòa tan được Cu(OH)2 ở nhiệt độ thường.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Lysine là một amino acid thiết yếu đóng vai trò quan trọng trong việc duy trì hệ miễn dịch, phát triển xương và hỗ trợ sản xuất các enzyme. Lysine có điểm đẳng điện pI = 9,7 (pI là giá trị pH mà khi đó amino acid có nồng độ ion lưỡng cực là cực đại. Khi pH < pI thì amino acid đó tồn tại chủ yếu ở dạng cation, còn khi pH > pI thì amino acid đó tồn tại chủ yếu ở dạng anion).
a) Lysine thuộc loại hợp chất hữu cơ tạp chức, trong phân tử chứa hai loại nhóm chức.
b) 1 mol lysine tác dụng với tối đa 1 mol HCl trong dung dịch.
c) Trong dung dịch pH = 12,0, lysine tồn tại chủ yếu ở dạng: H2N(CH2)4CH(NH2)COO-.
d) Trong một thí nghiệm điện di ở pH = 6,0 lysine di chuyển về cực âm (cathode), còn glutamic acid (pI = 3,2) di chuyển về cực dương (anode).
(Xem giải) Câu 20. Tiến hành thí nghiệm theo các bước sau:
• Bước 1. Cho vào cốc thủy tinh 30 mL dung dịch H2SO4 0,5 M.
• Bước 2. Cho một lá nhôm và một lá đồng vào cốc sao cho chúng không tiếp xúc với nhau. Để yên khoảng 1 phút.
• Bước 3. Dùng dây dẫn điện nối lá nhôm với lá đồng với một vôn kế (như hình vẽ).
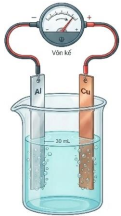
Biết: E°Al3+/Al = -1,676V; E°2H+/H2 = 0,0V; E°Cu2+/Cu = +0,340V.
a) Ở bước 3, kim vôn kế chỉ 1,336 V.
b) Ở bước 3, khí chỉ thoát ra ở bề mặt lá đồng, còn lá nhôm không có khí thoát ra.
c) Ở bước 2, lá nhôm bị ăn mòn hóa học còn lá đồng không bị ăn mòn.
d) Ở bước 3, có sự tạo thành cặp pin điện hóa, trong đó lá nhôm là cathode và lá đồng là anode.
(Xem giải) Câu 21. Trong phòng thí nghiệm, aspirin (acetylsalicylic acid) được tổng hợp từ salicylic acid và acetic anhydride theo sơ đồ:
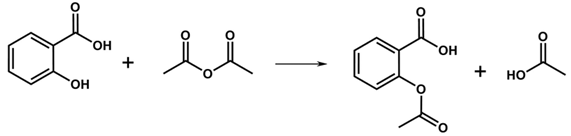
Phổ hồng ngoại (IR) của aspirin cho thấy các tín hiệu hấp thụ đặc trưng:
– Vùng 3300 – 2500 cm-1: Nhóm -OH của carboxyl.
– Vùng 1750 – 1680 cm-1: Nhóm C=O của ester và carboxyl.
a) Tín hiệu ở 1700 cm-1 đặc trưng cho liên kết C=O.
b) Trong phản ứng trên, anhydride acetic đóng vai trò là tác nhân acetyl hóa.
c) Trong thí nghiệm trên có thể thay acetic anhydride bằng acetic acid.
d) Nếu dùng 13,8 gam salicylic acid và 15,2 gam acetic anhydride (hiệu suất 80%) thì thu được 14,4 gam aspirin.
(Xem giải) Câu 22. Một nhóm học sinh tiến hành chuẩn độ dung dịch H2O2 bằng dung dịch chuẩn KMnO4 trong môi trường acid H2SO4. Phương trình phản ứng (chưa cân bằng):
KMnO4 + H2O2 + H2SO4 → MnSO4 + K2SO4 + O2 + H2O
• Bước 1: Lấy 10,00 mL dung dịch H2O2 pha loãng cho vào bình tam giác, thêm 5 mL H2SO4 2M.
• Bước 2: Chuẩn độ bằng dung dịch KMnO4 0,020 M đến khi xuất hiện màu hồng nhạt bền trong 20 giây. Thể tích KMnO4 tiêu tốn trung bình sau 3 lần chuẩn độ là 12,50 mL.
a) Khi chuẩn độ, dung dịch KMnO4 có thể được cho vào bình tam giác, còn dung dịch H2O2 được cho vào burette.
b) Nồng độ mol của dung dịch H2O2 ban đầu xác định được là 0,0625 M.
c) Trong quá trình chuẩn độ, ion MnO4- bị oxi hoá thành Mn2+.
d) Nếu không thêm H2SO4, phản ứng sẽ tạo kết tủa nâu đen MnO2.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Phân tử thuốc nhuộm Indigo có công thức khung phân tử như hình bên. Xác định tổng số nguyên tử có trong một phân tử Indigo.
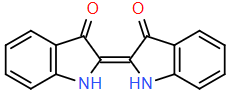
(Xem giải) Câu 24. Có bao nhiêu đồng phân cấu tạo amine ứng với công thức phân tử C4H11N?
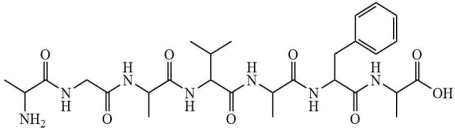
(Xem giải) Câu 25. Trong phân tử peptide cho dưới đây có bao nhiêu gốc alanine?
(Xem giải) Câu 26. Quặng argentite (sau khi đã tuyển quặng) có hàm lượng Ag2S là 86,8% (còn lại là tạp chất trơ). Từ loại quặng này người ta tách lấy kim loại Ag theo các bước sau:
• Bước 1: Xử lí quặng này với dung dịch NaCN bằng phương pháp nghiền ướt xảy ra phản ứng sau:
(1) Ag2S + 4NaCN → 2Na[Ag(CN)2] + Na2S
(2) 2NaCN + 2Na2S + 2H2O + O2 → 2NaSCN + 4NaOH
• Bước 2: Cho bột kẽm (Zn) vào dung dịch thu được xảy ra phản ứng
2Na[Ag(CN)2] + Zn → Na2[Zn(CN)4] + 2Ag
• Bước 3: Hòa tan hỗn hợp kim loại sau phản ứng trong H2SO4 loãng thu được kim loại Ag.
Biết các phản ứng xảy ra hoàn toàn, lượng Zn dùng dư 3% so với lượng cần thiết. Khi xử lí 1 tấn quặng argentite ở trên thì cần dùng bao nhiêu kg Zn? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
(Xem giải) Câu 27. Chỉ số acid (Acid Value – AV) là số miligam KOH cần thiết để trung hòa hết các acid béo tự do có trong 1 gam chất béo (dầu, mỡ). Một mẫu chất béo có chỉ số acid bằng 7. Để xà phòng hóa hoàn toàn 1 kg mẫu chất béo này cần dùng vừa đủ dung dịch chứa m gam NaOH, thu được dung dịch chỉ chứa muối stearate. Tính giá trị của m. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
(Xem giải) Câu 28. Một nhà máy sản xuất vôi sống (CaO) bằng cách nung đá vôi (CaCO3). Phản ứng nung đá vôi: CaCO3(s) → CaO(s) + CO2(g) có ![]() = +178 kJ.
= +178 kJ.
Để cung cấp nhiệt cho phản ứng nung 1 tấn đá vôi (chứa 90% CaCO3 về khối lượng, còn lại là tạp chất trơ), nhà máy sử dụng than đá (chứa 95% carbon, còn lại là tạp chất không cháy). Biết hiệu suất sử dụng nhiệt là 80%. Tính khối lượng than đá tối thiểu cần dùng (kg). Biết nhiệt đốt cháy của carbon là -393,5 kJ/mol. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).


Bình luận