[2026] Thi thử TN sở GDĐT Thanh Hóa (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 108
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3D | 4B | 5B | 6A | 7A | 8A | 9A |
| 10D | 11C | 12D | 13C | 14C | 15B | 16D | 17A | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | S | S | Đ | Đ |
| (b) | S | Đ | Đ | Đ |
| (c) | Đ | Đ | S | S |
| (d) | Đ | S | S | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 3 | 71 | 51 | 1235 | 2 | 273 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Liên kết trong mạng tinh thể kim loại là loại liên kết nào sau đây?
A. Ion. B. Cộng hoá trị. C. Kim loại. D. Van der Waals.
(Xem giải) Câu 2. Để có được bơ thực vật từ dầu thực vật người ta thực hiện quá trình
A. làm lạnh. B. xà phòng hóa.
C. hydrogen hóa. D. oxi hóa bởi oxygen không khí.
(Xem giải) Câu 3. Tên gọi của ester CH3COOCH2CH3 là
A. ethyl formate. B. methyl acetate.
C. methyl propionate. D. ethyl acetate.
(Xem giải) Câu 4. Ở trạng thái cơ bản, aluminium có cấu hình electron 1s2 2s2 2p6 3s2 3p1. Số elelctron lớp ngoài cùng của nguyên tử aluminium là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 5. Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tại đó
A. phản ứng hoá học không xảy ra nữa.
B. tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
C. tốc độ phản ứng thuận nhỏ hơn tốc độ phản ứng nghịch.
D. nồng độ các chất bằng nhau.
(Xem giải) Câu 6. Cho bảng thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
| Cặp oxi hóa – khử | Al3+/Al | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Ag+/Ag |
| Thế điện cực chuẩn (V) | -1,66 | -0,76 | -0,44 | +0,34 | +0,80 |
Một pin Galvani được thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên có sức điện động chuẩn là 2,46V. Hai cặp oxi hóa – khử hình thành pin lần lượt là
A. Al3+/Al và Ag+/Ag. B. Al3+/Al và Cu2+/Cu.
C. Fe2+/Fe và Cu2+/Cu. D. Zn2+/Zn và Al3+/Al.
(Xem giải) Câu 7. Chất thải nhựa, túi nylon,… gây ảnh hưởng nghiêm trọng đến môi trường còn gọi là “ô nhiễm trắng”. Giải pháp nào sau đây không giúp giảm thiểu tác động của rác thải nhựa, túi nylon,… đến môi trường?
A. Tiêu huỷ các chất thải nhựa và túi nylon bằng phương pháp đốt hoặc chôn lấp.
B. Thay thế túi lylon bằng túi giấy, túi vải tái sử dụng nhiều lần.
C. Tái sử dụng đồ nhựa, chai nhựa làm đồ dùng.
D. Phân loại rác thải nhựa từ đầu nguồn để tái chế.
(Xem giải) Câu 8. Propene tác dụng với dung dịch HBr tạo ra hai dẫn xuất bromo là CH3-CHBr-CH3 (sản phẩm chính) và CH3-CH2-CH2Br (rất ít). Giai đoạn (1) trong cơ chế phản ứng này có sự tạo thành các tiểu phân trung gian là carbocation I và carbocation II như sau:
CH3-CH=CH2 + H+ → (CH3)2HC+ (carbocation I)
CH3-CH=CH2 + H+ → CH3-CH2-H2C+ (carbocation II)
Trong giai đoạn (1) này, CH3‒CH=CH2 là chất phản ứng, H+ là tác nhân. Ở giai đoạn (2), ion Br‒ sẽ kết hợp với các tiểu phân trung gian tạo thành sản phẩm. Phát biểu nào dưới đây đúng?
A. Carbocation I bền hơn carbocation II.
B. Trong giai đoạn (1), khi phân cắt liên kết π, cặp electron được chia đều cho mỗi nguyên tử carbon.
C. Ở giai đoạn (2), ion Br‒ chỉ kết hợp với carbocation I mà không kết hợp được với carbocation II.
D. Ion H+ là tác nhân giàu electron, có khả năng nhường electron cho liên kết π.
(Xem giải) Câu 9. Chất nào sau đây là amine?
A. C6H5NH2. B. CH3COOCH3. C. CH3COOH. D. CH3OH.
(Xem giải) Câu 10. Phổ hồng ngoại (IR) của hợp chất hữu cơ (X) có công thức phân tử là CH4O được cho như hình bên dưới.

Chất này thường được dùng trong công nghiệp để làm chất chống đông, làm dung môi trong nước rửa kính xe, chất tẩy rửa sơn, mực in máy photocopy và làm nhiên liệu cho các bếp lò loại nhỏ… Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O–H (alcohol) | O–H (carboxylic acid) | C=O (ester, carboxylic acid) |
| Số sóng (cm⁻¹) | 3650 – 3200 | 3300 – 2500 | 1780 – 1650 |
Chỉ ra peak nào có thể dự đoán được chất (X) là một alcohol?
A. Peak (4). B. Peak (3). C. Peak (2). D. Peak (1).
(Xem giải) Câu 11. Chất nào sau đây không thể tạo được liên kết hydrogen?
A. CH3NH2. B. C2H5OH. C. C6H6. D. CH3COOH.
(Xem giải) Câu 12. Hợp chất nào sau đây là thành phần chính trong phân bón superphosphate?
A. KCl. B. CaSO4.2H2O. C. NaNO3. D. Ca(H2PO4)2.
(Xem giải) Câu 13. Trong ăn mòn điện hóa, nhận định nào sau đây là đúng?
A. Ở cực dương có quá trình oxi hóa.
B. Ở cực âm có xảy ra quá trình khử.
C. Ở cực âm có xảy ra quá trình oxi hóa, kim loại bị ăn mòn.
D. Ở cực dương có xảy ra quá trình oxi hóa, kim loại bị ăn mòn.
(Xem giải) Câu 14. Khử CH3COCH3 bằng LiAlH4 thu được sản phẩm là
A. ethanal. B. propan-1-ol. C. propan-2-ol. D. acetone.
(Xem giải) Câu 15. Nước cứng gây nhiều trở ngại cho đời sống thường ngày. Các nguồn nước ngầm hoặc nước ao hồ, sông suối thường có độ cứng cao bởi quá trình hòa tan nhiều các ion Ca2+, Mg2+ có trong thành phần của lớp trầm tích đá vôi. Cho các phát biểu sau:
(a) Có thể dùng Na2CO3 để làm mềm nước cứng.
(b) Nước cứng làm cho xà phòng có ít bọt, giảm khả năng giặt rửa của xà phòng.
(c) Nước tự nhiên có chứa ion Ca2+, Mg2+, HCO3- gọi là nước có tính cứng vĩnh cửu.
(d) Để loại bỏ lớp cặn trong ấm đun nước lâu ngày có thể dùng dung dịch giấm ăn.
Số phát biểu đúng là
A. 2. B. 3. C. 1. D. 4.
(Xem giải) Câu 16. Tinh bột là polymer thiên nhiên, gồm
A. dextrin và maltose. B. saccharose và maltose.
C. glucose và fructose. D. amylose và amylopectin.
(Xem giải) Sử dụng thông tin cho dưới đây để trả lời các câu 17 – 18:
Trong dung dịch, ion kim loại Cu2+ thường tồn tại dưới dạng phức chất aqua [Cu(OH2)6]2+ có màu xanh. Khi thêm dung dịch ammonia NH3 dư vào dung dịch copper(II) sulfate, ban đầu xuất hiện kết tủa xanh nhạt là [Cu(OH)2(OH2)4], sau đó kết tủa tan dần tạo thành dung dịch phức chất [Cu(NH3)4(OH2)2]2+ có màu xanh lam.
Câu 17. Khi thay thế các phối tử H2O bằng NH3, màu của dung dịch chuyển từ xanh nhạt sang xanh lam. Nhận định nào sau đây là đúng về sự thay đổi này?
A. Đây là phản ứng thế phối tử, phối tử NH3 có khả năng liên kết mạnh hơn H2O với ion Cu2+.
B. Đây là phản ứng oxi hóa – khử, trong đó số oxi hóa của Cu thay đổi từ +2 sang 0.
C. Dung dịch xanh lam được hình thành là do sự tạo thành của muối ammonium sulfate.
D. Khi tạo phức chất [Cu(NH3)4(OH2)2]2+ từ [Cu(OH)2(OH2)4] thì có hai phối tử nước bị thay thế bằng phối tử NH3 .
Câu 18. Cho các phát biểu sau liên quan đến thí nghiệm trên:
(a) Phức chất [Cu(NH3)4(OH2)2]2+ có nguyên tử trung tâm là Cu.
(b) Trong phức chất [Cu(NH3)4(OH2)2]2+, số liên kết cho – nhận giữa phối tử với ion trung tâm là 6.
(c) Phân tử NH3 và H2O đóng vai trò là các phối tử trong các phức chất nêu trên.
(d) Quá trình hòa tan kết tủa Cu(OH)2 bởi dung dịch NH3 dư minh chứng NH3 có tính base mạnh hơn H2O.
Số phát biểu đúng là
A. 3. B. 2. C. 4. D. 5.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Một loại bột thạch cao có lượng nước tiêu chuẩn là 68 – 72% (là tỷ lệ khối lượng nước so với khối lượng bột thạch cao khi sử dụng). Sau khi thêm nước vào bột thạch cao trên và trộn đều thành hồ nhão có công thức hóa học là G.xH2O, sau một khoảng thời gian ngắn sẽ đông cứng lại.
a) Lượng nước cần thêm vào khi sử dụng 50 kg bột thạch cao trên khoảng từ 34L – 63L (Biết D nước = 1g/mL), tỉ lệ này giúp bột thạch cao đạt được độ dẻo tối ưu để đổ khuôn hoặc trát tường trước khi đông cứng hoàn toàn.
b) Biết thành phần phần trăm theo khối lượng của sulfur trong G.xH2O là 18,6%. Giá trị của x là 3. (Kết quả được làm tròn đến hàng đơn vị)
c) Hàm lượng phần trăm theo khối lượng của O trong G.xH2O là 55,8% (kết quả được làm tròn đến hàng phần mười).
d) Muối G trong thành phần hồ nhão là CaSO4.
(Xem giải) Câu 20. Cho các chất X, Y, Z, T được xếp không theo thứ tự gồm: CH3COOH, C2H5OH, CH3CHO, C3H8. Nhiệt độ sôi (°C) của chúng được cho trong bảng sau:
| Chất | X | Y | Z | T |
| Nhiệt độ sôi (°C) | -42,1 | 21,0 | 78 | 118 |
a) Trong công nghiệp, chất Y được điều chế trực tiếp từ việc oxi hóa không hoàn toàn chất Z bằng CuO nung nóng.
b) Chất T có nhiệt độ sôi cao nhất vì giữa các phân tử T tạo được liên kết hydrogen liên phân tử bền vững nhất, T là CH3COOH.
c) Ở điều kiện thường, chất X và Y tồn tại ở trạng thái khí. X là C3H8, Y là CH3CHO.
d) Lên men 100 lít rượu thực phẩm 8° (chứa chất Z, DZ = 0,8 g/mL) với hiệu suất 92% để sản xuất giấm ăn (chứa chất T). Giả thiết không có sự thất thoát nước và cho biết D nước = 1g/mL. Nồng độ % của chất T trong dung dịch sau lên men là 7,63% (kết quả chỉ làm tròn ở phép tính cuối cùng và làm tròn đến hàng phần trăm).
(Xem giải) Câu 21. Cho phản ứng tổng hợp polymer sau:

Polymer tạo thành được sử dụng làm sợi aramide, một loại sợi rất bền. Khi bện thành sợi aramide, các mạch polymer sẽ liên kết với nhau bằng các liên kết hydrogen được biểu diễn như sau: N-H•••O=C. Trong đó, N và O là các nguyên tử ở hai mạch polymer cạnh nhau.
a) Liên kết hydrogen giữa các mắt xích làm tăng độ bền của sợi aramide.
b) Polymer tạo nên sợi aramide thuộc loại polyamide.
c) Phản ứng trên thuộc loại phản ứng trùng hợp.
d) Phần trăm theo khối lượng của carbon trong polymer tạo sợi aramide là 72,0%.
(Xem giải) Câu 22. Một học sinh tiến hành điện phân dung dịch NaCl trong phòng thí nghiệm như sau:
+ Chuẩn bị:
Hoá chất: dung dịch NaCl bão hoà, cánh hoa màu hồng, dung dịch phenolphtalein.
Dụng cụ: nguồn điện một chiều (3 – 6 vôn), cốc thuỷ tinh 100 mL, hai điện cực than chì, dây dẫn, kẹp kim loại.
+ Tiến hành:
• Bước 1: Lắp thiết bị thí nghiệm điện phân dung dịch NaCl với điện cực trơ như hình dưới:
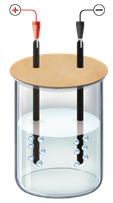
• Bước 2: Rót khoảng 80 mL dung dịch NaCl bão hòa vào cốc rồi nhúng hai điện cực than chì vào dung dịch.
• Bước 3: Nối hai điện cực than chì với hai cực của nguồn điện và tiến hành điện phân trong khoảng 5 phút.
• Bước 4: Cho một mẩu cánh hoa màu hồng vào cốc chứa khoảng 5 mL dung dịch sau điện phân.
a) Sau bước 4, cánh hoa màu hồng bị mất màu do dung dịch thu được là nước Javel có tính tẩy màu.
b) Nếu thêm vài giọt dung dịch phenolphthalein vào cốc khi tiến hành điện phân ở bước 3, màu của dung dịch tại khu vực xung quanh cực âm (cathode) sẽ chuyển sang màu hồng.
c) Việc đậy nắp cốc trong quá trình điện phân chủ yếu nhằm mục đích duy trì nồng độ NaCl bão hòa để tốc độ phản ứng không bị giảm theo thời gian.
d) Ở bước 3, tại cực dương (anode) xảy ra quá trình oxi hóa ion Cl-, giải phóng khí chlorine (Cl2) nên có hiện tượng sủi bọt khí.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho các phát biểu về tính chất hoá học của dung dịch methylamine:
(1) Làm quỳ tím hóa hồng.
(2) Phản ứng với HCl tạo thành CH3NH3Cl.
(3) Hoà tan Cu(OH)2 tạo thành dung dịch màu xanh lam.
(4) Phản ứng với HNO3 ở nhiệt độ thường tạo thành CH3OH.
(5) Phản ứng với FeCl3 tạo thành kết tủa Fe(OH)3.
Số phát biểu đúng là bao nhiêu?
(Xem giải) Câu 24. Khi tiêu thụ các loại thực phẩm và đồ uống thì carbohydrate, protein và chất béo sẽ cung cấp năng lượng cho cơ thể. Hình bên là nhãn thực phẩm trên một loại coffee đóng chai.

Dưới đây là giá trị nhiên liệu của một số chất có trong chai coffee. Giá trị nhiên liệu là năng lượng giải phóng khi đốt cháy hoàn toàn 1 gam chất.
| Chất | Giá trị nhiên liệu (kJ/g) |
| Carbohydrate | 17 |
| Protein | 17 |
| Chất béo | 38 |
Giả sử, trong quá trình học tập, một học sinh tiêu thụ trung bình 7 kJ năng lượng mỗi phút thì hoạt động này có thể được duy trì trong bao nhiêu phút từ năng lượng thu được trong một khẩu phần coffee đóng chai? (kết quả được làm tròn đến hàng đơn vị).
(Xem giải) Câu 25. Vitamin A là một chất dinh dưỡng thiết yếu cho con người. Trong thực phẩm, vitamin A tồn tại ở dạng chính là retinol (chứa C, H, O). Trong phân tử retinol, phần trăm về khối lượng nguyên tố carbon và oxygen lần lượt là 83,916% và 5,594%. Biết phổ khối lượng của retinol có giá trị m/z lớn nhất bằng 286. Tính tổng số nguyên tử có trong một phân tử retinol.
(Xem giải) Câu 26. Sự kết hợp giữa aspartic acid và phenylalanine tạo thành peptide, peptide này có thể được chuyển đổi thành methyl ester gọi là aspartame. Công thức của aspatic acid, phenylalanine và aspartame được cho dưới đây:
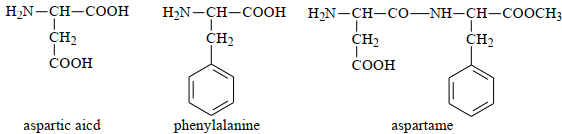
Aspartame là một loại chất tạo ngọt nhân tạo không chứa saccharide nên được sử dụng trong thực phẩm không đường dành cho người bị tiểu đường. Ở nhiệt độ trên 30°C aspartame bị phân hủy tạo ra các amino acid tự do không có vị ngọt. Cho các nhận định sau:
(1) Tên thay thế của aspartic acid là 2-aminobutane-1,4-dioic acid.
(2) Biết ở pH = 2,98, aspartic acid chủ yếu ở dạng ion lưỡng cực có tổng điện tích bằng không. Tại pH = 7,0, khi đặt vào một điện trường, aspatic acid sẽ di chuyển về phía cực dương (+).
(3) Aspartame có công thức phân tử là C14H18N2O5.
(4) Có thể sử dụng aspartame để thay thế đường saccharose trong quá trình làm các loại bánh nướng ở nhiệt độ cao.
(5) Aspartame không có khả năng tạo thành sản phẩm màu tím đặc trưng với thuốc thử biuret.
Liệt kê các nhận định đúng theo số thứ tự tăng dần? (Ví dụ: 1234, 24,…).
(Xem giải) Câu 27. Số alkyne có công thức phân tử C5H8 tác dụng được với dung dịch AgNO3 trong NH3 (dư) thu được kết tủa là bao nhiêu?
(Xem giải) Câu 28. Theo QCVN 01-1:2018/BYT, hàm lượng sắt tối đa cho phép trong nước sinh hoạt là 0,30 mg/L. Một mẫu nước dùng nghiên cứu có hàm lượng sắt cao gấp 44,8 lần ngưỡng cho phép. Giả thiết sắt trong mẫu nước tồn tại ở dạng Fe2(SO4)3 và FeSO4 với tỉ lệ mol tương ứng là 1 : 8. Nếu phải tách sắt có trong 10 m³ loại nước trên về ngưỡng cho phép, thì cần sử dụng m gam vôi tôi để tăng pH, sau đó sục không khí theo các phản ứng sau:
(1) 4FeSO4 + 4Ca(OH)2 + O2 + 2H2O → 4Fe(OH)3 + 4CaSO4
(2) Fe2(SO4)3 + 3Ca(OH)2 → 2Fe(OH)3 + 3CaSO4
Giả thiết lượng Ca(OH)2 đã phản ứng bằng 70% khối lượng vôi tôi cần đưa vào, ngoài ra không còn chất nào tham gia phản ứng với các muối sắt. Tính giá trị của m (làm tròn đến hàng đơn vị).

Bình luận