[2025] Thi thử TN sở GDĐT Quảng Nam (Lần 1 – Đề 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 074
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2D | 3B | 4A | 5B | 6A | 7B | 8A | 9B |
| 10B | 11B | 12B | 13B | 14D | 15D | 16C | 17C | 18A |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | S | S | Đ | 2 | 2 | 4,7 |
| (b) | S | Đ | Đ | Đ | 26 | 27 | 28 |
| (c) | S | S | S | S | 4 | 24 | 6,77 |
| (d) | Đ | S | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Trong cây mía, củ cải đường, quả thốt nốt có chứa loại đường nào sau đây?
A. Saccharose. B. Maltose. C. Fructose. D. Glucose.
(Xem giải) Câu 2: Đất sét polymer là một loại đất sét dựa trên poly(vinyl chloride) (PVC). Đất sét polymer không chứa khoáng chất đất sét, nhưng khi trộn PVC với một chất lỏng sẽ thu được vật liệu giống như đất sét; do đó, thường được gọi là đất sét và được dùng để làm đồ chơi, đồ thủ công, đồ trang trí. Các ứng dụng này dựa trên tính chất nào của PVC?
A. Tính cứng. B. Tính không độc hại. C. Tính đàn hồi. D. Tính dẻo.
(Xem giải) Câu 3: Trong pin Gavani Zn-Cu,
A. điện cực cathode là Zn. B. điện cực anode là Zn.
C. điện cực âm là Cu. D. điện cực anode là Cu.
(Xem giải) Câu 4: Từ giữa thế kỷ 18, chloroform chủ yếu sử dụng làm chất gây mê. Hơi chloroform ảnh hưởng đến hệ thần kinh trung ương của người bệnh, gây ra chóng mặt, mỏi mệt và ngất, cho phép bác sĩ phẫu thuật. Công thức phân tử chloroform là
A. CHCl3. B. CCl4. C. CH2Cl2. D. CH3Cl.
(Xem giải) Câu 5: Cho bảng giá trị enthalpy tạo thành chuẩn của một số chất sau: butane khí (1); octane lỏng (2); propane khí (3); methane khí (4)
| Chất | C8H18(l) | C3H8(g) | C4H10(g) | CH4(g) | CO2(g) | H2O(g) |
| ∆fHo298 (kJ/mol) | -250,1 | -103,8 | -126,15 | -74,87 | -393,5 | -241,8 |
Một khu dân cư sử dụng khoảng 1,0.10¹¹ kJ năng lượng mỗi ngày. Giả sử, tất cả năng lượng đó đến từ quá trình đốt cháy một trong các nhiên liệu sau: octane lỏng (C8H18) hoặc khí propane (C3H8) hoặc butane (C4H10) hoặc khí methane (CH4) để tạo thành hơi nước và khí carbon dioxide. Dựa vào lượng khí CO2 (mol) phát thải khi tiêu thụ một nhiên liệu có thể đánh giá mức độ ảnh hưởng của nhiên liệu đó đến sự nóng lên toàn cầu. Mức độ ảnh hưởng đến sự nóng lên toàn cầu của các loại nhiên liệu trên theo chiều hướng tăng dần là
A. (2) < (4) < (3) < (1). B. (4) < (3) < (1) < (2).
C. (2) < (1) < (3) < (4). D. (1) < (3) < (4) < (2).
(Xem giải) Câu 6: Pin mặt trời bao gồm nhiều tế bào quang điện làm biến đối năng lượng ánh sáng thành năng lượng điện. Nhược điểm của loại pin này là
A. chi phí trang bị quá cao. B. thân thiện với môi trường.
C. khó di chuyển. D. thời gian sử dụng dài.
(Xem giải) Câu 7: Nước cứng không gây ra tác hại nào dưới đây?
A. Làm hỏng các dung dịch pha chế, làm thực phẩm lâu chín và giảm mùi vị thực phẩm.
B. Gây ngộ độc nước uống.
C. Làm mất tính tẩy rửa của xà phòng, làm hư hại quần áo.
D. Gây hao tốn nhiên liệu và không an toàn cho các nồi hơi, làm tắc các đường ống dẫn nước.
(Xem giải) Câu 8: Các nhà nghiên cứu thuộc Viện Công nghệ sinh học và Công nghệ Nano (IBN) của Singapore vừa phát hiện một sơ đồ hóa học mới có thể chuyển hóa đường glucose thành adipic acid như sau:
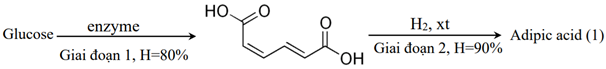
Trong công nghiệp, adipic acid được dùng để sản xuất poly(hexamethylene adipamide) qua phản ứng trùng ngưng giữa hexamethylenediamine và adipic acid với hiệu suất đạt 90%.
Có các phát biểu sau:
(a) Poly(hexamethylene adipamide) thuộc loại tơ polyamide.
(b) Poly(hexamethylene adipamide) kém bền với acid và kiềm.
(c) Poly(hexamethylene adipamide) có tên gọi khác là nylon-6,6.
(d) Lượng adipic acid được tạo từ 225 kg glucose theo sơ đồ (1) có thể sản xuất được 179 kg chỉ nha khoa. Biết rằng chỉ nha khoa chứa 92% về khối lượng poly (hexamethylene adipamide).
Các phát biểu đúng là
A. (a), (b), (c). B. (b), (c), (d). C. (a), (b), (c), (d). D. (a), (b), (d).
(Xem giải) Câu 9: Loại polymer nào sau đây thuộc loại tơ?
A. PVC. B. Nylon-6,6. C. Cao su buna. D. PS.
(Xem giải) Câu 10: M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
– Ở trạng thái cơ bản, nguyên tử M có 1 electron ở lớp ngoài cùng.
– Trong hợp chất, số oxi hóa phổ biến của nguyên tố M là +2.
M là nguyên tố nào sau đây?
A. Ni. B. Cu. C. Mn. D. Fe.
(Xem giải) Câu 11: Muối nào sau đây có độ tan lớn nhất trong các muối sau?
A. BaSO4. B. MgSO4. C. CaCO3. D. MgCO3.
(Xem giải) Câu 12: Ester ethyl propionate có mùi thơm của quả dứa chín. Công thức của ethyl propionate là
A. C2H5COOC6H5. B. C2H5COOC2H5. C. C2H3COOC2H5. D. CH3COOC2H5.
(Xem giải) Câu 13: Cảnh sát giao thông sử dụng các dụng cụ phân tích ethanol (rượu ethylic) có chứa CrO3. Khi tài xế hà hơi thở vào dụng cụ phân tích trên, nếu trong hơi thở có chứa hơi rượu thì hơi rượu sẽ tác dụng với CrO3 có màu da cam và biến thành Cr2O3 có màu xanh lục tối theo phản ứng hóa học sau:
CrO3 (màu đỏ đậm) + C2H5OH → Cr2O3 (màu lục tối) + CH3COOH + H2O
Có các phát biểu sau:
(a) Dựa vào sự biến đổi màu sắc mà dụng cụ phân tích sẽ thông báo cho cảnh sát biết được mức độ sử dụng rượu của tài xế.
(b) Trong phản ứng trên C2H5OH là chất khử.
(c) Người tham gia giao thông bằng các phương tiện giao thông đường bộ là ô tô, xe mô tô, xe gắn máy, máy kéo, xe máy chuyên dùng hay xe đạp, xe đạp máy đều có thể bị Cảnh sát giao thông tạm giữ xe vì lỗi vi phạm nồng độ cồn theo Nghị định 168/2024/NĐ-CP của Chính phủ quy định.
(d) Một lái xe thổi 50 mL khí thở vào máy đo nồng độ cồn, thấy tạo ra 0,0912 miligam chất rắn màu lục tối. Nồng độ cồn có trong khí thở của lái xe đó là 0,552 miligam/lít.
Các phát biểu đúng là
A. (b), (c), (d). B. (a), (b), (c). C. (a), (c), (d). D. (a), (b), (c), (d).
(Xem giải) Câu 14: Một nhóm học sinh được giao nhiệm vụ khảo sát sự thay đổi tốc độ phản ứng của calcium carbonate với dung dịch hydrochloric acid theo thời gian. Nhóm học sinh đã tiến hành thí nghiệm như sau: Cho 4 gam calcium carbonate (dạng bột) phản ứng với 100 mL dung dịch HCl 0,1M. Thể tích khí carbon dioxide được đo và ghi lại trong bảng sau:
| Thời gian (giây) | 30 | 60 | 90 | 120 | 150 | 180 | 210 | 240 |
| Thể tích khí CO2 (mL) | 40 | 70 | 87 | 101 | 109 | 115 | 119 | 119 |
Cho các phát biểu sau:
(a) Tốc độ phản ứng thay đổi theo thời gian vì số va chạm giữa các chất phản ứng ít dần.
(b) Với kết quả thí nghiệm trên, có thể kết luận thời gian phản ứng càng tăng thì thể tích khí carbon dioxide tạo ra càng nhiều.
(c) Phản ứng giữa calcium carbonate với dung dịch hydrochloric acid đã dừng lại sau 240 giây.
(d) Phản ứng dừng lại vì calcium carbonate phản ứng hết.
Các phát biểu đúng là
A. (a), (c). B. (a), (b). C. (a), (d). D. (a).
(Xem giải) Câu 15: Ammonia có nhiều ứng dụng quan trọng trong đời sống và sản xuất. Trong công nghiệp, ammonia được tổng hợp từ nitrogen và hydrogen theo phương trình phản ứng: N2(g) + 3H2(g) ⇋ 2NH3(g) (1)
Kết quả nghiên cứu sự phụ thuộc của hiệu suất phản ứng tổng hợp ammonia vào áp suất và nhiệt độ được thể hiện trong giản đồ sau:
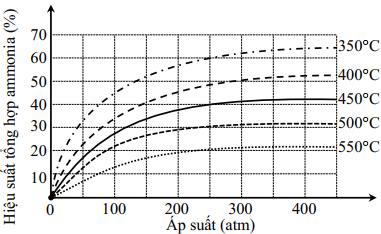
Cho các phát biểu sau:
(a) Hiệu suất của phản ứng ở 500°C, 300 atm cao hơn hiệu suất ở 450°C, 200 atm.
(b) Khi tăng áp suất thì cân bằng của phản ứng (1) chuyển dịch theo chiều thuận.
(c) Phản ứng (1) thực hiện ở nhiệt độ cao nên là phản ứng thu nhiệt.
(d) Ở nhiệt độ 500°C, 250 atm, 2 mol N2 tác dụng với 3 mol H2 thu được 0,6 mol NH3.
Các phát biểu đúng là
A. (a), (c). B. (b), (c). C. (a), (b). D. (b), (d).
(Xem giải) Câu 16: Khi bị ốm, mất sức hoặc sau các ca phẫu thuật, nhiều người bệnh thường được truyền dịch để cơ thể sớm hồi phục. Chất trong dịch truyền có tác dụng trên là
A. saccharose. B. sodium chloride. C. glucose. D. amine.
(Xem giải) Câu 17: Thế điện cực chuẩn (E°M3+/M2+) của các kim loại Cr, Mn, Fe và Co lần lượt là -0,408V; 1,57V; 0,771V và 1,97V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất?
A. Mn. B. Fe. C. Cr. D. Co.
(Xem giải) Câu 18: Tính chất và đại lượng nào sau đây của kim loại kiềm biến đổi theo xu hướng rõ rệt?
A. Tính khử, bán kính nguyên tử, độ cứng, nhiệt độ nóng chảy.
B. Giá trị thế điện cực chuẩn, bán kính nguyên tử, độ cứng.
C. Tính oxi hóa, khối lượng riêng, nhiệt độ nóng chảy.
D. Tính khử, khối lượng riêng, độ cứng, nhiệt độ nóng chảy.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Trong vỏ Trái Đất, sắt và nhôm là hai nguyên tố kim loại có hàm lượng cao hơn so với các nguyên tố kim loại khác.
a. Sắt hoặc nhôm đều được sử dụng với vai trò là kim loại cơ bản trong sản xuất các hợp kim nặng.
b. Từ quặng bauxite sẽ tách được sắt bằng phương pháp điện phân.
c. Khi tráng một lớp kẽm lên đinh thép sẽ hạn chế được sự ăn mòn sắt trong thép theo phương pháp điện hóa.
d. Nhiệt độ cần để tái chế thép cao hơn nhiệt độ cần để tái chế nhôm.
(Xem giải) Câu 20: Một nhóm học sinh tiến hành thí nghiệm về ăn mòn của kim loại (đinh thép). Nhóm học sinh đưa ra giả thuyết: “Sự ăn mòn kim loại không xảy ra hoặc xảy ra nhanh hay chậm chỉ phụ thuộc vào các chất có trong môi trường”
Thí nghiệm được tiến hành theo các bước sau:
– Rót dung dịch sodium chloride (NaCl) bão hòa vào cốc 1, cốc 2, cốc 3, dầu nhờn (bản chất là hỗn hợp các hydrocarbon) vào cốc 4.
– Cho một đinh thép vào cốc 1 và cốc 4, cho đinh thép được quấn bởi dây kẽm (Zn) vào cốc 2, cho đinh thép được quấn dây đồng (Cu) vào cốc 3 (các đinh thép là thép carbon thường và đã được làm sạch bề mặt).
Các bước được minh họa như hình vẽ dưới đây:
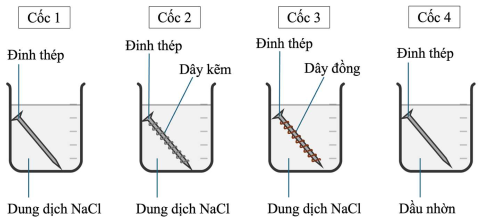
Để 4 cốc trong không khí sau 5 ngày, kết quả thí nghiệm được nhóm học sinh ghi lại theo bảng sau:
| STT | Cốc 1 | Cốc 2 | Cốc 3 | Cốc 4 |
| Hiện tượng | Cây đinh bị gỉ; có lớp chất rắn màu đỏ bám lên trên đinh sắt. | Dây kẽm bị ăn mòn, cây đinh gần như không bị ăn mòn. | Cây đinh bị gỉ. dây đồng hầu như không bị ăn mòn. | Không có hiện tượng |
a. Ở cốc 1, khi nhúng đinh vào nước muối, sắt bị ăn mòn hóa học.
b. Ở cốc 2, khi quấn kẽm vào đinh thép rồi ngâm chúng trong dung dịch NaCl, xuất hiện hiện tượng ăn mòn điện hóa, kẽm có tính khử mạnh hơn sắt nên kẽm bị ăn mòn, do đó đinh thép được bảo vệ.
c. Quấn một dây đồng quanh đinh thép là cách để chống ăn mòn đinh thép trong môi trường có chất điện li.
d. Với kết quả thí nghiệm như trên, giả thuyết của nhóm học sinh là đúng.
(Xem giải) Câu 21: Hai ống nghiệm (1) và (2) đều chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Tiến hành hai thí nghiệm sau ở 20°C.
• Thí nghiệm 1: Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc (nồng độ khoảng 11M) không màu vào ống nghiệm (1) thu được dung dịch Y có màu vàng chanh, do có quá trình:
[Cu(OH2)6]2+(aq) + 4Cl-(aq) ⇌ [CuCl4]2-(aq) + 6H2O(l) Kc = 4,18.10^5 (1)
• Thí nghiệm 2: Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride bão hòa (nồng độ khoảng 5,3M) không màu vào ống nghiệm (2) thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
a. Trong thí nghiệm (1), phức chất [CuCl4]2- kém bền hơn phức chất [Cu(OH2)6]2+.
b. Trong thí nghiệm (2), không có dấu hiệu của phản ứng hình thành phức chất.
c. Khả năng thay thế phối tử trong phức chất [Cu(OH2)6]2+ không phụ thuộc vào nồng độ của ion Cl- trong dung dịch mà phụ thuộc vào tính acid mạnh của hydrochloric acid.
d. Khi cho dung dịch HCl có nồng độ khoảng 5,3M vào dung dịch copper(II) sulfate 0,5% thì không quan sát thấy dấu hiệu của phản ứng tạo thành phức chất [CuCl4]2-.
(Xem giải) Câu 22: Thủy phân hoàn toàn tripeptide X (xúc tác enzyme) thu được dung dịch Y chứa các amino acid gồm: Glu, Gly và Lys. Điều chỉnh dung dịch Y về pH = 6, tại đó các amino acid tồn tại dưới dạng sau: +H3N[CH2]4CH(NH3+)COOH (Lys), +H3NCH2COO- (Gly) và -OOC[CH2]2CH(NH2)COO- (Glu).
a. Ở điều kiện thường, các amino acid Glu, Gly và Lys đều là chất rắn, không màu khi ở dạng kết tinh.
b. Trong các amino acid Glu, Gly và Lys, có 1 chất làm quỳ tím hóa xanh.
c. Có 2 amino acid trong hỗn hợp Y bị dịch chuyển về phía cực dương.
d. X có 3 công thức cấu tạo thỏa mãn và X tạo được hợp chất màu vàng với nitric acid.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Thủy phân một chất béo X (trong môi trường acid) thu được stearic acid và palmitic acid có tỉ lệ mol 2 : 1 và glycerol. Số đồng phân cấu tạo của X thỏa mãn đặc điểm trên?
(Xem giải) Câu 24: Cho các chất sau: glucose, fructose, maltose, saccharose và tinh bột. Trong số các chất trên, có bao nhiêu chất vừa tạo hợp chất màu xanh lam với Cu(OH)2/NaOH, vừa tạo kết tủa Ag với thuốc thử Tollens và làm mất màu nước bromine?
(Xem giải) Câu 25: Hấp phụ là khả năng của vật liệu tạo liên kết và giữ các chất trên bề mặt của nó. Đốt vỏ trấu trong điều kiện yếm khí (thiếu oxygen) thu được phần bã rắn gọi là than tồn tính. Loại than này có cấu trúc xốp, diện tích bề mặt lớn nên có khả năng hấp phụ cao. Để đánh giá khả năng hấp phụ ion kim loại chì của than tồn tính so với cát, một nhóm học sinh đã cho nước nhiễm ion kim loại chì chảy qua vật liệu hấp phụ (100 gam cát hoặc 100 gam cát và 15 gam than tồn tính) theo sơ đồ thiết bị dưới đây với tốc độ dòng chảy 0,33 lít/phút. Phần nước ra (xem trong sơ đồ 1) được lấy mang đi phân tích là phần nước sau cùng sau khi cho lượng nước nhiễm ion kim loại chì chảy qua hệ lần lượt là 0 lít (nước chưa xử lí), 4 lít, 8 lít, 12 lít, 16 lít. Mức độ hấp phụ (A%) được tính bằng tỉ lệ phần trăm khối lượng ion kim loại chì đã hấp phụ so với lượng ion kim loại chì có trong dung dịch ban đầu. Kết quả thu được như sau
| Thể tích nước nhiễm chì được xử lí | 0 lít | 4 lít | 8 lít | 12 lít | 16 lít |
| Mức độ hấp phụ của cát (A1%) | 16,7 | 10,3 | 9,1 | 3,7 | |
| Mức độ hấp phụ của hỗn hợp cát và than (A2%) | 84,5 | 80,2 | 72,0 | 60,4 |
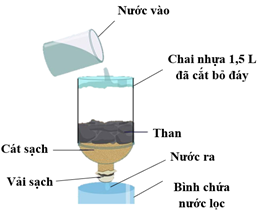
Sơ đồ thiết bị xử lý nước bằng than tồn tính làm từ vỏ trấu
Căn cứ kết quả thí nghiệm, tại cuối thời điểm xử lý 8 lít nước nhiễm ion kim loại chì, mức độ hấp phụ ion kim loại chì của 1 gam than tồn tính là? (Làm tròn kết quả đến hàng phần mười)
(Xem giải) Câu 26: Trong công nghiệp chlorine-kiềm, công nghệ sử dụng phổ biến để điều chế khí Cl2 và NaOH là điện phân dung dịch NaCl bão hòa có màng ngăn. Mô hình thiết bị điện phân được thể hiện trong hình vẽ sau:
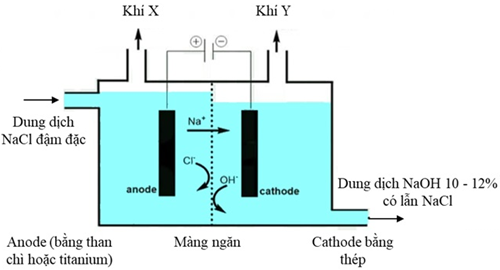
(1) Khí X là hydrogen và khí Y là chlorine.
(2) Để thu được dung dịch NaOH tinh khiết hơn (nồng độ 50%) có thể tăng nồng độ dung dịch NaCl ban đầu.
(3) Ở cathode, nước bị khử thay cho Na+ do thế điện cực của cặp 2H+/H2 nhỏ hơn Na+/Na.
(4) Dung dịch NaCl được đưa vào từ anode và được duy trì ở mức cao hơn bên cathode giúp chất lỏng chảy từ trái sang phải, ngăn không cho dung dịch NaOH chảy sang anode.
Liệt kê các phát biểu đúng (theo thứ tự tăng dần)?
(Xem giải) Câu 27: Cho các cặp oxi hoá – khử và thế điện cực chuẩn tương ứng:
| Cặp oxi hóa – khử | Sn2+/Sn | Zn2+/Zn | Fe2+/Fe | Mg2+/Mg | H2O/H2, OH– | Ag+/Ag |
| Thế điện cực chuẩn, V | – 0,137 | – 0,76 | – 0,44 | – 2,356 | – 0,414 | + 0,8 |
Xét ở điều kiện chuẩn, cho các phát biểu sau:
(1) Tính oxi hoá tăng dần theo thứ tự Mg2+, Zn2+, Sn2+, Fe2+, Ag+.
(2) Kim loại Mg tác dụng được với nước.
(3) Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Ag; Fe và Zn; Fe và Sn; Fe và Mg. Khi nhúng các cặp kim loại trên vào dung dịch acid, số cặp kim loại trong đó Fe bị phá huỷ trước là 1.
(4) Có 1 kim loại không phản ứng với hydrochloric acid ở điều kiện thường.
Liệt kê các phát biểu đúng (theo thứ tự tăng dần)?
(Xem giải) Câu 28: Chuẩn độ hàm lượng ion Fe2+ trong môi trường acid (chứa trong bình tam giác) bằng dung dịch KMnO4 đã biết nồng độ (chứa trên burette). Trong quá trình chuẩn độ, nếu dung dịch trên burette được thêm vào bình tam giác quá nhanh thì trong bình sẽ xuất hiện kết tủa nâu MnO2 theo phương trình hóa học dưới đây, dẫn đến sai lệch kết quả chuẩn độ:
MnO4-(aq) + H+(aq) + Fe2+(aq) → MnO2(s) + Fe3+ + H2O(l)
Giả sử một học sinh thao tác chuẩn độ sai, làm 55% lượng MnO4- chuẩn độ chuyển thành MnO2 (phần còn lại vẫn phản ứng tạo Mn2+), tổng lượng Fe2+ bị oxi hóa là 2,4 mmol. Thể tích dung dịch KMnO4 0,02M đã dùng tăng bao nhiêu mL so với khi chuẩn độ với thao tác phù hợp? (Kết quả làm tròn đến hàng phần trăm)


Bình luận