[2024] Thi thử TN sở GDĐT Nghệ An (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Giải chi tiết và đáp án:
⇒ Mã đề: 122
| 41A | 42A | 43B | 44C | 45D | 46A | 47D | 48B | 49B | 50B |
| 51A | 52A | 53B | 54B | 55C | 56B | 57A | 58B | 59A | 60A |
| 61C | 62A | 63C | 64D | 65C | 66A | 67B | 68A | 69D | 70C |
| 71D | 72A | 73D | 74C | 75B | 76D | 77B | 78A | 79D | 80A |
Câu 41. Chất nào sau đây không phản ứng với dung dịch H2SO4 loãng?
A. BaSO4. B. Fe. C. Na2CO3. D. Ba(OH)2.
Câu 42. Natri hidrocacbonat có nhiều ứng dụng trong đời sống. Công thức phân tử của hợp chất natri hidrocacbonat là
A. NaHCO3. B. HCOONa. C. NaHSO3. D. Na2CO3.
Câu 43. Công thức hóa học của kali đicromat là
A. KCl. B. K2Cr2O7. C. K2CrO4. D. KNO3.
Câu 44. Trong hợp chất Fe2O3 sắt có số oxi hoá là
A. +4. B. +1. C. +3. D. +2.
Câu 45. Chất nào sau đây vừa phản ứng với dung dịch NaOH, vừa phản ứng với dung dịch HCl?
A. Al2(SO4)3. B. NaAlO2. C. AlCl3. D. Al2O3.
Câu 46. Phân tử este nào sau đây chỉ có 2 nguyên tử cacbon?
A. metyl fomat. B. etyl axetat. C. metyl propionat. D. metyl axetat.
Câu 47. Chất nào sau đây là phenol?
A. C6H5CH2OH. B. C6H5CHO. C. C6H5COOH. D. C6H5OH.
Câu 48. Số nguyên tử cacbon trong phân tử axit stearic là
A. 17. B. 18. C. 19. D. 20.
Câu 49. Kali nitrat được dùng làm phân bón và chế tạo thuốc nổ. Công thức của kali nitrat là
A. KHCO3. B. KNO3. C. K3PO4. D. KNO2.
Câu 50. Ở nhiệt độ cao, Al khử được ion kim loại trong oxit nào sau đây?
A. K2O. B. Fe2O3. C. MgO. D. BaO.
(Xem giải) Câu 51. Trong thực tế, không sử dụng cách nào sau đây để bảo vệ kim loại sắt khỏi bị ăn mòn?
A. Gắn đồng với kim loại sắt.
B. Tráng kẽm lên bề mặt sắt.
C. Phủ một lớp sơn lên bề mặt sắt.
D. Tráng thiếc lên bề mặt sắt.
Câu 52. Kim loại nhẹ, màu trắng bạc, được ứng dụng rộng rãi trong đời sống là
A. Al. B. Ag. C. Fe. D. Cu.
(Xem giải) Câu 53. Đun nước cứng lâu ngày trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là
A. CaCl2. B. CaCO3. C. CaO. D. Na2CO3.
Câu 54. Hiệu ứng nhà kính là hiện tượng Trái đất đang ấm dần lên, do các bức xạ bước sóng dài trong vùng hồng ngoại bị giữ lại, mà không bức xạ ra ngoài vũ trụ. Khí CO2 là một trong những nguyên nhân gây ra hiệu ứng nhà kính. Tên gọi của CO2 là
A. cacbon tetraoxit. B. cacbon dioxit. C. cacbon trioxit. D. cacbon monoxit.
Câu 55. Chất nào sau đây thuộc loại amin bậc hai?
A. Anilin. B. Metylamin. C. Dimetylamin. D. Trimetylamin.
Câu 56. X là kim loại cứng nhất, được sử dụng để mạ các dụng cụ kim loại, chế tạo các loại thép chống gỉ, không gi…. Kim loại X là
A. Fe. B. Cr. C. W. D. Ag.
Câu 57. Cacbohiđrat nhất thiết phải chứa nhóm chức của
A. ancol. B. amin. C. axit. D. anđehit.
Câu 58. Peptit bị thủy phân hoàn toàn nhờ xúc tác axit tạo thành các
A. amin. B. α-amino axit. C. amino axit. D. ancol.
Câu 59. Polime nào sau đây thuộc loại polime thiên nhiên?
A. Tơ tằm. B. Poli(vinyl clorua). C. Polietilen. D. Poliacrilonitrin.
Câu 60. Kim loại natri (Na) tác dụng với nước tạo ra khí H2 và chất nào sau đây?
A. NaOH. B. Na2CO3. C. Na2O. D. NaHCO3.
(Xem giải) Câu 61. Dãy gồm các chất đều tác dụng được với dung dịch Ca(HCO3)2 là
A. NaCl, Na2SO4 và Ca(OH)2. B. HNO3, Ca(OH)2 và KNO3.
C. HNO3, Ca(OH)2 và NaHSO4. D. HNO3, NaCl và Na2SO4.
(Xem giải) Câu 62. Cho 0,48 gam kim loại M (hóa trị 2) vào cốc đựng dung dịch H2SO4 loãng, dư. Sau khi phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch tăng thêm 0,44 gam. Kim loại M là
A. Mg. B. Zn. C. Ca. D. Fe.
(Xem giải) Câu 63. Xà phòng hoá hoàn toàn 17,24 gam chất béo cần vừa đủ 0,06 mol NaOH. Cô cạn dung dịch sau phản ứng thu được khối lượng xà phòng là
A. 18,38 gam. B. 16,68 gam. C. 17,8 gam. D. 18,24 gam.
(Xem giải) Câu 64. Số chất hữu cơ có công thức phân tử C3H6O2 có thể tác dụng được với dung dịch NaOH nhưng không tác dụng được với kim loại Na là
A. 4. B. 5. C. 3. D. 2
(Xem giải) Câu 65. Phát biểu nào sau đây là đúng?
A. Poli (etylen terephtalat) được điều chế bằng phản ứng trùng hợp các monome tương ứng.
B. Trùng ngưng buta-1,3-đien với acrilonitrin có xúc tác Na được cao su buna-N.
C. Polietilen và poli(vinyl clorua) là sản phẩm của phản ứng trùng hợp.
D. Tơ visco, tơ axetat là tơ tổng hợp.
(Xem giải) Câu 66. Cho 10,8 gam một amin X tác dụng vừa đủ với dung dịch HCl thu được 19,56 gam muối. Đốt cháy hoàn toàn lượng amin X trên thu được CO2, H2O và V lít khí N2 (đktc). Giá trị của V là
A. 2,688. B. 1,344. C. 5,376. D. 2,764.
(Xem giải) Câu 67. Tiến hành thí nghiệm sau: Cho một ít bột đồng kim loại vào ống nghiệm chứa dung dịch FeCl3, lắc nhẹ ống nghiệm sẽ quan sát thấy hiện tượng nào sau đây?
A. Có khí màu vàng lục thoát ra.
B. Đồng tan và dung dịch có màu xanh.
C. Không có hiện tượng gì xẩy ra.
D. Kết tủa sắt xuất uất hiện và dung dịch có màu xanh.
(Xem giải) Câu 68. Cho 6 gam bột kim loại Mg tác dụng hoàn toàn với 500 ml dung dịch chứa Fe2(SO4)3 0,1M và CuSO4 0,3M, sau phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 12,4. B. 12,0. C. 15,2. D. 15,8.
(Xem giải) Câu 69. Phát biểu nào sau đây không đúng?
A. Nhỏ vài giọt dung dịch iot vào hồ tinh bột thấy xuất hiện màu xanh tím.
B. Xenlulozơ có phản ứng thủy phân trong môi trường axit (H+).
C. Glucozơ và fructozơ là đồng phân của nhau.
D. Saccarozơ có phản ứng tráng gương với dung dịch AgNO3/NH3.
(Xem giải) Câu 70. Lên men 72 gam glucozơ với hiệu suất 75% thu được ancol etylic và V lít CO2 (đktc). Giá trị của V là
A. 6,72. B. 8,96. C. 13,44. D. 17,92.
(Xem giải) Câu 71. Đồng (II) sunfat ngậm nước hay còn gọi là đá xanh có công thức phân tử là CuSO4.5H2O thường được ứng dụng làm chất sát khuẩn, diệt nấm, diệt cỏ, … Khi làm lạnh dung dịch đồng (II) sunfat bão hòa sẽ có chất rắn kết tinh là các tinh thể CuSO4.5H2O. Hòa tan hoàn toàn 0,2 mol cacbonat bazơ đồng CuCO3.Cu(OH)2 bằng dung dịch H2SO4 20% (vừa đủ, đun nóng nhẹ), sau phản ứng thu được dung dịch A. Làm lạnh dung dịch A đến nhiệt độ 10°C thấy có kết tinh m gam chất rắn, biết độ tan của CuSO4 ở 10°C là 17,37 gam. Giá trị của m gần nhất với giá trị nào sau đây
A. 65,0. B. 38,7. C. 37,8. D. 60,5
(Xem giải) Câu 72. Cho các phát biểu sau:
(a) 1 mol peptit Gly-Ala-Glu-Lys phản ứng được tối đa với 5 mol NaOH.
(b) Cho 5 giọt anilin vào 10 ml dung dịch HCl 1M trong ống nghiệm, sau một thời gian tạo thành hai lớp chất lỏng.
(c) Lực bazơ của amin bậc 2 > amin bậc 1 > anilin > NH3.
(d) Trong phân tử peptit mạch hở Gly-Ala-Lys có 3 nguyên tử nitơ.
(e) Muối đinatri glutamat có cấu tạo là NaOOC-CH2-CH2-CH(NH2)-COOH.
Số phát biểu đúng là
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 73. Cho các phát biểu sau:
(a) Trùng hợp metylmetacrylat thu được polime dùng để chế tạo thuỷ tinh hữu cơ.
(b) Khi cho anilin vào dung dịch HCl (dư) thì ban đầu thấy hiện tượng phân lớp và sau đó trở nên đồng nhất.
(c) Saccarozơ là nguyên liệu dùng trong kĩ thuật tráng gương và tráng ruột phích vì saccarozơ phản ứng với dung dịch AgNO3/NH3 đun nóng thu được Ag.
(d) Chất béo là trieste của glixerol với axit béo. Chất béo dễ tan trong nước và trong dung môi hữu cơ.
(e) Độ pH của dung dịch glyxin 0,1 M nhỏ hơn độ pH của dung dịch axit glutamic 0,1M.
Số phát biểu đúng là
A. 3. B. 5. C. 4. D. 2
(Xem giải) Câu 74. Đun nóng hỗn hợp X gồm Mg và C thu được hỗn hợp Y. Hoà tan Y vào dung địch HNO3 dư thu được 3,92 lít hỗn hợp gồm hai khí nặng 8,02 gam. Biết các phản ứng xảy ra hoàn toàn và các khí đều đo ở đktc. Phần trăm khối lượng Mg trong hỗn hợp X là
A. 40,00%. B. 76,92%. C. 86,96%. D. 60,00%.
(Xem giải) Câu 75. Cho 38,08 gam hỗn hợp X gồm Fe, Fe2O3, Fe3O4 và FeCO3 tác dụng với dung dịch HCl vừa đủ, thu được dung dịch Y và 4,032 lít hỗn hợp khí Z có tỉ khối so với H2 là 15. Cho Y tác dụng hoàn toàn với dung dịch AgNO3 dư, thu được 184,54 gam 2 chất kết tủa gồm AgCl và Ag. Mặt khác, hòa tan hoàn toàn m gam X trong dung dịch H2SO4 (đặc, nóng, dư), thu được 5,6 lít hỗn hợp khí T gồm CO2 và SO2 (SO2 sản phẩm khử duy nhất của S+6). Biết các khí đều đo ở đktc và các phản ứng xẩy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây
A. 25,80. B. 25,73. C. 25,64. D. 25,68.
(Xem giải) Câu 76. Cho hỗn hợp X gồm Fe, Fe2O3, Fe(OH)2, Fe(OH)3 và CuO. Hòa tan hết 87,7 gam hỗn hợp X vào 315 gam dung dịch HNO3 68%, thu được dung dịch Y (chỉ chứa muối của ion kim loại, trong đó nồng độ phần trăm của Cu(NO3)2 là 9,779%) và 11,2 lít (đktc) hỗn hợp khí Z gồm NO, NO2 có tỉ khối so với H2 là 18,2. Cô cạn Y thu được hỗn hợp muối khan T. Nung T đến khối lượng không đổi thu được chất rắn E và hỗn hợp khí F có tỉ lệ mol là 29 : 6. Biết trong X, tỉ lệ khối lượng giữa Fe(OH)2 và Fe(OH)3 là 90 : 107. Phần trăm khối lượng của Fe2O3 trong hỗn hợp X gần nhất với
A. 24,0%. B. 41,6%. C. 34,3%. D. 27,5%.
(Xem giải) Câu 77. Đun nóng m gam hợp chất X là este 2 chức với 150 ml dung dịch NaOH 2M đến khi phản ứng xảy ra hoàn toàn. Để trung hòa lượng NaOH dư, người ta cho vào 40 ml dung dịch HCl 1,5M. Làm bay hơi cẩn thận dung dịch sau khi trung hòa, thu được 11,04 gam hỗn hợp 2 ancol đơn chức (Y), (Z) và 22,71 gam muối khan, trong đó có một muối (T) của axit cacboxylic (Q).
Cho các phát biểu sau đây:
(a) Axit (Q) có chứa 3 liên kết đôi trong phân tử.
(b) Số nguyên tử hiđro trong (X) gấp 6 lần số nguyên tử hiđro trong (T).
(c) Hai ancol (Y) và (Z) là 2 chất đồng đẳng liên tiếp với nhau.
(d) Chất hữu cơ (X) có 2 công thức cấu tạo.
(e) Số nguyên tử cacbon trong axit (Q) bằng một nửa số nguyên tử cacbon trong hợp chất este (X).
(g) Đun nóng hỗn rắn gồm muối (T) với NaOH và CaO thu được khí axetilen
Số lượng phát biểu đúng là
A. 4. B. 3. C. 6. D. 5.
(Xem giải) Câu 78. Cho hình vẽ mô tả thí nghiệm điều chế kim loại bằng cách dùng khí H2 để khử oxit kim loại ở nhiệt độ cao:
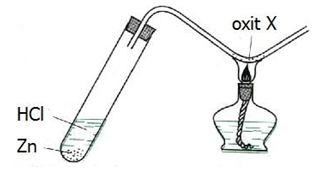
Hình vẽ trên minh họa cho các phản ứng trong đó oxit X là
A. Fe2O3 và CuO. B. Na2O và ZnO. C. MgO và Fe2O3. D. Al2O3 và CuO.
(Xem giải) Câu 79. Thực hiện các thí nghiệm sau:
(1) Ngâm đinh sắt vào dung dịch HCl.
(2) Đốt dây sắt trong hơi brom.
(3) Ngâm đinh sắt vào dung dịch AgNO3 dư.
(4) Cho Fe(OH)2 vào dung dịch HNO3 loãng, dư.
(5) Cho FeCO3 vào dung dịch H2SO4 loãng dư.
Số thí nghiệm thu được muối sắt (II) là
A. 5. B. 3. C. 4. D. 2.
(Xem giải) Câu 80. Một trong các phương pháp dùng để loại bỏ sắt trong nguồn nước nhiễm sắt là sử dụng lượng với tôi vừa đủ để tăng pH của nước nhằm kết tủa ion sắt khi có mặt oxi, theo sơ đồ phản ứng:
(1) Fe3+ + OH- → Fe(OH)3
(2) Fe2+ + OH- + O2 + H2O → Fe(OH)3
Một mẫu nước có hàm lượng sắt cao gấp n lần so với ngưỡng cho phép quy định là 0,30 mg/l (theo QCVN01-1:2018/BYT). Giả thiết sắt trong mẫu nước trên chỉ tồn tại ở hai dạng là Fe3+ và Fe2+ với tỉ lệ mol Fe3+ : Fe2+ = 1 : 3. Cần tối thiểu 149,85 gam Ca(OH)2 để kết tủa hoàn toàn lượng sắt trong 8 m³ mẫu nước trên. Giá trị của n là
A. 42. B. 6. C. 14. D. 21.


Bình luận