[2025 – 2026] Thi học sinh giỏi lớp 12 – Tỉnh Hưng Yên
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề 021-H12A năm 2025-2026
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1C | 2B | 3D | 4D | 5D | 6A | 7A | 8C | 9B | 10B |
| 11C | 12A | 13D | 14B | 15A | 16C | 17B | 18D | 19C | 20A |
| Câu 21 | Câu 22 | Câu 23 | Câu 24 | Câu 25 | Câu 26 | |
| (a) | S | Đ | Đ | S | Đ | Đ |
| (b) | Đ | S | Đ | S | Đ | S |
| (c) | S | S | S | Đ | S | Đ |
| (d) | S | S | S | Đ | S | S |
| Câu 27 | Câu 28 | Câu 29 | Câu 30 | Câu 31 | Câu 32 |
| 7532 | 235 | —- | 245 | 1305 | 1 |
PHẦN I (8,0 điểm). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 20. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Phát biểu nào sau đây về carbohydrate là đúng?
A. Glucose phản ứng với methanol khi có mặt HCl khan, tạo thành methyl glycoside.
B. Amylopectin được cấu tạo từ nhiều đơn vị β-glucose liên kết với nhau qua liên kết β-1,4-glycoside và β-1,6-glycoside hình thành cấu trúc mạch phân nhánh.
C. Amylose chiếm khoảng (0 – 30%) khối lượng tinh bột, hàm lượng amylose trong gạo ảnh hưởng đến độ dẻo và mềm của hạt cơm, hàm lượng amylose càng cao thì hạt cơm càng khô và cứng. Một phân tử amylose có cấu tạo như sau:
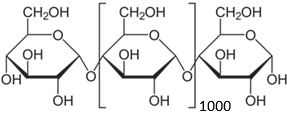
Phân tử khối của amylose trên là 162342.
D. Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)n.
(Xem giải) Câu 2: Poly(butylene terephthalate) (PBT) là một polymer kị nước được sử dụng rộng rãi trong hệ thống đánh lửa của động cơ ô tô. Polymer này có công thức cấu tạo như sau:
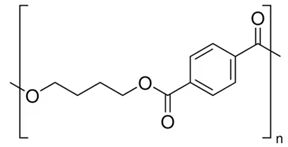
Cho các phát biểu:
(a) PBT thuộc loại polyester được điều chế từ phản ứng trùng ngưng các monomer tương ứng.
(b) Hai monomer dùng để điều chế PBT là p-HOC6H4COOH (-C6H4-chứa vòng benzene) và HO[CH2]4OH.
(c) Số mắt xích có trong 26,4 gam PBT là 7,224.10²².
(d) Phần trăm khối lượng nguyên tố oxygen trong một mắt xích của PBT là 29,2 (Kết quả làm tròn kết quả đến hàng phần mười).
Số phát biểu đúng là
A. 3. B. 2. C. 1. D. 4.
(Xem giải) Câu 3: Isoamyl acetate (D = 0,876 g/mL) có mùi chuối nên được dùng làm hương liệu nhân tạo. Trong ngành sơn, isoamyl acetate được dùng làm dung môi sơn mài. Isoamyl acetate được điều chế theo các bước sau:
• Bước 1: Cho vào bình cầu 15 mL isoamyl alcohol (D = 0,810 g/mL), 10 mL acetic acid (D = 1,049 g/mL) và 7,0 mL H2SO4 đậm đặc, cho thêm vào bình vài viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng đứng vào miệng bình cầu. Sau đó đun nóng bình cầu trong khoảng 1 giờ.
• Bước 2: Sau khi đun, để nguội rồi rót sản phẩm vào phễu chiết, lắc đều rồi để yên khoảng 5 phút, chất lỏng tách thành hai lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
• Bước 3: Cho từ từ dung dịch Na2CO3 10% vào phần chất lỏng thu lấy ở bước 2 và lắc đều cho đến khi không còn khi thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hòa rồi để yên, khi đó chất lỏng tách thành hai lớp. Chiết lấy phần chất lỏng phía trên, làm khan, ta thu được isoamyl acetate. Cho các phát biểu sau:
(a) Isoamyl acetate rất ít tan trong nước vì có khối lượng riêng nhỏ hơn khối lượng riêng của nước.
(b) Ở bước 3, không thể thay dung dịch Na2CO3 bằng dung dịch NaOH dư.
(c) Ở bước 1, xảy ra phản ứng thế nhóm -OH của alcohol bằng gốc CH3COO-.
(d) Nếu hiệu suất phản ứng este hóa là 54% và lượng isoamyl acetate bị hao hụt tối đa 6% thì thể tích isoamyl acetate thu được là 10,4 mL (Làm tròn kết quả đến hàng phần mười).
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 4: Thủy phân hoàn toàn 1 mol peptide X mạch hở, thu được 3 mol Gly, 1 mol Ala và 1 mol Val. Nếu thủy phân không hoàn toàn X thì thu được tripeptide Gly-Gly-Ala; dipeptide Ala-Gly, Gly-Ala và Y (chứa Val nhưng không phải Val-Gly). Trong phân tử X có chứa a liên kết peptide, dipeptide Y có phân tử khối là b. Tổng giá trị (a + b) là
A. 179. B. 196. C. 121. D. 178.
(Xem giải) Câu 5: Trong dung dịch, glycine có cân bằng sau:
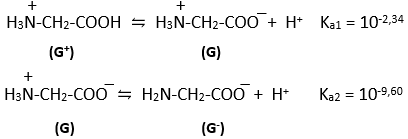
Trong dung dịch có pH = 2 nồng độ ion dạng (G+) chiếm x% so với tổng nồng độ các dạng (G), (G+) và (G-). Giá trị của x là (Kết quả làm tròn đến hàng phần trăm)
A. 78,54. B. 58,71. C. 46,95. D. 68,63.
(Xem giải) Câu 6: Một nhà máy sản xuất túi nylon, từ HDPE cần sản xuất túi đựng hình chữ nhật (chiều rộng 20 cm, chiều dài 30 cm, bề dày của lớp nylon là 0,02 cm). Biết hiệu suất phản ứng trùng hợp ethylene để điều chể HDPE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và khối lượng riêng của nhựa HDPE là 0,95 g/cm³. Coi kích thước của túi không thay đổi so với chiều dài và chiều rộng của mỗi mặt nylon. Khối lượng nguyên liệu ethylene dùng đề sản xuất đơn hàng 120 000 túi trên là x tấn. Giá trị x là
A. 4,8. B. 2,4. C. 2,0. D. 1,0.
(Xem giải) Câu 7: Trong quá trình chuyển hóa lipid trong cơ thể (thành phần chính là triglyceride), các triglyceride được thủy phân thành các chất nhỏ hơn là glycerol và các acid béo, sau đó các chất này được sử dụng cho nhiều mục đích khác nhau trong cơ thể. Triglyceride X có công thức cấu tạo như hình sau:
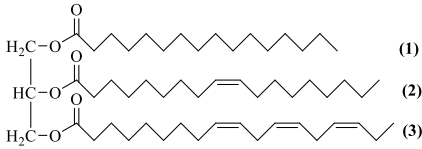
Cho các phát biểu sau:
(a) Acid béo có gốc kí hiệu (2) thuộc loại acid béo omega-3.
(b) Công thức phân tử của X là C55H98O6.
(c) Trong điều kiện thích hợp, X có thể phản ứng với hydrogen tạo thành chất béo chứa gốc acid béo no.
(d) Đun nóng X với dung dịch NaOH đặc hoặc KOH đặc, là phương pháp sản xuất chất giặt rửa tổng hợp.
(e) X có gốc hydrocarbon lớn, do đó khi để lâu ngoài không khí không bị oxi hóa bởi oxygen.
(g) Các gốc acid béo trong phân tử X đều có cấu hình dạng cis-.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 2.
(Xem giải) Câu 8: Sodium dodecylbenzene sulfonate (SDBS) có công thức C15H25C6H4SO3Na. SDBS là một loai chất hoạt động bề mặt đa năng có nhiều ứng dụng trong chất giặt rửa tổng hợp, sản phẩm làm sạch và nhiều quy trình công nghiệp khác nhau. Phát biểu đúng khi nói về SDBS là
A. SDBS có đuôi kị nước là -C15H25.
B. SDBS có đầu ưa nước là Na+.
C. SDBS có thể dùng giặt rửa trong nước cứng.
D. SDBS có giá thành hợp lý, không gây ô nhiễm môi trường.
(Xem giải) Câu 9: Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Nhỏ 3 giọt aniline vào ống nghiệm chứa 2 mL nước cất, lắc đều, sau đó để yên.
• Bước 2: Nhúng giấy quỳ tím vào dung dịch trong ống nghiệm, sau đó nhấc giấy quỳ ra.
• Bước 3: Nhỏ tiếp 1 mL dung dịch HCl đặc vào ống nghiệm, lắc đều, sau đó để yên.
• Bước 4: Nhỏ tiếp 1 mL dung dịch NaOH đặc vào ống nghiệm, lắc đều, sau đó để yên.
Cho các phát biểu sau:
(a) Kết thúc bước 1, aniline hầu như không tan và lắng xuống đáy ống nghiệm.
(b) Két thúc bước 2, giấy quỳ tím chuyển thành màu xanh do aniline có tính base.
(c) Kết thúc bước 3, thu được dung dịch trong suốt do dung dịch có chứa muối phenylammonium chloride tan tốt trong nước.
(d) Kết thúc bước 4, trong ống nghiệm có aniline được tạo thành.
(e) Kết thúc bước 4, trong ống nghiệm chứa hai muối.
(f) Ở thí nghiệm trên, nếu thay aniline bằng methylamine thì thu được kết quả tương tự.
(g) Ở bước 3, nếu thay HCl bằng Br2 thì sẽ thấy xuất hiện kết tủa màu vàng.
Số phát biểu đúng là
A. 2. B. 3. C. 4. D. 5.
(Xem giải) Câu 10: Thuỷ phân không hoàn toàn một đoạn phân tử insulin, thu được peptide X (Glu–Arg–Gly). Cho công thức cấu tạo và kí hiệu một số nhóm chức của các amino acid:
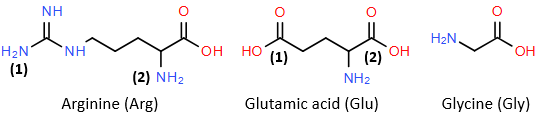
Cho các phát biểu sau:
(a) Trong phân tử X còn nhóm carboxyl số (1) của Glu.
(b) Trong phân tử X, nhóm –NH2 số (1) của Arg đã tham gia tạo liên kết peptide.
(c) Có thể tách biệt được hỗn hợp Glu, Arg, Gly bằng phương pháp điện di ở pH thích hợp.
(d) X có amino acid đầu N là Glu, amino acid đầu C là Gly.
(e) Tổng số nguyên tử nitrogen và oxygen trong một phân tử X là 12.
Số phát biểu đúng là
A. 1. B. 4. C. 3. D. 2.
(Xem giải) Câu 11: Để xác định hàm lượng oxygen tan trong nước người ta tiến hành theo các bước sau:
• Bước 1: Thêm MnSO4 dư vào 100,00mL nước, sau đó thêm tiếp dung dịch kiềm iodide vào, đậy nút và để yên cho kết tủa lắng.
• Bước 2: Thêm H2SO4 đặc, đậy nút chai lắc kĩ để kết tủa tan.
• Bước 3: Chuẩn độ dung dịch thu được bằng Na2S2O3 thấy vừa hết 10,5 mL Na2S2O3 9,8.10^-3M.
Biết các phản ứng xảy ra theo sơ đồ sau:
Mn2+ + OH- → Mn(OH)2
Mn(OH)2 + O2 → MnO(OH)2
MnO(OH)2 + H+ + Mn2+ → Mn3+ + H2O
Mn3+ + I- → Mn2+ + I3-
I3- + S2O32- → I- + S4O62-
Hàm lượng (mg/L) của oxygen tan trong nước là
A. 8,224. B. 16,464. C. 8,232. D. 12,336.
(Xem giải) Câu 12: Thực hiện các thí nghiệm với 4 kim loại (X, Y, Z, T) và dung dịch muối của chúng (X2+, Y2+, Z+, T2+) cho kết quả như sau:
(1) T đẩy được Z ra khỏi dung dịch muối của nó.
(2) Y không đẩy được Z ra khỏi dung dịch muối của nó.
(3) X đẩy được Z ra khỏi dung dịch muối của nó.
(4) X không đẩy được T ra khỏi dung dịch muối của nó.
(5) X không đẩy được Y ra khỏi dung dịch muối của nó.
Nhận định nào sau đây là đúng?
A. Trong 4 ion kim loại trên, Y2+ có tính oxi hoá yếu nhất.
B. T2+ có tính oxi hoá yếu hơn Y2+ .
C. Trong 4 kim loại trên, X có tính khử yếu nhất.
D. T có tính khử yếu hơn X.
(Xem giải) Câu 13: Cho các phát biểu sau:
(a) Trong siêu thị, rau xanh thường được chứa trong túi nylon có lỗ.
(b) Phenol tham gia phản ứng cộng với dung dịch nước bromine.
(c) Ethanal, acetone đều phản ứng với iodine trong môi trường kiềm tạo kết tủa màu vàng.
(d) Từ ethanol có thể chuyền hóa thành ethanal bằng 1 phản ứng và ngược lại.
(e) Oxi hóa acetone bằng LiAlH4 ta được alcohol bậc hai.
(g) Methanal, ethanal và acetone tan tốt trong nước.
Số phát biểu đúng là
A. 6. B. 5. C. 3. D. 4.
(Xem giải) Câu 14: Kết quả thí nghiệm của các chất X, Y, Z,T được sắp xếp không theo thứ tự methylamine, albumin, aniline, Ala-Gly-Lys như sau:
| Mẫu thử | Thuốc thử | Hiện tượng |
| X | Đun nóng | Đông tụ |
| Y | Quỳ tím | Không chuyển màu |
| Z | Cu(OH)2 | Dung dịch màu xanh |
| X, T | Cu(OH)2 | Dung dịch màu tím |
Cho các phát biểu sau:
(a) Chất Y và phenol phản ứng với nước bromine đều thu được kết tủa trắng.
(b) Chất T có công thức phân tử là C10H17N3O6.
(c) Chất X là protein dạng hình cầu.
(d) Chất Z có thể được điều chế từ ammonia và iodoform.
(e) Tổng số nguyên tử nitrogen trong các chất Y, Z, T là 5.
Số phát biểu đúng là
A. 1. B. 2. C. 4. D. 3.
(Xem giải) Câu 15: Saccharose monolaurate là một trong những chất phụ gia có chức năng kép do khả năng nhũ hóa và hoạt tính kháng khuẩn của nó. Saccharose monolaurate là hợp chất thu được khi cho saccharose tác dụng với lauric acid, saccharose monolaurate có công thức như sau:
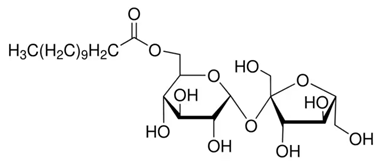
Từ 171 gam saccharose và 200 gam lauric acid, với hiệu suất phản ứng đạt 52% thì điều chế được bao nhiêu gam saccharose monolaurate?
A. 136,24. B. 262,00. C. 65,50. D. 272,48.
(Xem giải) Câu 16: Trong nước thải của một nhà máy, hàm lượng ion ammonium là 175 mg/L. Để xử lí ion ammonium về nồng độ cho phép là không quá 5 mg/L (theo quy chuẩn Việt Nam), người ta tiến hành xử lí nước thải theo phương pháp Anammox (Anaerobic Ammonium Oxidation). Phương pháp này gồm 2 giai đoạn:
• Giai đoạn 1: Oxi hóa ion ammonium thành ion nitrite theo phương trình sau: (dùng NaHCO3 dư 10% so với lượng cần thiết):
aNH4+ + bO2 + cHCO3- → xNO2- + yCO2 + zH2O
• Giai đoạn 2: Diễn ra trong điều kiện yếm khí, ion amonium sẽ được oxi hoá trực tiếp thành khí nitrogen theo phản ứng:
NH4+ + NO2- → N2 + 2H2O
Biết các phản ứng xảy ra hoàn toàn. Khối lượng (kg) NaHCO3 tối thiểu cần dùng để xử lí 750 m³ nước thải trên là
A. 675,68. B. 595,00. C. 654,50. D. 872,67.
(Xem giải) Câu 17: Sử dụng vôi sữa là phương pháp phổ biến để xử lí khí thải SO2. 90% lượng SO2 trong khí thải được hấp thụ theo phương trình hóa học: Ca(OH)2 + SO2 → CaSO3 + H2O. Sau đó CaSO3 bị oxi hóa hoàn toàn thành CaSO4 dưới tác dụng của oxygen. CaSO4 được lọc tách, làm sạch, nung khô và thu hồi dưới dạng thạch cao thương phẩm (2CaSO4.H2O) với hiệu suất 80%. Một nhà máy trong một ngày thải ra 3000 m³ khí thải (ở đkc) chứa 1% SO2 về thể tích. Khối lượng 2CaSO4.H2O (kg) thu được trong 30 ngày theo phương pháp trên là (Kết quả làm tròn đến hàng phần mười)
A. 3509,4. B. 3790,2. C. 3948,1. D. 3158,5.
(Xem giải) Câu 18: Melibiose là một disaccharide có vị ngọt gấp 30 lần saccharose có công thức cấu tạo như sau:
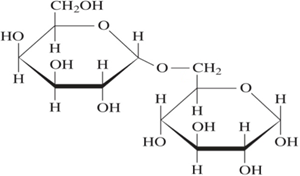
Cho các phát biểu sau về melibiose:
(a) Melibiose được cấu tạo nên từ hai đơn vị monosaccharide liên kết với nhau qua liên kết α-1,4-glycoside.
(b) Melibiose được cấu tạo nên từ một đơn vị glucose và một đơn vị fructose.
(c) Melibiose tham gia phản ứng với Cu(OH)2 cho dung dịch có màu xanh lam.
(d) Melibiose có tham gia phản ứng với thuốc thử Tollens.
Số phát biểu đúng là
A. 1. B. 4. C. 3. D. 2.
(Xem giải) Câu 19: Salbutamol có công thức cấu tạo thu gọn nhất như sau:
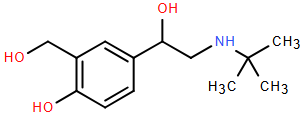
Cho các phát biểu sau:
(a) Công thức phân tử của salbutamol là C13H19NO3.
(b) Trong phân tử salbutamol có chứa nhóm chức amine bậc I.
(c) Salbutamol vừa tác dụng được với K, vừa tác dụng được với dung dịch KOH.
(d) Salbutamol có khả năng phản ứng với dung dịch bromine ở điều kiện thường.
(e) Cho 0,1 mol salbutamol phản ứng với dung dịch chứa 0,2 mol HCl thu được dúng dịch X. Dung dịch X sau phản ứng cho tác dụng với dung dịch NaOH dư thu được dung dịch Y. Khối lượng muối thu được trong dung dịch Y là 34,875 gam.
Số phát biểu đúng là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 20: Sơ đồ quy trình dưới đây mô tả các quá trình sản xuất phân bón từ chất Z:

Cho các phát biểu sau:
(a) X, T và khí SO2 đều là các khí góp phần gây ra hiện tượng mưa acid.
(b) Hợp chất Q là chất khí, không màu, không mùi và làm quỳ tím ẩm chuyển màu xanh.
(c) Theo thuyết Bronsted Lowry, Z có tính chất lưỡng tính.
(d) Acid Y có tính oxi hoá mạnh.
Số phát biểu đúng là
A. 2. B. 3. C. 1. D. 4.
PHẦN II (8,4 điểm). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 21 đến câu 26. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 21: Adipic acid là hóa chất quan trọng được dùng trong sản xuất vải sợi (nylon-6,6) và nhiều sản phẩm thông dụng khác như thảm, dây thừng hay lông bàn chải đánh răng… Các nhà nghiên cứu thuộc Viện Công nghệ sinh học và Công nghệ Nano (IBN) của Singapore vừa phát hiện một sơ đồ hóa học mới có thể chuyển hóa đường glucose thành adipic acid như sau:
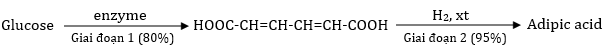
Trong công nghiệp adipic acid được dùng để sản xuất poly(hexamethylene adipamide) qua phản ứng trùng ngưng giữa hexamethylenediamine và adipic acid với hiệu suất đạt 80%.
a) Tơ nylon-6,6 thuộc loại polypeptide.
b) Hiện nay, nylon-6,6 được dùng để sản xuất chỉ nha khoa chứa 90% poly(hexamethylene adipamide). Lượng adipic acid được tạo ra từ 270 kg glucose theo sơ đồ (1) có thể sản xuất được 229 kg chỉ nha khoa (Kết quả làm tròn đến hàng đơn vị).
c) 1,0 mol mucic acid làm mất màu tối đa 2,0 mol Br2 tạo ra chất hữu cơ có phần trăm khối lượng bromine là 52,98% (Kết quả được làm tròn đến hàng phần trăm).
d) Trong 1 phân tử adipic acid có 6 nhóm methylene.
(Xem giải) Câu 22: Isopropyl myristate là một ester thường được sử dụng trong kem dưỡng da, dầu tẩy trang và sản phẩm chăm sóc tóc như một chất làm mềm, chất kết dính và chất tăng hương thơm vì khả năng thẩm thấu tốt mà không gây nhờn rít. Ester này được tạo ra từ phản ứng giữa acid béo bão hòa myristic và isopropyl alcohol. Công thức khung phân tử của isopropyl myristate như sau:
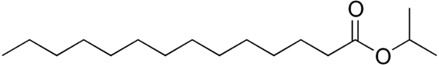
a) Một lọ kem dưỡng da có thể tích thực là 100 mL cho biết thành phần có chứa 3% isopropyl myristate theo khối lượng. Giả sử khối lượng riêng của kem dưỡng da đã cho là 0,85 g/mL. Lượng ester cần dùng để sản xuất 500 lọ kem trên là 1,275 kg.
b) Isopropyl alcohol có tên thay thế là propan-1-ol.
c) Isopropyl myristate là một chất béo bão hòa.
d) Số liên kết sigma (σ) trong 1 phân tử isopropyl myristate là 53.
(Xem giải) Câu 23: X là một peptide mạch hở có công thức phân tử C13H24N4O6. Thực hiện các phản ứng sau (theo đúng tỉ lệ mol các chất):
(1) X + 4KOH → X1 + NH2CH2COOK + X2 + 2H2O
(2) X1 + 3HCl → C5H10NO4Cl + 2KCl
a) Hợp chất T (muối của một trong các amino acid tạo nên peptide X, MT = MX1 – 38). Biết độ tan trong nước của T ở 60°C là 112 g/100g nước; ở 25°C là 75 g/100g nước. Khối lượng tinh thể T.5H2O kết tinh khi làm nguội 388 gam dung dịch bão hòa có chứa muối T từ 60°C xuống 25°C là 158,5 gam (Kết quả làm tròn đến hàng phần mười).
b) Cho 0,1 mol X2 tác dụng với dung dịch HCl dư thì thu được 29,35 gam muối.
c) Trong dung dịch, X1 không làm quỳ tím đổi màu.
d) X là một tetrapeptide và có 6 công thức cấu tạo thỏa mãn.
(Xem giải) Câu 24: Một hợp chất T có công thức phân tử C28H38O19 được tạo ra bởi phản ứng giữa saccharose với acetic anhydride (điều kiện xúc tác đầy đủ), dùng làm chất nhũ hoá, chất kháng nấm trong các chế phẩm thuộc lĩnh vực dược phẩm, mĩ phẩm, chất phụ gia thực phẩm, chất chống cắn móng tay và mút ngón tay ở trẻ do tính chất rất đắng của nó.
a) T không độc nên được sử dụng làm dược phẩm, mỹ phẩm, 1 mol phân tử T phản ứng tối đa với 6 mol NaOH.
b) Theo phương pháp “Hoá học xanh”, người ta tiến hành ester hoá saccharose trong điều kiện chiếu xạ siêu âm, cho 136,8 gam saccharose phản ứng với 340 mL acetic anhydride (D = 1,08 g/mL) hiệu suất phản ứng là 68,5% thu được khối lượng của T là 187 gam (Kết quả làm tròn đến hàng đơn vị).
c) Dung dịch thu được sau khi thủy phân hoàn toàn saccharose có thể làm mất màu nước bromine.
d) Phân tử saccharose, được tạo bởi 1 gốc α-glucose và 1 gốc β-fructose.
(Xem giải) Câu 25: Sulfuric acid là một trong những hóa chất quan trọng nhất được sử dụng trong công nghiệp, được sản xuất hàng trăm triệu tấn mỗi năm. Phương pháp sản xuất sulfuric acid phổ biến nhất là phương pháp tiếp xúc, theo đó acid có thể được sản xuất từ quặng pyrite qua các giai đoạn sau:
• Giai đoạn 1: Sản xuất SO2
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g) (1)
• Giai đoạn 2: Sản xuất SO3
2SO2(g) + O2(g) ⇋ 2SO3(g)  = -196kJ (2)
= -196kJ (2)
• Giai đoạn 3: Sản xuất H2SO4
H2SO4(aq) + nSO3(g) → H2SO4.nSO3) (oleum) (3)
H2SO4.пSO3() + nH2O(1) → (n + 1)H2SO4(aq) (4)
a) Trong quá trình sản xuất H2SO4, giai đoạn (1) có nguy cơ cao gây ô nhiễm môi trường.
b) Dùng dung dịch H2SO4 98% hấp thụ SO3 bằng phương pháp ngược dòng.
c) Để xác định công thức của oleum thu được, người ta pha loãng 8,36 gam oleum vào nước thành 1,0 lít dung dịch acid H2SO4, sau đó tiến hành chuẩn độ 10,00 mL dung dịch acid này bằng dung dịch chuẩn NaOH 0,1M. Thể tích NaOH trung bình cần sử dụng để chuẩn độ là 20,00mL. Công thức của oleum thu được ở trên là H2SO4.2SO3
d) Khi tăng nhiệt độ của giai đoạn (2), tỉ khối của hỗn hợp sau phản ứng so với H2 tăng.
(Xem giải) Câu 26: Quá trình điện phân để mạ đồng lên tấm huy chương hình trụ, đáy tròn với bán kính 2,5 cm, chiều cao hình trụ 0,3 cm với lớp mạ dày 0,05 cm được mô tả như hình sau:
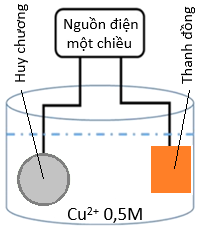
Tiến hành điện phân dung dịch CuSO4 0,5M với cường độ dòng điện không đổi 1,5A, khi kết thúc điện phân (quá trình mạ hoàn thành) thì thời gian là t giây. Biết khối lượng riêng của copper là 8,95 g/cm³ và hiệu suất điện phân là 100%, giả thiết lớp mạ huy chương dày như nhau, toàn bộ lượng copper tạo ra đều bám hết vào tấm huy chương. Cho hằng số Faraday F = 96500, π = 3,14.
a) Trong quá trình mạ điện tại điện cực anode không có khí thoát ra.
b) Chiều dòng electron di chuyển từ huy chương được mạ qua dây dẫn đến thanh đồng.
c) Giá trị t là 41018 (Kết quả làm tròn đến hàng đơn vị).
d) Thanh đồng là cathode, huy chương được mạ sẽ đóng vai trò anode.
PHẦN III (3,6 điểm). Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 27 đến câu 32.
(Xem giải) Câu 27: Một pin Galvani được thiết lập ở điều kiện chuẩn theo sơ đồ như hình sau:
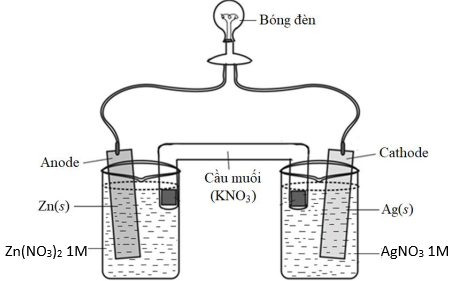
Cho biết:
– Thế điện cực chuẩn: E°Zn2+/Zn = -0,762V; E°Ag+/Ag = +0,799V.
– Điện lượng mà pin đã cung cấp: q = ne.F
– Điện năng cực đại (công cực đại) mà pin đã cung cấp cho bóng đèn ở điều kiện chuẩn:
A max pin cung cấp = q.E°pin = P.t
Trong đó: Amax là điện năng cực đại (J hay Ws), q là điện lượng (C hay As), ne là số mol electron đi qua dây dẫn, E°pin là sức điện động chuẩn của pin (V), P là công suất của bóng đèn (W), t là thời gian bóng đèn được thắp sáng liên tục (s). Coi toàn bộ điện năng cực đại (công cực đại) do pin sinh ra khi tiêu thụ hết 16,25 gam Zn ở điều kiện chuẩn dùng để thắp sáng một bóng đèn với công suất 10 W thì thời gian (giây) bóng đèn được thắp sáng liên tục là? (Kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 28: Cho sơ đồ phản ứng sau:
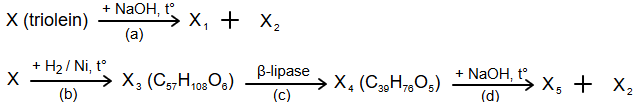
Cho biết:
– X1, X2 và X5 là các hợp chất hữu cơ chỉ chứa một loại nhóm chức.
– Trong chuyển hoá (b), X phản ứng với H2 (xúc tác Ni, đun nóng) thu được hỗn hợp sản phẩm trong đó có X3.
– Ở phản ứng (c), enzyme β-lipase chỉ xúc tác cho sự thuỷ phân nhóm chức ester liên kết với nguyên tử carbon số 2 của gốc glycerol.
Cho các nhận xét sau:
(1) X1 là glycerol.
(2) X2 tan vô hạn trong nước.
(3) Để tạo thành X3, 1 phân tử X cần phản ứng với 2 phân tử H2.
(4) X4 là hợp chất hữu cơ không no, mạch hở.
(5) Thuỷ phân hoàn toàn 1 mol X4 bằng dung dịch NaOH dư thu được 2 mol X5.
(6) Có 2 công thức cấu tạo của X3 thỏa mãn sơ đồ phản ứng trên.
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
(Xem giải) Câu 29: Phản ứng tổng hợp ammonia trong công nghiệp theo phương trình hoá học trong bình kín: N2(g) + 3H2(g) ⇋ 2NH3(g)  = -91,8 kJ
= -91,8 kJ
Cho các phát biếu sau:
(1) Phản ứng thuận toả nhiệt và tăng áp suất.
(2) Nhiệt tạo thành của NH3 là 45,9 kJ/mol.
(3) Phản ứng đang ở trạng thái cân bằng, nếu cho một lượng khí trơ Ne vào hỗn hợp thì cân bằng chuyển dịch theo chiều thuận.
(4) Hỗn hợp gồm X gồm 4 mol N2 và 14 mol H2 được nạp vào bình kín có dung tích không đổi 10 lít và giữ ở nhiệt độ không đổi, khi phản ứng đạt trạng thái cân bằng thì ta thấy áp suất trong bình bằng 95% áp suất lúc đầu. Hằng số cân bằng của phản ứng là 1,257.10^−2.
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
(Xem giải) Câu 30: Insulin (C257H383N65O77S6) là một loại hormone từ các tế bào đảo tụy ở tuyến tụy tiết ra. Chúng có tác dụng chuyến hóa carbohydrate trong cơ thể điều tiết lượng đường trong máu. Một protein đơn (monomer) cùa insulin người chứa 51 amino acid gồm hai chuỗi peptide liên kết với nhau bởi các cầu nối disulfur. Hình vẽ dưới đây mô tả đơn giản cấu tạo của insulin.
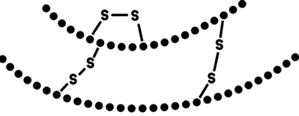
Thủy phân một phần insulin thu được heptapeptide (X). Khi thủy phân không hoàn toàn X thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu; Val-Glu-Ala; His-Leu-Val; Gly-Ser-His. Cho các phát biểu sau:
(1) Có 50 liên kết peptide trong một phân tử insulin.
(2) Insulin thuộc loại protein đơn giản.
(3) Một protein đơn của insulin người có khối lượng phân tử là 5808 amu.
(4) Insulin thúc đẩy sự hấp thu glucose của các tế bào và dự trữ glucose dư thừa trong gan và cơ.
(5) Nếu đánh số amino acid đầu N trong X là số 1 thì amino acid ở vị trí số 2 và số 6 lần lượt là Ser và Glu.
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
(Xem giải) Câu 31: Carbon dioxide (CO2) là thành phần chính trong khí thải nhà máy nhiệt điện (than, khí,…), nó là một khí thải gây hiệu ứng nhà kính và gây ra sự biến đổi khí hậu toàn cầu. Để giảm tác động của nó tới môi trường, người ta hấp thụ và tách CO2 từ khí thải nhiệt điện, sau đó lưu trữ hoặc sử dụng CO2 cho các mục đích khác nhau như tái chế hoặc sản xuất các sản phẩm hóa học (urea, soda,…).
Một nhà máy nhiệt điện khí có sản lượng điện 3,10⁶ kWh/ngày (1 kWh = 3600 kJ) đã sử dụng khí thiên nhiên làm nhiên liệu (chứa 90% CH4, 10% C2H6 về thể tích) làm nhiên liệu. Các nhiên liệu bị đốt cháy hoàn toàn (biết 58% nhiệt lượng tỏa ra của quá trình đốt cháy được chuyển hóa thành điện năng). Toàn bộ lượng khí CO2 mà nhà máy này thải ra trong 1 ngày được sử dụng để tổng hợp được m tấn urea chứa 98% (NH2)2CO, với hiệu suất là 90% (làm tròn đến hàng đơn vị). Biết CH4, C2H6 cháy theo các phương trình:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
C2H6(g) + 3,5O2(g) → 2CO2(g) + 3H2O(g)
Các giá trị nhiệt tạo thành của các chất ở điều kiện chuẩn được cho trong bảng sau:
| Chất | CH4(g) | C2H6(g) | CO2(g) | H2O(g) |
 (kJ/mol) (kJ/mol) |
–74,6 | –84,7 | –393,5 | –241,8 |
Tính giá trị của m (Kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 32: Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl không màng ngăn, nồng độ Na+ không đổi sau điện phân.
(b) Nhiệt phân muối NH4NO3 thu được NH3 và HNO3.
(c) Có thể dùng soda khan (Na2CO3) để loại bỏ ion Fe3+, Al3+ trong nước bị nhiễm phèn.
(d) Trong điện phân NaOH nóng chảy, ở cathode xảy ra quá trình: 2OH- → O2 + 2H+ + 2e.
(e) Trong điện phân Al2O3 nóng chảy với các điện cực bằng than chì, ở cathode điện cực bị khử bởi O2 sinh ra sau điện phân.
Trong các phát biểu trên, có bao nhiêu phát biểu đúng?

Bình luận