[2025] Thi thử TN sở GDĐT Bắc Ninh (Lần 4)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 114
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2B | 3D | 4D | 5B | 6B | 7B | 8A | 9D |
| 10D | 11B | 12B | 13C | 14D | 15C | 16A | 17B | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | Đ | S | 157 | 124 | 23 |
| (b) | Đ | S | Đ | Đ | 26 | 27 | 28 |
| (c) | S | S | S | S | 77 | 594 | 3 |
| (d) | S | S | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Trong nuôi thủy, hải sản, người ta có thể dùng phèn chua để làm giảm độ đục của nước do sinh vật phù du, thức ăn thừa, chất thải từ vật nuôi gây ra,… Sau khi dùng phèn chua nếu pH của nước thấp hơn quy định người ta có thể cho vào nước chất nào sau đây để đưa về đúng quy đinh?
A. Giấm ăn. B. Dung dịch nước vôi trong.
C. Dung dịch muối ăn. D. Dung dịch thuốc tím.
(Xem giải) Câu 2. Sơ cấp cứu là cung cấp sự trợ giúp y tế ngay lập tức cho nạn nhân hoặc người bệnh cho đến khi họ nhận được sự chăm sóc bởi nhân viên y tế chuyên nghiệp. Khi bị bỏng sulfuric acid, bước đầu tiên thực hiện để sơ cấp cứu là
A. chườm trực tiếp đá lạnh hoặc nước đá lên vết thương.
B. rửa sạch vết bỏng dưới vòi nước sạch.
C. cho dung dịch NaOH loãng vào vết bỏng.
D. xoa vết bỏng bằng các loại kem, gel, dầu,…
(Xem giải) Câu 3. Trong tự nhiên, kim loại nào sau đây tồn tại dạng đơn chất?
A. K. B. Al. C. Ca. D. Au.
(Xem giải) Câu 4. Phản ứng chlorine hóa methane khi chiếu sáng xảy ra theo cơ chế gốc gồm ba giai đoạn: khơi mào, phát triển mạch và tắt mạch. Trong đó, giai đoạn phát triển mạch diễn ra như sau:
Cl• + CH4 → HCl + •CH3
•CH3 + Cl2 → CH3Cl + Cl•
Nhận định nào sau đây không đúng về giai đoạn này?
A. Có sự hình thành liên kết H-Cl.
B. Có sự hình thành liên kết C-Cl.
C. Có sự phân cắt liên kết C-H.
D. Có sự hình thành liên kết π.
(Xem giải) Câu 5. Cho nhiệt độ sôi của các chất trong bảng sau:
| Chất | CH3COOC2H5 | CH3CH2CH3 | CH3CH2CH3 | CH3CHO |
| Nhiệt độ (°C) | 77,1 | -42,1 | -6,5 | 20,2 |
Ở điều kiện thường (25°C), chất nào sau đây ở trạng thái lỏng?
A. CH3CHO. B. CH3COOC2H5. C. CH3CH2CH3. D. CH3CH2CH3.
(Xem giải) Câu 6. Cho hình vẽ sau của amino acid X trong môi trường pH = 6 dưới tác dụng của điện trường:
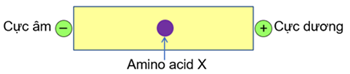
Chất X không thể là
A. glycine. B. lysine. C. alanine. D. valine.
(Xem giải) Câu 7. Trường hợp nào sau đây không xảy ra sự ăn mòn kim loại?
A. Tàu đánh cá làm bằng thép bị hoen gỉ sau thời gian đi biển về.
B. Nấu chảy vàng để đúc khuôn khi chế tác vàng trang sức.
C. Trống đồng bị chuyển màu xanh khi để lâu ngày trong không khí ẩm.
D. Vòng tay làm bằng bạc kim loại bị hóa đen khi sử dụng lâu ngày.
(Xem giải) Câu 8. Trong đời sống, PE được dùng làm màng bọc thực phẩm, túi nylon, chai lọ đưng hoá mĩ phẩm,… PE được điều chế từ monomer nào sau đây?
A. Ethylene. B. Styrene. C. Propylene. D. Vinyl chloride.
(Xem giải) Câu 9. Khi đốt cháy củi, nếu củi được chẻ nhỏ thì quá trình cháy xảy ra nhanh hơn. Vậy người ta đã đưa vào yếu tố nào sau đây để tăng tốc độ phản ứng?
A. Áp suất. B. Nồng độ. C. Nhiệt độ. D. Diện tích tiếp xúc.
(Xem giải) Câu 10. Nhiệt độ nóng chảy của kim loại nhóm IA (kim loại kiềm) có xu hướng giảm từ lithium đến caesium. Nhiệt độ nóng chảy cùa một số kim loại kiềm được cho ở bảng sau:
| Kim loại | Li | Na | Rb | Cs |
| Nhiệt độ nóng chảy (°C) | 180 | 98 | x | 29 |
Giá trị của x phù hợp là
A. 20. B. 100. C. 200. D. 39.
(Xem giải) Câu 11. Chất nào sau đây là alcohol?
A. Methyl formate. B. Ethanol. C. Phenol. D. Acetic acid.
(Xem giải) Câu 12. Cho biết độ tan (g/100 gam nước) ở 20°C cùa các muối sulfate như sau:
| Muối | MgSO4 | CaSO4 | SrSO4 | BaSO4 |
| Độ tan (g/100 g nước) | 33,7 | 0,20 | 0,0132 | 0,0028 |
Chất nào trong các chất đã cho có độ tan nhỏ nhất?
A. MgSO4. B. BaSO4. C. CaSO4. D. SrSO4.
(Xem giải) Câu 13. Chất nào sau đây là thành phần chính của chất giặt rửa tổng hợp?
A. CH3[CH2]14COOK. B. CH3[CH2]16COONa.
C. CH3[CH2]11C6H4SO3Na. D. (CH3[CH2]16COO)2Ca.
(Xem giải) Câu 14. Sục khí ethylene dư vào dung dịch bromine (có màu vàng), hiện tượng quan sát được là
A. xuất hiện kết tủa màu trắng. B. xuất hiện kết tủa màu vàng nhạt.
C. xuât hiện kết tủa màu nâu đen. D. dung dịch bị mất màu.
(Xem giải) Câu 15. Cho phức chất có công thức [CoCl4]2-. Số phối tử trong phức chất trên là
A. 1. B. 5. C. 4. D. 2.
(Xem giải) Câu 16. Nhỏ vài giọt nước bromine vào ống nghiệm chứa 2 mL dung dịch X, thu được kết tủa trắng. Chất X là
A. Aniline. B. Ethylamine. C. Methylamine. D. Dimethylamine.
(Xem giải) Câu 17. Hình ảnh dưới đây thể hiện tính chất vật lí nào của kim loại?
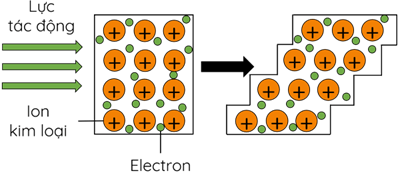
A. Tính dẫn nhiệt. B. Tính dẻo. C. Tính dẫn điện. D. Tính ánh kim.
(Xem giải) Câu 18. Phát biểu nào sau đây đúng?
A. Có thể phân biệt glucose và fructose bằng thuốc thử Tollens.
B. Ở dạng mạch hở, glucose có 6 nhóm -OH liền kề.
C. Phân tử tinh bột gồm nhiều gốc β-glucose liên kết với nhau.
D. Saccharose không tham gia phản ứng tráng bạc.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Một học sinh tiến hành thí nghiệm với giả thuyết: “Độ tan của CaSO4 tăng khi tăng nhiệt độ” như sau:
• Bước 1: Thêm lượng dư CaSO4.2H2O (3 gam) vào 100 mL nước cất trong các bình riêng biệt. Đặt mỗi bình ở các mức nhiệt độ khác nhau (cụ thể: 20°C, 40°C, 60°C, 80°C). Khuấy đều trong 15–20 phút để đạt cân bằng (đảm bảo vẫn còn chất rắn dư). Duy trì nhiệt độ ổn định ít nhất 10 phút trước khi lọc.
• Bước 2: Lọc nhanh dung dịch bão hòa trong khi vẫn giữ ở nhiệt độ ổn định như ban đầu. Thu lấy phần dịch lọc.
• Bước 3: Lấy 25 mL dung dịch đã lọc và làm bay hơi hết nước rồi cân phần chất khan rắn còn lại. Tính độ tan theo đơn vị gam chất tan trong 100 mL nước (xem thể tích thay đổi không đáng kể trong quá trình hòa tan).
Kết quả như sau:
| Nhiệt độ (°C) | 20 | 40 | 60 | 80 |
| Độ tan (g/100mL nước) | 0,285 | 0,168 | 0,162 | 0,155 |
a) Học sinh lọc dung dịch bão hòa trong điều kiện giữ nhiệt độ ổn định với mục đích tránh kết tinh muối làm sai lệch kết quả.
b) Mục tiêu của thí nghiệm là xác định sự thay đổi độ tan CaSO4 theo nhiệt độ.
c) Từ kết quả cho thấy giả thuyết ban đầu của học sinh là đúng.
d) Ở 40°C, khối lượng chất rắn thu được ở bước 3 là 0,168 gam.
(Xem giải) Câu 20. Cation Cu2+ có cấu hình electron [Ar]3d9 có thể tạo phức được với nhiều phối tử bằng liên kết cho-nhận giữa phối tử với các orbital trống của cation Cu2+. Một thí nghiệm về sự tạo thành hợp chất phức được thực hiện như sau:
(1) Hoà tan một lượng muối CuSO4 khan màu trắng vào nước, thu được dung dịch X có màu xanh
(2) Thêm tiếp dung dịch NH3 vào dung dịch X, thu được kết tủa (Y) màu xanh nhạt
(3) Tiếp tục thêm dung dịch NH3 đặc đến dư vào đến khi kết tủa bị hoà tan, thu được dung dịch Y có màu xanh lam.
Chuỗi thí nghiệm trên được biểu diễn qua sơ đồ sau:
CuSO4(s) → [Cu(OH2)6]SO4(aq) → [Cu(OH)2(OH2)4](s) → [Cu(NH3)4(OH2)2](OH)2(aq)
Màu xanh của kết tủa và dung dịch được lí giải là do sự hình thành các phức chất gây ra.
a) Các phản ứng (2), (3) đều có sự thay thế một số phối tử trong phức chất.
b) Màu xanh của dung dịch X là do anion trong phức chất gây ra.
c) Số electron lớp ngoài cùng của cation Cu2+ là 9.
d) Trong phức [Cu(NH3)4(OH2)2](OH)2, phối tử tạo phức là NH3, H2O, OH-.
(Xem giải) Câu 21: Pin kẽm-mangan (Zn-MnO2) là loại pin phổ biến trong các thiết bị điện tử do giá thành thấp và an toàn. Tuy nhiên, loại pin này thường có tuổi thọ ngắn do phản ứng phụ làm giảm hiệu suất hoạt động. Một nhóm học sinh nghiên cứu ảnh hưởng của nồng độ KOH đến hiệu suất và tuổi thọ của pin Zn-MnO2. Thí nghiệm được tiến hành như sau:
• Bước 1: Pha các dung dịch KOH với nồng độ 2M, 6M, 10M.
• Bước 2: Lắp ráp pin Zn-MnO2
– Điện cực cực âm (anode): Dùng tấm kẽm (Zn).
– Điện cực cực dương (cathode): Dùng MnO2 trộn với than hoạt tính và chất kết dính để tạo thành điện cực.
– Nhúng điện cực vào dung dịch KOH tương ứng.
• Bước 3:
– Đo hiệu suất ban đầu, ghi nhận các giá trị vào bảng số liệu.
-Sử dụng máy đo dung lượng pin để tiến hành sạc-xả 50 chu kỳ.Ghi lại dung lượng sau mỗi 10 chu kỳ.
– So sánh dung lượng ban đầu và dung lượng sau 50 chu kỳ.
– Xác định hiệu suất Coulombic (%) của từng mẫu.
– Kiểm tra sự suy giảm hiệu suất do ăn mòn kẽm hoặc hòa tan MnO2.
| Nồng độ KOH (M) | Dung lượng ban đầu (mAh/g) | Dung lượng sau 50 chu kỳ (mAh/g) | Hiệu suất Coulombic (%) |
| 2M | 180 | 120 | 85% |
| 6M | 210 | 170 | 92% |
| 10M | 190 | 100 | 80% |
a) Giả thuyết phù hợp với mục đích và quá trình tiến hành thí nghiệm trên là “nếu sử dụng chất điện ly kiềm (KOH) có nồng đọ tối ưu, thì hiệu suất và tuổi thọ của pin Zn-MnO2 sẽ được cải thiện”.
b) Khi nồng độ KOH quá cao thúc đẩy quá trình tiêu thụ zinc, làm giảm tuổi thọ của pin.
c) Cực âm xảy ra quá trình khử kẽm và cực dương xảy ra quá trình oxi hóa MnO2 .
d) Trong thí nghiệm, pin với KOH 6M có hiệu suất cao nhất, dung lượng duy trì tốt sau 50 chu kỳ.
(Xem giải) Câu 22. Lương khô (bánh lương khô) là một loại thực phẩm được làm sẵn và ép khô thành bánh với thành phần chủ yếu là tinh bột, đường, chất béo, protein. Lương khô thường được dùng khi hành quân, dã ngoại,… do có ưu điểm là dễ dự trữ, dễ bảo quản và sử dụng tiện lợi. Thông tin về thành phần dinh dưỡng của một loại lương khô X như sau:
| Giá trị dinh dưỡng trên / Nutrition per | 100g |
| Năng lượng / Energy | 385 kcal – 495 kcal |
| Glucide / Carbohydrate | 70 g – 80 g |
| Chất béo / Lipid | 9 g – 15 g |
| Đạm / Protein | 6 g – 10 g |
Cho biết: mỗi 1 gam carbohydrate, lipid, protein cung cấp năng lượng cho cơ thể lần lượt là 4 kcal, 9 kcal và 4 kcal.
a) Trong mẫu lương khô X, protein cung cấp năng lượng nhiều hơn chất béo.
b) Thành phần chính của lương khô X là carbohydrate.
c) 100 gam lương khô X cung cấp năng lượng từ 280 – 320 kcal.
d) Phần trăm khối lượng chất béo trong mẫu lương khô X luôn dưới 10%.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 1. Sodium carbonate (Na2CO3) là chất thường dùng để làm mềm nước cứng theo phương pháp kết tủa. Độ cứng của nước có thể được tính theo số mg CaCO3 trong 1 lít nước, trong đó độ cứng không vượt quá 60 mg/L là nước mềm. Để xử lí một mẫu nước cứng vĩnh cửu có độ cứng a (mg CaCO3/L) người ta cho 1 lít dung dịch Na2CO3 0,020 M vào 19 lít mẫu nước cứng, lắc đều, thu được kết tủa CaCO3 và nước mềm Y. Nồng độ Ca2+ và CO32- có trong nước mềm Y lần lượt là 5,00.10^-4 M và 8,93.10-6 M. Giả thiết rằng, mẫu nước cứng chứa Ca2+ và các ion khác, các ion khác này không tham gia phản ứng, ion CO32- và ion Ca2+ không bị thuỷ phân trong nước. Tính giá trị của a (làm tròn đến hàng đơn vị).
(Xem giải) Câu 2. Để làm đậu phụ từ đậu tương, ban đầu người ta xay đậu tương với nước lọc và đun sôi. Sau đó, thêm nước chua vào dung dịch nước đậu tương đã được nấu chín, khi đó “óc đậu” sẽ bị kết tủa. Sau khi trải qua quá trình lọc, ép, chế biến, sẽ thu được thành phẩm đậu phụ. Nước chua có thể làm từ nước đậu phụ lên men hoặc giấm ăn. Để thu hồi đậu phụ nhanh và mịn, thay vì dùng nước chua để làm óc đậu, người ta có thể sử dụng thạch cao với hàm lượng an toàn với sức khỏe là không quá 1 g/1 kg đậu phụ. Cho các phát biểu sau:
(1) Bản chất sự tạo thành “óc đậu” từ dung dịch nước đậu tương xảy ra sự đông tụ protein.
(2) Nước chua có tính acid làm protein trong dung dịch nước đậu tương bị đông tụ.
(3) Thành phần chính của thạch cao là calcium carbonate.
(4) Nếu hàm lượng thạch cao vượt ngưỡng 1 gam / kg đậu phụ thì ảnh hưởng không tốt đến sức khỏe người dùng.
Các nhận định đúng gồm những nhận định nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 123; 234; …)
(Xem giải) Câu 3. Sodium dodecylbenzene sulfonate (SDBS) có công thức C15H25C6H4SO3Na. SDBS là một loại chất hoạt động bề mặt đa năng có nhiều ứng dụng trong chất giặt rửa tổng hợp, sản phẩm làm sạch và nhiều quy trình công nghiệp khác nhau.(1) SDBS có đầu ưa nước là Na+.
(2) SDBS được sản xuất từ dầu mỏ qua nhiều giai đoạn.
(3) SDBS có thể dùng giặt rửa trong nước cứng.
(4) SDBS có giá thành thấp, không gây ô nhiễm môi trường.
Các nhận định đúng gồm những nhận định nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 123; 234;…).
(Xem giải) Câu 4. Một nhà máy gang thép sản xuất thép thành phẩm từ m tấn quặng hematite đỏ (chứa 84% Fe2O3 về khối lượng, còn lại là tạp chất không chứa sắt) với hiệu suất cả quá trình đạt 90% theo sơ đồ: Quặng hematit đỏ → Gang trắng → Thép → Thép thành phẩm
Toàn bộ lượng thép thành phẩm được cán thành 1434 cây thép hình trụ “phi 20” (đường kính 20 mm) dài 11,7m. Giá trị của m là bao nhiêu? (Chỉ làm tròn kết quả ở phép tính cuối cùng; kết quả làm tròn tới hàng đơn vị). (Cho π = 3,14; thép thành phẩm chứa 98% sắt về khối lượng và thép thành phẩm có khối lượng riêng là 7,9 tấn/m³).
(Xem giải) Câu 5. Tín chỉ carbon (carbon credit) là chứng nhận quyền phát thải khí CO2 hoặc khí nhà kính khác được quy đổi tương đương sang CO2 (CO2tđ). Cho biết 1 tín chỉ carbon tương đương với 1 tấn khí CO2 được phát thải vào bầu khí quyển. CO2tđ là đơn vị mua bán trên thị trường carbon, tín chỉ carbon. Bên bán là bên có khả năng giảm hoặc loại bỏ phát thải được công nhận. Cuối 2013, Bộ Nông nghiệp và Phát triển Nông thôn bán 10,3 triệu tấn CO2 cho Ngân hàng Thế giới (World Bank), thu về 51,5 triệu USD, tương đương 5 USD một tín chỉ carbon. Một quả đồi có diện tích 30000 m² trồng cây keo với mật độ 10 m²/1 cây, trung bình mỗi cây khai thác 243 kg gỗ (chứa 50% cellulose về khối lượng). Ứng với quá trình tạo ra lượng cellulose ở đồi keo trên đã tiết kiệm được được bao nhiêu tín chỉ carbon? (Chỉ làm tròn kết quả ở phép tính cuối cùng; kết quả làm tròn đến hàng đơn vị)
(Xem giải) Câu 6. Để tái chế nhôm, người ta có thể sử dụng phế liệu kim loại như vỏ của các lon, hộp chứa nước giải khát hay thực phẩm. Phế liệu này còn lẫn các tạp chất là các hợp chất hữu cơ và vô cơ (có trong nhãn, mác in hoặc son trên vỏ lon, hộp). Phế liệu được cắt, băm nhỏ rồi cho vào lò nung đến khi chảy lỏng. Phần lớn các tạp chất biến thành xỉ lỏng, nổi lên trên, được vớt ra khỏi lò. Phần còn lại trong lò là nhôm tái chế ở trạng thái nóng chảy.
Cho các nhận định sau:
(1) Cắt, băm nhỏ phế liệu nhôm trước khi nung chảy để quá trình nung xảy ra nhanh hơn.
(2) Xỉ lỏng được đùng để chế tạo các vật dụng như xoong, nồi, chảo…
(3) Tái chế nhôm phế liệu giúp tiết kiệm nguồn tài nguyên thiên nhiên, giảm thiểu sự khai thác quặng bauxite, làm giảm tác động tiêu cực đến môi trường.
(4) Do các sản phẩm từ nhôm tái chế có độ tinh khiết thấp, dễ lẫn các tạp chất kim loại nặng khác như chì, asen, cadimi… Vì vậy nhôm tái chế không được dùng để chế tạo dụng cụ y tế.
(5) Trong quá trình tái chế nhôm xảy ra quá trình khử ion Al3+ thành Al .
Có bao nhiêu nhận định đúng?


Bình luận