[2026] Thi thử TN cụm trường phía nam Hưng Yên (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 095
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2D | 3D | 4C | 5B | 6A | 7A | 8A | 9D |
| 10D | 11C | 12C | 13A | 14D | 15D | 16D | 17A | 18A |
| 19 | 20 | 21 | 22 | |
| (a) | S | Đ | S | S |
| (b) | S | Đ | Đ | Đ |
| (c) | Đ | S | Đ | Đ |
| (d) | Đ | Đ | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 87,4 | 94,8 | 2,05 | 200 | 2796 | 22 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Quá trình xảy ra ở cathode khi điện phân nóng chảy NaCl là
A. khử ion Cl-. B. oxi hóa ion Cl-. C. khử ion Na+. D. oxi hóa ion Na+.
(Xem giải) Câu 2. Dung dịch chất nào sau đây không có tác dụng làm mềm nước cứng tạm thời?
A. Na2CO3. B. Ca(OH)2. C. Na3PO4. D. HCl.
(Xem giải) Câu 3. Sức điện động chuẩn của pin Galvani tạo bởi các cặp oxi hóa – khử X2+/X và Y2+/Y là 0,78 V. Biết X có tính khử yếu hơn Y, thế điện cực chuẩn của X2+/X và Y2+/Y lần lượt là +0,34 V và a V. Giá trị của a là
A. -1,12. B. +0,44. C. +1,12. D. -0,44.
(Xem giải) Câu 4. Sản phẩm thiên nhiên nào sau đây không chứa tinh bột?
A. Quả chuối xanh. B. Hạt ngô. C. Sợi bông. D. Củ khoai.
(Xem giải) Câu 5. Đốt muối chloride của kim loại M trên ngọn lửa đèn khí, thấy ngọn lửa nhuốm màu tím. M là
A. Li. B. K. C. Ca. D. Na.
(Xem giải) Câu 6. Thủy phân hoàn toàn protein đơn giản nhờ xúc tác men thu được sản phẩm là
A. α-amino acid. B. β-amino acid. C. α-glucose. D. Glycerol.
(Xem giải) Câu 7. Trong tự nhiên, kim loại nào sau đây ngoài dạng hợp chất còn tồn tại chủ yếu ở dạng đơn chất?
A. Au. B. Al. C. Fe. D. Na.
(Xem giải) Câu 8. Ester tạo bởi ethyl alcohol và propionic acid có công thức cấu tạo là
A. CH3CH2COOCH2CH3. B. CH3COOCH2CH3.
C. CH3CH2COOCH3. D. CH3COOCH2CH2CH3.
(Xem giải) Câu 9. Chọn phát biểu sai về cân bằng hóa học sau: HS-(aq) + H2O(l) ⇋ S2-(aq) + H3O+(aq)
A. Khi thêm dung dịch NaOH, cân bằng chuyển dịch theo chiều thuận.
B. Các base trong cân bằng trên là S2- và H2O.
C. HS- là một acid theo chiều thuận của cân bằng trên.
D. Các cặp acid/base liên hợp của cân bằng trên là HS-/S2- và H2O/H3O+.
(Xem giải) Câu 10. Chất nào sau đây không thuộc loại acid béo?
A. CH3[CH2]10COOH. B. CH3[CH2]16COOH. C. CH3[CH2]14COOH. D. CH3CH2COOH.
(Xem giải) Câu 11. Phosphorus là nguyên tố quan trọng trong việc hình thành cấu trúc của xương, răng ở động vật và thúc đẩy phát triển bộ rễ, ra hoa ở cây trồng. Cấu hình electron của nguyên tử phosphorus (Z = 15) là
A. 1s22s22p63s23p2. B. 1s22s22p63s13p4.
C. 1s22s22p63s23p3. D. 1s22s22p63s33p2.
(Xem giải) Câu 12. Cho các chất: Vinyl acetate, styrene, ethylene glycol, caprolactam, hexamethylenediamine, acrylonitrile. Số chất thỏa mãn điều kiện của monomer tham gia phản ứng trùng hợp là
A. 5. B. 2. C. 4. D. 3.
(Xem giải) Câu 13. Phát biểu nào sau đây đúng khi nói về các hợp chất của nitrogen?
A. Trong điện trường có pH = 7, glutamic acid di chuyển về phía cực dương.
B. Có 4 amine thể khí ở điều kiện thường, chúng đều phản ứng được với nitrous acid tạo ra alcohol.
C. Các peptide đều có tính chất hóa học đặc trưng là phản ứng màu biuret.
D. Dung dịch aniline làm quỳ tím hóa xanh, còn phenolphthalein chuyển sang màu hồng.
(Xem giải) Câu 14. Aspirin là một dược chất có tác dụng giảm đau, hạ sốt, được điều chế theo phản ứng sau:
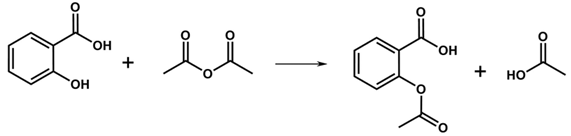
Phản ứng trên thuộc loại nào sau đây?
A. Phản ứng trao đổi. B. Phản ứng cộng.
C. Phản ứng tách. D. Phản ứng thế.
(Xem giải) Câu 15. Kim loại nhôm có nhiều ứng dụng trong công nghiệp và đời sống. Ứng dụng sản xuất xoong nồi, ấm đun nước dựa trên tính chất vật lí chủ đạo nào của nhôm?
A. Tính dẻo. B. Khối lượng riêng. C. Tính dẫn điện. D. Tính dẫn nhiệt.
(Xem giải) Câu 16. X và Y là hai hydrocarbon đều chứa 85,71 % khối lượng nguyên tố carbon. Phổ MS của hai mẫu hợp chất này được cho trong hình sau:
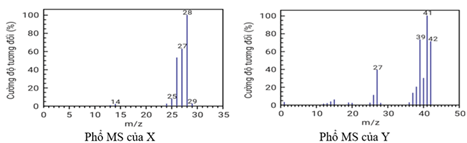
Công thức phân tử của X và Y lần lượt là
A. C3H6 và C2H4. B. C2H5 và C3H6.
C. C3H6 và C2H5. D. C2H4 và C3H6.
(Xem giải) Câu 17. Phức chất nào dưới đây thuộc loại phức bát diện?
A. [Ni(NH3)6]2+. B. [Fe(CO)5]. C. [Ag(NH3)2]+. D. [PtCl4]2-.
(Xem giải) Câu 18. Người ta nung vôi từ đá vôi, nhiệt lượng thường lấy từ quá trình đốt cháy than cốc (chủ yếu chứa carbon vô định hình) hay đốt cháy khí thiên nhiên (chủ yếu chứa methane). Phát biểu nào dưới đây không đúng? Biết các phản ứng chính và enthalpy tạo thành chuẩn của một số chất như sau:
(1) CaCO3(s) → CaO(s) + CO2(g)
(2) C(s) + O2(g) → CO2(g)
(3) CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
| Chất | CaCO3(s) | CaO(s) | CO2(g) | H2O(g) | CH4(g) |
| -1207,6 | -634,9 | -393,5 | -241,8 | -74,6 |
A. Biến thiên enthalpy chuẩn của phản ứng (2) cũng là enthalpy tạo thành chuẩn của CO2(g).
B. Biến thiên enthalpy chuẩn của phản ứng (3) là -802,5 kJ.
C. Phản ứng nung vôi thu nhiệt, còn phản ứng đốt cháy than cốc hay khí thiên nhiên đều tỏa nhiệt.
D. Phản ứng (1) có biến thiên enthalpy chuẩn là +179,2 kJ.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Hoa bưởi không chỉ có hương thơm thanh tao mà còn mang lại nhiều giá trị trong đời sống, từ ẩm thực, làm đẹp đến chăm sóc sức khỏe. Mùi thơm của hoa bưởi chủ yếu do tinh dầu chứa các hợp chất thơm dễ bay hơi có trong cánh hoa tạo nên, trong đó linalool là thành phần chính, ngoài ra còn có các chất thơm khác như limonene, geraniol, nerolidol,… Cấu tạo của linalool và limonene lần lượt như sau:
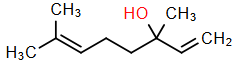
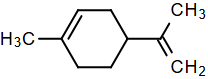
a) Hương thơm của hoa bưởi chủ yếu do linalool và limonene là hai thành phần chính trong tinh dầu ở cánh hoa tạo nên.
b) Linalool và limonene đều làm mất màu nước bromine, nhưng chỉ linalool bị oxi hóa bởi CuO nung nóng tạo ra ketone.
c) Phần trăm về khối lượng của bromine làm tròn đến hàng phần trăm trong sản phẩm cộng tối đa Br2 vào limonene là 70,18%.
d) Linalool và limonene đều tác dụng tối đa với H2 (xúc tác Ni, t°) theo cùng tỉ lệ mol.
(Xem giải) Câu 20. Cho sơ đồ mô tả các bước sản xuất một loại phân bón như sau:
![]()
a) T là phân đạm hai lá, bón dư thừa phân T cũng là nguyên nhân gây ra hiện tượng phú dưỡng.
b) Phần trăm về khối lượng của nguyên tố nitrogen trong T là 35,0%.
c) X, Y là các chất khí không màu, khi phát thải hàm lượng lớn từ động cơ, nhà máy vào khí quyển gây ô nhiễm môi trường và gây hiện tượng mưa acid.
d) Tổng hệ số nguyên tối giản của các chất trong phản ứng (2) là 19.
(Xem giải) Câu 21. X là một hợp chất hữu cơ đơn chức (phân tử chứa C, H, O). Trên phổ MS của X, thấy xuất hiện peak ion M+ có giá trị m/z lớn nhất là 88. Từ X, thực hiện sơ đồ phản ứng theo đúng tỉ lệ mol như sau:
X + NaOH (t°) → X1 + X2
X2 + CuO (t°) → X3 + Cu + H2O
X3 + Br2 + H2O → X4 + 2HBr
X1 + HBr → X4 + NaBr
a) X2 được dùng sản xuất xăng sinh học hiện nay, trong xăng E5 có chứa 95% thể tích X2.
b) X ít tan trong nước nhưng dễ tan trong dung môi hữu cơ, còn X2 và X4 tan vô hạn trong nước.
c) Có 4 hợp chất hữu cơ có cùng số nguyên tử carbon trong sơ đồ trên.
d) Nhiệt độ sôi của X2, X3, X4 được sắp xếp theo chiều tăng dần là X3 < X2 < X4.
(Xem giải) Câu 22. Đồng hồ mạ vàng có vỏ và dây làm từ thép không gỉ, được mạ một lớp vàng mỏng bên ngoài (0,5 – 5 μm) để tạo thẩm mỹ và sự sang trọng cho người dùng. Một trong các phương pháp mạ vàng cho chiếc đồng hồ là điện phân dung dịch muối K[Au(CN)2] với 1 điện cực là thanh kim loại vàng nguyên chất, 1 điện cực là vỏ và dây của chiếc đồng hồ đã được xử lí bề mặt để tăng độ bám dính khi mạ. Biết trong dung dịch tồn tại cân bằng: [Au(CN)2]- ⇌ Au+ + 2CN-; Khối lượng riêng của vàng là 19,3 g/cm³; Mật độ dòng là 1 A/dm² (j = I/S, j là mật độ dòng, I là cường độ dòng điện có đơn vị là A, S là diện tích bề mặt).
a) Nồng độ ion Au+ trong dung dịch giảm dần theo thời gian điện phân.
b) Anode là thanh kim loại vàng, cathode là vỏ và dây của chiếc đồng hồ, cả 2 điện cực được nhúng trong dung dịch K[Au(CN)2].
c) Khi có dòng điện một chiều chạy qua, các ion Au+ bị khử tại cathode thành Au và phủ lên bề mặt vỏ và dây của chiếc đồng hồ.
d) Mất 222,45 giây để hoàn thành mạ vàng cho một chiếc đồng hồ có tổng diện tích bề mặt 100 cm² với độ dày đồng đều của lớp mạ 2 μm, hiệu suất điện phân là 85%. (Kết quả làm tròn đến hàng phần trăm).
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Theo QCVN 01-1:2018/BYT, hàm lượng sắt tối đa cho phép trong nước sinh hoạt là 0,30 mg/L. Một loại nước giếng khoan có mùi tanh do chứa hàm lượng sắt cao gấp 3 lần ngưỡng cho phép (90% dạng Fe2+, 10% dạng Fe3+). Người ta loại bỏ sắt ra khỏi loại nước trên bằng cách thêm một lượng vôi tôi, kết hợp khuấy trộn và sục không khí. Các phản ứng chính xảy ra như sau:
4Fe2+(aq) + O2(aq) + 10H2O(l) → 4Fe(OH)3(s) + 8H+(aq)
H+(aq) + OH-(aq) → H2O(l)
Fe3+(aq) + 3OH-(aq) → Fe(OH)3(s)
Khối lượng vôi tôi (làm tròn đến hàng phần chục) cần vừa đủ cho các phản ứng trên để loại bỏ hoàn toàn sắt ra khỏi 70 m³ nước là bao nhiêu gam? Giả sử vôi tôi đã dùng chỉ chứa Ca(OH)2.
(Xem giải) Câu 24. Trong ngành dược, diethyl phthalate (DEP) là một hoạt chất được dùng trị ghẻ, ngứa do viêm da hay bị côn trùng cắn. Phản ứng tổng hợp DEP từ phthalic anhydride và lượng dư ethyl alcohol như sau:
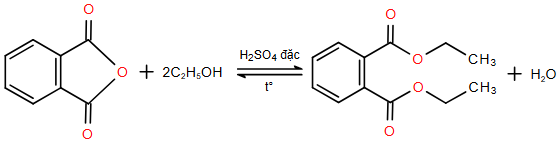
Để sản xuất 20000 lọ thuốc DEP cần bao nhiêu kg phthalic anhydride? Biết hiệu suất phản ứng là 90%, mỗi lọ thuốc có khối lượng 8 gam, trong đó có 80% khối lượng DEP, còn lại là tá dược. (Chỉ làm tròn phép tính ở kết quả cuối cùng, đến hàng phần chục).
(Xem giải) Câu 25. Một dung dịch NaOH tính toán theo lí thuyết sau khi pha chế có nồng độ là 0,25M. Để kiểm tra bằng thực nghiệm, người ta chuẩn độ dung dịch NaOH này bằng dung dịch chuẩn HCl 0,20M với chất chỉ thị phenolphthalein, các bước tiến hành như sau:
• Bước 1: Dùng pipette lấy 10 mL dung dịch NaOH vào bình tam giác (erlen) đã rửa sạch rồi thêm tiếp 2 – 3 giọt chất chỉ thị phenolphtalein.
• Bước 2: Tráng sạch burette (loại 25 mL) bằng nước cất, sau đó tráng lại bằng dung dịch HCl 0,20M ở trên. Sau khi xả nước tráng, rót dung dịch HCl 0,20M vào burette rồi điều chỉnh về mức 0.
• Bước 3: Mở từ từ khóa burette, nhỏ từng giọt dung dịch chuẩn vào erlen (lắc đều trong quá trình chuẩn độ) cho đến khi dung dịch vừa mất màu hồng thì dừng chuẩn độ.
• Bước 4: Ghi lại thể tích dung dịch chuẩn đã dùng.
Trong phép chuẩn độ này, thể tích dung dịch HCl đã dùng sau 3 lần thực hiện lần lượt là 12,24 mL, 12,25 mL và 12,24 mL. Sai số về nồng độ mol/L của dung dịch NaOH ở trên giữa lí thuyết và thực nghiệm là bao nhiêu %? (Chỉ làm tròn phép tính ở kết quả cuối cùng, đến hàng phần trăm).
(Xem giải) Câu 26. Tyrosine là nguyên liệu thô để cơ thể tổng hợp nên các hormone và chất dẫn truyền thần kinh thiết yếu, nó được ví như kiến trúc sư cho bộ não và tinh thần. Cấu tạo của phân tử tyrosine như hình sau:
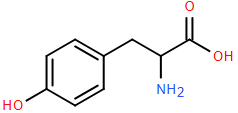
Thể tích dung dịch NaOH 0,5M cần dùng để phản ứng vừa đủ với 9,05 gam tyrosine là bao nhiêu mL?
(Xem giải) Câu 27. Quặng argentite sau khi tuyển nổi có hàm lượng Ag2S là 70% (còn lại là tạp chất không chứa Ag). Từ loại quặng này, người ta tách lấy kim loại Ag theo các bước sau:
• Bước 1: Nghiền quặng với dung dịch NaCN loãng, kết hợp thổi luồng không khí, xảy ra phản ứng:
2Ag2S + 8NaCN + 2H2O + O2 → 4Na[Ag(CN)2] + 4NaOH + 2S
• Bước 2: Cho bột kẽm vào dung dịch thu được, xảy ra phản ứng:
2Na[Ag(CN)2] + Zn → Na2[Zn(CN)4] + 2Ag
• Bước 3: Hòa tan hỗn hợp kim loại trong dung dịch H2SO4 loãng, dư. Lọc kim loại không tan, nấu luyện ở nhiệt độ trên 1000°C, thêm chất trợ dung rồi vớt xỉ, thu lấy kim loại nóng chảy để nguội được bạc thô.
• Bước 4: Tinh luyện Ag bằng cách điện phân dung dịch AgNO3, cathode là thanh bạc nguyên chất, anode là thanh bạc thô.
Biết hiệu suất của các bước 1, 2, 3, 4 lần lượt là 95%, 98%, 99,5% và 99%. Từ 5 tấn quặng argentite ở trên, sau quy trình tách và tinh luyện thu được bao nhiêu kg kim loại Ag? (Chỉ làm tròn phép tính ở kết quả cuối cùng, đến hàng đơn vị).
(Xem giải) Câu 28. Cây đoạn trường thảo (lá ngón độc) có độc tính rất mạnh, chủ yếu do các alkaloid như koumine, gelsemine, gelsenicine,… gây ra, trong đó gelsenicine có độc tính mạnh nhất. Chỉ cần ăn phải 2 đến 3 lá ngón độc là đủ gây tử vong cho một người trưởng thành nếu không được cấp cứu kịp thời. Dựa vào cấu trúc hóa học của gelsenicine (hình dưới), hãy xác định số nguyên tử hydrogen có trong phân tử này.
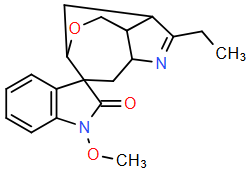

Bình luận