[2026] Thi thử TN sở GDĐT Hải Phòng (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 130
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2B | 3D | 4B | 5A | 6B | 7D | 8A | 9C |
| 10C | 11A | 12C | 13A | 14B | 15D | 16A | 17A | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | S | S |
| (b) | S | Đ | Đ | S |
| (c) | Đ | S | S | Đ |
| (d) | S | S | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 588 | 3 | 234 | 5,21 | 4 | 4 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Nhận xét nào sau đây đúng khi nói về cellulose?
A. Cellulose thuộc loại disaccharite.
B. Cellulose và tinh bột là đồng phân của nhau.
C. Cellulose là nguyên liệu để chế tạo thuốc súng không khói.
D. Công thức của cellulose là C6H10O5.
(Xem giải) Câu 2. Hợp chất nào sau đây là hợp chất ion?
A. HCl. B. KCl. C. NH3. D. H2O.
(Xem giải) Câu 3. Xét các cặp oxi hóa – khử sau:
| Cặp oxi hóa – khử | Mg2+/Mg | Al3+/Al | Fe2+/Fe | 2H+/H2 | Cu2+/Cu | Ag+/Ag |
| Thế điện cực chuẩn (V) | -2,356 | -1,676 | -0,440 | 0,000 | +0,340 | +0,799 |
Phát biểu nào sau đây đúng?
A. Sức điện động chuẩn của pin điện hoá Fe – Cu là 0,920 V.
B. Khi cho cùng một lượng Mg và Fe lần lượt vào 2 ống nghiệm đựng V ml dung dịch H2SO4 0,2M thì tốc độ thoát khí thoát ra ở cốc Fe nhanh hơn.
C. Mg được điều chế bằng phương pháp nhiệt nhôm.
D. Ion kim loại có tính oxi hóa mạnh nhất là Ag+.
(Xem giải) Câu 4. Cho sơ đồ: ![]()
Trong quá trình trên, từ 1 mol saccharose tạo được tối đa bao nhiêu mol bạc kim loại?
A. 1 mol. B. 4 mol. C. 2 mol. D. 3 mol.
(Xem giải) Câu 5. Cho bảng số liệu sau:
| Chất | Nước (H2O) | Hydrogen sulfide (H2S) |
| Nhiệt độ sôi (°C) ở 1atm | 100,0 | -60,7 |
Phát biểu nào sau đây đúng?
A. Do nước có liên kết hydrogen giữa các phân tử nên nước có nhiệt độ sôi cao hơn hydrogen sulfide.
B. Số liên kết trong phân tử H2O nhiều hơn số liên kết trong phân tử H2S.
C. Trong phân tử H2O và phân tử H2S chỉ có các liên kết cộng hóa trị không phân cực.
D. Liên kết O-H trong phân tử H2O kém phân cực hơn liên kết S-H trong phân tử H2S.
(Xem giải) Câu 6. Aniline được điều chế bằng cách khử hợp chất X theo phương trình hóa học X + 6[H] → C6H5NH2 + 2H2O. Chất X có thể là
A. C6H5COOCH3. B. C6H5NO2. C. C6H5OH. D. C6H5COOH.
(Xem giải) Câu 7. Tên gọi theo danh pháp thay thế của CH3CH2COOCH3 là
A. methyl ethanoate. B. propyl acetate.
C. methyl propionate. D. methyl propanoate.
(Xem giải) Câu 8. Hang Sơn Đoòng tại tỉnh Quảng Bình, Việt Nam là hang động tự nhiên lớn nhất và có thạch nhũ đẹp nhất thế giới. Thạch nhũ tăng kích thước với tốc độ 0,13 – 3 mm mỗi năm. Thạch nhũ trong hang động được tạo thành bởi phản ứng nào sau đây?
A. Ca(HCO3)2 → CaCO3 + CO2 + H2O. B. CaCO3 + CO2 + H2O → Ca(HCO3)2.
C. CaCl2 + Na2CO3 → CaCO3 + 2NaCl. D. Ca(OH)2 + CO2 → CaCO3 + H2O.
(Xem giải) Câu 9. Cho phản ứng hoá học CH2=CH2 + Br2 → CH2Br-CH2Br. Phản ứng này thuộc loại phản ứng
A. ester hoá. B. hydrate hoá. C. cộng. D. thế.
(Xem giải) Câu 10. Trường hợp nào sau đây không xảy ra ăn mòn điện hóa?
A. Tại vị trí nối dây phơi làm bằng đồng nối với dây phơi bằng sắt để trong không khí ẩm.
B. Gang và thép để trong không khí ẩm.
C. Đồ trang sức bằng bạc có thể bị chuyển sang màu đen do bạc tác dụng với O2 và H2S khi đeo lâu ngày.
D. Một tấm tôn (lá thép tráng kẽm) che mái nhà bị xước sâu khi trời mưa.
(Xem giải) Câu 11. Xét cân bằng: C(s) + H2O(g) ⇋ CO(g) + H2(g). Biểu thức hằng số cân bằng của hệ là
A. Kc = [CO][H2]/[H2O]. B. Kc = [CO][H2]/[C][H2O]
C. Kc = [CO][H2]. D. Kc = ([CO] + [H2])/([C] + [H2O])
(Xem giải) Câu 12. Ở trạng thái cơ bản, sau khi nguyên tử Cr (Z = 24) nhường đi 2 electron để tạo thành Cr2+ thì số electron còn lại trên phân lớp d là
A. 3. B. 5. C. 4. D. 1.
(Xem giải) Câu 13. Phương trình hóa học nào sau đây biểu diễn quá trình điều chế kim loại bằng phương pháp điện phân dung dịch?
A. CuCl2 → Cu + Cl2. B. Zn + CuSO4 → ZnSO4 + Cu.
C. 2Al2O3 → 4Al + 3O2. D. 2Al + Cr2O3 → Al2O3 + 2Cr.
(Xem giải) Câu 14. Cho phản ứng hạt nhân sau: ![]() . Phát biểu nào sau đây đúng?
. Phát biểu nào sau đây đúng?
A. Số khối của X là 62. B. Số hạt neutron trong hạt nhân X là 34.
C. Phản ứng trên là phản ứng nhiệt hạch. D. X là nguyên tố thuộc chu kì 3 bảng tuần hoàn.
(Xem giải) Câu 15. Peptide X có công thức cấu tạo như hình sau:

Cho các phát biểu sau:
(1) Phân tử peptide X là một tetrapeptide.
(2) Khi thủy phân hoàn toàn X trong môi trường acid, thu được 3 loại amino acid.
(3) X có khả năng phản ứng với Cu(OH)2 trong môi trường kiềm tạo thành dung dịch có màu tím đặc trưng.
(4) Ở điều kiện thường, dung dịch X có khả năng làm quỳ tím chuyển sang màu đỏ.
Có bao nhiêu phát biểu đúng ?
A. 1. B. 2. C. 1. D. 3.
(Xem giải) Câu 16. Cho các tiểu phân sau: +CH3 (I), -CH3 (II), •CH3 (III). Tiểu phân nào đóng vai trò là tác nhân nucleophile (ái nhân) trong các phản ứng hóa hữu cơ?
A. Chỉ có (II). B. Chỉ có (I). C. Chỉ có (III). D. Cả (I) và (III).
(Xem giải) Câu 17. Cao su thiên nhiên được lấy từ mủ cao su, có cấu tạo gồm nhiều mắt xích isoprene:
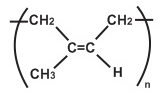
Một đoạn mạch polyisoprene có phân tử khối là 254320 chứa bao nhiêu mắt xích?
A. 3740. B. 2890. C. 5780. D. 3179.
(Xem giải) Câu 18. Cho các dung dịch có cùng nồng độ 0,2M gồm: Na2CO3, LiOH, CsCl, H2SO4. Số dung dịch có khả năng làm phenolphtalein chuyển sang màu hồng là
A. 1. B. 2. C. 3. D. 4.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Pin nhiên liệu hydrogen – oxygen (loại sử dụng chất điện li kiềm – AFC) có cấu tạo gồm hai điện cực xốp (thường làm bằng than chì có chứa chất xúc tác như Ni, Pt hoặc Pd). Hai điện cực này được nhúng vào dung dịch chất điện li là KOH nồng độ khoảng 30%. Khí H2 và O2 được bơm liên tục vào hai điện cực tương ứng. Phản ứng tổng cộng xảy ra khi pin hoạt động phát điện là: H2(g) + O2(g) → H2O(l).
a) Giả thiết, một hệ thống pin nhiên liệu hydrogen cỡ nhỏ được dùng để cung cấp điện cho một thiết bị bay không người lái (drone). Bình chứa của thiết bị đã nạp 0,450 kg khí H2. Khi vận hành, pin hoạt động với hiệu suất 60% và tạo ra dòng điện có cường độ trung bình 250A cung cấp cho động cơ. Giả sử không có tổn hao nào khác, thời gian tối đa mà thiết bị bay có thể hoạt động liên tục là 28,95 giờ. (Cho biết: điện tích của 1 mol electron là 96500 C/mol; công thức: q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s))
b) Trong quá trình pin hoạt động, khối lượng của các điện cực xốp liên tục giảm xuống do bị ăn mòn.
c) Tại anode, khí hydrogen bị oxi hóa.
d) Tại cathode, quá trình khử oxygen tạo ra các ion OH-, các ion này sau đó di chuyển qua dây dẫn để đi về anode.
(Xem giải) Câu 20. Phức chất của iron(III) với phối tử cyano (CN-) được ứng dụng nhiều trong phân tích. Quá trình điều chế thực hiện theo sơ đồ sau:
![]()
a) Các phức chất trong chuỗi phản ứng trên đều là phức bát diện.
b) Phức chất [Fe(OH2)6]2+ là phức aqua.
c) Các phức chất [Fe(CN)6]4- và [Fe(CN)6]3- có cùng nguyên tử trung tâm, phối tử và cấu trúc phức do đó các phức sẽ có màu sắc giống nhau.
d) Các phản ứng (1) và (2) đều có sự thay đổi điện tích phức chất nên các phản ứng (1), (2) đều là phản ứng oxi hoá – khử.
(Xem giải) Câu 21. PLA (polylactic acid) là loại nhựa được làm từ tinh bột ngô hoặc mía. Việc sản xuất PLA từ tinh bột ngô là một quy trình chuyển hóa sinh học (biotransformation) kết hợp với các phản ứng hóa học công nghiệp tiến hành theo sơ đồ sau:

Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O–H (alcohol) | O–H (carboxylic acid) | C=O (ester, carboxylic acid) |
| Số sóng (cm⁻¹) | 3650 – 3200 | 3300 – 2500 | 1780 – 1650 |
a) Từ 500 kg ngô (hàm lượng tinh bột 80%), nhà máy có thể sản xuất tối đa 7877 chiếc cốc nhựa PLA dạng hình trụ rỗng. Biết: mỗi chiếc cốc có bán kính ngoài 3 cm, chiều cao 10 cm, độ dày thành cốc và đáy cốc đều bằng 0,1 cm; khối lượng riêng của nhựa PLA là 1,25 g/cm³; hiệu suất của toàn bộ quy trình đạt 60% (lấy π = 3,14, kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
b) Trong công nghiệp, để tổng hợp PLA có phân tử khối lớn, phương pháp trùng hợp mở vòng lactide được ưu tiên sử dụng thay vì trùng ngưng trực tiếp lactic acid.
c) Trên phổ hồng ngoại của lactic acid, tín hiệu (peak) ở 1733 cm⁻¹ đặc trưng cho liên kết O–H.
d) Nhựa PLA dễ bị phân hủy sinh học trong môi trường tự nhiên hơn so với nhựa PE (polyethene) do phân tử PLA có chứa các liên kết ester .
(Xem giải) Câu 22. Biodiesel (diesel sinh học d = 0,88 g/mL) là một loại nhiên liệu lỏng, thân thiện hơn với môi trường so với diesel truyền thống. Biodiesel được sản xuất thông qua phản ứng giữa chất béo với các alcohol mạch ngắn (thường là methanol), với xúc tác là kiềm, thu được biodiesel (ester của acid béo) và glycerol (d = 1,26 g/mL).
Một nhà máy tái chế dầu ăn đã qua sử dụng để sản xuất biodiesel theo phương trình phản ứng tổng quát sau:
(RCOO)3C3H5 + 3CH3OH → 3RCOOCH3 + C3H5(OH)3 (1)
a) Biodiesel có thành phần nguyên tố giống dầu diesel truyền thống.
b) Từ 500 kg một loại dầu ăn đã qua sử dụng có chứa 86% chất béo (phân tử khối trung bình của chất béo là 860 amu), còn lại là tạp chất không có khả năng chuyển hóa thành biodiesel, có thể tạo tối đa 432 kg biodiesel dạng methyl ester với hiệu suất chuyển hóa là 90%.
c) Phương pháp trên giúp tận dụng dầu ăn đã qua sử dụng, giảm ô nhiễm môi trường do dầu ăn thải gây ra.
d) Sau khi phản ứng (1) kết thúc, hỗn hợp sản phẩm thu được sẽ phân thành hai lớp chất lỏng không đồng nhất, trong đó lớp biodiesel nổi lên trên bề mặt.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Tại một công ty sản xuất phân bón và hoá chất, superphosphate kép được sản xuất từ tinh quặng phosphorite theo hai giai đoạn, hiệu suất của mỗi giai đoạn đạt 90%.
• Giai đoạn 1: Đun nóng quặng phosphorite với dung dịch sulfuric acid đặc để sản xuất phosphoric acid:
Ca3(PO4)2 + 3H2SO4 → 3CaSO4 + 2H3PO4
• Giai đoạn 2: Đun nóng quặng phosphorite với dung dịch phosphoric acid để sản xuất superphosphate kép:
Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2
Trung bình mỗi ngày, công ty sử dụng 1000 tấn tinh quặng phosphorite (chứa 93% Ca3(PO4)2 về khối lượng) làm nguyên liệu để sản xuất ra tối đa m tấn Ca(H2PO4)2. Giá trị của m bằng bao nhiêu? (Làm tròn kết quả đến phần nguyên.)
(Xem giải) Câu 24. M là nguyên tố kim loại chuyển tiếp dãy thứ nhất. Ở trạng thái cơ bản nguyên tử M có 4 electron độc thân. Cho các nhận định sau:
a) Có thể tách Ag ra khỏi hỗn hợp gồm M và Ag bằng dung dịch MCl3
b) Biết dung dịch muối M3+ bị thuỷ phân cho môi trường acid. Nếu thêm dung dịch Na2CO3 vào dung dịch muối M3+ sẽ xuất hiện kết tủa màu nâu đỏ và có bọt khí thoát ra.
c) Trong kỹ thuật mạ điện để phủ một lớp kẽm (Zinc) lên bề mặt vật làm bằng kim loại M, vật cần mạ đóng vai trò là cathode. Tại đây xảy ra quá trình oxi hóa các ion Zn2 trong dung dịch để tạo thành lớp kẽm bám vào bề mặt M.
d) Khi làm lạnh 102,7648 gam dung dịch MCl2 bão hoà ở 90°C xuống 10°C, thu được tinh thể MCl2.4H2O và dung dịch X. Cho X tác dụng với lượng dư dung dịch AgNO3 ở điều kiện thường, thu được 69,52 gam kết tủa. Biết độ tan của MCl2 ở 90°C là 100 và ở 10°C là 64.
Có bao nhiêu nhận định đúng?
(Xem giải) Câu 25. Phản ứng luyện gang trong lò cao có sơ đồ phản ứng như sau:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g) (1)
Biết nhiệt tạo thành chuẩn của Fe2O3(s) là -824,4 kJ/mol; CO(g) là -110,5 kJ/mol; CO2(g) là -393,5 kJ/mol.
Cho các phát biểu sau:
(1) Phản ứng (1) là phản ứng oxi hóa – khử, CO là chất bị oxi hóa.
(2) Phản ứng (1) là phản ứng thu nhiệt, cần đun nóng ở nhiệt độ cao.
(3) Biến thiên enthalpy chuẩn của phản ứng trên: ![]() = 541,4 kJ.
= 541,4 kJ.
(4) Cho 1 mol Fe2O3 phản ứng với 1 mol CO, giả sử chỉ xảy ra phản ứng (1) với hiệu suất 100% thì giải phóng một lượng nhiệt là 8,27 kJ.
Hãy liệt kê các phát biểu sai theo thứ tự từ nhỏ đến lớn, ví dụ: 24, 123…
(Xem giải) Câu 26. Citric acid là acid hữu cơ tự nhiên có nhiều trong trái cây chua (đặc biệt là chanh) và được dùng phổ biến làm chất tạo vị chua tự nhiên, chất bảo quản trong thực phẩm và dược phẩm. Citric acid có công thức cấu tạo thu gọn như hình bên phải. Để xác định nồng độ của citric acid có trong một loại dung dịch E được dùng làm phụ gia thực phẩm, một học sinh tiến hành thí nghiệm sau:
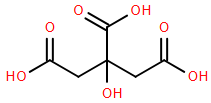
– Pha loãng 40,0 mL dung dịch E bằng nước cất trong bình định mức thu được 250,0 mL dung dịch F. Dùng pipette lấy 20,0 mL dung dịch F cho vào bình tam giác rồi thêm tiếp vài giọt phenolphtalein vào.
– Tráng sạch burette bằng nước cất, sau đó tráng lại bằng một ít dung dịch NaOH 0,15 M. Cho dung dịch NaOH 0,15 M vào burette, điều chỉnh dung dịch trong burette về mức 0.
– Mở khoá burette, nhỏ từng giọt dung dịch NaOH 0,15 M xuống bình tam giác (vừa cho dung dịch NaOH vừa lắc nhẹ bình tam giác) đến khi dung dịch trong bình tam giác chuyển sang màu hồng bền trong khoảng 20 giây thì dừng lại.
Lặp lại thí nghiệm trên thêm 2 lần. Thể tích dung dịch NaOH 0,15 M đã dùng trong 3 lần thí nghiệm được ghi lại như sau:
| Lần 1 | Lần 2 | Lần 3 | |
| V dd NaOH 0,15 M (mL) | 18,24 | 18,25 | 18,23 |
Giả thiết trong dung dịch E chỉ có citric acid tác dụng được với NaOH và sản phẩm là muối trisodium citrate (C3H4(OH)(COONa)3), khối lượng riêng của dung dịch E là 1,05 g/mL. Dựa vào các kết quả của thí nghiệm, học sinh đã tính toán được nồng độ phần trăm của citric acid có trong dung dịch E là a%. Giá trị của a bằng bao nhiêu? (kết quả làm tròn đến hàng phần trăm)
(Xem giải) Câu 27. Có bao nhiêu đồng phân arene ứng với công thức phân tử C8H10?
(Xem giải) Câu 28. Cho các chất sau: glycerol, dung dịch sodium choloride, ethanol, ethanal, albumin, methylamine. Có bao nhiêu chất có khả năng tác dụng với Cu(OH)2/trong môi trường kiềm ở nhiệt độ thích hợp?

Bình luận