[2024] Thi thử TN sở GDĐT Nam Định (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Giải chi tiết và đáp án:
⇒ Mã đề: 102
| 41A | 42C | 43C | 44A | 45D | 46B | 47B | 48A | 49B | 50B |
| 51B | 52A | 53C | 54D | 55A | 56D | 57C | 58C | 59D | 60B |
| 61A | 62C | 63C | 64A | 65D | 66A | 67B | 68A | 69A | 70D |
| 71B | 72C | 73B | 74B | 75D | 76C | 77D | 78C | 79B | 80B |
Câu 41. Dung dịch (có chứa chất tan nồng độ 1M) nào sau đây làm quỳ tím chuyển sang màu xanh?
A. NaOH. B. HCl. C. KNO3. D. NaCl.
Câu 42. Để làm mềm nước cứng vĩnh cửu, có thể dùng hóa chất nào sau đây?
A. NaNO3. B. NaCl. C. Na3PO4. D. Na2SO4.
Câu 43. Etylen glicol là nguyên liệu quan trọng để sản xuất polieste. Etylen glicol có công thức phân tử là
A. C2H6O. B. CH4O. C. C2H6O2. D. C3H8O3.
Câu 44. Nguồn nước sinh hoạt bị ô nhiễm nitrat là nước có hàm lượng ion nitrat cao. Một trong những nguyên nhân gây ra hiện tượng ô nhiễm trên là do việc sử dụng phân đạm dư thừa trong sản xuất nông nghiệp. Ion nitrat có công thức là
A. NO3-. B. NH4+. C. PO43-. D. NO2-.
Câu 45. Kim loại nào sau đây không thuộc nhóm các kim loại kiềm?
A. Na. B. K. C. Li. D. Ag.
Câu 46. Muối natri hiđrocacbonat được sử dụng làm thuốc kháng axit (dạ dày). Muối natri hiđrocacbonat có công thức là
A. CaCO3. B. NaHCO3. C. Ca(HCO3)2. D. Na2CO3.
Câu 47. Oxit sắt từ là hợp chất có khả năng nhiễm từ nên được sử dụng trong việc chế tạo ổ cứng máy tính. Oxit sắt từ có công thức là
A. FeO. B. Fe3O4. C. FeO2. D. Fe2O3.
Câu 48. Số nguyên tử oxi có trong phân tử triolein là
A. 6. B. 2. C. 4. D. 1.
Câu 49. Trong hợp chất nào sau đây, crom có số oxi hóa +6?
A. KCrO2. B. K2Cr2O7. C. Cr(OH)3. D. Cr2O3.
Câu 50. Khi đun nóng CH3COOH với CH3OH, có xúc tác H2SO4 đặc thu được este có tên gọi là
A. metyl fomat. B. metyl axetat. C. etyl fomat. D. etyl axetat.
Câu 51. Saccarozơ là một loại đisaccarit, có nhiều trong cây mía. Phân tử saccarozơ có chứa nhóm chức nào sau đây?
A. -COOH (cacboxyl). B. -OH (ancol). C. -NH2 (amin). D. -CH=O (anđehit).
Câu 52. Kim loại nào sau đây không tan trong dung dịch HCl 1M ở nhiệt độ thường?
A. Cu. B. Mg. C. Al. D. Fe.
Câu 53. Loại polime nào sau đây có chứa nguyên tố clo?
A. nilon-6. B. Xenlulozơ. C. PVC. D. PE.
Câu 54. Metylamin là nguyên liệu ban đầu để tổng hợp ephedrine – một loại dược phẩm. Phân tử khối của metylamin có giá trị là
A. 46. B. 34. C. 45. D. 31.
(Xem giải) Câu 55. Để bảo vệ ống thép dẫn dầu, người ta có thể sử dụng băng quấn vải mỡ bọc kín bề mặt của ống. Băng quấn vải mỡ gồm có lớp vải, lớp mỡ và chất kết dính bề mặt.

Phương pháp bảo vệ kim loại, chống lại sự ăn mòn như trên là phương pháp
A. bảo vệ bề mặt. B. kết tủa. C. trao đổi ion. D. điện hóa.
Câu 56. Dung dịch nước vôi trong là dung dịch chứa chất tan nào sau đây?
A. Ba(OH)2. B. Sr(OH)2. C. Mg(OH)2. D. Ca(OH)2.
(Xem giải) Câu 57. Kim loại nhôm có thể tan nhanh trong dung dịch nào sau đây?
A. Dung dịch HNO3 đặc, nguội. B. Dung dịch H2SO4 đặc, nguội.
C. Dung dịch HCl đặc, nguội. D. Dung dịch NaCl bão hòa.
Câu 58. Một số loại đá quý như hồng ngọc, bích ngọc có thành phần chính là nhôm oxit. Công thức của nhôm oxit là
A. Al(NO3)3. B. AlCl3. C. Al2O3. D. Al2(SO4)3.
Câu 59. Aminoaxit đơn giản nhất là glyxin. Công thức phân tử của glyxin là
A. C3H7NO2. B. C3H9NO2. C. C2H7NO2. D. C2H5NO2.
Câu 60. Tại điều kiện thường, kim loại X ở trạng thái lỏng. Dựa vào đặc điểm này, kim loại X được ứng dụng để chế tạo nhiệt kế. Kim loại X là
A. lưu huỳnh. B. thủy ngân. C. cacbon. D. kẽm.
(Xem giải) Câu 61. Isoamyl axetat có thể phản ứng với chất nào sau đây?
A. Dung dịch NaOH (đun nóng). B. H2 (đun nóng, xúc tác Ni).
C. Na (ở nhiệt độ thường). D. Dung dịch Br2/H2O (ở nhiệt độ thường).
(Xem giải) Câu 62. Thí nghiệm nào sau đây xuất hiện kết tủa?
A. Cho dung dịch Na2CO3 vào dung dịch KOH. B. Cho dung dịch FeCl3 vào dung dịch H2SO4.
C. Cho dung dịch BaCl2 vào dung dịch Na2SO4. D. Cho dung dịch KOH vào dung dịch HCl.
(Xem giải) Câu 63. Để khử hoàn toàn 1,12 gam Fe2O3 bằng phản ứng nhiệt nhôm, tạo thành kim loại sắt cần vừa đủ m gam Al. Giá trị của m là
A. 0,135. B. 0,108. C. 0,378. D. 0,162.
(Xem giải) Câu 64. Glucozơ đóng vai trò chất oxi hóa khi phản ứng với chất nào sau đây?
A. H2, xúc tác Ni, đun nóng. B. dung dịch H2SO4 loãng (phản ứng thủy phân).
C. Cu(OH)2, ở nhiệt độ thường. D. dung dịch AgNO3/NH3, đun nóng.
(Xem giải) Câu 65. Thủy phân hoàn toàn một lượng tristearin bằng dung dịch NaOH dư, đun nóng thu được a gam natri stearat và 3,68 gam glixerol. Giá trị của a là
A. 12,24. B. 36,48. C. 12,16. D. 36,72.
(Xem giải) Câu 66. Một mẫu sợi bông thô (được lấy từ quả bông) gồm xenlulozơ và tạp chất. Thủy phân 16,2 gam mẫu bông thô trên bằng dung dịch axit dư, đun nóng, thu được dung dịch X. Trung hòa lượng axit trong dung dịch X rồi cho sản phẩm hữu cơ phản ứng với dung dịch AgNO3/NH3 dư thu được 19,44 gam Ag. Giả thiết phần tạp chất không tham gia phản ứng thủy phân và phản ứng tráng bạc. Các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của xenlulozơ trong mẫu sợi bông thô là
A. 90%. B. 49%. C. 87%. D. 72%.
(Xem giải) Câu 67. Hòa tan hoàn toàn 1,28 gam Cu vào dung dịch H2SO4 đặc, đun nóng, thu được V lít khí SO2 (SO2 là sản phẩm khử duy nhất của S+6) và dung dịch X. Giá trị của V là
A. 0,112. B. 0,448. C. 0,224. D. 0,336.
(Xem giải) Câu 68. Nhận xét nào sau đây không đúng?
A. Cao su Buna-S thu được khi trùng hợp monome buta-1,3-đien với lưu huỳnh.
B. Tơ visco thuộc loại tơ bán tổng hợp.
C. Thủy tinh hữu cơ plexiglat thu được khi trùng hợp monome metyl metacrylat.
D. Nilon-6,6 thu được từ phản ứng trùng ngưng.
(Xem giải) Câu 69. Thủy phân hoàn toàn 2,64 gam peptit Gly-Gly (NH2-CH2-CO-NH-CH2-COOH) bằng dung dịch NaOH vừa đủ, đun nóng, thu được dung dịch chỉ chứa a gam muối NH2-CH2-COONa. Giá trị của a là
A. 3,88. B. 3,95. C. 4,18. D. 4,24.
(Xem giải) Câu 70. Hợp chất nào sau đây khi tác dụng với HNO3 đặc, nóng, không xảy ra phản ứng oxi hóa – khử?
A. FeCO3. B. Fe3O4. C. Fe(NO3)2. D. Fe(OH)3.
(Xem giải) Câu 71. Có 4 dung dịch không ghi nhãn, mỗi dung dịch chứa một trong số sáu chất tan sau đây: NaOH, Na2CO3, HCl, H2SO4, Na2SO4, BaCl2. Để nhận biết chất tan trong mỗi dung dịch, tiến hành thí nghiệm cho thuốc thử phản ứng với các dung dịch và thu được kết quả như sau:
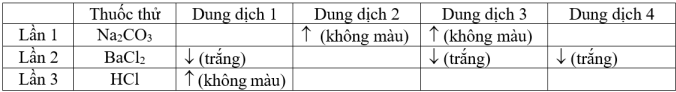
Chú ý: ô để trống là không có hiện tượng xảy ra. Nhận xét nào sau đây đúng?
A. Dung dịch 3 chứa Na2CO3. B. Dung dịch 2 chứa HCl.
C. Dung dịch 4 chứa BaCl2. D. Dung dịch 1 chứa H2SO4.
(Xem giải) Câu 72. Metan clarat (hay còn gọi là băng cháy) là dạng chất cấu tạo từ phân tử metan được bao bọc bởi các phân tử nước. Metan clarat có công thức dạng nCH4.mH2O.

Để xác định công thức của băng cháy, người ta tiến hành đốt cháy hoàn toàn 7,170 gam metan clarat bằng oxi dư thu được nước và 1,344 lít CO2. Tỉ lệ n : m là
A. 2 : 17. B. 3 : 22. C. 4 : 23. D. 5 : 18.
(Xem giải) Câu 73. Cho các thí nghiệm sau:
(a) Nhỏ dung dịch Ca(OH)2 vào dung dịch KHCO3.
(b) Nhỏ dung dịch Ba(OH)2 đến dư vào dung dịch Al2(SO4)3.
(c) Dẫn khí CO2 đến dư vào dung dịch Ba(OH)2.
(d) Nhỏ dung dịch AgNO3 đến dư vào dung dịch FeCl2.
(đ) Nhỏ dung dịch Na2CO3 đến dư vào dung dịch chứa hỗn hợp BaCl2.
Sau khi kết thúc các thí nghiệm, số trường hợp thu được kết tủa chỉ chứa một chất là
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 74. Hợp chất hữu cơ X mạch hở có công thức phân tử C4H9O2N. Từ X thực hiện sơ đồ các phản ứng sau:
(1) X + NaOH (t°) → Y + Z
(2) Y + CuO (t°) → T + Cu + H2O
(3) T + 2AgNO3 + 3NH3 + H2O (t°) → Q + 2Ag + 2NH4NO3
Hợp chất Q có công thức phân tử là C2H7NO2. Các chất T và Z thỏa mãn sơ đồ trên có công thức cấu tạo lần lượt là
A. C2H5OH; NH2CH2COOH. B. CH3CHO; NH2CH2COONa.
C. HCHO; NH2CH(CH3)COONa. D. CH3OH; NH2CH(CH3)COONa.
(Xem giải) Câu 75. Hỗn hợp X gồm Cu, CuO, Fe, Fe2O3, Fe3O4. Hòa tan m gam hỗn hợp X vào dung dịch chứa 0,42 mol HCl (lượng HCl dư 50% so với lượng phản ứng), thu được 0,448 lít khí H2 và dung dịch Y. Toàn bộ lượng dung dịch Y có thể hòa tan tối đa a gam Fe. Mặt khác, hòa tan m gam hỗn hợp X vào dung dịch H2SO4 đặc, nóng (lấy axit dư 20% so với lượng phản ứng) thu được 1,008 lít khí SO2 (SO2 là sản phẩm khử duy nhất của S+6) và dung dịch Z. Cho dung dịch Z phản ứng dung dịch Ba(OH)2 dư thu được kết tủa T. Nung nóng T ngoài không khí đến khi khối lượng không đổi thu được 58,631 gam hỗn hợp rắn Q. Các phản ứng xảy ra hoàn toàn. Giá trị của a gần nhất với giá trị nào sau đây?
A. 7,0. B. 3,9. C. 4,5. D. 7,9.
(Xem giải) Câu 76. Hợp chất hữu cơ X có công thức phân tử C4H6O5. Trong phân tử X không chứa nhóm chức nào khác ngoài các nhóm -OH; -CHO; -COO-; -COOH. Thêm vài giọt dung dịch phenolphtalein vào bình có chứa sẵn 1,34 gam X. Cho từ từ dung dịch NaOH 1M vào bình đó, lắc đều, đến khi dung dịch chuyển từ không màu sang màu hồng nhạt thì dừng lại, thấy đã dùng hết 10 ml dung dịch NaOH. Thí nghiệm diễn ra ở nhiệt độ thường (chỉ xảy ra phản ứng trung hòa axit – bazơ). Mặt khác, đun nóng 1,34 gam X với 250 ml dung dịch NaOH 0,1M, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Làm bay hơi chất lỏng trong dung dịch Y thu được a gam chất rắn Z và hợp chất hữu cơ T. Hợp chất T ở trạng thái lỏng tại nhiệt độ thường, có thể hòa tan được Cu(OH)2 tạo thành dung dịch màu xanh lam. Giá trị của a là
A. 2,34. B. 2,61. C. 1,54. D. 1,98.
(Xem giải) Câu 77. Hòa tan hoàn toàn 0,36 gam cacbon vào dung dịch H2SO4 đặc, nóng, dư, thu được dung dịch Y và hỗn hợp khí Z gồm CO2 và SO2. Hấp thụ hết toàn bộ lượng khí Z vào 500 ml dung dịch NaOH xM, thu được được dung dịch T có chứa 11,54 gam chất tan và không có khí bay ra. Dung dịch T không chứa muối axit. Giá trị của x là
A. 0,2. B. 0,3. C. 0,1. D. 0,4.
(Xem giải) Câu 78. Ba este X, Y, Z đều được tạo thành từ axit cacboxylic đơn chức, mạch hở và ancol đơn chức, mạch hở, trong đó MX < MY < MZ và MZ – MY = 2. Đốt cháy m gam hỗn hợp E gồm 3 este X, Y, Z cần vừa đủ 5,824 lít khí O2, thu được CO2 và 3,24 gam nước. Mặt khác, thủy phân m gam hỗn hợp E bằng dung dịch NaOH dư, đun nóng thu được hỗn hợp T (gồm 2 ancol no là đồng đẳng liên tiếp) và 4,72 gam hỗn hợp Q gồm 2 muối natri cacboxylat. Đốt cháy toàn bộ lượng hỗn hợp T ở trên cần vừa đủ 2,352 lít khí O2 thu được CO2 và nước. Các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Y trong hỗn hợp E gần nhất với giá trị nào sau đây?
A. 44%. B. 35%. C. 22%. D. 42%.
(Xem giải) Câu 79. Tương tự etanol, glixerol cũng có thể phản ứng với các axit vô cơ như HBr, HNO3,… (xảy quá trình gốc axit thế nhóm -OH của phân tử ancol). Glixerol trinitrat đã được nhà hóa học Alfred Nobel sử dụng làm nguyên liệu chính để chế tạo ra thuốc nổ dynamit năm 1866. Glixerol trinitrat được tổng hợp bằng phản ứng giữa glixerol và axit nitric đặc dư (xúc tác axit sunfuric đặc) ở nhiệt độ 22°C. Phản ứng diễn ra như sau:
C3H5(OH)3 + 3HNO3 (đặc) (H2SO4 đặc, 22°C) → C3H5(ONO2)3 + 3H2O
Khi glixerol trinitrat nổ tạo thành sản phẩm cacbonic, nước, nitơ và khí oxi. Có các nhận xét sau đây:
(a) Glixerol thuộc loại ancol no.
(b) Nguyên tử oxi trong phân tử nước ở sản phẩm có nguồn gốc từ glixerol.
(c) Glixerol có thể hòa tan được Cu(OH)2 tạo thành dung dịch màu xanh lam.
(d) Trong phân tử glixerol trinitrat có chứa liên kết giữa nguyên tử cacbon với nguyên tử nitơ.
(đ) Khi xảy ra phản ứng nổ hoàn toàn, 1 mol glixerol trinitrat tạo thành 8,25 mol sản phẩm.
Số nhận xét đúng là
A. 4. B. 3. C. 5. D. 2.
(Xem giải) Câu 80. Tiến hành điện phân 400 ml dung dịch chứa hỗn hợp CuSO4 aM và NaCl bM bằng dòng điện một chiều có cường độ không đổi, điện cực trơ, màng ngăn xốp. Mối liên hệ giữa giá trị pH của dung dịch và thời gian tiến hành điện phân được mô tả bằng đồ thị sau:
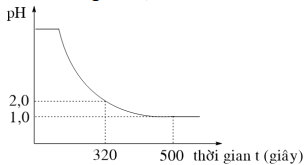
Từ thời điểm t = 500 giây trở đi, giá trị pH của dung dịch hầu như không thay đổi. Giả thiết thể tích dung dịch không thay đổi trong quá trình điện phân; hiệu suất quá trình điện phân là 100%; các chất HCl, NaOH, H2SO4 (cả 2 nấc) trong dung dịch điện ly hoàn toàn. Tổng (a + b) có giá trị là
A. 0,385. B. 0,275. C. 0,325. D. 0,425.

Bình luận