[2026] Thi thử TN sở GDĐT Cần Thơ (Đề 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 129
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2B | 3A | 4D | 5C | 6B | 7D | 8C | 9B |
| 10A | 11C | 12A | 13A | 14C | 15B | 16D | 17C | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | S | Đ | Đ | S |
| (b) | Đ | S | S | Đ |
| (c) | Đ | S | Đ | Đ |
| (d) | Đ | S | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 13,4 | 4 | 117 | 6 | 42,1 | 720 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Trong công nghiệp, việc tinh chế đồng từ đồng thô được thực hiện bằng phương pháp điện phân dung dịch với anode làm bằng
A. đồng tinh khiết. B. thép. C. đồng thô. D. graphite.
(Xem giải) Câu 2. “Phần lớn …(1)… là những protein xúc tác cho các phản ứng hóa học và sinh hóa”. Nội dung phù hợp trong chỗ trống (1) là
A. lipid. B. enzyme. C. carbohydrate. D. peptide.
(Xem giải) Câu 3. Bơ thực vật (chất béo no ở dạng rắn) được tạo ra từ dầu thực vật (chất béo không no ở dạng lỏng) nhờ thực hiện quá trình
A. hydrogen hóa. B. cô cạn. C. chưng cất thường. D. xà phòng hóa.
(Xem giải) Câu 4. Kim loại X có nhiệt độ nóng chảy cao nhất, được sử dụng làm dây tóc bóng đèn sợi đốt. X là
A. Al (aluminium). B. Cu (copper). C. Cr (chromium). D. W (tungsten).
(Xem giải) Câu 5. Chất nào sau đây khi tan trong nước tạo thành dung dịch có môi trường base?
A. Ba(NO3)2. B. NH4Cl. C. Na2CO3. D. Al2(SO4)3.
(Xem giải) Câu 6. Chất nào sau đây làm bột nở trong chế biến thực phẩm và làm chất chữa cháy dạng bột?
A. Na2CO3. B. NaHCO3. C. NaOH. D. NaCl.
(Xem giải) Câu 7. Việc tách các chất ra khỏi nhau bằng phương pháp sắc kí dựa trên đặc tính chủ yếu nào sau đây của chất?
A. Nhiệt độ sôi. B. Phân tử khối.
C. Nhiệt độ nóng chảy. D. Khả năng hấp phụ và hoà tan.
(Xem giải) Câu 8. Quá trình kết hợp nhiều phân tử nhỏ (monomer) thành phân tử lớn (polymer), đồng thời giải phóng những phân tử nhỏ khác (thường là H2O) được gọi là phản ứng
A. thế. B. trùng hợp. C. trùng ngưng. D. tách.
(Xem giải) Câu 9. Hợp chất nào sau đây có phản ứng tạo iodoform?
A. CH≡CH. B. CH3CHO. C. CH2=CH2. D. C6H5OH.
(Xem giải) Câu 10. Mưa acid là hiện tượng nước mưa có pH thấp hơn 5,6. Hai tác nhân chính gây mưa acid là:
A. SO2, NOx. B. N2, NH3. C. Cl2, HCl. D. S, H2S.
(Xem giải) Câu 11. Polymer A trong suốt, được dùng làm hộp đựng thực phẩm, đồ chơi trẻ em, vỏ đĩa CD,… Trong công nghiệp sản xuất chất dẻo, polymer A được tổng hợp theo sơ đồ:
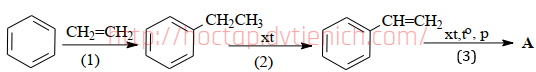
Từ 150 kg benzene và 50 m³ ethylene (ở 25°C, 1 bar), với hiệu suất mỗi quá trình (1), (2), (3) lần lượt là 50%, 75% và 60% thì khối lượng polymer A thu được là
A. 85 kg. B. 25 kg. C. 45 kg. D. 35 kg.
(Xem giải) Câu 12. Trong sản xuất nông nghiệp, người nông dân được khuyến cáo không bón vôi sống (thành phần chính là CaO) cùng với phân superphosphate (thành phần chính là Ca(H2PO4)2). Nguyên nhân của khuyến cáo này là
A. giảm hiệu quả vì tạo ra hợp chất không tan.
B. thất thoát lân vì tạo ra hợp chất dễ bay hơi.
C. tạo acid làm ảnh hưởng tới cây trồng.
D. tăng pH vì giải phóng phosphoric acid.
(Xem giải) Câu 13. Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử?
A. NH3. B. PH3. C. CO2. D. CH4.
(Xem giải) Câu 14. Sự xuất hiện lớp silver sulfide (Ag2S) màu đen xám ở bề mặt đồ trang sức bằng bạc là do phản ứng: 4Ag(s) + O2(g) + 2H2S(g) → 2Ag2S(s) + 2H2O(l). Trong phản ứng trên, chất bị oxi hóa là
A. O2. B. H2S. C. Ag. D. Ag2S.
(Xem giải) Câu 15. Trong các phản ứng hữu cơ thường có sự tạo thành các tiểu phân trung gian hoạt động như gốc tự do, carbanion, carbocation. Cho phương trình hóa học của phản ứng monochlorine hóa methane: CH4 + Cl2 → CH3Cl + HCl (1)
Một giai đoạn trong cơ chế của phản ứng (1) xảy ra như sau: •CH3 + Cl2 → CH3Cl + Cl• (∗)
Nhận định nào sau đây đúng?
A. CH3Cl là tiểu phân trung gian hoạt động.
B. Giai đoạn (∗) có sự phân cắt liên kết σ (sigma).
C. Giai đoạn (∗) có sự hình thành liên kết π (pi).
D. Phản ứng (1) thuộc loại phản ứng cộng.
(Xem giải) Câu 16. Trong cơ thể người, leucine đóng vai trò quan trọng trong việc thúc đẩy tổng hợp protein, điều hòa đường huyết. Với mỗi môi trường có giá trị pH bằng 2,3 và 6,0, coi leucine chỉ tồn tại ở dạng cho dưới đây:

Trong quá trình điện di, ion sẽ di chuyển về phía điện cực trái dấu với ion. Cho các phát biểu sau về quá trình điện di của leucine:
(a) Với môi trường pH = 2,3 thì dạng (I) di chuyển về phía cực dương.
(b) Với môi trường pH = 6,0 thì dạng (II) hầu như không dịch chuyển về các điện cực.
(c) Với môi trường pH = 6,0 thì leucine tồn tại ở dạng ion lưỡng cực.
(d) Dạng tồn tại chủ yếu của leucine ở pH = 12,0 là (CH3)2CHCH2CH(NH2)COO−.
Số phát biểu đúng là
A. 1. B. 2. C. 4. D. 3.
(Xem giải) Câu 17. Tiến hành chuẩn độ dung dịch FeSO4 (nồng độ khoảng 0,1 M) bằng dung dịch chuẩn KMnO4 2,2E-2M theo các bước sau:
• Bước 1: Dùng pipette lấy 10 mL dung dịch FeSO4 cho vào bình tam giác rồi acid hóa bằng dung dịch H2SO4 2M.
• Bước 2: Cho dung dịch KMnO4 vào burette, điều chỉnh thể tích dung dịch trong burette về mức 0.
• Bước 3: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO4 đã sử dụng.
Lặp lại thí nghiệm thêm 2 lần. Trường hợp nào sau đây dẫn đến nồng độ FeSO4 tính toán được thấp hơn nồng độ thực tế?
A. Ở bước 2, burette chỉ được tráng bằng nước cất rồi thêm vào dung dịch KMnO4 khi burette vẫn còn ướt.
B. Trước khi tiến hành chuẩn độ, ở đầu burette có bóng khí, nhưng biến mất trong quá trình chuẩn độ.
C. Pipette chỉ được tráng bằng nước cất và vẫn còn ướt khi lấy 10 mL dung dịch FeSO4 ở bước 1.
D. Dung dịch FeSO4 không được acid hóa kỹ dẫn đến sự hình thành một ít MnO2 trong quá trình chuẩn độ ở bước 3.
(Xem giải) Câu 18. Gói làm nóng thức ăn (Flameless Ration Heater − FRH) được phát minh nhằm hâm nóng bữa ăn một cách tiện lợi. FRH có thành phần chính gồm bột kim loại Mg trộn với một lượng nhỏ bột Fe và NaCl. Khi sử dụng, chỉ cần cho khoảng 30 mL nước vào hỗn hợp FRH, phản ứng giữa Mg và H2O xảy ra mãnh liệt, cung cấp nhiệt lượng làm nóng thức ăn nhanh chóng. Mg phản ứng chậm với H2O ở nhiệt độ thường nhưng lại có thể nhanh chóng phản ứng với H2O trong gói FRH là do
A. việc trộn Mg với Fe tạo ra hợp kim có hoạt tính hóa học mạnh hơn so với Mg nguyên chất.
B. Mg và Fe tiếp xúc với nhau trong môi trường chất điện li khiến Mg bị ăn mòn điện hóa.
C. NaCl là chất điện li mạnh, tạo điều kiện cho các phân tử H2O dễ dàng tiếp xúc với Mg.
D. sự có mặt của dung dịch NaCl tạo nên pin điện hóa Fe−Mg, trong đó Mg là cực dương.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Việc pha ethanol vào xăng góp phần hạn chế sự phụ thuộc vào nhiên liệu hóa thạch và giảm phát thải CO2. Sơ đồ sau đây tóm tắt quá trình sản xuất và tiêu thụ xăng E85 (chứa 85% ethanol về thể tích):

Khối lượng riêng và nhiệt tỏa ra khi đốt cháy hoàn toàn C8H18(l) và C2H5OH(l), tạo thành CO2(g) và H2O(l) được cho trong bảng sau:
| Chất | Khối lượng riêng (g/mL) | Nhiệt tỏa ra khi đốt cháy (kJ/mol) |
| C8H18(l) | 0,7 | 5400 |
| C2H5OH(l) | 0,79 | 1500 |
Giả thiết xăng truyền thống là C8H18; xăng E85 chỉ gồm C8H18 và ethanol.
a) X là cellulose – thành phần chính của thành tế bào thực vật, làm nên bộ khung của cây.
b) Giai đoạn [1] có xảy ra phản ứng thủy phân và lên men rượu.
c) Phản ứng trong giai đoạn [4] xảy ra nhờ ánh sáng mặt trời và chất diệp lục trong lá cây.
d) Với cùng lượng nhiệt tạo thành thì xăng truyền thống phát thải lượng CO2 gấp 1,1 lần so với xăng E85. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
(Xem giải) Câu 20. Benzylamine được sử dụng làm tiền chất trong tổng hợp hữu cơ. Benzylamine được điều chế từ ammonia và CxHyBr theo phản ứng: CxHyBr + NH3 → C6H5CH2NH2 + HBr
a) Nguyên tử nitrogen trong phân tử benzylamine có cặp electron hóa trị chưa liên kết.
b) Oxi hóa benzylamine bằng hydrogen chloride thu được benzylamine hydrochloride.
c) CxHyBr được tổng hợp từ phản ứng của benzene với bromine có mặt FeBr3 làm xúc tác.
d) Benzylamine phản ứng với nitrous acid ở nhiệt độ thấp (0 – 5°C) sinh ra muối diazonium.
(Xem giải) Câu 21. Vanadium (23V) màu xám bạc, cứng, có khả năng chống ăn mòn tốt. Vanadium có thể được sản xuất từ quặng shcherbinaite (chứa 40% vanadium pentoxide về khối lượng, còn lại là tạp chất không chứa V) bằng phương pháp nhiệt luyện với hiệu suất toàn bộ quá trình đạt 75%.
a) Vanadium là nguyên tố kim loại chuyển tiếp dãy thứ nhất.
b) Vanadium thuộc chu kì 4, nhóm IIIB trong bảng tuần hoàn các nguyên tố hóa học.
c) Vanadium thể hiện số oxi hóa cao nhất trong hợp chất vanadium pentoxide.
d) Khối lượng quặng shcherbinaite cần sử dụng để sản xuất 1 kg kim loại V là 5,95 kg. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần trăm).
(Xem giải) Câu 22. Trong công nghiệp, magnesium (Mg) được sản xuất từ quặng carnallite (có thành phần chính là KCl.MgCl2.6H2O) bằng phương pháp điện phân nóng chảy. Trước khi điện phân, carnallite được nung nóng để loại bỏ nước. Sơ đồ thiết bị điện phân như hình bên:

Biết rằng, thực tế một trong hai điện cực làm bằng thép, điện cực còn lại làm bằng than chì.
a) Khối lượng riêng của Mg lỏng lớn hơn khối lượng riêng của hỗn hợp nóng chảy.
b) Ở cực âm, ion Mg2+ được ưu tiên điện phân trước do có tính oxi hóa mạnh hơn ion K+.
c) Khí trơ giúp bảo vệ kim loại Mg nóng chảy không bị oxi hóa bởi oxygen từ không khí.
d) Điện cực (1) được làm bằng thép, điện cực (2) được làm bằng than chì.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Ethyl acetate (EA) có mùi thơm đặc trưng được dùng làm dung môi pha sơn, hương liệu,… EA được sản xuất từ acetic acid và ethanol, sử dụng dung dịch H2SO4 đặc làm xúc tác theo phản ứng: CH3COOH + C2H5OH (H2SO4 đặc, t°) ⇋ CH3COOC2H5 + H2O (∗)
Hiệu suất phản ứng (∗) tính theo acetic acid là 75% thì khối lượng acetic acid cần sử dụng để sản xuất 100 thùng EA thương phẩm là bao nhiêu tấn? Biết mỗi thùng chứa 150 kg EA thương phẩm có độ tinh khiết 98%. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
(Xem giải) Câu 24. Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa−khử:
| Cặp oxi hóa – khử | Cu2+/Cu | Fe3+/Fe2+ | Ag+/Ag | Au3+/Au | 2H+/H2 |
| Thế điện cực chuẩn (V) | 0,340 | 0,771 | 0,799 | 1,520 | 0,0 |
Để tinh chế Au từ hỗn hợp Au và Cu, tiến hành ngâm hỗn hợp trong lượng dư dung dịch chất X có nồng độ 1M, đến khi khối lượng chất rắn không thay đổi, lọc lấy phần chất rắn này, rửa sạch và làm khô, thu được vàng tinh khiết. Cho các chất được đánh số như sau: (1) HCl; (2) AgNO3; (3) CuSO4; (4) FeCl3. Liệt kê chất phù hợp là X trong số những chất trên và sắp xếp theo trình tự tăng dần (ví dụ: 2; 34; 124;…).
(Xem giải) Câu 25. Peptide X có cấu trúc sau đây được tạo nên từ sự kết hợp của các đơn vị α-amino acid, trong đó α-amino acid Y có phân tử khối lớn nhất so với các đơn vị α-amino acid khác trong X:

Phân tử khối của Y là bao nhiêu?
(Xem giải) Câu 26. Trong phức chất, tổng số liên kết σ (sigma) giữa nguyên tử trung tâm với các phối tử được gọi là số phối trí của nguyên tử trung tâm đó. Số phối trí của nguyên tử trung tâm trong phân tử [Co(NH3)5Br]SO4 là bao nhiêu?
(Xem giải) Câu 27. Phần trăm khối lượng carbon trong maltose là a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
(Xem giải) Câu 28. Trong công nghiệp chlorine – kiềm, dung dịch NaCl bão hòa chỉ được điện phân một phần thành “nước muối nghèo”. Biết trong 1 lít dung dịch NaCl bão hòa có chứa 300 gam NaCl, còn 1 lít “nước muối nghèo” có chứa 220 gam NaCl. “Nước muối nghèo” sau đó được dẫn ra khỏi bể điện phân, trong khi nước muối bão hòa mới được bơm vào. Dung dịch NaOH tạo thành được cô đặc để sản xuất dung dịch NaOH có nồng độ mong muốn. Giả thiết NaOH không bị thất thoát trong quá trình cô đặc, thể tích dung dịch NaCl thay đổi không đáng kể trong quá trình điện phân. Để sản xuất x lít dung dịch NaOH 50% (khối lượng riêng 1,52 g/mL) cần điện phân 10 m³ dung dịch NaCl bão hoà. Giá trị của x là bao nhiêu? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).

Bình luận