Ethyl acetate là một ester được sử dụng là dung môi để tách, chiết chất hữu cơ. Hợp chất này được điều chế từ acetic acid, ethanol theo phản ứng và mô hình thí nghiệm sau: CH3COOH + C2H5OH ⇋ CH3COOC2H5 + H2O (∗)
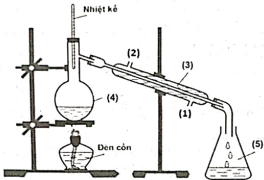
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65 – 70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C. Cho biết nhiệt độ sôi của các hợp chất như sau:
Chất.. C2H5OH.. CH3COOH.. H2O.. CH3COOC2H5.. H2SO4
t°s……… 78,3……… 118…… 100……… 77…………… 337
a) Khi thực hiện đun nóng 6,0 gam acetic acid với 6,0 gam ethanol có H2SO4 đặc làm xúc tác. Khối lượng ester tạo thành với hiệu suất phản ứng 60% là 6,9 gam.
b) Chất lỏng trong bình hứng (5) có ethyl acetate. Vai trò của ống sinh hàn (3) để ngưng tụ hơi, nước vào ở (1) và nước ra ở (2).
c) Ban đầu bình cầu (4) chứa acetic acid, ethanol và sulfuric acid đặc. Nếu nhiệt độ phản ứng ở bình cầu (4) càng cao thì hiệu suất phản ứng điều chế ethyl acetate càng cao.
d) Trong phản ứng (∗) phân tử H2O tạo nên từ -OH trong nhóm –COOH của acetic acid và H trong nhóm –OH của ethanol.
Câu trả lời tốt nhất
(a) Sai:
nCH3COOH = 0,1; nC2H5OH = 0,13
H = 60% —> nCH3COOC2H5 = 0,1.60% = 0,06
—> mCH3COOC2H5 = 5,28 gam
(b) Đúng, bình hứng (5) chứa CH3COOC2H5 và tạp chất, ống sinh hàn dùng để ngưng tụ hơi ester, ống hoạt động nhờ nước làm mát đi vào ở vị trí thấp (1) và đi ra ở vị trí cao (2).
(c) Sai, nếu nhiệt độ quá cao (vượt quá điểm sôi của các chất), các chất phản ứng (C2H5OH sôi ở 78,3°C, CH3COOH sôi ở 118°C) sẽ bay hơi quá nhanh khỏi hệ thống trước khi kịp phản ứng, hoặc gây ra các phản ứng phụ (như tạo ether hoặc sản phẩm oxy hóa). Do đó, nhiệt độ luôn được khống chế ở mức tối ưu (thường là đun cách thủy hoặc giữ ở 65 – 70°C như đề bài nêu).
(d) Đúng
