[2024 – 2025] Khảo sát HSG trường Đông Thụy Anh – Thái Bình (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề 024-H12A năm 2024-2025
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1C | 2D | 3D | 4A | 5C | 6A | 7D | 8A | 9B | 10A |
| 11D | 12B | 13B | 14C | 15D | 16B | 17B | 18A | 19B | 20C |
| Câu 21 | Câu 22 | Câu 23 | Câu 24 | Câu 25 | Câu 26 | |
| (a) | S | S | S | Đ | Đ | Đ |
| (b) | Đ | Đ | S | S | Đ | S |
| (c) | Đ | S | S | Đ | Đ | Đ |
| (d) | Đ | Đ | Đ | Đ | Đ | S |
| Câu 27 | Câu 28 | Câu 29 | Câu 30 | Câu 31 | Câu 32 |
| 6 | 66,0 | 4 | 4 | 2,6 | 6,76 |
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn (8 điểm/20 câu; mỗi câu 0,4 điểm. Thí sinh trả lời từ câu 1 đến câu 20, mỗi câu thí sinh chỉ chọn 1 phương án.
(Xem giải) Câu 1. Hiện tượng nào không phải là hiện tượng hóa học?
A. Trên mặt hồ nước vôi thường xuất hiện lớp váng mỏng màu trắng.
B. Nhỏ H2SO4 đặc vào đường saccarozơ thấy đường bị hóa than.
C. Mặt nạ phòng độc được bọc 1 lớp than hoạt tính để người đeo tránh hít phải khí độc có trong không khí nhiễm khí độc.
D. Dùng dung dịch NaHCO3 để rửa vết bỏng do H2SO4.
(Xem giải) Câu 2: Cho thí nghiệm được mô tả bằng hình vẽ dưới đây:
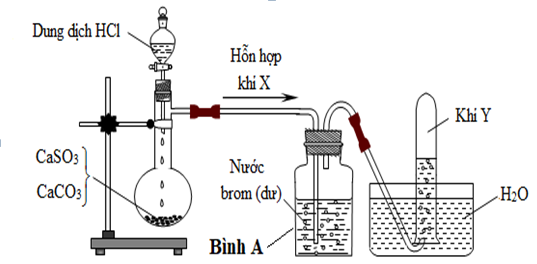
Nhận định nào sau đây sai?
A. Nhỏ dung dịch BaCl2 vào bình A sau thí nghiệm kết thúc thấy có kết tủa trắng.
B. Thay dung dịch brom bằng dung dịch KMnO4, khi thí nghiệm thấy dung dịch nhạt màu.
C. Cả X và Y đều phản ứng được với dung dịch NaOH.
D. Dẫn khí Y vào dung dịch CaCl2 thấy có kết tủa trắng tạo thành.
(Xem giải) Câu 3: Trong tự nhiên kali gồm 3 đồng vị K39 chiếm 93,26% và đồng vị K40 chiếm 0,012% và đồng vị K41. Brom là hỗn hợp hai đồng vị Br79 và Br81 với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của K39 trong KBr là
A. 30,56%. B. 29,92%. C. 31,03%. D. 30,55%.
(Xem giải) Câu 4: Cho các cân bằng sau:
(1) 2SO2(k) + O2(k) ⇋ 2SO3(k) (![]() < 0).
< 0).
(2) N2(k) + 3H2(k) ⇋ 2NH3(k) (![]() < 0)
< 0)
(3) C(r) + H2O(k) ⇋ CO(k) + H2(k) (![]() > 0)
> 0)
(4) 2HI(k) ⇋ H2(k) + I2(k) (![]() > 0)
> 0)
(5) CO2(k) + C(r) ⇋ 2CO(k) (![]() > 0)
> 0)
Khi tăng áp suất hoặc giảm nhiệt độ cân bằng đều chuyển dịch theo chiều thuận. Số cân bằng hoá học thỏa mãn đặc điểm trên là
A. 2. B. 1. C. 3. D. 4.
(Xem giải) Câu 5. Cho hai phản ứng cùng xảy ra ở điều kiện chuẩn:
(1) N2(g) + O2(g) → 2NO(g)  (1)
(1)
(2) NO(g) + ½O2(g) → NO2(g)  (2)
(2)
Phát biểu này sau đây không đúng?
A. Enthalpy tạo thành chuẩn của NO là ½ (1) kJ/mol.
(1) kJ/mol.
B. Enthalpy tạo thành chuẩn của NO2(g) là ½ +
+  (2) kJ/mol.
(2) kJ/mol.
C. Biến thiên enthalpy chuẩn của phản ứng giữa 1 mol khí NO với 1 mol khí O2 tạo thành 1 mol khí NO2 là  (2) kJ/mol.
(2) kJ/mol.
D. Biến thiên enthalpy chuẩn của phản ứng giữa 1 mol N2 với 1 mol O2 tạo thành 2 mol NO là  (1) kJ.
(1) kJ.
(Xem giải) Câu 6: Hoa đậu biếc tên tiếng Anh là butterfly pea, là một loại hoa được trồng phổ biến tại các quốc gia Nam Á và Đông Nam Á như Ấn Độ, Thái Lan, Singapore, Việt Nam…. Hoa có tên gọi như vậy vì cây đậu biếc thuộc họ đậu, sống dây leo và cánh hoa có màu xanh tím giống hình con bướm. Khi sử dụng đậu biếc làm chất tạo màu tự nhiên, người ta thường đun sôi hoa đậu biếc với nước, hoặc ngâm cánh hoa trong nước sôi từ 10 đến 15 phút, màu hoa sẽ được trích ly tạo thành màu xanh biếc. Sắc tố tạo màu đặc trưng cho đậu biếc là các hợp chất thuộc nhóm anthocyanin, một trong những chất chống oxy hóa tự nhiên. Điểm đặc biệt của nhóm anthocianin là màu của chúng thay đổi dưới tác dụng pH của môi trường. Ở môi trường pH < 7 (môi trường Acid), anthocyanin chuyển sang đỏ tím, ngược lại chúng chuyển sang màu xanh thẫm khi môi trường pH ≥ 7. Dự đoán màu của dung dịch khi trộn lẫn 20 mL dung dịch NaOH 0,01M với 20 mL dung dịch HCl 0,03 M được dung dịch Y. Dung dịch Y làm hoa đậu biếc chuyển sang màu
A. đỏ tím. B. xanh thẫm. C. tím. D. vàng.
(Xem giải) Câu 7. Quan sát hình mô phỏng thí nghiệm sau:
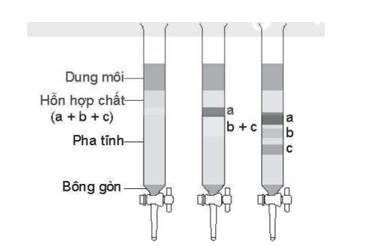
Cho các phát biểu sau đây:
(1) Hình mô phỏng thí nghiệm phương pháp sắc kí cột.
(2) Các chất a, b, c có khả năng tan trong dung môi (pha động) và khả năng bị hấp phụ bởi chất hấp phụ (pha tĩnh) khác nhau nên bị tách ra khỏi nhau trong cột sắc kí.
(3) Chất bị hấp phụ mạnh nhất là chất c.
(4) Chất hấp phụ kém nhất là chất a.
(5) Chất c hòa tan trong dung môi tốt nhất.
Số phát biểu đúng là
A. 5 B. 4 C. 2 D. 3
(Xem giải) Câu 8: Phát biểu nào sau đây sai:
A. HCOOH có lực acid yếu hơn CH3COOH.
B. Cao su thiên nhiên là polymer của isoprene, các mắt xích đều có cấu hình cis.
C. Len, tơ tằm, tơ enan kém bền nhiệt và bị thủy phân trong môi trường acid và kiềm.
D. Terephthalic acid (C6H4(COOH)2) được ứng dụng trong tổng hợp tơ Lapsan.
(Xem giải) Câu 9: Albuterol được sử dụng như một loại thuốc cho đường hô hấp, trị hen suyễn, có công thức:
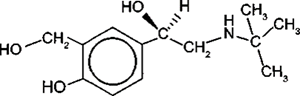
Phát biểu nào sau đây không đúng?
A. Albuterol có khả năng phản ứng với dung dịch HCl và dung dịch NaOH
B. Albuterol có 23 nguyên tử H
C. 1 mol albuterol phản ứng hết với kim loại Na thu được tối đa 1,5 mol khí H2.
D. Số nguyên tử carbon trong phân tử albuterol là 13.
(Xem giải) Câu 10: Hòa tan hết 1,69 gam oleum có công thức H2SO4.3SO3 vào 20,29 gam nước được dung dịch X. Trung hòa X cần vừa đủ 100,25 gam dung dịch Y gồm KOH 0,20M và Ba(OH)2 0,10M thu được dung dịch Z. Tính nồng độ phần trăm của dung dịch Z.
A. 1,45% B. 2,34% C. 4,56% D. 1,28%
(Xem giải) Câu 11. Polymer X được dùng chế tạo ra loại cao su có tính đàn hồi cao, bền với dầu mỡ, chịu nhiệt. X được điều chế theo sơ đồ phản ứng sau:
CH2=CH-CH=CH2 → CH2=CH-CHCl-CH2Cl → CH2=CH-CCl=CH2 → X.
Trong sơ đồ trên, chất X có tên là
A. poly(3-chlorobutadiene). B. polychlorobutadiene. C. polybutadiene. D. polychloroprene.
(Xem giải) Câu 12: Trypsin là enzyme đặc hiệu xúc tác cho phản ứng thủy phân liên kết peptide để tạo thành lysine (Lys) hoặc peptide ngắn hơn có đầu N là lysine. Thủy phân peptide ứng với công thức cấu tạo là Gly-Ala-Lys-Val-Lys-Val-Gly khi có mặt enzyme trypsin có thể thu được bao nhiêu dipeptide?
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 13: Cho các nhận xét sau:
(1) Chất béo không tan trong nước, nhẹ hơn nước nhưng tan nhiều trong dung môi hữu cơ.
(2) Có 4 ester có cùng công thức phân tử C5H8O2 phản ứng với dung dịch NaOH thu được muối và aldehyde.
(3) Trong công nghiệp, ethyl acetate được điều chế từ ethyl alcohol và giấm ăn.
(4) Phản ứng thủy phân chất béo trong môi trường acid là phản ứng thuận nghịch.
(5) Đun nóng hỗn hợp gồm methyl alcohol và methacrylic acid trong H2SO4 đặc thu được sản phẩm có thể dùng để điều chế thủy tinh hữu cơ.
(6) Trong công nghiệp để chuyển hóa chất béo lỏng (dầu) thành mỡ rắn hoặc thành bơ nhân tạo người ta thực hiện phản ứng hydrogen hóa chất béo lỏng.
Số nhận xét đúng là:
A. 3. B. 4. C. 5. D. 6.
(Xem giải) Câu 14: Trong quá trình bảo quản, một mẩu muối FeSO4.7H2O (có khối lượng m gam) bị oxi hóa bởi oxi không khí tạo thành hỗn hợp X gồm các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X trong dung dịch loãng chứa 0,035 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 20 mL dung dịch Y, thu được 2,33 gam kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 20 mL dung dịch Y, thu được dung dịch Z.
Nhỏ từ từ dung dịch KMnO4 0,03M vào Z đến khi phản ứng vừa đủ thì hết 18 mL.
Giá trị của m và phần trăm số mol Fe(II) đã bị oxi hóa trong không khí lần lượt là:
A. 4,17 và 5%. B. 13,90 và 27%.
C. 4,17 và 10%. D. 13,90 và 73%.
(Xem giải) Câu 15: Cho các phát biểu sau:
(a) Ethylene là ankene quan trọng bậc nhất, là nguyên liệu quan trọng của công nghiệp tổng hợp polymer và các hợp chất hữu cơ khác.
(b) Ethylen được sản xuất với lượng lớn mỗi năm từ ethanol.
(c) Sục khí acetylene vào dung dịch AgNO3 trong NH3 thu được kết tủa màu vàng nhạt.
(d) Có 4 đồng phân cấu tạo, mạch hở ứng với công thức phân tử C4H6.
(e) Styrene có công thức cấu tạo là C6H5-CH2-CH3.
(g) Có 4 hydrocarbon là chất khí ở điều kiện thường tác dụng được với dung dịch AgNO3/NH3
Số phát biểu đúng là:
A. 4. B. 2. C. 5. D. 3
(Xem giải) Câu 16: Thực hiện các thí nghiệm:
a) Sục từ từ a mol khí CO2 vào dung dịch chứa 0,65a mol Ba(OH)2
(b) Cho dung dịch NaHCO3 dư vào dung dịch Ca(OH)2
(c) Sục khí Cl2 vào dung dịch NaOH ở nhiệt độ thường.
(d) Cho dung dịch chứa x mol KHSO4 vào dung dịch chứa x mol NaHCO3.
(e) Cho Mg vào dung dịch FeCl3 dư
(f) Cho dung dịch NH3 dư vào dung dịch AlCl3.
(g) Cho Ba vào dung dịch CuSO4 dư.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa 2 muối?
A. 2 B. 3 C. 4 D. 5
(Xem giải) Câu 17: Một loại sắn chứa 60% tinh bột dùng để lên men sản xuất ethyl alcohol phục vụ cho pha chế xăng sinh học E5 (loại xăng chứa 5% thể tích C2H5OH, còn lại là xăng RON 95 hay xăng Mogas 95). Hỏi 10 tấn sắn trên sản xuất được bao nhiêu lít xăng sinh học E5? Biết hiệu suất toàn bộ quá trình lên men và pha chế là 85%; khối lượng riêng của C2H5OH là 0,8g/mL.
A. 3810,9 lít. B. 72407,4 lít. C. 36203,7 lít. D. 57925,9 lít.
(Xem giải) Câu 18. Tiến hành thí nghiệm theo các bước sau
Bước 1: Cho vào ống nghiệm 2 mL nước cất.
Bước 2: Nhỏ tiếp vài giọt aniline vào ống nghiệm, sau đó nhúng giấy quỳ tím vào dung dịch trong ống nghiệm.
Bước 3: Nhỏ tiếp 1 mL dung dịch HCl đặc vào ống nghiệm, lắc đều rồi để yên.
Cho các phát biểu sau:
(a) Sau bước 2, dung dịch thu được trong suốt.
(b) Sau bước 2, giấy quỳ tím chuyển thành màu xanh.
(c) Sau bước 3, dung dịch thu được trong suốt.
(d) Nhỏ dung dịch bromine vào dung dịch sau bước 3 thấy xuất hiện kết tủa màu trắng.
(e) Nếu thay aniline bằng benzyl amine thì hiện tượng thí nghiệm ở các bước vẫn không đổi.
Số phát biểu đúng là :
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 19: Cho các phát biểu sau:
(1) Dung dịch glucose hòa tan được Cu(OH)2 ở điều kiện thường, tạo phức xanh lam.
(2) Lòng trắng trứng hòa tan được Cu(OH)2 ở điều kiện thường, tạo phức màu xanh tím.
(3) Nhỏ dung dịch iodine vào dung dịch hồ tinh bột, xuất hiện màu tím.
(4) Cho dung dịch aniline vào nước bromine, xuất hiện kết tủa trắng.
(5) Cho dung dịch fructose vào dung dịch AgNO3/NH3, đun nóng thu được kết tủa bạc trắng.
(6) Cho aniline vào nước cất, để yên thấy dung dịch phân lớp.
Số phát biểu đúng là :
A. 5. B. 4. C. 3. D. 6.
(Xem giải) Câu 20: Thủy phân hoàn toàn một hexapeptide M, thu được Ala, Arg, Gly, Ile, Phe và Tyr. Các peptide E (chứa Phe, Arg) và G (chứa Arg, Ile, Phe) được tạo thành trong số các sản phẩm thủy phân không hoàn toàn M. Dùng 1-fluoro-2,4-dinitrobenzen xác định được amino acid đầu N là Ala. Thủy phân M nhờ tripsin thu được tripeptit A (chứa Ala, Arg, Tyr) và một chất. Thứ tự liên kết của các amino axit trong M là
A. Arg – Tyr – Ala – Phe – Ile – Gly.
B. Ala – Tyr – Arg – Phe – Gly –Ile.
C. Ala – Tyr – Arg – Phe – Ile – Gly.
D. Ala – Tyr – Phe –Arg – Ile – Gly.
PHẦN II: Câu trắc nghiệm đúng sai (8,4 điểm/6 câu; đúng 1 ý 0,2 điểm, đúng 2 ý 0,4 điểm, đúng 3 ý 0,7 điểm, đúng 4 ý 1,4 điểm). Thí sinh trả lời từ câu 21 đến câu 26. Trong mỗi ý a), b), c), d) ở mỗi câu thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 21: Thí nghiệm của các halogen với bông sắt cũng thể hiện tương quan về tính oxi hoá giữa các halogen.
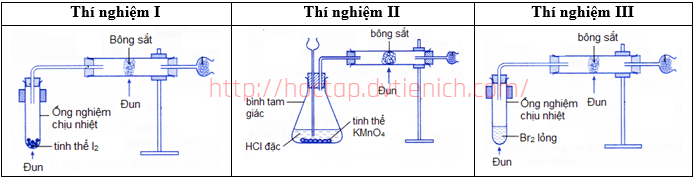
Các hiện tượng thí nghiệm không theo thứ tự như sau:
(1) Bông sắt cháy sáng tạo thành khói màu nâu.
(2) Bông sắt cháy vừa phải tạo thành làn khói màu nâu.
(3) Bông sắt cháy sáng mờ và từ từ, có ít chất rắn màu xám tạo thành.
Cho các nhận định:
a) Phản ứng tổng quát của iron trong 3 thí nghiệm là: 2Fe + 3X2 → 2FeX3
b) Hiện tượng trên ứng với 3 thí nghiệm lần lượt là: 1-II; 2 – III, 3 – I, chứng minh rằng tính oxi hóa của Cl2 > Br2 > I2.
c) Sản phẩm phản ứng của Fe trong 3 thí nghiệm trên đem tác dụng với dung dịch AgNO3 dư, thu được 4 kết tủa
d) Nếu thay dung dịch KMnO4 ở thí nghiệm II bằng MnO2 (t°) hoặc NaClO thì sản phẩm phản ứng của Fe vẫn là FeCl3
(Xem giải) Câu 22. Pin nhiên liệu cung cấp năng lượng điện và nhiệt giải phóng khi pin hoạt động. Ngoài ra, việc vận hành pin nhiên liệu không phát sinh tiếng ồn và chỉ giải phóng nước, không làm ô nhiễm môi trường như nhiên liệu hóa thạch.
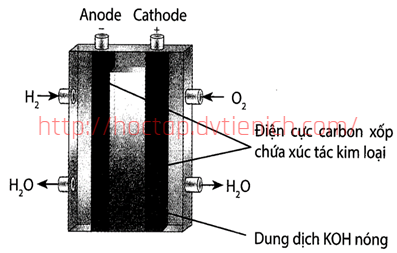
Nhiều hãng sản xuất xe đã nghiên cứu xe sử dụng năng lượng tái tạo là hydrogen, sử dụng tế bào nhiên liệu để chuyển hóa năng lượng và dùng động cơ điện để vận hành.
Anode (–): 2H2 + 4OH- → 4H2O + 4e (E°anode = -0,40V)
Cathode (+): O2 + 4e + 2H2O → 4OH- (E°cathode = 0,83V)
Phương trình hóa học của phản ứng xảy ra: 2H2 + O2 → 2H2O
a. Sức điện động của pin nhiên liệu trên là 0,43 V.
b. Pin nhiên liệu có ưu điểm là không phát thải khí gây ô nhiễm môi trường do chỉ thải ra hơi nước.
c. Về phương diện hóa học, pin nhiên liệu có phản ứng tương đương với sự điện phân.
d. Pin nhiên liệu có thể bị rò rỉ hydrogen, gây nguy hiểm nếu không được bảo quản đúng cách.
(Xem giải) Câu 23. Fluoxetine được sử dụng trong điều trị trầm cảm và rối loạn ám ảnh cưỡng chế, được bán với tên thương mại Prozac. Công thức cấu tạo của fluoxetine như hình bên
a. Fluoxetine là một arylamine.
b. Fluoxetine có công thức phân tử là C17H16F3NO.
c. Fluoxetine tác dụng với nitrous acid ở nhiệt độ thường giải phóng khí nitrogen.
d. Mỗi phân tử fluoxetine có 5 nguyên tử có khả năng tạo liên kết hydrogen với chất khác.
(Xem giải) Câu 24. Hợp chất hữu cơ X gồm 3 nguyên tố C, H, O. Kết quả phân tích nguyên tố của hợp chất hữu cơ X có mC : mH : mO = 42 : 7 : 16. X có mạch không phân nhánh, có phổ khối lượng và phổ hồng ngoại như sau:
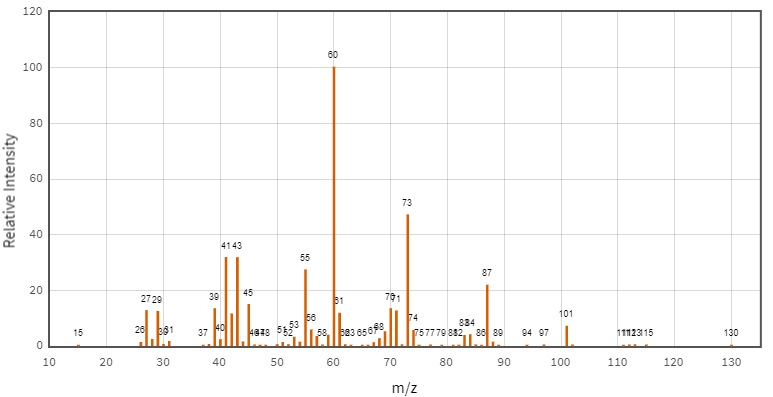
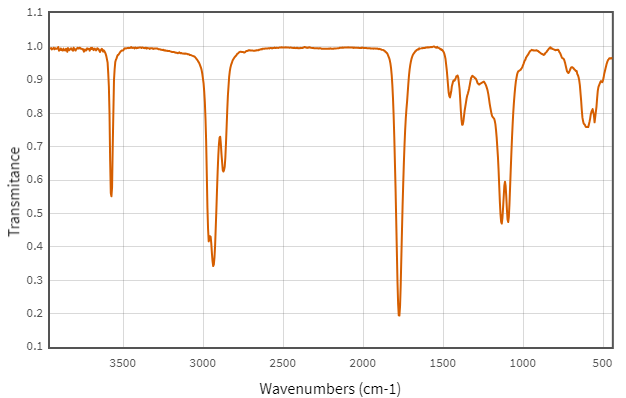
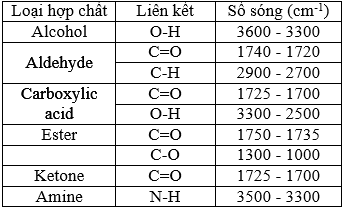
Cho bảng số sóng đặc trưng của các liên kết ở bảng bên. Cho các phát biểu sau:
a) X có 7 nguyên tử carbon.
b) X thuộc loại hợp chất ester
c) X tác dụng được với NaHCO3.
d) X hòa tan trong nước kém hơn acetic acid
(Xem giải) Câu 25: Cho các phát biểu sau:
a) Công thức phân tử của methyl fomate và glucose lần lượt là C2H4O2; C6H12O6. Chúng có cùng công thức đơn giản nhất là CH2O
b) Người ta thường xác định tỉ khối hơi của một chất khí X (chưa biết phân tử khối) so với không khí (dX/kk) rồi tính tính phân tử khối của X theo công thức: MX = 29.d(X/kk)
c) Trong phương pháp phổ khối lượng, đối với các hợp chất đơn giản, thường mảnh có giá trị m/z lớn nhất ứng với mảnh ion phân tử [M+] và giá trị này bằng giá trị nguyên tử khối của chất nghiên cứu.
d) Octane là một alkane có công thức phân tử là C8H18, là chất lỏng không màu, có tính chống nổ cao, không tan trong nước, nhẹ hơn nước, có trong dầu mỏ.
(Xem giải) Câu 26: Thủy phân hoàn ester hai chức E (C11H12O4, chứa vòng benzene) bằng dung dịch NaOH, thu được sản phẩm gồm alcohol X và hai chất hữu cơ Y, Z. Biết rằng X và Y có cùng số nguyên tử carbon. Cho Z tác dụng với dung dịch H2SO4 loãng, dư, thu được hợp chất hữu cơ T (C7H6O3). Cho các phát biểu sau:
a) Cho a mol T tác dụng với tối đa với 2a mol NaOH trong dung dịch.
b) Có 1 công thức cấu tạo thõa mãn tính chất của E.
c) Oxi hóa alcohol X bằng CuO, thu được aldehyde no, đơn chức, mạch hở.
d) Acid hóa Y thu được propionic acid.
PHẦN 3. Câu trắc nghiệm yêu cầu trả lời ngắn (3,6 điểm/6 câu, mỗi câu 0,6 điểm). Thí sinh trả lời từ câu 27 đến câu 32.
(Xem giải) Câu 27. Hợp chất hữu cơ X (C9H23O4N3) tác dụng với dung dịch NaOH dư, đun nóng, thu được sản phẩm hữu cơ gồm muối disodium glutamate và amine (chất khí ở điều kiện thường). Số công thức cấu tạo của X là bao nhiêu?
(Xem giải) Câu 28. Tổng công ty dệt may Hòa Thọ (Cẩm Lệ – Đà Nẵng) nhận một đơn đặt hàng cung cấp sợi nguyên liệu nitron cho Công ty dệt may Hà Nội để hoàn thành đơn hàng áo len nam (3 size theo kích cỡ tăng dần là S, M, L), mỗi size 20000 chiếc. Biết mỗi chiếc áo len size S cần phải dùng khoảng 500 gam sợi nitron và khối lượng len tăng thêm mỗi 10% theo mỗi size. Biết hiệu suất cả quá trình điều chế là 50%. Khối lượng nguyên liệu vinyl cyanide cần dùng để nhà máy sản xuất được đơn hàng trên là bao nhiêu tấn? (kết quả làm tròn đến hàng phần mười sau dấu phẩy)
(Xem giải) Câu 29. Hỗn hợp G gồm các chất hữu cơ mạch hở: carboxylic acid đơn chức G1; alcohol no, đa chức G2 và G3 là sản phẩm phản ứng ester hoá giữa G1 và G2. Trong G, số mol của G1 lớn hơn số mol của G2. Tiến hành các thí nghiệm sau:
• Thí nghiệm 1: Cho 1 mol G phản ứng với dung dịch NaHCO3 dư thu được 5,9496 lít khí CO2 (đkc).
• Thí nghiệm 2: Cho 1 mol G vào dung dịch NaOH dư đun nóng, có 1,36 mol NaOH tham gia phản ứng thu được 69,92 gam ancol G2.
• Thí nghiệm 3: Đốt cháy 1 mol G bằng oxi dư thu được 6,36 mol CO2 và 4,64 mol H2O. Biết các phản ứng xảy ra hoàn toàn.
1) G1 làm mất màu dung dịch Br2.
2) G2, G3 là các hợp chất đa chức.
3) Khối lượng hỗn hợp trong G là 147,68g.
4) Phần trăm khối lượng của G2 trong hỗn hợp là 12,46%.
5) G2 tan vô hạn trong nước.
Có bao nhiêu phát biểu trên là đúng?
(Xem giải) Câu 30: Cho các nhận định sau về nitrogen và hợp chất nitrogen
(1) Phản ứng nhiệt phân NH4NO3(s) → N2O(g) + 2H2O(g); ![]() = – 36 kJ, tỏa nhiệt, diễn ra thuận lợi về mặt năng lượng, đây là nguyên nhân chính của nhiều vụ nổ ammonium nitrate trên thế giới, điển hình là vụ nổ 04/8/2020 tại cảng Beirut, Lebannon.
= – 36 kJ, tỏa nhiệt, diễn ra thuận lợi về mặt năng lượng, đây là nguyên nhân chính của nhiều vụ nổ ammonium nitrate trên thế giới, điển hình là vụ nổ 04/8/2020 tại cảng Beirut, Lebannon.
(2) Mưa acid là hiện tượng nước mưa có pH thấp hơn 5,6, do các khí SO2, NOx trong khí quyển gây nên.
(3) Trong sản xuất rượu bia, khí nitrogen monoxide được bơm vào các bể chứa để loại bỏ khí oxygen.
(4) Hệ thống túi khí SRS (Supplemental Restraint System) được trang bị trên ô tô để hạn chế va đập gây tổn thương cho người ngồi trên xe khi va chạm xảy ra có thành phần chính là NaN3
(5) Các muối NH4HCO3, (NH4)2CO3, NaHCO3 đều có thể dùng làm bột nở.
Hãy cho biết số nhận định đúng?
(Xem giải) Câu 31: Điện phân dung dịch chứa x mol CuSO4, y mol H2SO4 và z mol NaCl (với điện cực trơ có màng ngăn xốp, hiệu suất điện phân là 100%). Khối lượng dung dịch giảm và khối lương Al2O3 bị hòa tan tối đa trong dung dịch sau điện phân ứng với mỗi thí nghiệm được cho ở bảng dưới đây:
| Thí nghiệm 1 | Thí nghiệm 2 | Thí nghiệm 3 | |
| Thời gian điện phân | t | 4t | 8t |
| Khối lượng dung dịch giảm (gam) | 27 | 83,2 | 103,1 |
| Khối lương Al2O3 bị hòa tan tối đa (gam) | 13,6 | 10,2 |
Biết tại catot ion Cu2+ điện phân hết thành Cu trước khi ion H+ điện phân tạo thành H2, cường độ dòng điện bằng nhau và không đổi trong các thí nghiệm trên. Xác định tổng giá trị (x + y + z)?
(Xem giải) Câu 32. Cho dung dịch A chứa KOH và Ca(OH)2
Tiến hành 3 thí nghiệm với cùng một khối lượng dung dịch A như sau:
– Thí nghiệm 1: Sục 2,7269 lít khí CO2 (đkc) vào dung dịch A thu được dung dịch chứa m gam chất tan
– Thí nghiệm 2: Sục 3,4706 lít khí CO2 (đkc) vào dung dịch A thu được dung dịch chứa (m + 2,86) gam chất tan
– Thí nghiệm 3: Sục từ từ tới dư khí CO2 vào dung dịch A thì sự phụ thuộc của số mol kết tủa theo số mol CO2 hấp thụ được biểu diễn bằng đồ thị hình (bên)
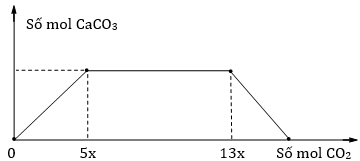
Tính giá trị của m?



Bình luận