[2020 – 2021] Thi học sinh giỏi lớp 12 – Tỉnh Ninh Bình
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Thời gian làm bài: 180 phút
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2A | 3A | 4C | 5D | 6A | 7B | 8C | 9D | 10C |
| 11C | 12C | 13B | 14C | 15C | 16A | 17B | 18A | 19C | 20D |
| 21B | 22A | 23D | 24A | 25D | 26B | 27B | 28D | 29C | 30D |
| 31C | 32B | 33B | 34D | 35D | 36C | 37A | 38A | 39D | 40A |
| 41B | 42B | 43A | 44A | 45D | 46D | 47D | 48D | 49C | 50A |
| 51D | 52A | 53B | 54B | 55D | 56A |
I. TRẮC NGHIỆM (14,0 điểm)
(Xem giải) Câu 1: Thủy phân hoàn toàn 1 mol pentapeptit X mạch hở thu được 3 mol glyxin (Gly), 1 mol alanin (Ala) và 1 mol valin (Val). Thủy phân không hoàn toàn X thu được hai đipeptit Gly-Ala, Ala-Gly và tripeptit Gly-Gly-Val nhưng không thu được peptit nào sau đây?
A. Gly-Gly-Gly. B. Gly-Ala-Gly. C. Ala-Gly-Gly. D. Gly-Gly.
(Xem giải) Câu 2: Cho ancol X có công thức phân tử là C5H12O. Đun nóng X với H2SO4 đặc ở 170°C thu được anken duy nhất. Số công thức cấu tạo có thể có của X là
A. 3. B. 4. C. 6. D. 5.
(Xem giải) Câu 3: Cho chất hữu cơ X mạch hở, có công thức phân tử là C4H6O4 tác dụng với dung dịch NaOH đun nóng, thu được ancol Y và muối natri của axit cacboxylic Z. Biết rằng Y và Z có cùng số nguyên tử cacbon. Phát biểu nào sau đây đúng?
A. Đun nóng Y với H2SO4 đặc ở 170°C thu được một anken duy nhất.
B. Y hòa tan được Cu(OH)2 ở điều kiện thường tạo phức xanh lam.
C. X là hợp chất hữu cơ đa chức.
D. Z có phản ứng tráng gương.
(Xem giải) Câu 4: Axit salixylic (axit o-hiđroxi benzoic) tác dụng với ancol metylic (có xúc tác, t°) tạo ra este X, tác dụng với anhiđrit axetic tạo ra este Y. Cho X, Y lần lượt tác dụng với dung dịch NaOH đều thu được chất hữu cơ M. Công thức cấu tạo của M là
A. CH3COONa. B. o-HO-C6H4-COOCH3.
C. o-NaO-C6H4-COONa. D. o-HOOC-C6H4-OOC-CH3.
(Xem giải) Câu 5: Cho các phát biểu sau
(a) Tinh bột, tripanmitin và lòng trắng trứng đều bị thủy phân trong môi trường kiềm, đun nóng
(b) Xenlulozơ là chất rắn dạng sợi, màu trắng, không tan trong nước Svayde.
(c) Glucozơ thể hiện tính oxi hóa khi cho tác dụng với H2 (Ni, t°).
(d) Ở điều kiện thường, etylamin là chất lỏng, tan nhiều trong nước.
(e) Metylamin có tính bazơ mạnh hơn phenylamin.
(g) Gly-Ala và Gly-Ala-Gly đều có phản ứng với Cu(OH)2 tạo ra hợp chất màu tím.
(h) Có thể phân biệt axit fomic và but-1-in bằng dung dịch AgNO3 trong NH3.
Số phát biểu đúng là
A. 6. B. 5. C. 4. D. 3.
(Xem giải) Câu 6: Chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong quả nho chín nên còn gọi là đường nho. Khử chất X bằng H2 thu được chất hữu cơ Y. Tên gọi của X và Y lần lượt là
A. glucozơ và sobitol. B. fructozơ và sobitol.
C. glucozơ và fructozơ. D. saccarozơ và glucozơ.
Câu 7: Dãy các kim loại nào sau đây tan hết trong axit HCl loãng, dư, ở điều kiện thường?
A. Na, K, Cu. B. Ca, Mg, Al. C. Cr, Mg, Hg. D. Na, Ag, Be.
(Xem giải) Câu 8: Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl với điện cực trơ, thu được khí H2 ở catot.
(b) Cho CO dư qua hỗn hợp MgO và Fe3O4 nung nóng, thu được MgO và Fe.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, xảy ra ăn mòn điện hóa.
(d) Kim loại có nhiệt độ nóng chảy cao nhất là W, kim loại dẫn điện tốt nhất là Ag.
(e) Cho mẩu Na vào dung dịch muối CuSO4, sau phản ứng thu được Cu kim loại.
Số phát biểu đúng là
A. 5. B. 3. C. 4. D. 2.
Câu 9: Tơ nitron dai, bền với nhiệt và giữ nhiệt tốt nên thường được dùng để dệt vải may quần áo ấm hoặc bện thành sợi len đan áo rét. Tơ nitron được tổng hợp từ monome nào sau đây?
A. Axit ԑ – aminocaproic. B. Vinyl clorua.
C. Caprolactam. D. Acrilonitrin.
(Xem giải) Câu 10: Thực hiện các thí nghiệm sau:
(a) Sục khí etilen vào dung dịch KMnO4.
(b) Sục khí Cl2 vào dung dịch H2S.
(c) Sục khí NO2 vào dung dịch NaOH.
(d) Cho dung dịch Na2CO3 vào dung dịch AlCl3.
(e) Cho dung dịch HCl vào dung dịch Fe(NO3)2.
(f) Cho Fe2O3 vào dung dịch HI.
Số thí nghiệm có phản ứng oxi hóa – khử xảy ra là
A. 3. B. 4. C. 5. D. 6.
(Xem giải) Câu 11: Trong các chất: m-HOC6H4OH, p-CH3COOC6H4OH, CH3CH2COOH, CH3NH3HCO3, HOOCCH2CH(NH2)COOH, ClH3NCH(CH3)COOH. Có bao nhiêu chất phản ứng tối đa với NaOH theo tỉ lệ mol 1 : 2?
A. 3. B. 5. C. 4. D. 6.
(Xem giải) Câu 12: Thực hiện các thí nghiệm sau:
(a) Nung NH4NO3 rắn.
(b) Đun nóng tinh thể NaCl với dung dịch H2SO4 đặc.
(c) Cho CaOCl2 vào dung dịch HCl đặc.
(d) Cho (NH4)2CO3 vào dung dịch Ca(OH)2 dư.
(e) Cho K2S vào dung dịch AlCl3.
(f) Cho dung dịch KHSO4 vào dung dịch NaHCO3.
(g) Cho FeS vào dung dịch HCl loãng.
(h) Cho CuS vào dung dịch H2SO4 loãng.
Số thí nghiệm tạo ra chất khí là
A. 8. B. 5. C. 7. D. 6.
(Xem giải) Câu 13: Đun nóng hỗn hợp gồm chất X có công thức phân tử CH4ON2 và chất Y có công thức phân tử C2H10O3N2 với dung dịch NaOH (dư), thu được hỗn hợp Z gồm hai khí và dung dịch gồm hai chất tan, trong đó có một muối T. Phát biểu nào sau đây là không đúng?
A. Chất X tác dụng với dung dịch HCl thấy khí không màu thoát ra.
B. Muối T có công thức là NaNO3.
C. Y là chất lưỡng tính.
D. Hai khí trong Z là amoniac và metylamin.
Câu 14: Phát biểu nào sau đây không đúng?
A. CrO3 là chất rắn màu đỏ thẫm, có tính oxi hóa rất mạnh.
B. Cho dung dịch H2SO4 loãng vào dung dịch Na2CrO4, thu được dung dịch có màu da cam.
C. Cr2O3 vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH loãng.
D. Trong môi trường axit, các muối Cr(III) thể hiện tính oxi hóa.
(Xem giải) Câu 15: Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 thu được chất rắn X và khí Y. Cho chất rắn X vào nước thu được chất rắn không tan E và dung dịch Z. Cho E vào dung dịch NaOH dư thấy tan một phần. Biết các phản ứng xảy ra hoàn toàn, dung dịch Z chứa
A. Ba(AlO2)2 và Mg(OH)2. B. Ba(OH)2.
C. Ba(AlO2)2. D. Ba(OH)2 và Ba(AlO2)2.
(Xem giải) Câu 16: Cho các phản ứng hóa học sau:
(a) BaCl2 + H2SO4 → (b) Ba(OH)2 + Na2SO4 →
(c) Ba(OH)2 + (NH4)2SO4 → (d) Ba(OH)2 + H2SO4 →
Số phản ứng có phương trình ion thu gọn Ba2+ + SO42- → BaSO4 là
A. 2. B. 4. C. 1. D. 3.
(Xem giải) Câu 17: Hoà tan hoàn toàn hỗn hợp X gồm x mol Fe, y mol Cu, z mol Fe2O3 và t mol Fe3O4 trong dung dịch HCl không thấy khí bay ra khỏi bình, dung dịch thu được chỉ chứa 2 muối. Phương trình biểu diễn mối quan hệ giữa số mol các chất có trong hỗn hợp X là
A. x + y = z + 2t. B. x + y = z + t. C. x + y = z + 2t. D. x + y = 2z + 3t.
(Xem giải) Câu 18: Cho các chất: Cu, Al2O3, FeCl2, Fe2(SO4)3, BaCl2, NaHCO3. Số chất tác dụng được với dung dịch chứa hỗn hợp gồm NaNO3 và NaHSO4 là
A. 5. B. 3. C. 6. D. 4.
(Xem giải) Câu 19: Cho bột Fe vào dung dịch AgNO3 dư, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch gồm các chất tan là
A. Fe(NO3)2, AgNO3. B. Fe(NO3)2, AgNO3, Fe(NO3)3.
C. Fe(NO3)3, AgNO3. D. Fe(NO3)2, Fe(NO3)3.
(Xem giải) Câu 20: Thực hiện các thí nghiệm sau:
(a) Đốt dây sắt trong khí clo dư.
(b) Nung hỗn hợp gồm bột sắt và lưu huỳnh (trong điều kiện không có không khí).
(c) Cho bột sắt dư vào dung dịch axit nitric loãng.
(d) Cho bột sắt vào dung dịch đồng (II) sunfat.
(e) Cho bột đồng vào dung dịch sắt (III) clorua.
(f) Cho oxit sắt từ tác dụng với dung dịch axit clohiđric.
Số thí nghiệm chỉ tạo ra muối sắt (II) là
A. 6. B. 5. C. 3. D. 4.
(Xem giải) Câu 21: Cho cân bằng hóa học: 2SO2 (k) + O2 (k) ⇌ 2SO3 (k) ∆H < 0. Phát biểu nào sau đây đúng?
A. Cân bằng chuyển dịch theo chiều thuận khi tăng nhiệt độ.
B. Cân bằng chuyển dịch theo chiều nghịch khi giảm nồng độ O2.
C. Cân bằng chuyển dịch theo chiều thuận khi giảm áp suất hệ phản ứng.
D. Cân bằng chuyển dịch theo chiều nghịch khi giảm nồng độ SO3.
(Xem giải) Câu 22: Cho hỗn hợp X gồm silic và nhôm. X tan hoàn toàn trong dung dịch chứa chất nào sau đây?
A. NaOH. B. KHCO3. C. HCl. D. BaCl2.
(Xem giải) Câu 23: Cho các chất sau: C2H5NH2 (1), C6H5NH2 (2), NH3 (3), NaOH (4), p-O2N-C6H4NH2 (5). Lực bazơ của các chất giảm dần theo thứ tự là
A. (2), (5), (3), (1), (4). B. (4), (1), (3), (5), (2).
C. (5), (2), (3), (1), (4). D. (4), (1), (3), (2), (5).
(Xem giải) Câu 24: Cho các dung dịch sau đều có nồng độ 0,1M: KOH, Ba(OH)2, NaCl, H2SO4, Na2CO3. Số dung dịch làm đổi màu quỳ tím là
A. 4. B. 3. C. 2. D. 5.
Câu 25: Hiệu ứng nhà kính là hiện tượng Trái Đất đang ấm dần lên do một phần bức xạ trong vùng hồng ngoại bị giữ lại mà không bức xạ ra ngoài vũ trụ. Khí nào dưới đây là nguyên nhân chính gây ra hiệu ứng nhà kính?
A. O2. B. SO2. C. N2. D. CO2.
Câu 26: Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A. Cu. B. Al. C. Cr. D. Ag.
(Xem giải) Câu 27: Cho ba lá kẽm giống nhau vào ba dung dịch có nồng độ mol và thể tích như nhau (lấy dư), đựng trong ba ống nghiệm riêng biệt được đánh số thứ tự (1), (2), (3). Sau khi phản ứng kết thúc, lấy ba lá kẽm ra cân thấy: lá kẽm thứ nhất không thay đổi khối lượng; lá kẽm thứ hai có khối lượng giảm đi; lá kẽm thứ ba có khối lượng tăng lên. Giả sử toàn bộ kim loại sinh ra đều bám vào lá kẽm, ống nghiệm (1), (2), (3) lần lượt chứa dung dịch
A. Pb(NO3)2, NiSO4, MgCl2. B. MgCl2, FeCl2, AgNO3.
C. FeSO4, NaCl, Cr(NO3)3. D. AlCl3, CuCl2, FeCl2.
(Xem giải) Câu 28: Cho sơ đồ: NaHCO3 + X → Na2SO4 + Y → NaCl + Z → NaNO3. Chất X, Y, Z lần lượt là
A. (NH4)2SO4, HCl, HNO3. B. H2SO4, BaCl2, HNO3.
C. K2SO4, HCl, AgNO3. D. NaHSO4, BaCl2, AgNO3.
(Xem giải) Câu 29: Cho chất X có công thức phân tử là C11H10O4 và sơ đồ phản ứng sau :
(1) X + NaOH → Y + Z + T + H2O
(2) Y + NaOH → CH4 + Na2CO3 (Biết nY : nNaOH = 1 : 2)
(3) Z + AgNO3 + NH3 + H2O → M + Ag + NH4NO3
(4) T + CO2 + H2O → C6H5OH + NaHCO3
Phát biểu nào sau đây đúng?
A. Công thức phân tử của Y là C2H3O2Na. B. Chất X có 2 công thức cấu tạo phù hợp.
C. Trong phân tử Z có 4 nguyên tử hiđro. D. T là chất lưỡng tính.
(Xem giải) Câu 30: Cho sơ đồ các phản ứng sau (theo đúng tỉ lệ mol):
(a) X → Y + CO2 (tº) (b) Y + H2O → Z
(c) T + Z → R + X + H2O (d) 2T + Z → Q + X + 2H2O
Các chất R, Q thỏa mãn sơ đồ trên lần lượt là
A. KHCO3, Ba(OH)2. B. Ba(OH)2, KHCO3.
C. K2CO3, KOH. D. KOH, K2CO3.
(Xem giải) Câu 31: Cho các polime: tơ tằm, sợi bông, tơ visco, nilon-6, tơ nitron. Những polime có nguồn gốc từ xenlulozơ là
A. sợi bông, tơ visco và tơ nilon-6. B. tơ tằm, sợi bông và tơ nitron.
C. sợi bông và tơ visco. D. tơ visco và tơ nilon-6.
Câu 32: Dung dịch nào sau đây làm quỳ tím chuyển màu xanh?
A. Alanin. B. Metylamin. C. Axit axetic. D. Phenylamin.
(Xem giải) Câu 33: Trong các chất: axetilen, anđehit fomic, vinyl axetat, isoamyl axetat, triolein, axit acrylic. Số chất có khả năng làm mất màu nước brom ở điều kiện thường là
A. 6. B. 5. C. 4. D. 3.
(Xem giải) Câu 34: Để mô tả một số phương pháp thu khí thường tiến hành trong phòng thí nghiệm người ta có các hình vẽ (1), (2), (3) như sau:
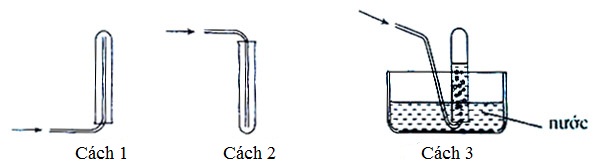
Phát biểu đúng liên quan đến các hình vẽ này là:
A. Phương pháp theo hình (1) có thể áp dụng thu các khí: H2, SO2, Cl2, NH3.
B. Phương pháp theo hình (1), (3) đều có thể áp dụng thu các khí: NH3, H2, N2.
C. Phương pháp theo hình (2) có thể áp dụng thu các khí: CO2, N2, SO2, Cl2.
D. Phương pháp theo hình (3) có thể áp dụng thu các khí: O2, H2, N2.
(Xem giải) Câu 35: Cho 7,6 gam hỗn hợp X gồm Mg và Ca phản ứng vừa đủ với 4,48 lít (đktc) hỗn hợp khí Y gồm Cl2 và O2 thu được 19,85 gam chất rắn Z chỉ gồm các muối clorua và các oxit kim loại. Khối lượng của Mg trong X là
A. 1,8 gam. B. 4,6 gam. C. 2,4 gam. D. 3,6 gam.
(Xem giải) Câu 36: Hòa tan hoàn toàn 5,22 gam hỗn hợp X gồm Mg và Al trong dung dịch HNO3 loãng, dư. Sau khi phản ứng kết thúc thu được dung dịch Y và khí N2O duy nhất. Cho dung dịch NaOH dư vào X, thấy khí mùi khai thoát ra đồng thời thu được 8,7 gam kết tủa. Số mol HNO3 đã tham gia phản ứng là
A. 0,64 mol. B. 0,5 mol. C. 0,6 mol. D. 0,56 mol.
(Xem giải) Câu 37: Xenlulozơ trinitrat được điều chế từ xenlulozơ và axit nitric đậm đặc có H2SO4 đặc, nóng xúc tác. Để thu được 29,7 kg xenlulozơ trinitrat cần dùng vừa đủ dung dịch chứa m kg axit nitric. Biết hiệu suất phản ứng đạt 90%, giá trị của m là
A. 21 kg. B. 42 kg. C. 30 kg. D. 10 kg.
(Xem giải) Câu 38: Cho 4,12 gam α–amino axit X (phân tử có một nhóm –COOH và một nhóm –NH2) phản ứng với dung dịch HCl (dư) thì thu được 5,58 gam muối. Chất X là
A. H2NCH(C2H5)COOH. B. H2NCH(CH3)COOH.
C. H2N[CH2]2COOH. D. H2NCH2CH(CH3)COOH.
(Xem giải) Câu 39: Tiến hành phản ứng nhiệt nhôm hoàn toàn hỗn hợp X gồm Al; 0,02 mol Cr2O3 và 0,03 mol FeO thu được 7,36 gam hỗn hợp Y. Hỗn hợp Y tác dụng vừa đủ với V lít dung dịch NaOH 0,1M. Giá trị của V là
A. 0,2. B. 0,5. C. 1,2. D. 0,8.
(Xem giải) Câu 40: Cho hỗn hợp bột X chứa 0,02 mol Al và x mol Fe vào 400ml dung dịch Y gồm AgNO3 0,2M và Cu(NO3)2 0,1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Z và 12,32 gam kim loại. Giá trị của x là
A. 0,07. B. 0,035. C. 0,06. D. 0,05.
(Xem giải) Câu 41: Hỗn hợp M gồm một este no, đơn chức, mạch hở và 2 amin X, Y no, đơn chức, mạch hở, là đồng đẳng kế tiếp (MX < MY). Đốt cháy hoàn toàn một lượng M thu được N2, 7,56 gam nước và 5,376 lít khí CO2 (đktc). Phân tử khối của chất X là
A. 59. B. 31. C. 45. D. 73.
(Xem giải) Câu 42: Hỗn hợp X gồm C4H4, C4H2, C4H6, C4H8 và C4H10. Tỉ khối của X so với H2 là 27. Đốt cháy hoàn toàn X cần dùng vừa đủ V lít khí O2 (đktc), thu được CO2 và 0,03 mol H2O. Giá trị của V là
A. 3,696. B. 1,232. C. 7,392. D. 2,464.
(Xem giải) Câu 43: Đốt cháy hoàn toàn m gam FeS2 bằng một lượng O2 vừa đủ, thu được khí X. Hấp thụ hết X vào 1 lít dung dịch chứa Ba(OH)2 0,15M và KOH 0,1M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa. Giá trị của m là
A. 18,0. B. 24,0. C. 23,2. D. 12,6.
(Xem giải) Câu 44: Hỗn hợp E chứa hai hợp chất hữu cơ mạch hở gồm este X (CnH2n-2O2) và axit Y (CmH2m-4O4). Đốt cháy hoàn toàn 28,0 gam E thu được CO2 có số mol nhiều hơn H2O là 0,35 mol. Nếu đun nóng 28,0 gam E với dung dịch KOH vừa đủ, cô cạn dung dịch sau phản ứng thu được 0,15 mol CH3OH và a gam muối. Giá trị của a là
A. 39,2. B. 33,6. C. 42,8. D. 41,0.
(Xem giải) Câu 45: Đốt cháy hoàn toàn 29,16 gam hỗn hợp X gồm RCOOCH3, HCOOC2H3 và CH3COOCH3 thu được m gam H2O và 21,952 lít khí CO2 (đktc). Mặt khác, cho 29,16 gam hỗn hợp X phản ứng vừa đủ với dung dịch chứa 0,5 mol NaOH. Giá trị của m là
A. 8,1 gam. B. 9,0 gam. C. 10,8 gam. D. 12,6 gam.
(Xem giải) Câu 46: Hỗn hợp X gồm 3 este đơn chức, tạo thành từ cùng một ancol Y với 3 axit cacboxylic (phân tử chỉ có nhóm –COOH); trong đó có hai axit no là đồng đẳng kế tiếp nhau và một axit không no (có đồng phân hình học, chứa một liên kết đôi C = C trong phân tử). Thủy phân hoàn toàn 5,88 gam X bằng dung dịch NaOH thu được hỗn hợp muối và m gam ancol Y. Cho m gam Y vào bình đựng natri dư, sau phản ứng thu được 896 ml khí (đktc) và khối lượng bình tăng 2,48 gam. Mặt khác, nếu đốt cháy hoàn toàn 5,88 gam X thì thu được CO2 và 3,96 gam H2O. Phần trăm khối lượng este không no trong X gần nhất với giá trị là
A. 40,8%. B. 38,8%. C. 29,3%. D. 34,1%.
(Xem giải) Câu 47: Cho dung dịch X gồm NaHCO3 0,1M và K2CO3 0,2M; dung dịch Y gồm HCl 0,2M và NaHSO4 0,6M. Nhỏ từ từ từng giọt đến hết 300 ml dung dịch X vào 100 ml dung dịch Y và khuấy đều thu được V lít khí CO2 thoát ra (đktc) và dung dịch Z. Thêm 100 ml dung dịch gồm KOH 0,6M và BaCl2 1,5M vào dung dịch Z, thu được m gam kết tủa. Các phản ứng đều xảy ra hoàn toàn. Giá trị của V và m là
A. 0,448 và 25,8. B. 0,448 và 11,82.
C. 1,0752 và 8,274. D. 1,0752 và 22,254.
(Xem giải) Câu 48: Đốt cháy hoàn toàn m gam triglixerit X cần vừa đủ 2,31 mol O2, thu được H2O và 1,65 mol CO2. Cho m gam X tác dụng với dung dịch NaOH vừa đủ, thu được glixerol và 26,52 gam muối. Mặt khác, m gam X tác dụng được tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A. 0,18. B. 0,12. C. 0,15. D. 0,09.
(Xem giải) Câu 49: Điện phân dung dịch chứa đồng thời NaCl và CuSO4 với cường độ dòng điện không đổi (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của các khí trong nước và sự bay hơi của nước). Kết quả thí nghiệm được ghi ở bảng sau:
| Thời gian điện phân (giây) | Khối lượng catot tăng (gam) | Khí thoát ra ở anot | Dung dịch thu được sau điện phân có khối lượng giảm so với khối lượng dung dịch ban đầu (gam) |
| 1930 | m | Một khí duy nhất | 2,70 |
| 7720 | 4m | Hỗn hợp khí | 9,15 |
| t | 5m | Hỗn hợp khí | 11,11 |
Giá trị của t là
A. 10615. B. 9650. C. 11580. D. 8202,5.
(Xem giải) Câu 50: Đốt cháy hoàn toàn 9 gam hỗn hợp X gồm etylamin và đimeylamin bằng lượng O2 vừa đủ. Cho toàn bộ sản phẩm cháy sinh ra vào bình đựng dung dịch Ba(OH)2, sau khi các phản ứng xảy ra hoàn toàn thu được 59,1 gam kết tủa và dung dịch có khối lượng giảm m gam so với khối lượng dung dịch Ba(OH)2 ban đầu. Giá trị của m là
A. 28,9. B. 50,1. C. 26,1. D. 35,2.
(Xem giải) Câu 51: Cho hai axit cacboxylic X, Y đều đơn chức, mạch hở, không no (có một liên kết đôi C=C; MX < MY); Z là ancol có cùng số nguyên tử cacbon với X; T là este ba chức tạo bởi X, Y và Z. Chia 40,38 gam hỗn hợp E gồm X, Y, Z, T làm 3 phần bằng nhau:
– Phần 1: Đem đốt cháy hoàn toàn thu được 0,5 mol CO2 và 0,53 mol H2O.
– Phần 2: Cho tác dụng với dung dịch brom dư thấy có 0,05 mol Br2 phản ứng.
– Phần 3: Cho tác dụng với lượng vừa đủ dung dịch gồm KOH 1M và NaOH 3M rồi cô cạn được m gam rắn khan.
Giá trị của m là
A. 6,66. B. 6,80. C. 5,04. D. 5,18.
(Xem giải) Câu 52: Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2 thu được dung dịch X. Nhỏ từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau:
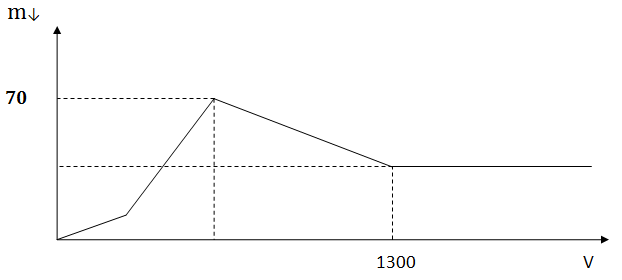
Giá trị của a là
A. 8,10. B. 4,05. C. 5,40. D. 6,75.
(Xem giải) Câu 53: Nung nóng 60,01 gam hỗn hợp X gồm KMnO4, KClO3 và MnO2, sau một thời gian thu được khí O2 và 48,81 gam chất rắn Y gồm K2MnO4, MnO2, KMnO4, KCl. Để hòa tan hoàn toàn Y cần vừa đủ dung dịch chứa 1,6 mol HCl thu được 9,688 lít khí Cl2 (đktc). Phần trăm khối lượng KMnO4 bị nhiệt phân là
A. 70,83%. B. 72,92%. C. 77,08%. D. 75,00%.
(Xem giải) Câu 54: Đun nóng 0,25 mol hỗn hợp T gồm hai peptit mạch hở T1, T2 (T1 nhiều hơn T2 một liên kết peptit, đều được tạo thành từ hai amino axit X và Y có công thức dạng H2NCnH2nCOOH; MX < MY) với dung dịch NaOH vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 1,05 mol muối của X và 0,35 mol muối của Y. Mặt khác, đốt cháy hoàn toàn 66,0 gam T cần vừa đủ 3,15 mol O2. Phân tử khối của T1 là
A. 359. B. 402. C. 303. D. 387.
(Xem giải) Câu 55: Hỗn hợp X gồm M2CO3, MHCO3 và MCl (M là kim loại kiềm). Cho 32,65 gam X tác dụng vừa đủ với dung dịch HCl, thu được dung dịch Y và 8,96 lít khí CO2 (đktc). Cho dung dịch AgNO3 dư vào Y, thu được 100,45 gam kết tủa. Kim loại M là
A. Na. B. Rb. C. K. D. Li.
(Xem giải) Câu 56: Cho 20,88 gam hỗn hợp X gồm Fe, Fe(NO3)2 và Fe(NO3)3 vào nước (dư) thấy còn lại 10,08 gam rắn không tan. Mặt khác, hòa tan hoàn toàn 20,88 gam X trong dung dịch HCl loãng thu được dung dịch Y chỉ gồm các muối của kim loại và hỗn hợp khí Z gồm hai khí không màu (trong đó có một khí hóa nâu). Tỉ khối của Z so với He bằng 4,7. Cho dung dịch AgNO3 (dư) vào Y thu được m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 101. B. 106. C. 103. D. 104.
II. TỰ LUẬN (6,0 điểm)
Câu 1. (2,0 điểm)
(Xem giải) 1. Viết phương trình hóa học biểu diễn dãy biến hoá sau:
![]()
Biết X là muối amoni chứa lưu huỳnh có phân tử khối là 51.
(Xem giải) 2. Đốt cháy hoàn toàn 1 mol chất hữu cơ X no, mạch hở thu được sản phẩm cháy gồm CO2 và 1 mol H2O. X phản ứng với được dung dịch AgNO3/NH3. Viết công thức cấu tạo có thể có của X và phương trình hóa học xảy ra.
Câu 2. (2,0 điểm)
(Xem giải) 1. Hỗn hợp E gồm hai este đơn chức, là đồng phân cấu tạo của nhau và đều chứa vòng benzen. Đốt cháy hoàn toàn m gam E cần vừa đủ 8,064 lít khí O2 (đktc) thu được 14,08 gam CO2 và 2,88 gam H2O. Cho m gam E phản ứng tối đa với dung dịch chứa 2,8 gam NaOH (đun nóng) thu được dung dịch T chứa 6,62 gam hỗn hợp ba muối. Tính khối lượng muối của axit cacboxylic trong T.
(Xem giải) 2. Hỗn hợp E gồm chất X (CnH2n+4O4N2, là muối của axit cacboxylic hai chức) và chất Y (CmH2m+3O2N, là muối của axit cacboxylic đơn chức). Đốt cháy hoàn toàn 0,12 mol E cần vừa đủ 0,24 mol O2 thu được N2, H2O và 0,2 mol CO2. Mặt khác, cho 0,12 mol E tác dụng hết với dung dịch NaOH thu được hỗn hợp Z gồm hai khí đều làm xanh quỳ tím ẩm. Cô cạn dung dịch sau phản ứng thu được m gam hỗn hợp muối khan. Tính m.
Câu 3. (2,0 điểm)
(Xem giải) 1. Nhỏ từ từ dung dịch HCl loãng (đến dư) vào dung dịch X gồm 0,05 mol Ba(OH)2 và 0,15 mol Ba(AlO2)2 (hoặc Ba[Al(OH)4]2). Vẽ đồ thị biểu diễn sự phụ thuộc của số mol kết tủa thu được vào số mol HCl phản ứng và giải thích.
(Xem giải) 2. Hòa tan hoàn toàn 21,78 gam hỗn hợp X gồm Mg, Al, MgCO3, Al(NO3)3 trong dung dịch chứa 0,12 mol HNO3 và 0,65 mol H2SO4. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa các muối trung hòa và hỗn hợp khí Z gồm CO2, N2, N2O và H2 (trong đó số mol của H2 là 0,06 mol). Tỉ khối của Z so với He bằng 7,25. Cho dung dịch Y tác dụng với dung dịch NaOH dư, thấy lượng NaOH phản ứng tối đa là 57,6 gam; đồng thời thu được 24,36 gam kết tủa. Tính phần trăm khối lượng của N2O trong hỗn hợp khí Z.


Bình luận