[2022] Thi thử TN chuyên Quốc học Huế (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Giải chi tiết và đáp án:
⇒ Mã đề: 120
| 1C | 2A | 3D | 4C | 5A | 6D | 7B | 8D | 9A | 10D |
| 11B | 12D | 13C | 14A | 15C | 16D | 17A | 18D | 19B | 20B |
| 21A | 22A | 23D | 24D | 25C | 26A | 27D | 28B | 29C | 30D |
| 31C | 32D | 33A | 34A | 35A | 36C | 37C | 38A | 39B | 40D |
(Xem giải) Câu 1. Hoá chất được sử dụng để phân biệt CO2 và SO2 là
A. dung dịch Ba(OH)2. B. dung dịch Ca(OH)2.
C. dung dịch nước brom. D. dung dịch NaCl.
(Xem giải) Câu 2. Dung dịch X chứa: Na+ (x mol), PO43- (y mol) và SO42- (z mol). Mối quan hệ giữa x, y, z là
A. x = 3y + 2z. B. 2x = 3y + 2z. C. x = 2y + 2z. D. x = y + z.
(Xem giải) Câu 3. Trong phản ứng: 2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O. Vai trò của NaCrO2 là
A. môi trường. B. vừa oxi hoá vừa khử. C. chất oxi hoá. D. chất khử.
(Xem giải) Câu 4. Clo hoá pentan với tỉ lệ mol 1 : 1, số sản phẩm monoclo tối đa thu được là
A. 1. B. 4. C. 3. D. 2.
(Xem giải) Câu 5. Sơ đồ thí nghiệm dưới đây có thể dùng thu khí nào?
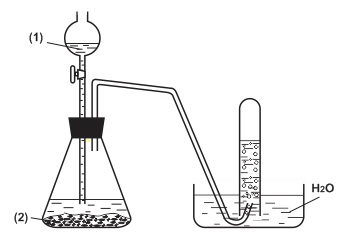
A. H2. B. NH3. C. H2S. D. SO2.
Câu 6. Hợp chất C6H5NHCH3 có tên thay thế là
A. metylbenzylamin. B. metylphenylamin. C. N-metylanilin. D. N-metylbenzenamin.
Câu 7. Polime nào sau đây có thể được điều chế bằng phản ứng trùng ngưng?
A. Poli(metyl metacrylat). B. Poli(hexametylen-ađipamit).
C. Polibutadien. D. Poliacrylonitrin.
(Xem giải) Câu 8. Một mẫu nước cứng có chứa các ion: Ca2+, Mg2+, HCO3-, Cl-, SO42-. Chất có khả năng làm mềm mẫu nước cứng trên là
A. NaHCO3. B. MgCl2. C. HCl. D. Na2CO3.
Câu 9. Amin nào sau đây tồn tại ở trạng thái lỏng trong điều kiện thường?
A. Anilin. B. Dimetylamin. C. Trimetylamin. D. Etylamin.
Câu 10. Hợp chất nào sau đây có tính lưỡng tính?
A. Cr(OH)2. B. CrCl2. C. CrO3. D. Cr2O3.
Câu 11. Sản phẩm của quá trình quang hợp là glucozơ (C6H12O6) và
A. CO2. B. O2. C. Cl2. D. hồ tinh bột.
Câu 12. Một đoạn mạch polime có dạng -CH2-CH(CH3)-CH2-CH(CH3)-CH2-CH(CH3)-CH2-CH(CH3)-. Cấu tạo một mắt xích của polime trên là
A. -CH(CH3)-. B. CH2=CH(CH3). C. CH2=CH2. D. -CH2-CH(CH3)-
Câu 13. Khử Fe2O3 bằng CO dư ở nhiệt độ cao để điều chế sắt là phương pháp
A. điện phân nóng chảy. B. thuỷ luyện. C. nhiệt luyện. D. điện phân dung dịch.
Câu 14. Kim loại nào dẫn điện tốt nhất?
A. Ag. B. Fe. C. Al. D. Au.
Câu 15. Hợp chất nào sau đây thuộc loại đisaccarit?
A. Tinh bột. B. Xenlulozơ. C. Saccarozơ. D. Glucozơ.
Câu 16. Đun nóng este CH2=CHCOOCH3 trong dung dịch NaOH thu được sản phẩm là
A. CH2=CHOH và CH3COONa. B. CH2=CHCOOH và CH3OH.
C. CH2=CHCH2OH và CH3ONa. D. CH2=CHCOONa và CH3OH.
Câu 17. Kim loại nào sau đây là kim loại kiềm?
A. Na. B. Mg. C. Be. D. Al.
Câu 18. Kim loại bị thụ động trong dung dịch H2SO4 đặc nguội là
A. Na. B. Zn. C. Cu. D. Al.
Câu 19. Chất nào dưới đây không phải là este?
A. CH3COOC6H5. B. CH3COOH. C. CH3COOC2H5. D. CH3COOCH=CH2.
Câu 20. “Nước đá khô” được dùng để bảo quản thực phẩm. Nước đá khô là
A. CO rắn. B. CO2 rắn. C. I2. D. nước đá.
(Xem giải) Câu 21. Cho 13,6 gam hỗn hợp gồm C2H5OH và C3H7OH tác dụng vừa đủ với Na thu được m gam muối và 2,8 lít khí (đktc). Giá trị của m là
A. 19,100. B. 16,225. C. 16,475. D. 19,350.
Câu 22. A, B, C, D là các chất khác nhau trong số 4 chất: etyl axetat, ancol etylic, axit axetic, axit fomic. Nhiệt độ sôi của chúng được ghi trong bảng sau:
| Chất | A | B | C | D |
| Nhiệt độ sôi (°C) | 77,1 | 78 | 100,8 | 118 |
Nhận xét nào sau đây đúng?
A. A là etyl axetat. B. C là ancol etylic. C. B là axit axetic. D. D là axit fomic.
(Xem giải) Câu 23. Cho dãy các chất sau: benzen, phenyl fomat, saccarozơ, glucozơ, fructozơ, (Gly-Val), etylen glicol, triolein. Số chất làm mất màu dung dịch nước brom là
A. 4. B. 6. C. 5. D. 3.
(Xem giải) Câu 24. Cây xanh là nguồn sống quý giá của con người, là lá phổi xanh duy trì sự sống của trái đất. Chúng ta không thể tồn tại mà không có cây xanh và bảo vệ nó là trách nhiệm của tất cả chúng ta. Thống kê cho thấy, trung bình mỗi người hít thở 16 lần mỗi phút, mỗi lần hấp thụ khoảng 0,5 lít không khí. Và để bảo đảm sự sống cho 7,5 tỷ người đang sinh sống trên hành tinh này, chúng ta cần 562 tỷ cây xanh. Trung bình mỗi người mỗi năm hấp thụ tối thiểu khoảng bao nhiêu mét khối không khí? Biết 1 năm có 365 ngày.
A. 2400. B. 2600. C. 5000. D. 4200.
(Xem giải) Câu 25. Thí nghiệm nào dưới đây vừa tạo kết tủa, vừa có khí thoát ra?
A. Dung dịch HCl tác dụng với dung dịch NaAlO2 dư. B. Al vào dung dịch HNO3 dư.
C. Na vào dung dịch AlCl3 dư. D. Dung dịch Al2(SO4)3 tác dụng với dung dịch BaCl2.
(Xem giải) Câu 26. Cho m gam hỗn hợp bột gồm Fe và Zn tác dụng với dung dịch CuSO4. Sau một thời gian phản ứng, thu được dung dịch Y và 1,1m gam chất rắn Z. Nhận định nào sau đây luôn đúng?
A. Fe đã tham gia phản ứng. B. Zn chưa phản ứng hết.
C. dung dịch Y vẫn còn màu xanh. D. dung dịch Y có màu vàng nâu.
(Xem giải) Câu 27. Đốt cháy hoàn toàn a gam hỗn hợp X gồm CH3COOCH3 và HCOOCH3 cần vừa đủ 1,232 lít O2 (đktc) thu được H2O và 2,2 gam CO2. Giá trị của a là
A. 1,29. B. 2,17. C. 2,22. D. 1,34.
(Xem giải) Câu 28. Đốt cháy hoàn toàn hỗn hợp X gồm glucozơ và xenlulozơ thu được CO2, H2O với nCO2 – nH2O = 0,01 mol. Số gốc glucozơ trong phân từ xenlulozơ trên là
A. 1,204.10^22. B. 6,02.10^21. C. 6,02.10^23. D. 3,01.10^23
(Xem giải) Câu 29. Thuốc thử duy nhất để phân biệt các dung dịch NaCl, NH4NO3, K2CO3, NaHCO3, HNO3 đựng trong các lọ mất nhân là
A. NaOH. B. HCl C. Ba(NO3)2. D. AgNO3.
(Xem giải) Câu 30. Cho các nhận định sau:
(1) Hỗn hợp chứa K và Al có tỉ lệ mol 1 : 1 tan hết trong nước dư.
(2) Hỗn hợp gồm Fe3O4 và Cu (có tỉ lệ mol tương ứng 1 : 2) tan hết trong dung dịch HCl loãng dư.
(3) Zn hoà tan trong dung dịch Fe2(SO4)3 dư là quá trình ăn mòn điện hoá học.
(4) Osimi (Os) là kim loại nặng nhất.
Số nhận định đúng là
A. 4. B. 3. C. 1. D. 2.
(Xem giải) Câu 31. Cho đồ phản ứng sau:
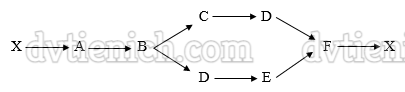
Trong đó: X là hidrocacbon có tỉ khối hơi so với hiđro là 8. Mỗi chữ cái ứng với một hợp chất hữu cơ. Mỗi mũi tên là một phương trình phản ứng (chất phản ứng là vô cơ và xúc tác). D có thể là
A. C2H5OH. B. CH3COOC2H5. C. CH3COOH. D. CH3COONa.
(Xem giải) Câu 32. A là kim loại khá hoạt động. Chất B là hoá chất thông dụng, chỉ chứa ba nguyên tố K, O và A (trong đó % theo khối lượng của K, O lần lượt là 40,27% và 32,96%). Nhỏ dung dịch HCl đến dư vào dung dịch chất B thì dung dịch đổi màu. B có phân tử khối là
A. 94. B. 294. C. 127. D. 194.
(Xem giải) Câu 33. Một muối kép có dạng KCl.MCl2.nH2O (M là kim loại). Hoà tan hoàn toàn m gam muối kép này vào nước thu được dung dịch X. Cho dung dịch X tác dụng với lượng dư dung dịch NaOH tạo 5,8 gam kết tủa. Lọc kết tủa, rửa sạch rồi nung trong điều kiện không có không khí đến khối lượng không đổi thu được 4 gam chất rắn. Mặt khác, nung m gam muối kép trên đến khối lượng không đổi thì thấy khối lượng giảm 38,92%. m có giá trị gần nhất là
A. 28. B. 32. C. 30. D. 26.
(Xem giải) Câu 34. Hòa tan hoàn toàn m gam hỗn hợp gồm Na, K vào 50 ml dung dịch Y gồm HCl 0,6M và H2SO4 0,2M thù được dung dịch chỉ chứa muối trung hòa. Thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn là
A. 0,56 lít. B. 0,448 lít. C. 0,672 lit. D. 0,224 lít.
(Xem giải) Câu 35. Cho các sơ đồ phản ứng sau:
A1 → A2 + H2O
A1 + O2 → A3
A2 → A4 (polime) có phân tử khối trung bình là 420000
A2 + KMnO4 + H2O → A5 + …
A5 + A3 → A6 (C4H8O3) +…
Số mắt xích trong A4 là
A. 15000. B. 20000. C. 14000. D. 16000.
(Xem giải) Câu 36. Cho 4 dung dịch A, B, C, D (mỗi dung dịch chỉ chứa một loại cation và một loại anion). Tiến hành các thí nghiệm sau:
TN 1: Trộn dung dịch A và dung dịch B đồng thời đun nóng thu được kết tủa trắng.
TN 2: Cho từ từ dung dịch A vào dung dịch C thì sau một thời gian thu được khí X.
TN 3: Trộn dung dịch B và dung dịch D thì thu được kết tủa trắng có phân tử khối là 217 và chất khí Y (Y làm quỳ ẩm hoá xanh và có tỉ khối so với X là 0,5).
TN 4: Đun nóng hoàn toàn D thì thu được khí Y và khí Z. X tác dụng với Z tạo chất rắn đơn chất.
Nhận định nào dưới đây là chưa chính xác
A. Dung dịch C là muối trung hoà của X.
B. Dung dịch A làm cho quỳ tím hóa đỏ.
C. Muối B có thể là BaCl2 hoặc Ba(NO3)2.
D. Trong điều kiện thích hợp khí X tác dụng với O2 cũng thu được chất rắn màu vàng.
(Xem giải) Câu 37. X là hỗn hợp gồm 2 peptit hơn kém nhau một liên kết peptit, tổng số nguyên tử O trong cả 2 peptit là 11. Cho m gam X tác dụng với dung dịch KOH vừa đủ, thu được (m + 45,68) gam hỗn hợp muối của glyxin và alanin. Đốt cháy hoàn toàn lượng muối sinh ra với oxi vừa đủ thu được sản phẩm cháy gồm CO2, H2O, N2 và K2CO3. Dẫn hỗn hợp sản phẩm hơi và khí qua bình đựng dung dịch Ca(OH)2 dư, sau phản ứng thu được 168 gam kết tủa và 9,856 lít khí (đktc) thoát ra khỏi bình. Các phản ứng xảy ra hoàn toàn. Số đồng phân của peptit nhỏ hơn là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 38. Khí hỗn hợp X gồm Fe3O4, Fe2O3, CuO (trong đó nguyên tố oxi chiếm 27,03% theo khối lượng) bằng CO ở nhiệt độ cao, sau một thời gian thu được chất rắn Y và khí Z. Hoà tan Y trong dung dịch HNO3 dư thu được dung dịch T và khí NO (sản phẩm khử duy nhất). Cho thanh nhôm có khối lượng m gam vào dung dịch T thấy thoát ra 2,24 lít khí NO (chất khí duy nhất ở đktc) và khối lượng thanh nhôm thay đổi theo thời gian được biểu diễn bằng đồ thị dưới đây
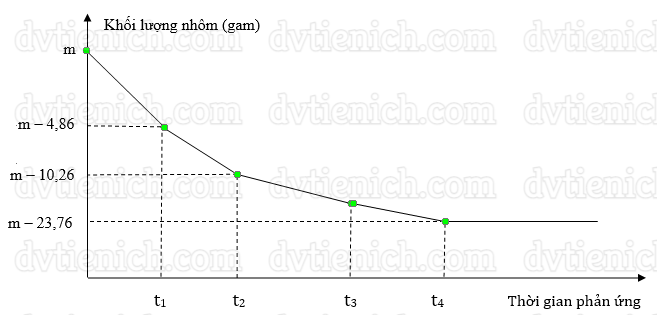
Biết các phản ứng xảy ra hoàn toàn và giả sử kim loại sinh ra không bám vào thanh nhôm. Số mol của Fe2O3 là
A. 0,15 mol. B. 0,2 mol. C. 0,1 mol. D. 0,05 mol.
(Xem giải) Câu 39. Cho m gam hỗn hợp X gồm Zn và Fe vào 500 ml dung dịch Y gồm AgNO3 và Cu(NO3)2 với tỉ lệ nồng độ mol tương ứng là 2 : 5. Sau khi phản ứng xảy ra hoàn toàn, thu được 20 gam chất rắn Z và dung dịch E. Cho dung dịch NaOH dư vào dung dịch E, lọc kết tủa và nung ngoài không khí đến khối lượng không đổi thu được 2,4 gam một oxit. Để hòa tan hết m gam X thì cần dùng 500 ml dung dịch HCl 1M. Nồng độ mol của dung dịch AgNO3 trong dung dịch Y là
A. 0,5M. B. 0,12M. C. 0,24M. D. 0,36M.
(Xem giải) Câu 40. Hỗn hợp A gồm: hai axit cacboxylic đơn chức X, Y (X, Y đều có số nguyên tử C không quá 3) và Z là este thuần chức được tạo ra từ X và Y. Cho 3,21 gam hỗn hợp A tác dụng vừa đủ với dung dịch NaOH, sau phản ứng thu được 4,12 gam hỗn hợp muối và một ancol B. Nếu đốt cháy 0,01 mol B thì thu được 0,672 lít khí CO2 (đktc). Lấy 4,12 gam hỗn hợp muối trên cho vào dung dịch AgNO3 trong NH3 dư thì thu được 10,29 gam kết tủa gồm hai chất. Tổng số mol của X và Y trong hỗn hợp A là
A. 0,025 mol. B. 0,03 mol. C. 0,02 mol. D. 0,035 mol

Bình luận