[2025 – 2026] Thi học sinh giỏi lớp 12 – Tỉnh Phú Thọ
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Tổng hợp đề hsg theo năm học
⇒ Mã đề 020-H12B năm 2025-2026
⇒ Thời gian làm bài: 150 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1C | 2D | 3B | 4A | 5D | 6D | 7B | 8D |
| 9A | 10C | 11A | 12A | 13B | 14D | 15A | 16B |
| 17C | 18C | 19B | 20D | 21C | 22A | 23A | 24D |
| 25A | 26C | 27C | 28B | 29A | 30A | 31D | 32C |
| Câu 1 | Câu 2 | Câu 3 | Câu 4 | |
| (a) | Đ | Đ | Đ | Đ |
| (b) | Đ | S | Đ | S |
| (c) | S | S | S | S |
| (d) | Đ | Đ | Đ | Đ |
| Câu 1 | Câu 2 | Câu 3 | Câu 4 | Câu 5 | Câu 6 |
| 1,03 | 125 | 21,95 | 2356 | 1245 | 135 |
I. PHẦN TRẮC NGHIỆM
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn (8,0 điểm). Thí sinh trả lời từ câu 1 đến câu 32. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho các quá trình chuyển hoá N2 tạo thành một loại đạm nitrate trong tự nhiên:
![]()
Số quá trình nitrogen thay đổi số oxi hoá là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 2. Quá trình chuyển hóa glucose thành acetic acid qua hai phản ứng:
C6H12O6 (glucose) → 2C2H5OH + 2CO2 (enzyme) (1)
C2H5OH + O2 → CH3COOH + H2O (enzyme) (2)
Cho các phát biểu sau:
(a) Glucose vừa là chất oxi hóa vừa là chất khử.
(b) Ethanol bị khử thành acetic acid bởi oxygen.
(c) Số oxi hóa trung bình của carbon trong glucose, ethanol và acetic acid đều bằng 0.
(d) Phản ứng (1) và (2) không có sự thay đổi số oxi hóa của hydrogen.
Phát biểu đúng là
A. (a) và (c). B. (a) và (b). C. (c) và (d). D. (a) và (d).
(Xem giải) Câu 3. Acetylene thường được dùng làm nhiên liệu, ví dụ đèn xì oxygen–acetylene dùng để hàn cắt kim loại. Khí methane là thành phần chính của khí thiên nhiên cũng được sử dụng làm nhiên liệu. Phản ứng cháy của methane và acetylene theo phương trình hóa học sau:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) (1)
2C2H2(g) + 5O2(g) → 4CO2(g) + 2H2O(g) (2)
Cho biết nhiệt tạo thành chuẩn của các chất:
| Chất | CH4(g) | C2H2(g) | CO2(g) | H2O(g) |
| -74,9 | +227,0 | -393,5 | -241,8 |
Phát biểu nào sau đây không đúng?
A. Biến thiên enthalpy chuẩn của phương trình (2) là -2511,6 kJ.
B. Nếu xét cùng số mol thì lượng nhiệt tỏa ra từ C2H2 gấp CH4 xấp xỉ 3,131 lần.
C. Nếu xét cùng khối lượng thì lượng nhiệt tỏa ra khi đốt cháy CH4 gấp C2H2 xấp xỉ 1,038.
D. Biến thiên enthalpy chuẩn của phương trình (1) là -802,2 kJ.
(Xem giải) Câu 4. Các sơ đồ dưới đây biểu diễn quá trình phản ứng X ⇋ Y:
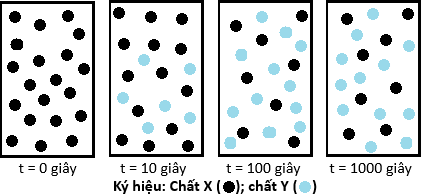
Phát biểu nào mô tả chính xác nhất phản ứng tại thời điểm 1000 giây?
A. Phản ứng đạt trạng thái cân bằng vì nồng độ của X và nồng độ của Y không thay đổi.
B. Phản ứng chưa đạt trạng thái cân bằng vì chưa tiêu thụ hết X.
C. Phản ứng không đạt trạng thái cân bằng vì nồng độ của X không bằng nồng độ của Y.
D. Phản ứng chưa đạt trạng thái cân bằng vì vị trí của các phân tử vẫn đang thay đổi.
(Xem giải) Câu 5. Trong công nghiệp, khí NH3 được sản xuất từ N2 và H2 theo phương trình hoá học của phản ứng: N2(g) + 3H2(g) ⇋ 2NH3(g). Nung nóng hỗn hợp gồm N2 và H2 (tỉ lệ mol tương ứng 1 : 3) trong bình kín có dung tích không đổi với xúc tác Fe (có thể tích không đáng kể) sau một thời gian đưa về nhiệt độ ban đầu, thu được hỗn hợp khí có áp suất giảm 12,25% so với áp suất ban đầu. Hiệu suất của phản ứng tổng hợp NH3 là
A. 24,0%. B. 25,25%. C. 26,25%. D. 24,5%.
(Xem giải) Câu 6. Cho biết thế điện cực chuẩn của các cặp oxi hóa – khử:
| Cặp oxi hoá – khử | X+/X | Y2+/Y | Z2+/Z | T+/T |
| Thế điện cực chuẩn E° (V) | +0,799 | -0,440 | +0,340 | -2,713 |
Cho các phát biểu sau:
(a) Tính oxi hóa được xếp theo thứ tự giảm dần: T+ > Y2+ > Z2+ > X+.
(b) Kim loại Z khử được ion Y2+ trong dung dịch.
(c) Kim loại X khử được ion H+ trong dung dịch HCl.
(d) Ở điều kiện chuẩn, pin Galvani Z-X có sức điện động bằng 0,459V.
Số phát biểu đúng là
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 7. Cần mạ bạc (silver) lên một vật hình trụ, đáy hình tròn với bán kính 3 cm, chiều cao hình trụ 0,3 cm, lớp mạ bạc dày 0,01 cm, tiến hành điện phân dung dịch AgNO3 dư với cường độ dòng điện không đổi 2A. Khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t phút. Biết khối lượng riêng của silver là 10,5 gam/cm³, hiệu suất điện phân là 100%, số mol electron (n) đi qua dây dẫn được tính theo công thức n = It/F với I là cường độ dòng điện (A), t là thời gian (s), F là hằng số Faraday (F = 96500 C/mol), π = 3,14. Giả thiết lớp mạ dày như nhau, toàn bộ lượng silver tạo ra đều bám hết vào vật hình trụ. Thời gian t cần mạ là
A. 47,285. B. 48,910. C. 44,189. D. 45,352.
(Xem giải) Câu 8. Khi điện phân dung dịch hỗn hợp Cu(NO3)2 1M và AgNO3 1M với điện cực trơ. Phát biểu nào sau đây đúng?
A. Tại cathode xảy ra quá trình khử Cu2+ trước.
B. Khối lượng dung dịch giảm bằng khối lượng của kim loại thoát ra bám vào cathode.
C. Khi bắt đầu điện phân có khí thoát ra tại cathode.
D. Tại anode xảy ra quá trình oxi hóa H2O.
(Xem giải) Câu 9. Một dung dịch được thử nghiệm định tính để xác định sự có mặt của một số ion. Lấy mẫu dung dịch cho vào 4 ống nghiệm, sau đó nhỏ mỗi loại thuốc thử lần lượt vào mỗi ống nghiệm và ghi nhận hiện tượng như bảng sau:
| Ống nghiệm | Thuốc thử | Hiện tượng |
| 1 | Hydrochloric acid | Sủi bọt khí |
| 2 | Sodium carbonate | Xuất hiện kết tủa |
| 3 | Sodium hydroxide | Xuất hiện kết tủa |
| 4 | Barium chloride | Xuất hiện kết tủa |
Dung dịch trên có chứa những ion nào trong số các ion sau: (1) Ca2+, (2) CO32-, (3) HCO3-, (4) SO42-?
A. (1), (3), (4). B. (2), (3), (4). C. (1), (2), (4). D. (1), (2), (3).
(Xem giải) Câu 10. Phát biểu nào sau đây sai?
A. Oxi hóa NH3 trong khí oxygen dư ở 900°C, xúc tác Pt, thu được NO và H2O.
B. Hỗn hợp Cu và Fe2O3 (tỉ lệ mol tương ứng 1 : 1) có thể tan hoàn toàn trong dung dịch HCl dư.
C. Điện phân CaCl2 nóng chảy (điện cực trơ), tại anode xảy ra sự khử ion Cl-.
D. Số oxi hóa của nitrogen trong nitric acid là +5.
(Xem giải) Câu 11. Cho các phát biểu sau:
(a) Dùng bình bằng sắt có thể đựng được dung dịch sulfuric acid đặc nguội.
(b) Điện phân dung dịch Na2SO4 (điện cực trơ) khí thoát ra ở cathode và anode lần lượt là O2 và H2.
(c) Cho FeCl2 tác dụng hoàn toàn với dung dịch AgNO3 dư, thu được kết tủa gồm hai chất.
(d) Cho Mg vào dung dịch FeCl3 dư đến khi phản ứng kết thúc, thu được Fe.
(e) Để bảo quản dung dịch muối iron(II), người ta ngâm vào dung dịch này chiếc đinh sắt.
Số phát biểu đúng là
A. 3. B. 4. C. 2. D. 5.
(Xem giải) Câu 12. Một loại phân bón NPK gồm hỗn hợp các muối NH4NO3, (NH4)2HPO4, KCl và các chất phụ gia không chứa nguyên tố dinh dưỡng. Trên bao bì chứa phân bón NPK có ghi các chỉ số biểu thị hàm lượng dinh dưỡng, chẳng hạn ghi 19-12-8 được hiểu là phần trăm khối lượng của N, P2O5, K2O lần lượt là 19%, 12% và 8%. Việc bón phân NPK cho cây cà phê sau khi trồng được 4 năm được chia thành ba thời kì sau:
| Thời kì | Lượng phân bón |
| Bón thúc ra hoa | 0,5 kg phân 10-12-5/cây |
| Bón đậu quả, ra quả | 0,7 kg phân 12-8-2/cây |
| Bón thúc quả lớn, tăng dưỡng chất cho quả | 0,6 kg phân 16-16-16/cây |
Cho các phát biểu sau:
(a) Tổng khối lượng nguyên tố postassium đã cung cấp cho mỗi cây cà phê trong cả ba thời kì là 135 gam.
(b) Cho dung dịch Ca(OH)2 lần lượt vào ba muối NH4NO3, (NH4)2HPO4, KCl đun nóng thì có hai muối phản ứng sinh ra khí mùi khai.
(c) Muối NH4NO3 chỉ cung cấp nguyên tố nitrogen cho cây cà phê dưới dạng ion NH4+.
(d) Nguyên tố nitrogen được bổ sung cho cây nhiều nhất ở giai đoạn bón thúc quả lớn, tăng dưỡng chất cho quả.
(e) Trong phản ứng của NH3 với HNO3 tạo ra phân đạm NH4NO3 thì NH3 đóng vai trò là base vì có khả năng nhường proton.
Số phát biểu đúng là
A. 2. B. 3. C. 4. D. 5.
(Xem giải) Câu 13. Cho các bước tiến hành (không theo thứ tự) của phương pháp kết tinh như sau:
(a) Lọc nóng loại bỏ chất rắn không tan.
(b) Hòa tan chất rắn vào dung môi để tạo dung dịch bão hòa ở nhiệt độ cao.
(c) Lọc để thu được chất rắn.
(d) Để nguội và làm lạnh dung dịch thu được, chất cần kết tinh sẽ kết tinh.
Sắp xếp các bước theo đúng thứ tự của phương pháp kết tinh là
A. (c), (b), (d), (a). B. (b), (a), (d), (c).
C. (b), (a), (c), (d). D. (b), (c), (d), (a).
(Xem giải) Câu 14. Myrcene và limonene là các monoterpene có trong tinh dầu thực vật với mùi hương dễ chịu. Các chất này có công thức cấu tạo lần lượt như hình dưới:

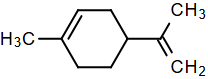
Chọn phát biểu đúng về myrcene và limonene
A. Myrcene và limonene là hai chất đồng đẳng của nhau.
B. Hydrogen hóa hoàn toàn 1 mol mycrene hoặc 1 mol limonene (xt Ni, t°) cần lượng H2 như nhau.
C. Hydrogen hóa hoàn toàn mycrene hoặc limonene đều thu được alkane.
D. Đốt cháy hoàn toàn 1 mol myrcene hoặc 1 mol limonene đều thu được cùng số mol carbon dioxide.
(Xem giải) Câu 15: Cho dãy chuyển hoá sau:
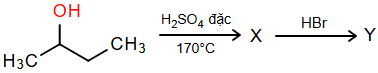
Biết X là sản phẩm chính, tên của X, Y lần lượt là:
A. But-2-ene và 2-bromobutane. B. But-1-ene và 2-bromobutane.
C. But-2-ene và 1-bromobutane. D. But-1-ene và 1-bromobutane.
(Xem giải) Câu 16. Muscone là hợp chất tạo nên mùi thơm đặc trưng của xạ hương, có công thức cấu tạo như hình bên:
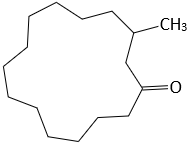
Cho các phát biểu sau:
(a) Muscone thuộc hợp chất ketone.
(b) Muscone có công thức phân tử là C16H30O.
(c) Muscone có phản ứng cộng với HCN.
(d) Muscone có nhiệt độ sôi cao hơn so với ethanal.
(e) Muscone tham gia phản ứng tráng bạc với thuốc thử Tollens.
Số phát biểu đúng là
A. 3. B. 4. C. 2. D. 5.
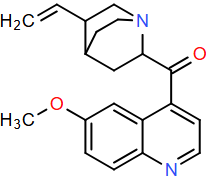
(Xem giải) Câu 17. Quinidine (X, C20H24N2O2) là chất có khả năng điều trị chứng loạn nhịp tim. Quinidine được tổng hợp từ quinidinone (Y, C20H22N2O2, cấu tạo như hình vẽ bên) bằng phản ứng với tác nhân lithium aluminium hydride (LiAlH4) theo qui trình thí nghiệm sau:
• Bước 1: Hoà tan 1,00 gam Y vào 50 mL một dung môi hữu cơ (THF) trong bình cầu 100 mL và làm lạnh dung dịch xuống 0°C, dung dịch được khuấy và thêm từ từ 0,59 gam LiAlH4 trong 15 phút và hỗn hợp tiếp tục được khuấy ở 0°C trong 2 giờ.
• Bước 2: Hỗn hợp sau phản ứng được xử lí lần lượt với 40 mL dung dịch HCl 2 M và 20 mL dung dịch NaOH 8 M ở 0°C. Toàn bộ hỗn hợp sau đó được chuyển vào phễu chiết, rồi thêm 50 mL diethyl ether, lắc đều, để yên khoảng 10 phút và tách lấy lớp hữu cơ. Thêm Na2SO4, lắc đều, sau đó lọc bỏ chất rắn, thu lấy dung dịch hữu cơ. Dung dịch hữu cơ được loại bỏ dung môi, thu được X ở dạng thô.
• Bước 3: Sản phẩm thô X được tinh chế bằng phương pháp sắc kí cột, thu được 0,54 gam chất rắn màu trắng X.
Cho các phát biểu sau về quá trình tổng hợp X ở trên:
(a) Trong phân tử X có một nhóm -OH.
(b) Ở bước 2, để yên phễu chiết khoảng 10 phút nhằm mục đích để X còn phân bố trong nước di chuyển vào lớp chất hữu cơ.
(c) Vai trò của Na2SO4 ở bước 2 có tác dụng hút nước, làm khan lớp chất hữu cơ.
(d) Hiệu suất của quá trình tổng hợp là 53,667% (kết quả làm tròn đến hàng phần nghìn).
Số phát biểu đúng là
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 18. Trùng hợp methyl methacrylate thu được polymer dùng làm chất dẻo còn gọi là thủy tinh hữu cơ. Công thức cấu tạo của methyl methacrylate là
A. CH2=CH-COO-CH3. B. CH3COO-CH=CH2.
C. CH2=C(CH3)-COOCH3. D. CH3COO-C(CH3)=CH2.
(Xem giải) Câu 19. Trong quả bồ kết có saponin, chất này có tính chất giặt rửa. Cho 20 quả bồ kết vào nồi và thêm 1 lít nước, đun sôi nhỏ lửa khoảng 30 phút tới khi được dung dịch có màu nâu sẫm. Cho các phát biểu sau:
(a) Dung dịch thu được có tính chất giặt rửa và được gọi là chất giặt rửa tự nhiên.
(b) Thành phần chính của chất giặt rửa tự nhiên tương tự với chất giặt rửa tổng hợp.
(c) Đặc điểm chung của phân tử các chất giặt rửa là có phần không phân cực và phần phân cực.
(d) Chất giặt rửa tự nhiên khó bị phân hủy sinh học, gây ô nhiễm môi trường.
Số phát biểu sai là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 20. Kết quả phân tích nguyên tố của ester đơn chức X (mạch hở) cho biết %C = 60%, %H = 8%, %O = 32% (về khối lượng). Trên phổ MS của X thấy xuất hiện tín hiệu của ion phân tử [M+] có giá trị m/z = 100. Biết X thu được từ phản ứng ester hoá giữa alcohol Y với carboxylic acid Z mạch phân nhánh. Cho các phát biểu sau:
(a) X có công thức phân tử C5H8O2 và có tên gọi là ethyl acrylate.
(b) X là monomer dùng để sản xuất thuỷ tinh hữu cơ.
(c) Trong phân tử của X có chứa 2 liên kết pi (π) và 13 liên kết sigma (σ).
(a) Y là một chất độc, khi vào cơ thể có thể gây mù mắt và thậm chí là tử vong.
Số phát biểu đúng là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 21. Carbohydrate X tham gia chuyển hóa sau:
X + Cu(OH)/OH- → dung dịch xanh lam;
X + Cu(OH)2/OH-, t° → kết tủa đỏ gạch.
Chất X không thể là chất nào dưới đây?
A. Glucose. B. Fructose. C. Saccharose. D. Maltose.
(Xem giải) Câu 22. Cho các phát biểu sau:
(a) Có thể phân biệt dung dịch fructose và glucose bằng nước bromine.
(b) Thủy phân hoàn toàn hỗn hợp saccharose và tinh bột chỉ thu được một loại monosaccharide.
(c) Phản ứng của glucose với hydrogen chứng minh glucose có tính khử.
(d) Tinh bột và cellulose là đồng phân của nhau.
Số phát biểu đúng là
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 23. Disacharide X là thành phần chính của đường mạch nha. Trong dung dịch nước, X tồn tại chủ yếu ở hai dạng cấu tạo (I) và (II). Hai dạng này tồn tại cân bằng sau:
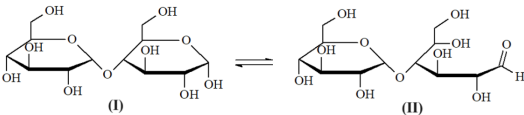
Cho các phát biểu sau:
(a) Dạng (I) có nhiều liên kết sigma hơn dạng (II).
(b) Liên kết giữa hai đơn vị monosaccharide trong phân tử X là liên kết β-1,4-glycoside.
(c) Enzyme maltase xúc tác đặc hiệu cho phản ứng thủy phân X.
(d) Phản ứng thủy phân X trong dung dịch H2SO4 98% xảy ra nhanh hơn trong dung dịch
H2SO4 50% vì nồng độ acid lớn hơn.
(e) Dạng (I) có một nhóm -OH hemiacetal.
(g) Số nhóm -OH ở dạng (I) và dạng (II) bằng nhau.
Số phát biểu đúng là
A. 4. B. 3. C. 2. D. 5.
(Xem giải) Câu 24: Cho các amine: CH3NHCH2CH3 (X1), C6H5NH2 (aniline) (X2), CH3CH2CH2NH2 (X3). Phát biểu nào sau đây sai?
A. X3 tác dụng với acid HNO2 ở nhiệt độ thường thu được alcohol bậc I.
B. X3 tạo được liên kết hydrogen với nước.
C. Tên thay thế của X1 là N-methylethanamine.
D. X1 và X2 đều làm quì tím ẩm chuyển sang màu xanh.
(Xem giải) Câu 25: Insulin là hormone có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp có chứa các peptide: Glu-Gln-Cys, Gly-Ile-Val, Gln-Cys-Cys, Val-Glu-Gln. Nếu đánh số thứ tự amino acid đầu N là số 1 thì amino acid ở vị trí số 5 trong X là
A. Gln. B. Cys. C. Glu. D. Val.
(Xem giải) Câu 26. Tyrosine là một trong những loại amino acid cần thiết và có thể bổ sung cho cơ thể thông qua các thực phẩm ăn uống hàng ngày. Tyrosine có cấu tạo như hình bên:
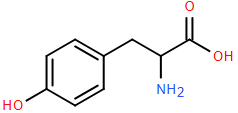
Cho các phát biểu sau:
(a) Tyrosine thuộc loại α-amino acid.
(b) Tyrosine tác dụng tối đa với KOH trong dung dịch theo tỉ lệ mol 1 : 1.
(c) Tyrosine là hợp chất hữu cơ đa chức.
(d) Tyrosine phản ứng với dung dịch Br2 thu được kết tủa.
Số phát biểu đúng là
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 27. Ethylhexyl palmitate còn có tên gọi khác là octyl palmitate. Ethylhexyl palmitate được ứng dụng rất phổ biến trong mỹ phẩm. Ethylhexyl palmitate có công thức cấu tạo như sau:
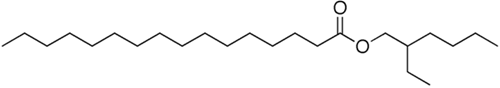
Trong công nghiệp, ethylhexyl palmitate được điều chế bằng phản ứng ester hóa giữa acid X và alcohol Y. Phát biểu nào sau đây sai?
A. Trong phân tử X có số nguyên tử hydrogen gấp hai lần số nguyên tử carbon.
B. Phân tử X có số nguyên tử carbon gấp hai lần số nguyên tử carbon trong phân tử Y.
C. Phần trăm khối lượng nguyên tử carbon trong chất Y là 68,83%.
D. Chất X có ít hơn linoleic acid hai liên kết π và ít hơn oleic acid 1 liên kết π.
(Xem giải) Câu 28. Cho các polymer: polybuta-1,3-diene, poly(vinyl chloride), poly(phenol formaldehyde), polyethylene, poly(methyl methacrylate). Số polymer dùng làm chất dẻo là
A. 2. B. 4. C. 3. D. 5.
(Xem giải) Câu 29. Hiện nay, nhu cầu sản xuất caprolactam trên thế giới khoảng 10 triệu tấn/năm, 90% trong đó dùng để tổng hợp tơ capron. Trong công nghiệp, caprolactam được điều chế theo sơ đồ bên:
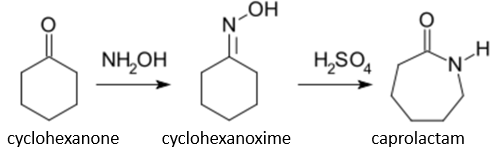
Để sản xuất 1,13 tấn caprolactam, cần sử dụng m tấn cyclohexanone (hiệu suất của cả quá trình trên là 80%). Giá trị của m là
A. 1,225. B. 1,375. C. 0,980. D. 0,784.
(Xem giải) Câu 30. Diethyl phthalate (DEP) là thuốc dùng trị ghẻ ngứa, có khối lượng riêng 1,125 gam/mL. DEP không tan trong nước, dễ tan trong ethanol và ether. Phản ứng tổng hợp DEP từ phthalic anhydride và ethyl alcohol như sau:
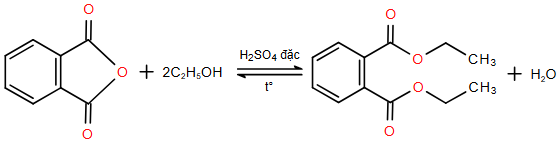
Từ m kg phthalic anhydride có thể sản xuất được 2000 lọ thuốc DEP. Biết mỗi lọ thuốc DEP chứa 8 mL DEP (còn lại là tá dược) và hiệu suất phản ứng tính theo phthalic anhydride là 80%. Giá trị của m là
A. 15,0. B. 13,73. C. 17,16. D. 12,0.
(Xem giải) Câu 31. Ephedrine được sử dụng với hàm lượng nhất định trong các loại thuốc điều trị cảm và dị ứng. Ephedrine có mùi tanh và dễ bị oxi hoá trong không khí, do đó người ta thường hạn chế sử dụng trực tiếp. Ephedrine aguetant là thuốc gây tê, gây mê, dạng bào chế dung dịch tiêm, thuốc có thành phần chính là ephedrine hydrochloride hàm lượng 30 mg/mL/ống.
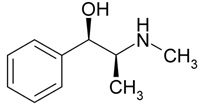
Cho các phát biểu sau:
(a) Công thức phân tử của ephedrine là C10H15NO.
(b) Ephedrine là chất hữu cơ tạp chức, chứa đồng thời nhóm chức alcohol và amine.
(c) Ephedrine hydrochloride được điều chế từ phản ứng của ephedrine với hydrochloric acid.
(d) Mỗi hộp ephedrine aguetant có 10 ống (mỗi ống 1 mL) có chứa tổng cộng 3 gam ephedrine hydrochloride.
Những phát biểu đúng là
A. (a), (d), (c). B. (b), (c), (d). C. (a), (b), (d). D. (a), (b), (c).
(Xem giải) Câu 32. Một nhà máy sử dụng mỡ động vật để sản xuất bánh xà phòng. Trong một loại mỡ lợn X có chứa 44,5% khối lượng tristearin; 44,2% khối lượng triolein; 8,06% khối lượng tripanmitin và 3,24% tạp chất trơ. Dưới đây là bảng giá nguyên liệu và các chi phí:
| STT | Nội dung | Đơn giá |
| 1 | Mỡ lợn | 30000 đồng/1 kg |
| 2 | Dung dịch NaOH 40% | 19000 đồng/1 kg |
| 3 | Phụ gia + chất độn | 100000 đồng/1 kg |
| 4 | Nhân công, máy móc, chi phí khác | 25000 đồng/1 kg thành phẩm |
Biết hiệu suất phản ứng xà phòng hóa là 80%, tất cả các muối sinh ra từ phản ứng đều dùng làm xà phòng, khối lượng muối của acid béo trong xà phòng thành phẩm chiếm 75% về khối lượng còn lại là phụ gia và chất độn, mỗi bánh có khối lượng tịnh là 90 gam (khối lượng tịnh là khối lượng của một vật thể nhưng không tính bao bì kèm theo), X tác dụng với dung dịch NaOH (vừa đủ). Giá tiền của 5 bánh xà phòng mà nhà máy trên sản xuất ra là m nghìn đồng. Giá trị của m gần nhất với giá trị nào sau đây?
A. 30,6. B. 40,2. C. 37,8. D. 52,4.
PHẦN II. Câu trắc nghiệm đúng sai (4,0 điểm). Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 1. Một nhóm học sinh thiết lập pin điện hoá ở điều kiện chuẩn theo sơ đồ như hình dưới. Các giá trị thế điện cực chuẩn của một số cặp oxi hoá – khử được cho ở trong bảng:
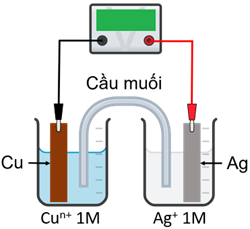
Cu2+(aq) + e → Cu+(aq) E° = +0,16V
Cu2+(aq) + 2e → Cu(s) E° = +0,34V
Cu+(aq) + e → Cu(s) E° = +0,52V
Ag+(aq) + e → Ag(s) E° = +0,80V
a) Với n = 1 hoặc n = 2, khi pin hoạt động, điện cực Ag luôn đóng vai trò là cathode.
b) Với n = 2 sức điện động chuẩn của pin đo được bằng 0,46V.
c) Với n = 1, khi pin hoạt động, nồng độ của ion Cu+ tăng dần.
d) Cầu muối có vai trò khép kín mạch điện và trung hoà dung dịch điện li ở hai điện cực.
(Xem giải) Câu 2. Trong công nghiệp, một lượng lớn NaHCO3 và Na2CO3 được sản xuất theo phương pháp Solvay bằng cách cho khí CO2 (lấy từ nhiệt phân đá vôi) vào dung dịch chứa sodium chloride (NaCI) bão hoà và ammonia (NH3) bão hoà.
CO2(aq) + H2O(l) + NH3(aq) + NaCl(aq) → NH4Cl(aq) + NaHCO3(s) (1)
NaHCO3 tách ra đem nhiệt phân thu được soda:
2NaHCO3 (t°) → Na2CO3 + CO2 + H2O (2)
và NH4Cl được sử dụng để tái tạo NH3 bằng cách tác dụng với Ca(OH)2 tạo ra từ CaO.
a) Phản ứng (1) xảy ra được là do NaHCO3 có độ tan kém hơn nên bị kết tinh trước.
b) Trong thực tế sản xuất, người ta đun nóng hỗn hợp các chất tham gia phản ứng (1) để thu được Na2CO3 ngay.
c) Nguyên liệu chính ban đầu của quá trình sản xuất soda bằng phương pháp Solvay là: NaCl, NH3, CaCO3 và H2O.
d) NaHCO3 được ứng dụng làm bột nở.
(Xem giải) Câu 3. Thuốc aspirin có tác dụng giảm đau, hạ sốt, chống viêm. Một công ty dược phẩm nhận đơn đặt hàng sản xuất 10000 hộp thuốc “Aspirin 81 mg” chứa hoạt chất chính là aspirin (o-CH3COOC6H4COOH). Aspirin được điều chế từ phenol theo sơ đồ sau:
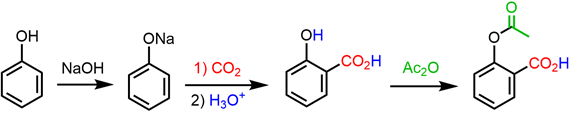
Cho biết mỗi hộp chứa 10 vỉ, mỗi vỉ chứa 10 viên nén, khối lượng mỗi viên là 200 mg, trong mỗi viên thuốc chứa 81 mg aspirin, phần còn lại là tá dược (chất độn, chất kết dính).
a) x mol aspirin tác dụng tối đa với 3x mol NaOH trong dung dịch.
b) Phần trăm khối lượng của tá dược có trong toàn bộ lô sản xuất 10000 hộp thuốc này là 59,5%.
c) Trong phân tử aspirin, liên kết C-O trong nhóm ester bền hơn liên kết O-H trong nhóm carboxyl nên aspirin không bị thủy phân trong môi trường acid ở dạ dày.
d) Hiệu suất toàn bộ quá trình chỉ đạt 75%, tuy nhiên, nhờ cải tiến nhà máy đã nâng hiệu suất toàn bộ quá trình lên 90%. Việc nâng cao hiệu suất này giúp công ty tiết kiệm được 470000 đồng mua phenol. Biết 1 kg phenol có giá 50000 đồng.
(Xem giải) Câu 4. Hợp chất X (chỉ chứa C, H, O trong phân tử) là một chất hóa học giữ vai trò quan trọng đối với sức khỏe của con người. Bằng phương pháp phổ khối lượng (MS) xác định được phân tử khối của X là 90. Bằng các phương pháp phổ hồng ngoại IR và phổ cộng hưởng từ hạt nhân NMR, xác định được trong phân tử của X chứa nhóm hydroxy và nhóm carboxyl cùng liên kết với một nguyên tử carbon. Đun nóng X với dung dịch sulfuric acid đặc (làm xúc tác), sau một thời gian thu được hỗn hợp các chất, trong đó có hợp chất hữu cơ Y (chỉ chứa 2 liên kết π). Trong phân tử Y, nguyên tố oxygen chiếm 44,44% về khối lượng và phân tử khối của Y nằm trong khoảng từ 75 đến 150.
a) X là hợp chất hữu cơ tạp chức.
b) Hợp chất Y có công thức phân tử là C6H10O4.
c) Trong phân tử của hợp chất X có chứa 10 liên kết sigma (σ).
d) Cả X và Y đều tác dụng được với dung dịch NaOH.
PHẦN III. Câu trắc nghiệm trả lời ngắn (3,0 điểm). Thí sinh trả lời từ câu 1 đến câu 6.
(Xem giải) Câu 1. Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber – Bosch theo phương trình hóa học:
N2(g) + 3H2(g) (400-450°C, 200 bar, Fe) ⇋ 2NH3(g) (1)
Trong đó khí H2 cung cấp cho nhà máy được sản xuất theo phản ứng:
CH4(g) + H2O(g) → CO(g) + 3H2(g) (2)
Để cung cấp nhiệt lượng cho phản ứng (2), người ta đốt cháy hoàn toàn CH4:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) (3)
Biết chỉ có 90% lượng nhiệt tỏa ra từ phản ứng (3) được cung cấp cho phản ứng (2), nhiệt tạo thành chuẩn của các chất cho ở bảng sau:
| Chất | CH4(g) | CO(g) | CO2(g) | H2O(g) |
| -74,9 | -110,5 | -393,5 | -241,8 |
Cần tổng bao nhiêu tấn CH4 để sản xuất 0,3 tấn H2? (kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 2. Thí nghiệm điều chế muối kết tinh FeSO4.nH2O (X) được tiến hành như sau:
• Bước 1: Cho 12 gam Fe nguyên chất vào 100 mL dung dịch H2SO4 15% có khối lượng riêng 1,10 g/cm³. Hỗn hợp được lắc đều đến khi phản ứng xảy ra hoàn toàn. Lọc dung dịch thu được, chuyển vào bình nón, thêm vài giọt dung dịch H2SO4 loãng. Hàn kín bình nón rồi làm lạnh đến nhiệt độ phòng và để yên trong hai ngày.
• Bước 2: Tiến hành lọc hỗn hợp trong bình nón, tách lấy chất rắn kết tinh. Phần dung dịch thu được, cho bay hơi một nửa khối lượng trong khí quyển CO2 sau đó để yên ở 20°C trong bình hàn kín trong hai ngày rồi lọc tách lấy chất kết tinh.
• Bước 3: Toàn bộ chất kết tinh ở bước 2 được rửa với cồn, làm khô nhanh trong giấy lọc. Kết quả thu được 32 gam tinh thể muối X (màu xanh) chứa 11,51% khối lượng lưu huỳnh.
Cho các phát biểu sau:
(1) Việc thêm vài giọt dung dịch H2SO4 loãng ở bước 1 nhằm mục đích chính là giảm sự thuỷ phân của muối sắt.
(2) Ở bước 2, có thể thay khí CO2 bằng khí N2.
(3) Hiệu suất của cả quá trình điều chế tinh thể X là 81,12%.
(4) Ở bước 1, có thể thay dung dịch H2SO4 15% bằng dung dịch H2SO4 80% để tăng tốc độ phản ứng.
(5) Tinh thể X có công thức là FeSO4.7H2O.
Liệt kê các phát biểu đúng theo thứ tự từ nhỏ đến lớn (ví dụ 1234,…)
(Xem giải) Câu 3. Nescafe đã sản xuất thành công lon coffee tự làm nóng. Để làm nóng coffee, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm dung dịch KOH hoặc NaOH rất loãng và CaO; 160 mL coffee trong lon sẽ được làm nóng đến khoảng 40°C. Giả sử nhiệt dung riêng của coffee là 4,18 J/g.K (Nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1°C). Cho ![]() (kJ/mol) của CaO(s), H2O(l), Ca(OH)2(aq) lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Khối lượng CaO cần cung cấp để làm nóng 160 mL coffee (d = 1,0 g/mL) từ 10°C đến 40°C là bao nhiêu gam? (kết quả làm tròn đến hàng phần trăm).
(kJ/mol) của CaO(s), H2O(l), Ca(OH)2(aq) lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Khối lượng CaO cần cung cấp để làm nóng 160 mL coffee (d = 1,0 g/mL) từ 10°C đến 40°C là bao nhiêu gam? (kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 4. Cho các phát biểu sau:
(1) (CH3)3N có danh pháp thay thế là trimethylamine.
(2) Glycine phản ứng được với dung dịch HCl.
(3) Phân tử lysine có hai nguyên tử nitrogen.
(4) Trong mỗi trường acid, dạng tồn tại chủ yếu của alanine là dạng cation.
(5) Protein là một trong những nguồn thức ăn bổ sung các amino acid thiết yếu cho cơ thể.
(6) “Gạch cua” nổi lên khi nấu riêu cua là hiện tượng đông tụ protein.
Liệt kê các phát biểu đúng theo thứ tự từ nhỏ đến lớn (ví dụ 1234,…)
(Xem giải) Câu 5. Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: HCOOH, CH3COOH, HCl, C6H5OH (phenol). Giá trị pH của các dung dịch trên (cùng nồng độ 0,01M), ở 25°C đo được như sau:
| Chất | X | Y | Z | T |
| pH | 6,48 | 3,22 | 2,00 | 3,45 |
Cho các phát biểu sau:
(1) X tác dụng với nước bromine xuất hiện kết tủa trắng.
(2) T được điều chế trực tiếp từ ethyl alcohol.
(3) T có thể tham gia phản ứng tráng bạc.
(4) Đun nóng Y với Cu(OH)2 trong môi trường kiềm thu được kết tủa đỏ gạch.
(5) Nhiệt độ sôi của X lớn hơn Y.
Liệt kê các phát biểu đúng theo thứ tự từ nhỏ đến lớn (ví dụ 1234,…)
(Xem giải) Câu 6. Y là một ester có mùi thơm của quả anh đào. Cho sơ đồ tổng hợp Y từ benzene như sau:
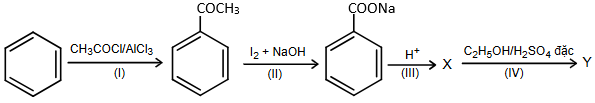
Cho các phát biểu sau:
(1) Chất X và chất Y đều có số liên kết π bằng nhau.
(2) Sau phản ứng (IV) có sự phân lớp vì chất Y ít tan trong dung môi không phân cực.
(3) Phản ứng (II) tạo ra chất kết tủa màu vàng là iodoform.
(4) Cho muối sodium benzoate tác dụng với carbonic acid thu được chất X.
(5) Chất Y không làm mất màu nước bromine ở điều kiện thường.
Liệt kê các phát biểu đúng theo thứ tự từ nhỏ đến lớn (ví dụ 1234,…)
II. PHẦN TỰ LUẬN
Câu 1. (2,0 điểm).
(Xem giải) 1. Ammonia đóng vai trò quan trọng trong ngành công nghiệp hoá chất. Ammonia được tạo thành từ nitrogen và hydrogen theo phản ứng sau:
N2(g) + 3H2(g) ⇋ 2NH3(g) ![]() = -91,80 kJ (1)
= -91,80 kJ (1)
Phản ứng (1) được thực hiện ở t = 450°C, trong một bình kín và có nắp là một piston có thể di chuyển không ma sát. Khi hệ đạt tới trạng thái cân bằng. Xác định chiều chuyển dịch cân bằng (có giải thích) của phản ứng (1) trong các trường hợp sau:
a) Tăng nhiệt độ của phản ứng.
b) Tăng áp suất bằng cách nén hỗn hợp phản ứng.
c) Nạp thêm 1 mol khí hiếm Ar vào bình trong điều kiện nhiệt độ và thể tích của hệ không thay đổi.
d) Nạp thêm 1 mol khí hiếm Ar vào bình trong điều kiện nhiệt độ và áp suất của hệ không thay đổi.
(Xem giải) 2. Trong quy trình sản xuất sulfuric acid (H2SO4) có giai đoạn dùng dung dịch H2SO4 98% hấp thụ sulfur trioxide (SO3) thu được oleum (H2SO4.SO3). Sulfur trioxide được tạo thành bằng cách oxi hóa sulfur dioxide bằng oxygen hoặc lượng dư không khí ở nhiệt độ 450°C – 500°C, chất xúc tác vanadium (V) oxide (V2O5) theo phương trình hóa học:
2SO2(g) + O2(g) ⇋ 2SO3(g) ![]() = -198,4 kJ
= -198,4 kJ
Nếu nồng độ ban đầu của SO2 và O2 tương ứng là 4M và 2M thì hiệu suất phản ứng tổng hợp SO3 đạt 80%. Để tăng hiệu suất phản ứng tổng hợp SO3 lên 90% thì cần cho SO2 nồng độ ban đầu 4M phản ứng với O2 có nồng độ x M. Tính giá trị x.
Câu 2 (2,0 điểm).
(Xem giải) 1. Thành phần chủ yếu của xăng dầu là hydrocarbon. Hãy giải thích vì sao:
a) Phải chứa xăng dầu trong các thùng chứa chuyên dụng và bảo quản ở những kho riêng.
b) Các sự cố tràn dầu trên biển thường gây ra thảm hoạ cho một vùng biển rất rộng.
c) Khi bị cháy xăng dầu không nên dùng nước để dập đám cháy.
d) Hiện nay chúng ta đang chuyển dần sang xăng sinh học E5. Nêu thành phần của xăng E5. Nêu những lợi ích khi sử dụng xăng sinh học
(Xem giải) 2. Xác định các chất: X1, X2, X3, X4, X5 và X (MX ≤ 362, chỉ chứa nhóm chức trong các nhóm: -OH, -COOH, -COO-) thoả mãn sơ đồ phản ứng sau:
(1) X + NaOH → X1 + X2 + H2O
(2) X1 + H2SO4 → Na2SO4 + X3
(3) X3 + X4 → poly (hexamethylene adipamide) + H2O
(4) X5 + X2 → poly(ethylene terephthalate) + H2O
(Xem giải) Câu 3 (1,0 điểm). Một nhóm học sinh tiến hành thí nghiệm điều chế nitrobenzene theo phương án 1 như hình vẽ. Cho con từ vào bình cầu, thêm 30 mL H2SO4 đặc, làm lạnh trong chậu nước đá rồi thêm từ từ 30 mL HNO3 đặc, sau đó cho 10 mL benzene và lắp sinh hàn hồi lưu rồi đun cách thủy trong 60 phút. Biết rằng, máy khuấy từ cung cấp nhiệt lượng đồng thời hệ thống nam châm quay tạo từ trường làm xoay con từ bên trong bình cầu.
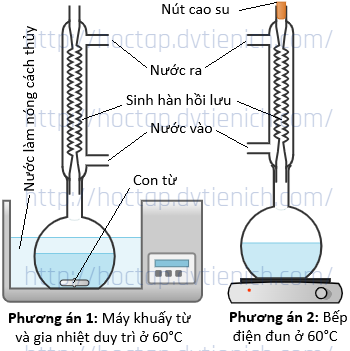
a) Viết phương trình hóa học của phản ứng và nêu hiện tượng quan sát được trong bình cầu khi ngừng khuấy, để yên hỗn hợp (khối lượng riêng của nitrobenzene là 1,2 g/cm³).
b) Sau phản ứng nitro hóa, hỗn hợp chất lỏng trong bình cầu gồm: nitrobenzene, benzene dư, các acid và nước. Biết CaCl2 khan có khả năng hút ẩm, nhiệt độ sôi của benzene là 80,1°C và của nitrobenzene là 210,9°C. Hãy trình bày các bước (sử dụng kỹ thuật chiết và chưng cất) tách loại tạp chất để thu được nitrobenzene.
c) Theo quy định an toàn, thí nghiệm này bắt buộc phải tiến hành trong tủ hút. Xác định các khí hoặc hơi độc hại thoát ra từ đầu ống sinh hàn hồi lưu trong quá trình đun nóng và giải thích nguồn gốc sinh ra chúng.
d) Một học sinh đề xuất tiến hành thí nghiệm theo phương án 2 như hình vẽ vì cho rằng:
– Không cần con từ khuấy hỗn hợp cho nên thay máy khuấy từ bằng bếp điện.
– Để ngăn khí độc thoát ra ngoài thì đậy kín đầu trên của ống sinh hàn hồi lưu.
Hãy đánh giá tính khả thi và dự báo những rủi ro có thể xảy ra khi tiến hành theo phương án này. Giải thích.


Bình luận