[2026] Thi thử TN sở GDĐT Bắc Ninh (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 132
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2C | 3A | 4C | 5C | 6C | 7A | 8C | 9D |
| 10A | 11A | 12B | 13C | 14D | 15C | 16D | 17D | 18D |
| 19 | 20 | 21 | 22 | |
| (a) | S | S | S | Đ |
| (b) | S | S | Đ | Đ |
| (c) | Đ | S | S | Đ |
| (d) | S | Đ | Đ | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 24 | 186 | 45 | 16,2 | 124 | 6,82 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Dung dịch chất nào sau đây làm quỳ tím chuyển sang màu đỏ?
A. Glycine. B. Glutamic acid. C. Lysine. D. Alanine.
(Xem giải) Câu 2. eMethanol (một loại nhiên liệu điện tử – eFuel) là một loại nhiên liệu lỏng tái tạo, có mật độ năng lượng cao, có cấu trúc hóa học giống với methanol thông thường, nhưng được sản xuất mà không cần nguyên liệu hóa thạch. Trong công nghiệp, eMethanol được sản xuất từ hydrogen (H2) và carbon dioxide (CO2) theo phản ứng:
CO2(g) + 3H2(g) ⇋ CH3OH(g) + H2O(g) ![]() = – 49,5 kJ
= – 49,5 kJ
Phát biểu nào sau đây không đúng?
A. Tách methanol ra khỏi hệ làm cân bằng chuyển dịch theo chiều thuận.
B. Sử dụng chất xúc tác phù hợp giúp phản ứng nhanh đạt tới trạng thái cân bằng.
C. Để đạt hiệu suất cao nhất, nên thực hiện phản ứng ở nhiệt độ thường và áp suất thấp.
D. Giảm áp suất của hệ phản ứng làm giảm hiệu suất tổng hợp methanol.
(Xem giải) Câu 3. Cho các chất sau:

Số chất phản ứng được với Na nhưng không phản ứng được với dung dịch NaOH là
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 4. PE là một loại chất dẻo, được dùng để sản xuất túi nylon, bao gói, màng bọc thực phẩm, chai lọ, đồ chơi trẻ em,… PE được tổng hợp trực tiếp từ monomer nào sau đây?
A. Vinyl chloride. B. Vinyl acetate. C. Ethylene. D. Propylene.
(Xem giải) Câu 5. Đối với động cơ xăng, để giảm bớt tác hại của khí thải tới môi trường, bên cạnh việc tăng hiệu quả đốt cháy, người ta còn sử dụng bộ chuyển đổi xúc tác giúp chuyển hóa các chất ô nhiễm, chất độc hại trong khí thải thành những chất ít gây hại hơn. Một phản ứng chuyển hoá xảy ra trong bộ chuyển đổi xúc tác như sau:
2CO(g) + 2NO(g) → 2CO2(g) + N2(g) (1)
Cho enthlpy tạo thành chuẩn (đơn vị kJ/mol) của CO(g), NO(g), CO2(g) lần lượt là -110,5; 91,3 và -393,5. Phản ứng (1) là phản ứng
A. thu nhiệt, hấp thụ 374,3 kJ. B. thu nhiệt, hấp thụ 748,6 kJ.
C. tỏa nhiệt, giải phóng 748,6 kJ. D. tỏa nhiệt, giải phóng 374,3 kJ.
(Xem giải) Câu 6. Trong cơ thể người, ion Mg2+ (Z = 12) là một vi chất quan trọng, tham gia cấu trúc tế bào, tổng hợp protein, hoạt hoá enzyme điều chỉnh phản ứng sinh hoá,… Số hạt electron của ion Mg2+ là
A. 12. B. 24. C. 10. D. 14.
(Xem giải) Câu 7. Vôi đen (quặng dolomite nghiền nhỏ) được sử dụng để cải tạo ao trong nuôi trồng thủy sản, làm phân bón và làm phụ gia trong luyện kim. Thành phần chính của vôi đen là
A. CaCO3.MgCO3. B. CaO. C. 3Ca3(PO4)2.CaF2. D. CaSO4.2H2O.
(Xem giải) Câu 8. Số nhóm hydroxy (-OH) có trong mỗi đơn vị β-glucose của cellulose là
A. 4. B. 6. C. 3. D. 5.
(Xem giải) Câu 9. Sodium hydrogencarbonate (NaHCO3) được sử dụng phổ biến trong sản xuất công nghiệp, phụ gia thực phẩm và y học. Cho độ tan (g/100 gam nước) của NaHCO3 ở các nhiệt độ như sau:
| Nhiệt độ, °C | 10 | 20 | 30 | 40 | 60 | |
| Độ tan | 7,0 | 8,1 | 9,6 | 11,1 | 12,7 | 16,0 |
Cho các phát biểu sau:
(a) Khi tăng nhiệt độ từ 0°C lên 60°C, độ tan của NaHCO3 tăng.
(b) Ở 20°C, nồng độ NaHCO3 trong dung dịch bão hoà là x%. Giá trị của x là 9,6. (Kết quả làm tròn đến hàng phần trăm)
(c) Trong thực tế, có thể dựa vào sự thay đổi độ tan theo nhiệt độ để tinh chế NaHCO3.
(d) NaHCO3 được sử dụng làm bột nở, bột chữa cháy, sản xuất viên sủi.
(đ) Khi cho NaHCO3 tác dụng với dung dịch HCl hoặc dung dịch NaOH đều tạo ra khí CO2.
Số phát biểu đúng là
A. 4. B. 2. C. 5. D. 3.
(Xem giải) Câu 10. Khi sử dụng xà phòng có thành phần chính là sodium palmitate trong nước cứng, hiệu quả giặt rửa bị giảm đáng kể do tạo thành các kết tủa. Một trong những chất kết tủa đó là
A. (C15H31COO)2Ca. B. C15H31COONa. C. C17H35COONa. D. (CH3COO)2Mg.
(Xem giải) Câu 11. Cho phản ứng sau:
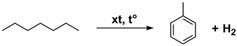
Phản ứng trên thuộc loại phản ứng nào sau đây?
A. Reforming. B. Cracking. C. Thế. D. Cộng.
(Xem giải) Câu 12. Để làm mềm nước cứng, người ta thường dẫn nước cứng qua cột có chứa nhựa cationite, khi đó các ion Ca2+, Mg2+ trong nước sẽ bị giữ lại, đồng thời các cation như Na+, H+ được giải phóng từ cột vào nước. Phương pháp làm mềm nước cứng này được gọi là
A. phương pháp chưng cất. B. phương pháp trao đổi ion.
C. phương pháp sắc kí cột. D. phương pháp kết tủa.
(Xem giải) Câu 13. Cho các cặp oxi hóa – khử của các kim loại và thế điện cực chuẩn tương ứng:
| Cặp oxi hóa – khử | Li+/Li | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Ag+/Ag |
| Thế điện cực chuẩn (V) | –3,040 | –0,762 | –0,440 | +0,340 | +0,799 |
Sức điện động chuẩn của pin điện hoá nào sau đây có giá trị là 0,78 V?
A. Zn – Cu. B. Li – Ag. C. Fe – Cu. D. Fe – Ag.
(Xem giải) Câu 14. Cho peptite X có công thức như sau:

Phát biểu nào sau đây đúng?
A. X phản ứng với Cu(OH)2 trong NaOH ở nhiệt độ thường tạo dung dịch màu xanh lam.
B. Amino acid đầu N của X là glycine.
C. Khi đun X với dung dịch NaOH dư, 1 mol X phản ứng tối đa với 7 mol NaOH.
D. X là Ala-Glu-Gly-Ala-Lys-Glu.
(Xem giải) Câu 15. Khi pha trà, người ta sử dụng trà khô (hoặc tươi) ngâm trong nước nóng để các dưỡng chất, chất có hương vị, màu sắc từ trà tan vào nước. Phương pháp tách các chất từ trà vào nước thuộc loại phương pháp nào sau đây?
A. Chiết lỏng – lỏng. B. Chưng cất. C. Chiết lỏng – rắn. D. Kết tinh.
(Xem giải) Câu 16. Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất, được dùng để chế tạo dây tóc bóng đèn sợi đốt?
A. Fe. B. Cr. C. Ag. D. W.
(Xem giải) Dữ liệu sử dụng cho các câu từ 17 đến câu 18
Phức chất [Fe(CN)6]3- có thể được điều chế từ [Fe(CN)6]4- theo phản ứng:
2[Fe(CN)6]4- + Cl2 → 2[Fe(CN)6]3- + 2Cl- (∗)
(X) (Y)
Câu 17. Phát biểu nào sau đây không đúng?
A. Nguyên tử trung tâm của X, Y lần lượt là Fe2+, Fe3+.
B. X và Y có cùng phân tử khối.
C. Phối tử của X, Y đều là CN-.
D. Phản ứng (∗) là phản ứng thế phối tử.
Câu 18. Dạng hình học của các phức chất [Fe(CN)6]4-, [Fe(CN)6]3- lần lượt là
A. bát diện và vuông phẳng. B. vuông phẳng và tứ diện.
C. bát diện và tứ diện. D. bát diện và bát diện.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Các công trình bằng thép (hợp kim của Fe và C) dễ bị ăn mòn điện hóa khi tiếp xúc với nước biển. Một trong số các phương pháp bảo vệ các công trình bằng thép khỏi sự ăn mòn điện hóa là gắn các khối nhôm (aluminium, Al), kẽm (zinc, Zn) hoặc hợp kim của chúng vào phần chìm dưới nước biển của công trình đó.
a) Trong thực tế, để đạt hiệu quả bảo vệ các công trình bằng thép cao hơn người ta thường phủ lên bề mặt thép một lớp kim loại kém hoạt động như Ag, Au,…
b) Thép bị ăn mòn điện hóa mà không cần tiếp xúc với dung dịch chất điện li.
c) Khi thép bị ăn mòn điện hóa, sắt trong thép bị oxi hoá.
d) Khi bảo vệ thép theo phương pháp điện hóa, nhôm hoặc kẽm đóng vai trò là cathode nên bị ăn mòn trước.
(Xem giải) Câu 20. Tơ capron là polymer có tính dai, đàn hồi, ít thấm nước, mềm mại, giặt mau khô. Tơ capron được dùng để dệt vải may mặc, làm võng, lưới bắt cá, chỉ khâu, sợi dây thừng,… Một quy trình sản xuất tơ capron từ cyclohexanol theo sơ đồ sau:
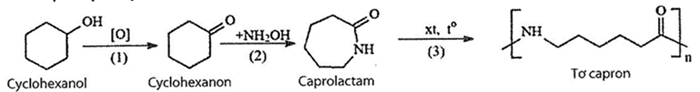
a) Theo quy trình trên, nếu dùng 1 tấn cyclohexanol với hiệu suất cả quá trình sản xuất là 80% thì thu được 0,94 tấn tơ capron. (Kết quả làm tròn đến hàng phần trăm)
b) Tơ capron thuộc loại polyester.
c) Trong giai đoạn (3), phản ứng chuyển hóa caprolactam thành tơ capron thuộc loại phản ứng trùng ngưng.
d) Trong mỗi mắt xích của tơ capron, phần trăm khối lượng nitrogen là x%. Giá trị của x là 12,4. (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 21. Pin nhiên liệu sử dụng ethanol (C2H5OH) được đặc biệt quan tâm do có nguồn nhiên liệu sinh học dồi dào, dễ vận chuyển và ít độc hại. Cấu tạo cơ bản của pin ethanol – oxygen gồm hai điện cực ngăn cách bởi màng trao đổi proton (PEM), màng này chỉ cho ion H+ đi qua.
Tại cực (-): C2H5OH bị oxi hóa và kết hợp với H2O tạo thành khí CO2, ion H+.
Tại cực (+): O2 bị khử và kết hợp với ion H+ tạo thành H2O.
Phản ứng chung trong pin ethanol – oxygen: C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l) (∗)
Một pin ethanol – oxygen phóng điện trong điều kiện chuẩn được dùng để thắp sáng một bóng đèn LED có công suất 5 W (1 W = 1 J/s). Giả thiết 70% lượng nhiệt sinh ra từ phản ứng được chuyển hoá thành điện năng. Cho biết nhiệt tạo thành chuẩn của các chất:
| Chất | C2H5OH(l) | CO2(g) | H2O(l) |
| -277,6 | -393,5 | -285,8 |
a) Tại anode xảy ra quá trình O2 + 4H+ + 4e → 2H2O.
b) Biến thiên enthalpy chuẩn của phản ứng (∗) là -x kJ. Giá trị của x là 1366,8. (Kết quả làm tròn đến hàng phần mười)
c) Các electron di chuyển từ cực (+) sang cực (-) qua dây dẫn.
d) Nếu pin tiêu thụ hết 2,3 gam ethanol có thể thắp sáng bóng đèn LED trên liên tục trong 2,7 giờ. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười)
(Xem giải) Câu 22. Trong phòng thí nghiệm, aniline (C6H5NH2) được điều chế từ nitrobenzene (C6H5NO2) theo sơ đồ:

Trong một thí nghiệm, sử dụng 6,15 gam nitrobenzene để điều chế aniline theo sơ đồ trên, thu được 3,72 gam aniline tinh khiết. Cho biết số sóng hấp thụ đặc trưng của một số nhóm chức trên phổ hồng ngoại như sau:
| Nhóm chức | –NO2 (nitro) | –NH2 (amine bậc 1) | C=C (vòng thơm) | C–N (amine) |
| Số sóng (cm-1) | 1550 – 1350 | 3500 – 3300 | 1600 – 1450 | 1360 – 1180 |
a) Dựa vào phổ hồng ngoại, phân biệt được nitrobenzene và aniline.
b) Để tách aniline ra khỏi hỗn hợp sau phản ứng (2) có thể dùng phương pháp chiết.
c) Trong phản ứng (1) nitrobenzene đóng vai trò là chất oxi hóa.
d) Hiệu suất của quá trình tổng hợp aniline trong thí nghiệm trên đạt x%. Giá trị của x là 75,6. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị)
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Một mẫu NaOH bị ẩm (chứa NaOH và H2O). Để xác định hàm lượng NaOH trong mẫu trên, một nhóm học sinh tiến hành như sau:
• Bước 1: Hòa tan 2,6 gam mẫu NaOH trên bằng nước cất trong cốc thủy tinh (loại 100 mL), rồi rót vào bình định mức 500 mL. Tráng cẩn thận cốc (vừa pha mẫu) nhiều lần bằng nước cất và chuyển hết nước tráng cốc vào bình định mức. Tiếp tục thêm nước cất vào bình định mức đến vạch và lắc đều, thu được dung dịch X.
• Bước 2: Dùng dung dịch X để tráng burette (loại 25 mL), sau đó rót đầy dung dịch X vào burette và điều chỉnh thể tích dung dịch trong burette về mức 0 (trong burette không còn bọt khí).
• Bước 3: Lấy 10 mL dung dịch HCl 0,06 M cho vào bình tam giác (loại 100 mL), thêm 2 giọt phenolphtalein rồi thực hiện chuẩn độ dung dịch X. Thể tích dung dịch X trung bình sau 3 lần chuẩn độ là 4,8 mL.
Cho các phát biểu sau:
(1) Trong thí nghiệm trên, tại điểm kết thúc chuẩn độ, dung dịch trong bình tam giác chuyển từ màu hồng sang không màu.
(2) Nồng độ của NaOH trong dung dịch X xác định được từ thí nghiệm là 0,125 mol/L. (Kết quả làm tròn đến hàng phần nghìn)
(3) Ở bước 1, nếu không chuyển hết nước tráng cốc (dùng pha mẫu) vào bình định mức thì thể tích dung dịch X trung bình sau 3 lần chuẩn độ ở bước 3 sẽ nhỏ hơn 4,8 mL.
(4) Phần trăm khối lượng của NaOH trong 2,6 gam mẫu ban đầu là x%. Giá trị của x là 96,2. (Kết quả làm tròn đến hàng phần mười)
Các phát biểu đúng gồm những phát biểu nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 12; 134;…)
(Xem giải) Câu 24. Tyrosine (Tyr) là một amino acid tiêu chuẩn, có nhiều vai trò quan trọng đối với cơ thể. Công thức của Tyrosine như hình sau:
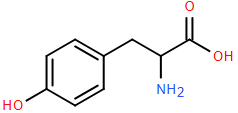
– Trong phân tử tyrosine có x loại nhóm chức.
– 1 mol tyrosine có thể phản ứng tối đa với y mol KOH trong dung dịch.
– Khối lượng phân tử của tyrosine là z amu.
Giá trị của tổng (x + y + z) bằng bao nhiêu?
(Xem giải) Câu 25. Vàng (gold) đơn chất tồn tại trong tự nhiên ở trong quặng vàng thường có hàm lượng vàng thấp. Để thu hồi vàng từ quặng vàng, người ta nghiền quặng, hòa tan chúng vào dung dịch KCN và liên tục sục không khí vào. Vàng bị hòa tan tạo thành phức chất:
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (∗)
Dùng bột kẽm (zinc) đẩy vàng ra khỏi hợp chất:
Zn(s) + 2K[Au(CN)2](aq) → K2[Zn(CN)4](aq) + 2Au(s) (∗∗)
Cho các phát biểu sau:
(1) Phương pháp tách vàng như trên thuộc phương pháp nhiệt luyện.
(2) Trong phản ứng (∗), KCN là chất bị oxi hóa.
(3) Để phản ứng (∗∗) đạt hiệu quả cao hơn người ta thường dùng kim loại sodium thay kim loại zinc.
(4) Bằng phương pháp trên, nếu dùng 10,4 gam KCN (giả thiết các chất khác trong quặng không phản ứng với KCN) với hiệu suất quá trình tách đạt 100% thì thu được 15,76 gam vàng. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)
(5) Để loại bỏ kẽm lẫn trong bột vàng, có thể dùng dung dịch HCl.
Các phát biểu đúng gồm những phát biểu nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 12; 234;…)
(Xem giải) Câu 26. Oleum Z (H2SO4.nSO3) được tạo thành khi cho 50 kg dung dịch H2SO4 98% hấp thụ hoàn toàn 15 kg SO3. Phần trăm khối lượng SO3 trong Z là x%. Xác định giá trị của x. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười)
(Xem giải) Câu 27. Biodiesel (diesel sinh học) là một loại nhiên liệu lỏng, thân thiện với môi trường hơn so với diesel truyền thống. Biodiesel được sản xuất thông qua phản ứng giữa chất béo với các alcohol mạch ngắn (thường là methyl alcohol) với xúc tác là kiềm, thu được biodiesel (ester của acid béo) và glycerol. Một nhà máy sản xuất biodiesel từ dầu ăn đã qua sử dụng, phản ứng tạo thành biodiesel (dạng methyl ester) xảy ra như sau:
(RCOO)3C3H5 + 3CH3OH (NaOH) → 3RCOOCH3 + C3H5(OH)3 (1)
Cho các phát biểu sau:
(1) Phản ứng (1) thuộc loại phản ứng xà phòng hóa.
(2) Biodiesel thân thiện với môi trường vì khi cháy hoàn toàn không tạo ra khí gây hiệu ứng nhà kính.
(3) Phương pháp sản xuất biodiesel trên giúp tận dụng dầu ăn đã qua sử dụng, góp phần giảm ô nhiễm môi trường do dầu ăn thải gây ra.
(4) Bằng phương pháp trên, nếu dùng 500 kg một loại dầu ăn đã qua sử dụng chứa 85% chất béo (phân tử khối trung bình của chất béo là 860, các tạp chất không có khả năng chuyển hóa thành biodiesel) với hiệu suất của quá trình sản xuất là 90% thì thu được 427 kg biodiesel.(Kết quả làm tròn đến hàng đơn vị)
Các phát biểu không đúng gồm những phát biểu nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 12; 234;…)
(Xem giải) Câu 28. Thực hiện các phản ứng ester hóa giữa glycerol với acetic acid (xúc tác H2SO4 đặc, đun nóng) theo sơ đồ sau:
![]()
Phần trăm khối lượng của hydrogen trong Y là x%. Giá trị của x bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)

Bình luận