[2026] Thi thử TN sở GDĐT Nghệ An (Lần 3)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 131
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2B | 3B | 4C | 5A | 6B | 7B | 8B | 9C |
| 10A | 11B | 12A | 13C | 14D | 15C | 16A | 17B | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | S | S | Đ | S |
| (b) | Đ | Đ | S | Đ |
| (c) | S | S | Đ | S |
| (d) | Đ | Đ | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 2 | 51,7 | 8216 | 234 | 9,5 | 4132 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho thế điện cực chuẩn của Cu2+/Cu và Sn2+/Sn lần lượt là +0,34V và -0,14V. Khi pin Galvani Sn-Cu hoạt động, phản ứng hóa học xảy ra ở điều kiện chuẩn như sau: Sn + Cu2+ → Sn2+ + Cu. Nhận định nào sau đây không đúng?
A. Sn đóng vai trò cathode, còn Cu đóng vai trò anode.
B. Sức điện động chuẩn của pin bằng +0,48V.
C. Trong dung dịch nồng độ ion Cu2+ giảm, nồng độ ion Sn2+ tăng.
D. Khối lượng của điện cực Cu tăng, khối lượng điện cực Sn giảm.
(Xem giải) Câu 2. Cho các phát biểu sau về glycine:
(a) Glycine là hợp chất hữu cơ tạp chức.
(b) Glycine phản ứng được với methanol ở điều kiện thích hợp.
(c) Glycine phản ứng được với cả dung dịch NaOH và dung dịch HCl.
(d) Khi đặt trong điện trường, ở pH = 2 thì glycine di chuyển về cực dương.
Số phát biểu đúng là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 3. Vàng (Au, gold) có thể dát mỏng đến 0,0001 mm, giúp nó được ứng dụng rộng rãi trong chế tác trang sức tinh xảo, kéo sợi, mạ vàng bề mặt (tranh sơn mài, kiến trúc). Ứng dụng này dựa trên tính chất vật lý nào của kim loại Au?
A. Nhiệt độ nóng chảy cao. B. Tính dẻo.
C. Khả năng dẫn nhiệt tốt. D. Khối lượng riêng nhỏ.
(Xem giải) Câu 4. Chất nào sau đây được sử dụng để khử trùng nước sinh hoạt?
A. N2. B. Br2. C. Cl2. D. CO2.
(Xem giải) Câu 5. Dấu hiệu nhận biết của hiện tượng phú dưỡng là
A. Tảo phát triển dày đặc, nước có màu xanh đục. B. Nước trong suốt, không màu.
C. Nước có nhiệt độ thấp. D. Nước có mùi thơm.
(Xem giải) Câu 6. Số đồng phân amine có công thức phân tử C2H7N là
A. 4. B. 2. C. 3. D. 1.
(Xem giải) Câu 7. Cho các phương trình hóa học sau:
(1) CuO(s) + CO(g) → Cu(s) + CO2(g).
(2) 2CuSO4(aq) + 2H2O(l) → 2Cu(s) + O2(g) + 2H2SO4(aq).
(3) Fe(s) + CuSO4(aq) → FeSO4(aq) + Cu(s).
(4) ZnO(s) + C(s) → CO(g) + Zn(s).
Số phương trình hoá học dùng để tách kim loại bằng phương pháp thuỷ luyện là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 8. Hiện tượng nào sau đây xảy ra sự ăn mòn kim loại?
A. Công trình bằng đá bị ăn mòn bởi mưa acid. B. Ống thép bị gỉ.
C. Nước cứng tạm thời tạo kết tủa khi đun nóng. D. Sự tạo thành thạch nhũ trong hang động.
(Xem giải) Câu 9. Để khử chua cho đất nhiễm phèn người ta thường dùng
A. NH4NO3. B. NaCl. C. Ca(OH)2. D. CuSO4.
(Xem giải) Câu 10. Chỉ số octane là một đại lượng quy ước để đặc trưng cho khả năng chống kích nổ của nhiên liệu. Chỉ số octane của isooctane (2,2,4-trimethylpentane) được quy ước là 100, một số hydrocarbon và alcohol khi pha trộn với xăng có chỉ số octane được cho trong bảng sau:
| Chất | Methanol | Ethanol | Cyclohexane | Isopentane | Toluene |
| Chỉ số octane | 127 – 136 | 120 – 135 | 83 | 92,3 | 115 |
Số chất trong bảng có chỉ số octane thấp hơn isooctane là
A. 2. B. 5. C. 3. D. 4.
(Xem giải) Câu 11. Hợp chất HCOOC2H5 có mùi thơm của quả đào. Tên gọi của hợp chất này là
A. methyl propionate. B. ethyl formate. C. ethyl acrylate. D. ethyl acetate.
(Xem giải) Câu 12. Protein là hợp chất cao phân tử được hình thành từ một hay nhiều chuỗi
A. polypeptide. B. polyester. C. polysaccharide. D. amylose.
(Xem giải) Câu 13. Phosphorus (P) dùng sản xuất bom, đạn cháy, đạn khói, diêm, điều chế H3PO4,… Ở trạng thái cơ bản cấu hình electron của nguyên tử P (số hiệu nguyên tử bằng 15) là
A. 1s22s22p63s23p2. B. 1s22s22p63s13p4.
C. 1s22s22p63s23p3. D. 1s22s22p63s33p2.
(Xem giải) Câu 14. Toluene được điều chế từ heptane theo phương trình hóa học C7H16 (xt, t°) → C7H8 + 4H2. Phản ứng trên là phản ứng
A. cracking. B. thế. C. thủy phân. D. reforming.
(Xem giải) Câu 15. Carbohydrate nào sau đây tạo với iodine hợp chất màu xanh tím?
A. Glucose. B. Saccharose. C. Tinh bột. D. Cellulose.
(Xem giải) Câu 16. Ở điều kiện thường, kim loại nào sau đây tan hoàn toàn trong nước dư?
A. Na. B. Cu. C. Be. D. Fe.
(Xem giải) Sử dụng thông tin dưới đây để trả lời cho câu 17-18:
Trong công nghiệp hiện nay, để hạn chế chất thải ra môi trường và làm tăng hiệu suất của quá trình sản xuất poly(vinyl chloride) (PVC) từ ethylene, người ta thực hiện quy trình sản xuất khép kín ứng với phản ứng (1), (2), (3), (4) theo sơ đồ sau:

PVC sau khi trùng hợp được làm mát, ly tâm tách nước và sấy khô thành bột PVC thành phẩm.
Câu 17. Cho các phát biểu sau:
(a) Phản ứng (1) là phản ứng cộng.
(b) Trong phản ứng (3), HCl bị khử thành Cl2.
(c) Sản phẩm phản ứng (1) có tên thay thế là 1,2-dichloroethane.
(d) Phản ứng (4) là phản ứng trùng hợp.
Số phát biểu đúng là
A. 4. B. 3. C. 1. D. 2.
Câu 18. Để sản xuất 1 tấn PVC theo quy trình trên cần m kg ethylene. Biết hiệu suất toàn bộ quá trình tổng hợp PVC từ ethylene là 95%. Giá trị m là
A. 479,15. B. 471,58. C. 425,60. D. 448,00.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Ethyl acetate là một ester được sử dụng làm dung môi để tách, chiết chất hữu cơ. Một học sinh tiến hành tổng hợp ethyl acetate từ acetic acid và ethanol theo phương trình hóa học sau:
CH3COOH + C2H5OH (H2SO4 đặc, t°) ⇋ CH3COOC2H5 + H2O (∗)
Sau thí nghiệm, tách các hợp chất hữu cơ từ hỗn hợp thu được ra khỏi nhau rồi tiến hành đo phổ hồng ngoại của từng chất. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O–H (alcohol) | O–H (carboxylic acid) | C=O (ester, carboxylic acid) |
| Số sóng (cm⁻¹) | 3650 – 3200 | 3300 – 2500 | 1780 – 1650 |
a) Để tăng hiệu suất phản ứng tổng hợp ethyl acetate, người ta thay H2SO4 đặc bằng H2SO4 loãng.
b) Bằng phương pháp chiết có thể tách ethyl acetate ra khỏi hỗn hợp sau phản ứng.
c) Trên phổ hồng ngoại của ethyl acetate, tín hiệu (peak) ở 3350 cm⁻¹ đặc trưng cho liên kết C=O.
d) Ở phản ứng (∗), H2O được tạo thành từ nhóm -OH trong nhóm -COOH của acetic acid và nguyên tử H trong nhóm -OH của ethanol.
(Xem giải) Câu 20. Một nhóm học sinh được giao cho 1 L mẫu nước cứng X có chứa các ion với nồng độ như sau: [Ca2+] = 2E-3 M; [Mg2+] = 2E-3 M; [HCO3-] = 5E-3 M; còn lại là ion Cl-, với nhiệm vụ nghiên cứu làm mềm mẫu cứng nước trên. Nhóm học sinh nêu giả thuyết: “Khi đun sôi mẫu nước X thì mẫu nước mất hoàn toàn tính cứng”. Để kiểm chứng giả thuyết, nhóm học sinh thực hiện các thí nghiệm:
• Bước 1: Đun sôi 200 mL mẫu nước X thấy xuất hiện kết tủa trắng, lọc bỏ kết tủa, thu được dung dịch Y.
• Bước 2: Thêm dung dịch Na2CO3 dư vào dung dịch Y, lại thấy xuất hiện kết tủa trắng.
a) Mẫu nước X là nước có tính cứng vĩnh cửu.
b) Thí nghiệm mà nhóm học sinh tiến hành phù hợp với mục đích kiểm chứng giả thuyết trên.
c) Kết tủa thu được ở Bước 1 chỉ có CaCO3.
d) Kết quả của thí nghiệm không phù hợp giả thuyết của nhóm học sinh.
(Xem giải) Câu 21. Không khí ở các vùng có lò luyện cốc thường có lẫn các khí H2, NH3, H2S, CH4, CO. Trong đó CO là một khí rất độc, cần được kiểm soát chặt chẽ. Để xác định hàm lượng khí độc CO trong không khí ở các vùng có lò luyện cốc người ta tiến hành như sau: Lấy 30 lít không khí, loại bỏ các khí H2, NH3, H2S, CH4 rồi dẫn toàn bộ mẫu khí còn lại đi từ từ qua thiết bị có ống đựng lượng dư I2O5 được đốt nóng để oxi hóa toàn bộ lượng CO có trong mẫu thành CO2 và I2, lượng I2 thành hơi và được hấp thụ hết vào bình đựng lượng dư dung dịch KI tạo ra KI3. Chuẩn độ KI3 bằng dung dịch chuẩn Na2S2O3 0,002 M thì thể dung dịch chuẩn Na2S2O3 đã sử dụng là 12,2 mL. Các phản ứng xảy ra theo phương trình hóa học sau:
(1) 5CO + I2O5 → I2 + 5CO2
(2) KI + I2 → KI3
(3) KI3 + 2Na2S2O32 → KI + 2NaI + Na2S4O6
Biết rằng các phản ứng xảy ra hoàn toàn, sau khi loại bỏ H2, NH3, H2S, CH4, phần khí còn lại chỉ có CO tác dụng được với I2O5.
a) Các phản ứng (1), (3) là phản ứng oxi hóa – khử.
b) Biết các khí NH3, H2S tác dụng với I2O5 tạo ra I2, nếu tiến hành phân tích trực tiếp 30 lít mẫu không khí trên thì thể tích Na2S2O3 0,002 M cần dùng bé hơn 12,2 mL.
c) Nếu trong quá trình đun nóng, I2 sinh ra không được dẫn ngay vào dung dịch KI mà bị thất thoát một phần thì kết quả xác định CO sẽ thấp hơn thực tế.
d) Nồng độ CO trong mẫu không khí trên là 0,057 (mg/L). (kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn).
(Xem giải) Câu 22. Dầu thô là một hỗn hợp phức tạp, chủ yếu gồm các hydrocarbon và một lượng nhỏ các hợp chất chứa các nguyên tố sulfur, nitrogen, oxygen. Dựa vào hàm lượng sulfur, dầu thô được phân loại như sau:
– Dầu “ngọt”: hàm lượng sulfur < 0,5% khối lượng.
– Dầu “chua”: hàm lượng sulfur > 2,0% khối lượng.
Trong công nghiệp, dầu thô được chế biến bằng phương pháp chưng cất phân đoạn để thu các sản phẩm khác nhau. Khoảng nhiệt độ sôi của một số sản phẩm chưng cất phân đoạn ở áp suất thường như sau:
| Sản phẩm | Xăng | Dầu hỏa | Dầu diesel | Dầu đốt |
| Khoảng nhiệt độ sôi (°C) | 38 – 205 | 180 – 260 | 200 – 350 | ∼ 600 |
Một nhà máy khi chưng cất 500 tấn dầu thô thì có 15% khối lượng dầu thô chuyển thành xăng và 60% khối lượng dầu thô chuyển thành dầu đốt. Toàn bộ lượng dầu đốt này tiếp tục được xử lí bằng quá trình cracking thì thu được lượng xăng có khối lượng bằng 50% khối lượng dầu đốt. Tổng khối lượng xăng thu được sau hai giai đoạn trên là m tấn.
a) Trong quá trình chưng cất, sản phẩm xăng khó bay hơi hơn sản phẩm dầu diesel.
b) Giá trị của m là 225.
c) Kết quả phân tích 11,5 mL một mẫu dầu thô (khối lượng riêng là 0,87 g/mL) thu được 3,6 mg sulfur. Mẫu dầu thô này thuộc loại dầu “chua”.
d) Trong chế biến dầu mỏ, người ta thực hiện quá trình cracking để chuyển đổi dầu đốt thành các sản phẩm như xăng, dầu diesel.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Trong số các chất: methanal, ethanal, propanone, propanal, có bao nhiêu chất phản ứng với I2 trong dung dịch NaOH tạo iodoform?
(Xem giải) Câu 24. Phương pháp chuẩn độ permanganate dùng để xác định hàm lượng FeSO4 trong một loại phèn iron(II) sulfate heptahydrate kĩ thuật được tiến hành theo các bước sau:
• Bước 1: Cân 5,0 gam phèn iron(II) sulfate heptahydrate kĩ thuật (FeSO4.7H2O và tạp chất trơ) cho vào bình định mức 100 mL, thêm tiếp 15 mL dung dịch H2SO4 2 M sau đó thêm nước cất đồng thời lắc đều đến vạch 100 mL thu được dung dịch X.
• Bước 2: Lấy 10 mL dung dịch X đem chuẩn độ bằng dung dịch chuẩn KMnO4 0,02 M đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây). Thể tích dung dịch KMnO4 trung bình của ba lần chuẩn độ là 17,0 mL.
Từ kết quả thực nghiệm ở trên tính được hàm lượng FeSO4 trong phèn iron(II) sulfate heptahydrate kĩ thuật là bao nhiêu phần trăm? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
(Xem giải) Câu 25. Trong nước thải của một nhà máy, hàm lượng ion NH4+ là 510 mg/L. Trước khi thải ra môi trường nhà máy phải xử lí lượng ion NH4+ để đạt tiêu chuẩn theo quy chuẩn quốc gia về nước thải công nghiệp (QCVN40:2025/BTNMT) là không quá 10 mg/L (tính theo hàm lượng nguyên tố N). Quá trình xử lí nước thải theo công nghệ Sharon kết hợp Anammox gồm 2 giai đoạn:
• Giai đoạn 1: Sục không khí (oxygen chiếm 21% về thể tích) vào bể thứ nhất chứa nước thải cần xử lí, vi khuẩn AOB và NaHCO3 dư để duy trì pH dung dịch bằng 7 – 8. Khi đó chỉ có 25% oxygen sục vào bể oxi hóa một phần ion NH4+ theo phản ứng sau:
2NH4+ + 3O2 + 4HCO3- → 2NO2- + 4CO2 + 6H2O
• Giai đoạn 2: Chuyển toàn bộ dung dịch thu được sau giai đoạn 1 sang bể thứ hai trong điều kiện không cung cấp oxygen và có vi khuẩn khử nitrogen để tiếp tục khử hoàn toàn ion NO2- theo phản ứng:
NH4+ + NO2- → N2 + 2H2O
Để xử lí 840 m³ nước thải của nhà máy trên đạt tiêu chuẩn thải ra môi trường thì ở giai đoạn 1 cần sục tối thiểu bao nhiêu m³ không khí (quy về điều kiện chuẩn)? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Phức chất X được dùng làm thuốc chữa bệnh ung thư với tên gọi thương phẩm là cisplatin có cấu trúc gồm nguyên tử trung tâm và các phối tử đều nằm trên cùng một mặt phẳng như hình sau:
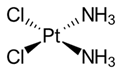
Cho các phát biểu về phức chất X:
(1) Dạng hình học của phức chất X là tứ diện.
(2) Phức chất X được tạo từ hai loại phối tử.
(3) Nguyên tử trung tâm của phức chất X là cation Pt2+.
(4) Trong phức chất X có 4 liên kết cho-nhận.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.
(Xem giải) Câu 27. Một loại chất béo có thành phần % về khối lượng các chất như sau:
| Thành phần | Tristearin | Stearic acid | Tạp chất |
| % khối lượng | 88,68% | 1,5% | 9,82% |
(cho biết trong quá trình sản xuất tạp chất không tạo ra muối của acid béo)
Một nhà máy cần sản xuất 120000 bánh xà phòng loại 100 gam/bánh (chứa 70% khối lượng muối sodium của acid béo, phần còn lại là chất độn, chất màu,…) bằng cách xà phòng hóa hoàn toàn m tấn chất béo nói trên với dung dịch NaOH dư. Biết rằng trong quá trình sản xuất lượng muối bị thất thoát 5%. Giá trị của m bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 28. Cho các phương trình phản ứng xảy ra được đánh số thứ tự từ (1) đến (4) dưới đây:
(1) C6H12O6 (enzyme) → 2CH3CH(OH)COOH
(2) CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH (t°) → CH2OH[CHOH]4COONH4 + 2Ag + 3NH3 + H2O
(3) [(C6H7O2(OH)3]n + 3nHNO3 (H2SO4 đặc, t°) → [C6H7O2(ONO2)3]n + 3nH2O
(4) C12H22O11 + H2O (H+) → C6H12O6 + C6H12O6
Hãy gán số thứ tự phương trình hoá học ở trên tương ứng với tên gọi: phản ứng thủy phân, phản ứng lên men, phản ứng với nitric acid, phản ứng với thuốc thử Tollens thành một dãy bốn số. (ví dụ: 1234, 4321,…)

Bình luận