Giải chi tiết 36 đề thầy Tào Mạnh Đức (01/36)
⇒ Đáp án và giải chi tiết:
| 1C | 2C | 3A | 4B | 5B | 6D | 7D | 8C | 9A | 10C |
| 11A | 12B | 13D | 14A | 15C | 16A | 17B | 18B | 19A | 20B |
| 21A | 22B | 23B | 24D | 25D | 26B | 27C | 28B | 29A | 30D |
| 31B | 32B | 33B | 34A | 35C | 36D | 37B | 38B | 39A | 40B |
Câu 1. Chất nào sau đây thuộc loại đisaccarit?
A. glucozơ B. amilozơ C. saccarozơ D. xenlulozơ
Câu 2. Dung dịch nào sau đây làm quì tím hóa xanh?
A. anilin B. alanin C. metanamin D. glyxin
Câu 3. Ở điều kiện thường, kim loại có độ cứng lớn nhất là.
A. Cr B. Fe C. Cu D. Al
Câu 4. Số oxi hóa của crom trong hợp chất K2Cr2O7 là?
A. +3 B. +6 C. +2 D. +4
Câu 5. Thủy phân hoàn toàn tristearin trong môi trường axit thu được?
A. C3H5(OH)3 và C17H33COOH B. C3H5(OH)3 và C17H35COOH
C. C3H5(OH)3 và C17H35COONa D. C3H5(OH)3 và C17H33COONa
Câu 6. Đốt cháy hoàn toàn este X thu được CO2 và H2O có tỉ lệ mol 1 : 1. Công thức tổng quát của X là.
A. CnH2n+1COOCmH2m+1 (n ≥ 1 ; m ≥ 1)
B. CnH2nO2 (n ≥ 1)
C. CnH2n+2O2( n ≥ 2)
D. CnH2n+1COOCmH2m+1 (n ≥ 0; m ≥ 1)
Câu 7. Chất nào sau đây không tạo kết tủa khi tác dụng với dung dịch Na3PO4?
A. CaCl2 B. Mg(HCO3)2 C. AgNO3 D. HCl
Câu 8. Nhận định nào sau đây là sai?
A. Nước cứng là nước chứa nhiều ion Mg2+ và Ca2+.
B. Nước tự nhiên thường có cả tính cứng tạm thời và tính cứng vĩnh cửu.
C. Phương pháp làm mềm tính cứng của nước cứng vĩnh cửu đơn giản nhất bằng cách đun nóng.
D. Dùng dung dịch Na3PO4 để làm mềm tính cứng của nước cứng tạm thời.
Câu 9. Xà phòng hóa hoàn toàn m gam tristearin bằng dung dịch KOH dư, thu được 115,92 gam muối. Giá trị của m là.
A. 106,80 gam B. 128,88 gam C. 106,08 gam D. 112,46 gam
⇒ Xem giải
Câu 10. Cho 26,46 gam axit glutamic tác dụng vừa đủ với V ml dung dịch NaOH 1M. Giá trị của V là.
A. 180 ml B. 240 ml C. 360 ml D. 480 ml
Câu 11. Nhúng thanh Zn tiếp xúc với thanh Cu vào dung dịch H2SO4 loãng, khi đó xảy ra quá trình ăn mòn điện hóa, đồng thời tạo thành dòng điện. Tại anot xảy ra quá trình:
A. Zn → Zn2+ + 2e
B. 2H2O → 2OH- + H2+ 2e.
C. 2H++ 2e → H2
D. Cu2+ + 2e → Cu
Câu 12. Cho dãy các kim loại: Na, Ca, Mg, Al, Cu. Số kim loại tác dụng với lượng dư dung dịch FeCl3, sau khi kết thúc phản ứng, thu được kết tủa là.
A. 3 B. 2 C. 5 D. 4
⇒ Xem giải
Câu 13. Cho 13,7 gam Ba vào 200 ml dung dịch Al2(SO4)3 0,2M, kết thúc thu được m gam kết tủa. Giá trị của m là.
A. 33,16 gam B. 29,54 gam C. 34,20 gam D. 28,50 gam
⇒ Xem giải
Câu 14. Thổi luồng khí CO đến dư qua ống sứ chứa m gam Fe3O4 nung nóng, kết thúc phản ứng, lấy phần rắn trong ống sứ cho vào dung dịch HCl loãng dư, thu được 4,032 lít khí H2 (đktc). Giá trị m là.
A. 13,92 gam B. 20,88 gam C. 6,96 gam D. 10,44 gam
⇒ Xem giải
Câu 15. Nhận định nào sau đây là sai?
A. Các este có khả năng hòa tan tốt các hợp chất hữu cơ, kể cả các hợp chất cao phân tử.
B. Các este thường là chất lỏng, nhẹ hơn nước, rất ít tan trong nước.
C. Chất béo rắn thành phần chủ yếu chứa các axit béo không no.
D. Chất béo lỏng để lâu ngày ngoài không khí sẽ bị ôi.
Câu 16. Tơ visco thuộc loại?
A. tơ nhân tạo B. tơ tổng hợp C. tơ thiên nhiên D. tơ poliamit
Câu 17. Phản ứng nào sau đây không tạo ra muối Fe (III)?
A. Fe2O3 tác dụng với dung dịch HCl loãng dư.
B. Cho bột Fe đến dư vào dung dịch AgNO3.
C. Fe tác dụng với dung dịch HNO3 đặc, nóng, dư.
D. Fe(OH)2 tác dụng với dung dịch HNO3 loãng, dư.
Câu 18. Phát biểu nào sau đây là sai?
A. Các kim loại kiềm đều mềm và có nhiệt độ nóng chảy thấp hơn so với các kim loại khác.
B. Các kim loại kiềm thổ có tính khử mạnh, khử được nước ngay ở điều kiện thường.
C. Nhôm là kim loại có màu trắng bạc, có tính dẫn điện, dẫn nhiệt tốt.
D. Trong vỏ trái đất, sắt đứng hàng thứ tư trong các nguyên tố, hàng thứ hai trong các kim loại.
Câu 19. Cho dãy các chất: metyl fomat, glucozơ, saccarozơ, alanin, triolein, metyl acrylat, tripanmitin, glyxin. Số chất trong dãy làm mất màu dung dịch Br2 là.
A. 4 B. 3 C. 5 D. 2
Câu 20. Phản ứng nào sau đây là sai?
A. H2N-CH2-COOH + CH3OH → H2N-CH2-COOCH3 + H2O
B. C12H22O11 (saccarozơ) + H2O → 2C6H12O6 (glucozơ)
C. CH3-NH3Cl + NaOH → NaCl + CH3-NH2 + H2O
D. CH3COOCH=CH2+ NaOH → CH3COONa + CH3CHO
Câu 21. Hòa tan hết 56,72 gam hỗn hợp gồm Ba, BaO, Al và Al2O3 trong lượng nước dư, thu được V lít khí H2 (đktc) và dung dịch X chỉ chứa một chất tan duy nhất. Sục khí CO2 đến dư vào X, thu được 37,44 gam kết tủa. Giá trị của V là.
A. 6,272 lít B. 6,720 lít C. 7,168 lít D. 4,928 lít
⇒ Xem giải
Câu 22. Nung nóng hỗn hợp gồm Al và Fe3O4 (tỉ lệ mol 1 : 1) trong điều kiện không có không khí, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Rắn X chứa?
A. Al2O3 và Fe B. Al2O3, Fe3O4, Fe
C. Al2O3, Al, Fe D. Al2O3, Fe3O4, Al, Fe
Câu 23. Glucozơ thể hiện tính oxi hóa trong phản ứng nào sau đây?
A. CH2OH-[CH2OH]4-CHO + 2AgNO3 + 3NH3+ H2O → HOCH2-[CH2OH]4-COONH4 + 2NH4NO3 + 2Ag
B. CH2OH-[CH2OH]4-CHO + H20 → CH2OH-[CH2OH]4-CH2OH
C. CH2OH-[CH2OH]4-CHO + Br2+ H2O → CH2OH-[CH2OH]4-COOH + 2HBr
D. 2C6H12O6+ Cu(OH)2 → (C6H11O6)2 + 2H2O
Câu 24. Lên men m gam glucozơ thu được ancol etylic và khí CO2 (hiệu suất phản ứng đạt 80%). Hấp thu toàn bộ khí CO2 sinh ra vào dung dịch Ca(OH)2, thu được 16,0 gam kết tủa; đồng thời thu được dung dịch có khối lượng giảm 5,44 gam so với dung dịch ban đầu. Giá trị của m là.
A. 21,6 gam B. 54,0 gam C. 43,2 gam D. 27,0 gam
⇒ Xem giải
Câu 25. Hợp chất hữu cơ X có công thức phân tử C5H11O2N. Đun nóng 17,55 gam X với dung dịch KOH vừa đủ, cô cạn dung dịch sau phản ứng, thu được 19,05 gam muối của α-amino axit. Công thức cấu tạo của X là.
A. H2N-CH2-CH2-COOC2H5. B. (CH3)2-CH-CH(NH2)-COOH.
C. CH3-CH-CH(NH2)-COOCH3. D. CH3-CH(NH2)-COOC2H5
⇒ Xem giải
Câu 26. Cho sơ đồ phản ứng sau:
(1) 2X + 2Y + 2H2O → 2Z + 3H2 (2) Z + CO2+ H2O → T + KHCO3
(3) 2X + 3Cl2 → 2XCl3 (4) 2X + 6HCl → 2XCl3 + 3H2
Các chất X, Y, Z, T lần lượt là.
A. Cr2O3, NaOH, NaCrO2, Cr(OH)3 B. Al, KOH, KAlO2, Al(OH)3.
C. Al, NaOH, NaAlO2, Al(OH)3 D. Cr2O3, KOH, KCrO2, Cr(OH)3
Câu 27. Este X mạch hở, không tồn tại đồng phân hình học và có công thức phân tử C6H8O4. Đun nóng 1 mol X với dung dịch NaOH dư, thu được muối Y và 2 mol ancol Z. Biết Z không tác dụng với Cu(OH)2 ở điều kiện thường, khi đun Y với H2SO4 đặc ở 170°C không tạo ra anken. Nhận định nào sau đây là đúng?
A. X có mạch cacbon không phân nhánh.
B. Chất Y có công thức phân tử là C4H4O4Na2.
C. Trong X chứa hai nhóm -CH3.
D. Chất X phản ứng với H2 (xúc tác Ni, t0) theo tỉ lệ mol 1 : 3.
⇒ Xem giải
Câu 28. Hóa hơi hoàn toàn 10,64 gam hỗn hợp X chứa hai este đều đơn chức, mạch hở thì thể tích hơi đúng bằng thể tích của 4,48 gam N2 (đo cùng điều kiện nhiệt độ và áp suất). Nếu đun nóng 10,64 gam X với 300 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng, thu được một ancol duy nhất và m gam rắn khan. Giá trị của m là.
A. 14,48 gam B. 17,52 gam C. 17,04 gam D. 11,92 gam
⇒ Xem giải
Câu 29. Cho dung dịch Ba(OH)2 đến dư lần lượt vào các dung dịch: Al2(SO4)3, (NH4)2CO3, FeCl3, CaCl2, NaHCO3, KHSO4, số dung dịch tạo ra kết tủa là.
A. 5 B. 4 C. 6 D. 3
⇒ Xem giải
Câu 30. Học sinh “Nguyễn Công Bảo” đã đọc các hợp chất amin dưới đây như sau:
(1) CH3-NH2: metanamin.
(2) CH3-NH-CH3: metylmetanamin.
(3) CH3-CH(NH2)-CH3: metyletan-2-amin.
(4) CH3-NH-CH(CH3)2: N-metylpropan-1-amin.
(5) C6H5-NH-CH3: N-metylphenylamin.
Số amin mà học sinh “Nguyễn Công Bảo” đọc sai là.
A. 3 B. 2 C. 1 D. 4
Câu 31. Thủy phân 0,15 mol peptit X, thu được hỗn hợp gồm 0,04 mol Gly-Gly-Ala; 0,06 mol Gly-Ala-Ala; 0,02 mol Ala-Ala; 0,04 mol Gly-Gly; 0,08 mol Gly và 0,10 mol Ala. Phân tử khối của X là.
A. 331 B. 274 C. 260 D. 288
⇒ Xem giải
Câu 32. Cho từ từ dung dịch Ba(OH)2 đến dư vào dung dịch chứa AlCl3 x (mol/l) và Al2(SO4)3 y (mol/l). Phản ứng được biểu diễn theo đồ thị sau:
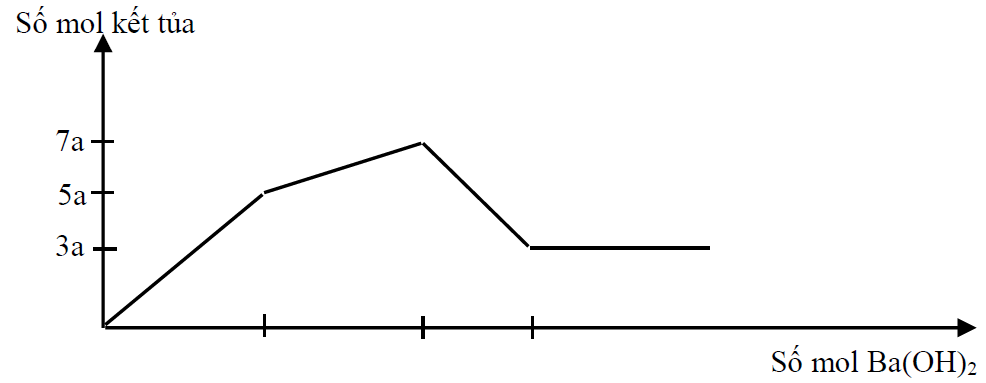
Tỉ lệ x : y là.
A. 2 : 3 B. 2 : 1 C. 1 : 2 D. 3 : 2
⇒ Xem giải
Câu 33. Cho các phát biểu sau:
(1) Đốt cháy bất kỳ một amin, luôn thu được nitơ đơn chất.
(2) Ở điều kiện thường, đimetylamin là chất khí, tan tốt trong nước.
(3) Nhỏ nước Br2 vào dung dịch alanin, xuất hiện kết tủa trắng.
(4) Dung dịch anilin không làm đổi màu phenolphtalein.
(5) Propan-2-amin là amin bậc 2.
(6) Các peptit đều cho phản ứng màu biurê.
Số phát biểu đúng là.
A. 5 B. 3 C. 4 D. 6
Câu 34. Tiến hành điện phân 200 ml dung dịch CuSO4 xM và NaCl 0,6M bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi I = 5A trong thời gian 7334 giây thì dừng điện phân, thấy khối lượng dung dịch giảm m gam. Dung dịch sau điện phân hòa tan tối đa 2,16 gam Mg. Nhận định nào sau đây là đúng?
A. Giá trị của m là 16,02 gam.
B. Dung dịch sau điện phân chứa Na+, Cu2+, H+ và SO42-.
C. Giá trị của x là 1,5M.
D. Nếu thời gian điện phân là 7720 giây thì nước bắt đầu điện phân ở cả hai cực.
⇒ Xem giải
Câu 35. Thực hiện các thí nghiệm sau:
(1) Cho a mol Mg vào dung dịch chứa a mol Fe2(SO4)3.
(2) Cho a mol Fe tác dụng với dung dịch chứa 3a mol HNO3, thu khí NO là sản phẩm khử duy nhất.
(3) Cho a mol Fe vào dung dịch chứa 3a mol AgNO3.
(4) Sục a mol khí CO2 vào dung dịch chứa a mol Ca(OH)2.
(5) Cho dung dịch chứa 3a mol NaOH vào dung dịch chứa a mol AlCl3.
Sau khi kết thúc phản ứng, số trường hợp thu được dung dịch chứa hai muối là.
A. 4 B. 5 C. 2 D. 3
⇒ Xem giải
Câu 36. Cho 33,26 gam hỗn hợp X gồm Fe3O4, Fe(OH)3, Fe(OH)2 và Cu vào 500 ml dung dịch HCl 1,6M thu được dung dịch Y và 7,68 gam rắn không tan. Cho dung dịch AgNO3 dư vào Y, thu được khí 0,045 mol khí NO (sản phẩm khử duy nhất của N+5) và 126,14 gam kết tủa. Các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Fe(OH)2 trong hỗn hợp X là.
A. 14,1% B. 21,1% C. 10,8% D. 16,2%
⇒ Xem giải
Câu 37. Hỗn hợp X gồm glucozơ, lysin và hexametylenđiamin. Đốt cháy hoàn toàn 0,2 mol X cần dùng 1,46 mol O2, sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua bình đựng H2SO4 đặc (dùng dư), khí thoát ra khỏi bình có thể tích là 28,672 lít (đktc). Mặt khác cho 24,06 gam X trên vào dung dịch HCl loãng dư, thu được dung dịch Y có chứa m gam các hợp chất hữu cơ. Giá trị của m là.
A. 10,05 gam B. 28,44 gam C. 12,24 gam D. 16,32 gam
⇒ Xem giải
Câu 38. Đốt cháy 16,8 gam bột Fe trong oxi, sau một thời gian thu được 19,84 gam rắn X. Hòa tan hoàn toàn X trong dung dịch chứa NaHSO4 và x mol NaNO3, thu được dung dịch Y chứa các muối trung hòa và hỗn hợp khí Z gồm NO và H2 (tỉ lệ mol 1 : 1). Cho dung dịch NaOH dư vào Y (không có mặt oxi), thu được 30,06 gam kết tủa. Biết khí NO là sản phẩm khử duy nhất của N+5. Giá trị của x là.
A. 0,06 B. 0,08 C. 0,09 D. 0,12
⇒ Xem giải
Câu 39. Hỗn hợp X gồm ba este đều no, mạch hở, trong phân tử chỉ chứa một loại nhóm chức. Đốt cháy hoàn toàn 35,34 gam X cần dùng 1,595 mol O2, thu được 22,14 gam nước. Mặt khác đun nóng 35,34 gam E với dung dịch NaOH vừa đủ, thu được hỗn hợp Y chứa hai muối của hai axit có mạch không phân nhánh và 17,88 gam hỗn hợp Z gồm một ancol đơn chức và một ancol hai chức có cùng số nguyên tử cacbon. Phần trăm khối lượng của este đơn chức trong hỗn hợp X là.
A. 4,98% B. 12,56% C. 4,19% D. 7,47%
⇒ Xem giải
Câu 40. Cho 0,15 mol hỗn hợp rắn X gồm Mg và Fe vào dung dịch chứa FeCl3 0,8M và CuCl2 0,6M thu được dung dịch Y và 7,52 gam rắn gồm hai kim loại. Cho dung dịch AgNO3 dư vào Y, thu được 29,07 gam kết tủa. Nếu cho 0,15 mol X trên vào dung dịch HNO3 loãng dư, thấy khí NO thoát ra; đồng thời thu được dung dịch Z có khối lượng tăng 4,98 gam so với dung dịch ban đầu. Cô cạn dung dịch Z thu được lượng muối khan là.
A. 33,86 gam B. 33,06 gam C. 30,24 gam D. 32,26 gam
⇒ Xem giải

