[2018] Giải đề thi thử THPT Lương Thế Vinh – Hà Nội (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Đáp án và giải chi tiết:
| 1A | 2B | 3D | 4A | 5B | 6A | 7B | 8A | 9C | 10C |
| 11B | 12C | 13A | 14B | 15B | 16B | 17C | 18C | 19C | 20B |
| 21C | 22B | 23D | 24C | 25C | 26A | 27B | 28C | 29D | 30B |
| 31D | 32B | 33A | 34A | 35B | 36A | 37D | 38C | 39C | 40A |
Câu 1. Vị trí kim loại kiềm trong bảng HTTH là:
A. Nhóm IA B. Nhóm IIA C. Nhóm IB D. Nhóm IIB
Câu 2. Tính chất hoá học chung của kim loại là:
A. Tính oxi hóa B. Tính khử C. Tính axit D. Tính bazơ
Câu 3. Để phân biệt 3 dung dịch glyxin; axit axetic; etylamin chỉ cần dùng một thuốc thử. Thuốc thử đó là:
A. natri kim loại B. Dung dịch HCl C. dung dịch NaOH D. Quỳ tím
Câu 4. Chất không có khả năng tham gia phản ứng trùng hợp là:
A. Toluen B. Stiren C. Caprolactam D. Etilen
Câu 5. Dầu thực vật hầu hết là lipit ở trạng thái lỏng do:
A. Chứa chủ yếu gốc axit béo no B. Chứa chủ yếu gốc axit béo không no
C. Trong phân tử có chứa gốc Glyxerol D. Chứa axit béo tự do
Câu 6. Thủy phân chất X thu được sản phẩm gồm glucozơ và fructozơ. Vậy X là:
A. Saccarozơ B. Glixerol C. Tinh bột D. Xenlulozơ
Câu 7. Cặp nào không có khả năng xảy ra phản ứng:
A. Dung dịch Cu(NO3)2 và dung dịch NaOH B. Nung hỗn hợp Fe và ZnO
C. Dung dịch ZnCl2 và dung dịch NaOH D. Na2CO3 và dung dịch HCl
Câu 8. Dung dịch FeSO4 có lẫn tạp chất là CuSO4. Để thu được FeSO4 tinh khiết ta dùng:
A. Bột Fe dư B. Bột Al dư C. Bột Cu dư D. Bột Zn dư
Câu 9. Cho từng chất sau vào dung dịch Na2CO3: Ag; CuO; Ba(OH)2; AgNO3; CO2; Quỳ tím; Fe; K; AlCl3. Số trường hợp xảy ra phản ứng là:
A. 4 B. 5 C. 6 D. 7
Câu 10. Trong số các loại polime sau: nilon-6; tơ axetat; tơ tằm; tơ visco; nilon-6,6; tơ nitron; cao su Buna; Poli (metyl metacrylat); cao su thiên nhiên; PVC. Số polime tổng hợp là:
A. 8 B. 5 C. 6 D. 7
Câu 11. Kim loại Zn có thể khử được ion nào sau đây:
A. Na+ B. H+ C. Ca2+ D. Mg2+
Câu 12. Khi điện phân dung dịch KCl có màng ngăn thì ở catot thu được:
A. Cl2. B. H2. C. KOH và H2. D. Cl2 và H2.
Câu 13. Cho bột Cu đến dư vào dung dịch hỗn hợp gồm Fe(NO3)3 và AgNO3 thu được chất rắn X và dung dịch Y. X và Y chứa:
A. X (Ag, Cu); Y (Cu2+, Fe2+). B. X (Ag); Y (Cu2+, Fe2+).
C. X (Ag); Y (Cu2+). D. X (Fe); Y (Cu2+).
Câu 14. Cho các chất: Al, Al2O3, Al2(SO4)3, Zn(OH)2, NaHS, K2SO3, (NH4)2CO3. Số chất đều phản ứng được với dung dịch HCl và dung dịch NaOH là:
A. 4 B. 5 C. 6 D. 7
Câu 15. Nhiệt phân hoàn toàn Fe(NO3)2 trong điều kiện không có không khí thu được các sản phẩm là:
A. FeO, NO2, O2 B. Fe2O3, NO2, O2 C. Fe2O3, NO2 D. Fe, NO2, O2
Câu 16. Đốt cháy hoàn toàn chất hữu cơ X mạch hở thu được CO2 và nước. Phân tử khối của X là 30. Số hợp chất hữu cơ thỏa mãn điều kiện trên là:
A. 1 B. 2 C. 3 D. 4
Câu 17. Cho các axit sau: Axit p-metyl benzoic (1); Axit p-amino benzoic (2); Axit p-nitro benzoic (3); Axit benzoic (4). Dãy nào sau đây được sắp xếp theo thứ tự tăng dần tính axit:
A. (1) < (2) < (3) <(4) B. (4) < (3) < (2) < (1).
C. (2) < (1) < (4 < (3) D. (4) < (3) < (1) < (2)
Câu 18. Có các kết luận sau:
1. Từ glyxin, alanin và valin sẽ tạo ra được 6 tripeptit chứa đồng thời glyxin, alanin và valin.
2. C8H10O có 2 ancol thơm khi tách nước tạo ra sản phẩm có khả năng tham gia phản ứng trùng hợp.
3. C4H8O2 có 6 đồng phân đơn chức mạch hở.
4. C4H11N có 4 đồng phân khi tác dụng với HCl tạo ra muối dạng RNH3Cl.
5. Glucozơ vừa có khả năng thể hiện tính oxi hóa, vừa có khả năng thể hiện tính khử.
6. Ở điều kiện thường các amino axit là chất rắn, màu trắng.
Số kết luận đúng là:
A. 3. B. 4. C. 5. D. 6.
Câu 19. Cho các nhận xét sau:
1. Tương tự như axit axetic, aminoaxit có thể tác dụng với bazơ tạo ra muối và nước.
2. Axit axetic và axit α-aminoglutaric có thể làm đổi màu quỳ tím thành đỏ.
3. Thủy phân không hoàn toàn peptit: Gly-Phe-Tyr-Gly-Lys-Gly-Phe-Tyr có thể thu được 6 tripeptit có chứa Gly.
4. Cho HNO3 đặc vào ống nghiệm chứa anbumin thấy tạo dung dịch màu tím.
5. Đipeptit có phản ứng màu biure
6. Liên kết của nhóm CO với nhóm NH giữa hai đơn vị amino axit được gọi là liên kết peptit.
Số nhận xét đúng là:
A. 2 B. 3 C. 4 D. 5
Câu 20. Hiện tượng xảy ra khi nhỏ từ từ tới dư dung dịch NaOH vào dung dịch Ba(HCO3)2 là:
A. Không có hiện tượng gì
B. Có kết tủa trắng xuất hiện không tan trong NaOH dư
C. Có kết tủa trắng xuất hiện trong tan NaOH dư
D. Có sủi bọt khí không màu thoát ra.
Câu 21. Cho các phát biểu sau:
1. Các kim loại Na, Ba, K đều có cấu trúc mạng tinh thể lập phương tâm khối.
2. Từ Li đến Cs (nhóm IA) khả năng phản ứng với nước mạnh dần.
3. Liti là kim loại có tính khử mạnh nhất.
4. NaHCO3 là chất lưỡng tính.
5. Thạch cao nung có công thức CaSO4.2H2O được ứng dụng bó bột, đắp tượng, đúc khuôn,…
6. Liti là kim loại nhẹ nhất.
Số phát biểu đúng là:
A. 2 B. 3 C. 4 D. 5
Câu 22. Thí nghiệm nào sau đây tạo ra kết tủa sau khi kết thúc phản ứng:
A. Cho dung dịch Ba(OH)2 dư vào dung dịch AlCl3.
B. Cho dung dịch NH3 dư vào dung dịch AlCl3.
C. Cho Al vào dung dịch NaOH dư.
D. Đun nóng nước có tính cứng vĩnh cửu.
Câu 23. Amin nào sau đây là amin bậc 2:
A. Isopropylamin B. Anilin. C. metylamin. D. Đimetylamin.
Câu 24. Polime X là chất rắn trong suốt, có khả năng cho ánh sáng truyền qua tốt nên được dùng chế tạo thủy tinh hữu cơ plexiglas. Tên gọi của X là:
A. poliacrilonitrin. B. polietilen.
C. poli(metyl metacrylat). D. poli(vinyl clorua).
Câu 25. Đốt cháy hoàn toàn hỗn hợp X gồm 2 este no đơn chức, mạch hở, thu được 1,8 gam H2O. Thủy phân hoàn toàn hỗn hợp 2 este trên thu được hỗn hợp Y gồm 1 ancol và axit. Nếu đốt cháy ½ hỗn hợp Y thì thể tích CO2 thu được ở đktc là:
A. 4,48 lít B. 2,24 lít C. 1,12 lít D. 3,36 lít
⇒ Xem giải
Câu 26. Để sản xuất ancol etylic người ta dùng nguyên liệu là mùn cưa và vỏ bào từ gỗ chứa 50% xenlulozơ. Nếu muốn điều chế một tấn ancol etylic, hiệu suất quá trình là 70% thì khối lượng nguyên liệu cần dùng gần nhất bằng:
A. 5031kg. B. 5000kg. C. 5100kg. D. 6200kg.
⇒ Xem giải
Câu 27. Để phản ứng hết 400 ml dung dịch hỗn hợp HCl 0,5M và FeCl3 0,8M khối lượng hỗn hợp gồm metylamin và etylamin có tỉ khối so với H2 là 17,25 cần dùng là:
A. 41,4 gam. B. 40,02 gam. C. 51,75 gam. D. 33,12 gam.
⇒ Xem giải
Câu 28. X là dung dịch HCl nồng độ x mol/l. Y là dung dịch Na2CO3 nồng độ y mol/l. Nhỏtừ từ 100 ml X vào 100 ml Y, sau các phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100 ml Y vào 100 ml X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 = 4 : 7. Tỉ lệ x : y là:
A. 11:7 B. 11 : 4. C. 7 : 5. D. 7 : 3.
⇒ Xem giải
Câu 29. Cho 0,02 mol amino axit X tác dụng vừa đủ với 200 ml dung dịch HCl 0,1M thu được 3,67 gam muối khan. Mặt khác 0,02 mol X tác dụng vừa đủ với 40 gam dung dịch NaOH 4%. Công thức phân tử của X là:
A. (H2N)2C3H5COOH. B. H2NC2H3(COOH)2. C. H2NC3H6COOH. D. H2NC3H5(COOH)2.
⇒ Xem giải
Câu 30. Một polime X được xác định có phân tử khối là 39062,5 đvC với hệ số trùng hợp để tạo nên polime này là 625. Polime X là?
A. PP B. PVC C. PE D. PS
Câu 31. Cho 7,65 gam hỗn hợp X gồm Al và Al2O3 (trong đó Al đơn chất chiếm 60% khối lượng) tan hoàn toàn trong dung dịch Y gồm H2SO4 và NaNO3, thu được dung dịch Z chỉ chứa 3 muối trung hòa và m gam hỗn hợp khí T (trong T có 0,015 mol H2). Cho dung dịch BaCl2 dư vào Z đến khi các phản ứng xảy ra hoàn toàn, thu được 93,2 gam kết tủa. Còn nếu cho Z phản ứng với NaOH thì lượng NaOH phản ứng tối đa là 0,935 mol. Giá trị của m gần giá trị nào nhất sau đây?
A. 2,5. B. 3,0. C. 1,0. D. 1,5.
⇒ Xem giải
Câu 32. Đun hỗn hợp etylen glicol và axit cacboxylic X (phân tử chỉ có nhóm -COOH) với xúc tác H2SO4 đặc, thu được hỗn hợp sản phẩm hữu cơ, trong đó có chất hữu cơ Y mạch hở. Đốt cháy hoàn toàn 3,95 gam Y cần 4,00 gam O2, thu được CO2 và H2O theo tỉ lệ mol tương ứng 2 : 1. Biết Y có công thức phân tử trùng với công thức đơn giản nhất, Y phản ứng được với NaOH theo tỉ lệ mol tương ứng 1 : 2. Phát biểu nào sau đây không đúng:
A. Tổng số nguyên tử hiđro trong hai phân tử X, Y bằng 8.
B. X có đồng phân hình học.
C. Y không có phản ứng tráng bạc.
D. Y tham gia được phản ứng cộng với Br2 theo tỉ lệ mol tương ứng 1 : 2.
⇒ Xem giải
Câu 33. Cho 1,12 gam bột Fe và 0,24 gam bột Mg vào 250ml dung dịch CuSO4. Sau khi phản ứng kết thúc khối lượng kim loại có trong dung dịch là 1,88 gam. Nồng độ mol/lít của dung dịch CuSO4 trước phản ứng là:
A. 0,1M. B. 0,04M. C. 0,06M. D. 0,12M.
⇒ Xem giải
Câu 34. Cho 19,2 gam Cu vào 500 ml dung dịch NaNO3 1M, sau đó thêm 500ml dung dịch HCl 2M. Thể tích khí NO (sản phẩm khử duy nhất ở đktc) thu được là:
A. 2,24 lít. B. 3,36 lít. C. 4,48 lít. D. 6,72 lít.
⇒ Xem giải
Câu 35. Hỗn hợp X gồm axit axetic, etyl axetat và metyl axetat. Cho m gam hỗn hợp X tác dụng vừa đủ với 200 ml dung dịch NaOH 1M. Mặt khác, đốt cháy hoàn toàn m gam hỗn hợp X cần V lít O2 (đktc) sau đó cho toàn bộ sản phẩm cháy vào dung dịch NaOH dư thấy khối lượng dung dịch tăng 40,3 gam. Giá trị của V là:
A. 19,04 lít B. 17,36 lít C. 15,12 lít D. 19,60 lít
⇒ Xem giải
Câu 36. Hỗn hợp E gồm peptit X mạch hở (cấu tạo từ Gly, Ala) và este Y (được tạo ra từ phản ứng este hóa giữa axit cacboxylic no đơn chức mạch hở và metanol). Đốt cháy hoàn toàn m gam E cần 15,68 lít O2 (đktc). Mặt khác thủy phân m gam E trong dung dịch NaOH vừa đủ thu được 24,2 gam hỗn hợp muối (trong đó số mol muối natri của Gly lớn hơn số mol muối natri của Ala). Đốt cháy hoàn toàn khối lượng muối trên cần 20 gam O2 thu được H2O, Na2CO3, N2 và 18,7 gam CO2. Tỉ lệ số mol Gly : Ala trong X là
A. 3:1 B. 2:1 C. 4:3 D. 3:2
⇒ Xem giải
Câu 37. Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thấy thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH dư thì được 1,75V lít khí. Thành phần % theo khối lượng của Na trong X là (biết các thể tích khí đo trong cùng điều kiện):
A. 39,87% B. 77,31% C. 49,87% D. 29,87%
⇒ Xem giải
Câu 38. Nhiệt phân hoàn toàn a mol Fe(NO3)2 thu được hỗn hợp khí X có tỉ khối so với H2 bằng T1. Nhiệt phân hoàn toàn a mol Fe(NO3)3 thu được hỗn hợp khí Y có tỉ khối so với H2 bằng T2. Biểu thức liên hệ giữa T1 và T2 là:
A. T1 = 0,972T2 B. T1 = T2 C. T2 = 0,972T1 D. T2 = 1,08T1
⇒ Xem giải
Câu 39. Mắc nối tiếp 2 bình điện phân: bình X chứa 500 ml dung dịch hỗn hợp CuCl2 x mol/lít và HCl 4x mol/lít với bình Y chứa 500 ml dung dịch AgNO3 5x mol/lít. Sau t giây điện phân thì ở catot bình X thoát ra m gam kim loại, còn ở catot bình Y thoát ra 10,8 gam kim loại. Sau 3t giây thì ở catot bình X thoát ra 2m gam kim loại, còn ở catot bình Y thoát ra 32,4 gam kim loại. Biết cường độ dòng điện không đổi, hiệu suất điện phân 100%. Nếu sau 3t giây ngừng điện phân, lấy 2 dung dịch thu được sau điện phân đổ vào nhau thì thu được:
1. 28,7 gam kết tủa
2. dung dịch có 0,5 mol HNO3
3. dung dịch có 0,6 mol H+
4. dung dịch có 16,25 gam chất tan
Kết luận không đúng là:
A. 2. B. 1. C. 4. D. 3.
⇒ Xem giải
Câu 40. Cho a mol Al tan hoàn toàn vào dung dịch chứa b mol HCl thu được dung dịch Y chứa 2 chất tan có cùng nồng độ mol. Thêm từ từ dung dịch NaOH vào dung dịch Y ta có đồ thị sau:
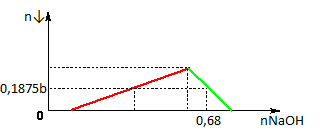
Cho a mol Al phản ứng với dung dịch hỗn hợp chứa 0,15b mol FeCl3 và 0,2b mol CuCl2. Sau khi phản ứng kết thúc thu được x gam chất rắn. Giá trị của x là:
A. 11,776. B. 12,896. C. 10,874. D. 9,864.
⇒ Xem giải

Bình luận