Để xác định nồng độ acetic acid có trong một mẫu giấm ăn, một nhóm học sinh tiến hành thí nghiệm sau:
• Bước 1: Pha loãng 10,00 mL giấm ăn bằng nước cất trong bình định mức 100,00 mL dung dịch X. Dùng pipet lấy 10,00 mL dung dịch X cho vào bình tam giác rồi thêm vài giọt chất chỉ thị phenolphthalein.
• Bước 2: Tráng sạch buret bằng nước cất, sau đó tráng lại bằng một ít dung dịch NaOH 0,02M. Lắp dụng cụ như hình bên. Cho dung dịch NaOH 0,02 M vào cốc thủy tinh, sau đó rót vào buret (đã khóa) và chỉnh về vạch 0.
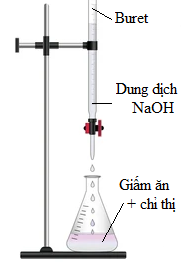
• Bước 3: Vặn khóa buret để dung dịch NaOH trong buret chảy từ từ từng giọt vào bình tam giác đồng thời lắc đều bình. Quan sát đến khi dung dịch trong bình tam giác chuyển từ không màu sang màu hồng bền trong khoảng 20 giây thì dừng lại.
• Bước 4: Ghi lại thể tích dung dịch NaOH đã dùng. Lặp lại thí nghiệm 3 lần.
a) Nếu không tráng buret bằng dung dịch NaOH 0,02 M sau khi rửa bằng nước cất, kết quả nồng độ acetic acid tính được sẽ cao hơn thực tế.
b) Thể tích dung dịch NaOH 0,02 M trong 3 lần thí nghiệm được ghi lại như sau:
Thí nghiệm………. Lần 1…. Lần 2…. Lần 3
Vdd NaOH (mL)….. 37,5….. 37,4…… 37,6
Nồng độ mol của acetic acid có trong mẫu giấm ăn ban đầu dựa trên các số liệu thực nghiệm là 0,75 M.
c) Trình tự các bước tiến hành thí nghiệm như trên là hoàn toàn hợp lý và đảm bảo tính chính xác về mặt kỹ thuật chuẩn độ.
d) Trong lần thí nghiệm thứ 2, tại thời điểm dung dịch trong bình tam giác đổi màu, thể tích đọc được trên buret là 37,4 mL và có một giọt dung dịch còn treo ở đầu dưới của buret. Một học sinh cho rằng cần lấy giọt dung dịch này vào bình tam giác. Một học sinh khác lại cho rằng nên bỏ giọt dung dịch này. Tại điểm kết thúc chuẩn độ, nếu còn một giọt dung dịch NaOH treo ở đầu buret mà không cho vào bình tam giác thì kết quả tính toán nồng độ acid sẽ bị thấp hơn thực tế.
Câu trả lời tốt nhất
(a) Đúng, nếu không tráng buret bằng NaOH 0,02M thì một lượng nước còn sót lại sau khi tráng bằng nước sẽ làm loãng dung dịch chuẩn (thấp hơn 0,02M)
CM CH3COOH = 0,02.Vdd NaOH / Vdd CH3COOH
Thể tích dung dịch NaOH đã dùng tăng lên (vì nồng độ thực nhỏ hơn 0,02 nên phải tốn nhiều thể tích hơn để trung hòa acid) —> Nồng độ CH3COOH tăng lên so với thực tế.
(b) Đúng:
V trung bình = (37,5 + 37,4 + 37,6)/3 = 37,5 ml
—> nCH3COOH = nNaOH = 37,5.0,02 = 0,75 mmol
10 mL X được tạo ra bởi 1 mL giấm nên:
CM CH3COOH = 0,75/1 = 0,75 mmol/mL = 0,75M
(c) Đúng, cách làm hợp lý (dung dịch NaOH trong buret), giấm + phenolphthalein trong bình tam giác) thuận lợi cho việc quan sát thay đổi màu sắc, cách tiến hành các bước đúng.
(d) Sai, chỉ đọc kết quả khi buret đang trong trạng thái khóa, vì vậy kết quả đã đọc xong rồi thì 1 giọt còn dính lại hay cho rơi xuống không ảnh hưởng đến kết quả được nữa.
