Nung hỗn hợp X gồm NaHCO3 và CaCO3 ở nhiệt độ cao đến khối lượng không đổi, thu được chất rắn Y. Cho Y vào nước dư, thu được 12 gam chất rắn Z và dung dịch E. Dẫn rất từ từ khí CO2 vào dung dịch E thu được đồ thị biểu diễn khối lượng chất tan (y gam) phụ thuộc vào khí CO2 (x mol) như hình vẽ bên.
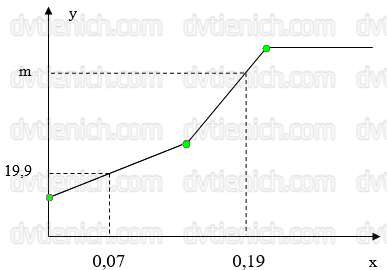
Giả sử xem như lượng khí CO2 tan trong nước không đáng kể, các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 26,16. B. 24,92. C. 29,88. D. 25,54.
Câu trả lời tốt nhất
X gồm NaHCO3 (2a) và CaCO3 (b)
Y gồm Na2CO3 (a) và CaO (b)
Khối lượng chất tan tăng qua 2 giai đoạn rồi không đổi nên E chứa NaOH (2b) và Na2CO3 dư (a – b)
nCaCO3 = b = 0,12
Khi nCO2 = 0,07 thì dung dịch chứa Na2CO3 (a – b + 0,07) và NaOH (2b – 0,14)
—> 106(a – b + 0,07) + 40(2b – 0,14) = 19,9
—> a = 0,2
Vậy E chứa NaOH (0,24) và Na2CO3 (0,08)
nCO2 = 0,19 —> Các sản phẩm là Na2CO3 (0,13) và NaHCO3 (0,14)
—> m = 25,54 gam
Em muốn hỏi một chút ạ
+ Vì sao ta có thể suy ra NaOH (2b) vậy ạ
+ Vì sao khi nCO2=0,07 ta có thể suy ra được số mol của Na2CO3 và NaOH như vậy ạ
+ Và khi số mol của CO2=0,19 , làm thế nào để tính được số mol các chất tan Na2CO3 và NaHCO3 như vậy ạ
( Với lại cho em hỏi dạng bài tập này ở phần nào vậy ạ )

