Khi đun nóng nhẹ ở nhiệt độ phù hợp, lượng nước kết tinh thường tách ra khỏi hợp chất. Để xác định hàm lượng nước kết tinh trong muối FeSO4.xH2O (hợp chất A, coi như không lẫn tạp chất) bằng phương pháp đun nóng, một nhóm học sinh thực hiện thí nghiệm theo các bước sau:
• Bước 1: Cân chén nung và ghi lại khối lượng vào bảng kết quả (m1).
• Bước 2: Thêm một lượng khoảng từ 1,45 gam đến 1,65 gam chất A (có màu xanh nhạt) vào chén nung. Cân và ghi khối lượng mới của chén nung có chứa A (m2).
• Bước 3: Đặt chén nung chứa A lên lưới tam giác và đun nóng nhẹ trong khoảng 2 phút, tránh đun nóng mạnh dẫn đến sự phân hủy FeSO4 tạo thành Fe2O3 (có màu đỏ nâu).
• Bước 4: Để nguội cân lại chén nung cùng phần chất rắn (không có màu đỏ nâu) còn lại bên trong, ghi khối lượng (m3).
Lặp lại bước 3 và bước 4 cho đến khi khối lượng cân được ở bước 4 không đổi. Kết quả thí nghiệm của nhóm học sinh được ghi trong bảng (hình trên).
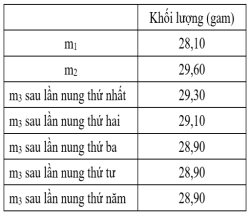
Dựa vào số liệu, học sinh tính phần trăm lượng nước kết tinh có trong A.
a) Giả thiết phù hợp với mục đích và quá trình tiến hành thí nghiệm trên là “Nếu đun nóng nhẹ mẫu rắn FeSO4.xH2O, thì nước kết tinh sẽ bị tách ra ở dạng hơi làm cho khối lượng mẫu rắn giảm, nhờ đó xác định được hàm lượng nước kết tinh”.
b) Chưa có dấu hiệu hình thành iron (III) oxide trong quá trình nung.
c) Phần trăm khối lượng (làm tròn đến hàng phần mười) của nước kết tinh trong muối FeSO4.xH2O xác định được từ số liệu của thí nghiệm trên là 13,3%.
d) Sự giảm khối lượng của chén nung chứa A là do nước kết tinh tách ra khỏi A và bay hơi.
Câu trả lời tốt nhất
(a) Đúng, đây là giả thuyết phù hợp, có thể đúng hoặc sai. Nếu H2O thoát ra hết, FeSO4 không bị phân hủy thì giả thuyết này đúng.
(b) Đúng, sau khi nung chất rắn không có màu đỏ nâu nên chưa có dấu hiệu hình thành iron (III) oxide trong quá trình nung.
(c) Sai
mFeSO4.xH2O = 29,60 – 28,10 = 1,50 gam
mFeSO4 = 28,90 – 28,10 = 0,80 gam
—> %H2O = (1,50 – 0,80)/1,50 = 46,67%
(d) Đúng
