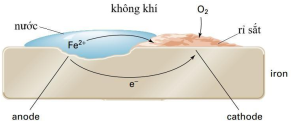
Quá trình ăn mòn điện hóa iron trong gang hoặc thép (hợp kim của Fe-C) tạo thành gỉ sắt (Fe2O3.xH2O) khi để gang hoặc thép trong không khí được mô tả bởi hình sau:
Cho các nhận định sau:
a) Thép không gỉ (inox) ít bị ăn mòn là nhờ tạo được lớp oxide thụ động rất mỏng, bền vững, thường là Cr2O3, ngăn cản sự tiếp xúc của sắt với môi trường.
b) Phản ứng tạo thành gỉ sắt (Fe2O3.xH2O) từ Fe(OH)2 là quá trình ăn mòn hóa học.
c) Gang ít bị ăn mòn hơn thép do chứa nhiều carbon có khả năng tạo lớp bảo vệ thụ động trên bề mặt.
d) Tại cathode xảy ra quá trình: O2(g) + 2H2O(l) + 4e → 4OH-(aq) và anode xảy ra quá trình: Fe(s) → Fe2+(aq) + 2e
Câu trả lời tốt nhất
(a) Đúng, chromium (Cr) trong inox khi tiếp xúc với không khí sẽ tạo ra một màng oxide Cr2O3 cực mỏng nhưng rất kín và bền, ngăn chặn các tác nhân ăn mòn xâm nhập vào lớp sắt bên trong.
(b) Sai, phản ứng tạo gỉ sắt là giai đoạn sau của quá trình ăn mòn điện hóa, không phải quá trình ăn mòn hóa học.
(c) Sai, thực tế, gang thường bị ăn mòn nhanh hơn thép trong môi trường điện ly. Carbon trong gang tồn tại dưới dạng các tinh thể graphite, đóng vai trò là các cực dương (cathode) tạo nên vô số pin điện hóa siêu nhỏ, thúc đẩy quá trình ăn mòn sắt.
(d) Đúng, sắt bị oxi hóa tại anode và oxy hòa tan bị khử tại cathode.

