Tiến hành điện phân dung dịch NaCl theo các bước:
• Bước 1: Lắp thiết bị thí nghiệm điện phân dung dịch NaCl với điện cực trơ như hình bên.
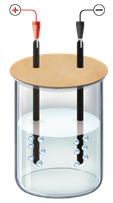
• Bước 2: Rót khoảng 80 mL dung dịch NaCl bão hòa vào cốc rồi nhúng hai điện cực than chì vào dung dịch.
• Bước 3: Nối hai điện cực than chì với hai cực của nguồn điện và tiến hành điện phân trong khoảng 5 phút.
• Bước 4: Cho một mẫu cánh hoa màu hồng vào cốc chứa khoảng 5 mL dung dịch sau điện phân.
Phát biểu nào sau đây không đúng?
A. Ở bước 3, trên bề mặt hai điện cực đều có khí thoát ra.
B. Ở bước 4, cánh hoa màu hồng dần bị nhạt màu.
C. Trong quá trình điện phân cần đậy nắp để hạn chế sự thoát khí Cl2.
D. Ở anode xảy ra sự khử ion Cl-.
Câu trả lời tốt nhất
A. Đúng, trên bề mặt 2 điện cực thấy có bọt khí nhưng chỉ bên cathode là khí bay ra ngoài, còn bên anode thấy sủi bọt rồi biến mất:
2NaCl + 2H2O —> H2 + Cl2 + 2NaOH
Cl2 + 2NaOH —> NaCl + NaClO + H2O
B. Đúng, cánh hoa hồng bị mất màu do NaClO có tính oxi hóa mạnh sẽ oxi hóa các chất hữu cơ gây sắc tố màu ở cánh hoa thành chất đơn giản không màu (bị tẩy trắng).
C. Đúng, mặc dù Cl2 đã phản ứng với OH- và bị giữ lại trong dung dịch nhưng không phải khi nào cũng bị giữ lại triệt để, vì vậy vẫn cần nắp đậy hoặc thực hiện trong tủ hốt để phòng độc.
D. Sai, ở anode xảy ra sự oxi hóa Cl-:
2Cl- —> Cl2 + 2e
