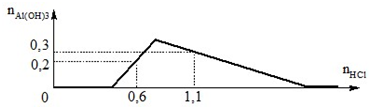
Cho từ từ dung dịch HCl vào dung dich A chứa a mol Ba(OH)2 và b mol Ba(AlO2)2. Đồ thị biểu diễn số mol Al(OH)3 theo số mol HCl như sau:
Nếu cho dung dịch A ở trên tác dụng với 820 ml dung dịch H2SO4 1M thì thu được bao nhiêu gam kết tủa?
A. 108,80. B. 106,20. C. 102,56. D. 101,78.
Câu trả lời tốt nhất
nOH- = 2a và nAlO2- = 2b
Khi kết tủa chưa bị hòa tan:
nH+ = 0,6 = 2a + 0,2
Khi kết tủa bị hòa tan một phần:
nH+ = 1,1 = 2a + 4.2b – 0,3.3
—> a = 0,2 và b = 0,2
nH2SO4 = 0,82 —> nBaSO4 = a + b = 0,4
nH+ = 0,82.2 = 2a + 4.2b – 3nAl(OH)3
—> nAl(OH)3 = 0,12
—> m↓ = 102,56
Cho em hỏi là tại sao đoạn 1.1 mol là nH+=nOH- + 4n AlO2 -3nAl(OH)3 ạ
×

