Ammonia đóng vai trò quan trọng trong sản xuất phân bón. Trong công nghiệp, ammonia được sản xuất bằng quá trình Haber theo phản ứng:
N2(g) + 3H2(g) ⇋ 2NH3(g) (1)
Nghiên cứu về hiệu suất tổng hợp NH3 của phản ứng trên trong các điều kiện về nhiệt độ và áp suất khác nhau được biểu diễn theo đồ thị sau.
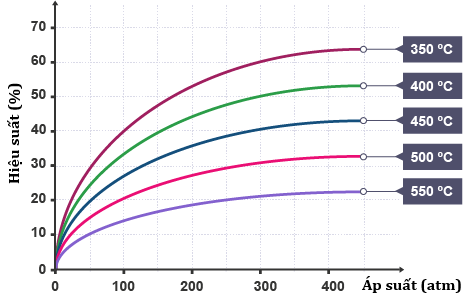
a) Dựa vào đồ thị, hãy cho biết và giải thích các trường hợp sau:
(i) Phản ứng (1) là phản ứng tỏa nhiệt hay thu nhiệt?
(ii) Hằng số cân bằng Kc của phản ứng (1) ở nhiệt độ 400°C so với ở nhiệt độ 500°C là nhỏ hơn hay lớn hơn?
b) Xác định chiều chuyển dịch của cân bằng (1) và giải thích khi thực hiện các tác động sau:
(i) tăng áp suất;
(ii) tăng nhiệt độ.
Câu trả lời tốt nhất
(a)
i. Dựa vào đồ thị ta thấy nhiệt độ càng cao, hiệu suất càng thấp —> (1) là phản ứng có chiều thuận tỏa nhiệt, chiều nghịch thu nhiệt.
ii. Ở 400°C, [NH3] lớn hơn, [N2] và [H2] nhỏ hơn so với cùng chất đó ở 500°C.
Vậy Kc = [NH3]²/[N2][H2]³ ở 400°C sẽ lớn hơn ở 500°C.
(b) Áp dụng nguyên lý chuyển dịch cân bằng Le Chatelier:
i. Tăng áp suất thì cân bằng chuyển dịch theo chiều giảm áp suất (chiều giảm số phân tử khí) —> Chiều thuận.
ii. Tăng nhiệt độ thì cân bằng chuyển dịch theo chiều giảm nhiệt độ (chiều thu nhiệt) —> Chiều nghịch.

