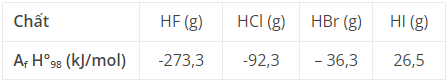
Biến thiên enthalpy tạo thành chuẩn của các halogen halide được cho trong bảng sau:
Câu 1.
a. Năng lượng liên kết HX tăng dần từ HF đến HI.
b. Phản ứng tổng hợp HCl: H2(g) + Cl2(g) → 2HCl (g) có  = -92,3 kJ.
= -92,3 kJ.
c. Phản ứng tổng hợp HBr: H2(g) + Br2(g) → 2HBr (g) là phản ứng tỏa nhiệt.
d. Phản ứng phân hủy HI: 2HI(g) → H2(g) + I2 (g) là phản ứng thu nhiệt.
Câu 2.
a) Năng lượng liên kết HX giảm dần từ HF đến HI.
b) Phản ứng tổng hợp HCl: H2(g) + Cl2(g) → 2HCl (g) có  = -184,6kJ.
= -184,6kJ.
c) Trong phản ứng giữa halogen với hydrogen, nhiệt lượng tỏa ra tăng dần từ F2 đến I2.
d) Phản ứng phân hủy HI: 2HI(g) → H2(g) + I2(g) là phản ứng thu nhiệt.
Câu trả lời tốt nhất
Câu 1.
(a) Sai, năng lượng liên kết HX giảm dần từ HF đến HI. Từ F- đến I- bán kính ion tăng nên mật độ điện tích âm trên ion giảm dẫn đến năng lượng liên kết giảm.
(b) Sai, phản ứng này có  = -92,3.2 = -184,6 kJ.
= -92,3.2 = -184,6 kJ.
(c) Đúng, phản ứng tổng hợp HBr có  = -36,3.2 < 0 nên tỏa nhiệt.
= -36,3.2 < 0 nên tỏa nhiệt.
(d) Sai, phản ứng phân hủy HI có  = -26,5.2 < 0 nên tỏa nhiệt.
= -26,5.2 < 0 nên tỏa nhiệt.
Câu 2.
(a) Đúng, năng lượng liên kết HX giảm dần từ HF đến HI. Từ F- đến I- bán kính ion tăng nên mật độ điện tích âm trên ion giảm dẫn đến năng lượng liên kết giảm.
(b) Đúng
(c) Sai, nhiệt lượng tỏa ra giảm dần từ F2 đến Br2, còn H2(g) + I2(g) là phản ứng thu nhiệt.
(d) Sai, phản ứng phân hủy 2HI(g) → H2(g) + I2(g) tỏa nhiệt do  = -26,5.2 < 0
= -26,5.2 < 0

