Cấu tạo và cơ chế hoạt động của pin Galvani Zn–Cu được biểu diễn ở sơ đồ sau:
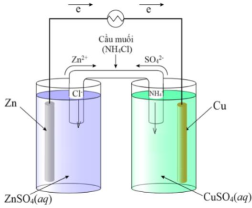
Cho biết: Thể tích của các dung dịch đều là 500 mL và nồng độ ban đầu của các muối đều là 1,00 M; nhiệt độ của thí nghiệm là 25°C; thế điện cực chuẩn của Cu2+/Cu là 0,34V; của Zn2+/Zn là –0,76V.
a) Nồng độ các ion (NH4+, Cl-) trong cầu muối giảm trong quá trình pin hoạt động.
b) Sức điện động của pin là 1,10V và không thay đổi trong quá trình pin hoạt động.
c) Trong pin Galvani Zn–Cu, điện cực Zn là anode và điện cực Cu là cathode.
d) Sau khi pin Galvani Zn–Cu dừng hoạt động (phản ứng kết thúc), khối lượng dung dịch CuSO4 giảm đúng bằng khối lượng Cu đã bám vào điện cực.
Câu trả lời tốt nhất
(a) Đúng, NH4+, Cl- di chuyển sang các cốc đựng dung dịch CuSO4, ZnSO4 tương ứng nên nồng độ của chúng trong cầu muối giảm dần.
(b) Sai, pin chỉ đạt 1,1V khi mạch ngoài hở (pin không hoạt động). Khi pin đang hoạt động, ngay từ thời điểm ban đầu cũng không đạt 1,1V và con số này giảm dần theo thời gian.
(c) Đúng, Zn có tính khử mạnh hơn Cu nên Zn là cực âm (anode), Cu là cực dương (cathode).
(d) Sai, ngoài Cu2+ bị khử thành Cu, cốc đựng dung dịch CuSO4 có nhận thêm Zn2+, NH4+ chuyển tới nên độ giảm khối lượng không bằng khối lượng Cu đã bám vào điện cực.

